El incremento de la demanda asistencial por afección renal asociada a enfermedades neoplásicas es una realidad en la mayoría de los servicios de nefrología. Para dar respuesta a esta situación, debe considerarse la creación de modelos asistenciales como consultas monográficas y desarrollar programas de formación en onconefrología que permitan optimizar la atención de estos pacientes.
A través de un estudio exploratorio y descriptivo, identificamos cuál es la situación actual de la afectación renal en pacientes con cáncer. El objetivo del presente estudio es establecer los criterios para la asistencia específica en el ámbito de la onconefrología. Para ello hemos revisado aspectos clave y analizado la situación actual en nuestro entorno, mediante una encuesta dirigida a todos los nefrólogos a través de la SEN, junto a la experiencia de 2 centros españoles. A partir de esta información hemos establecido una serie de requisitos y recomendaciones para la puesta en marcha de estas consultas.
The increase in demand for medical care for renal complications associated with neoplastic diseases is a reality in most nephrology departments. In response to this overall situation, the creation of healthcare models such as monographic consultations and develop training programs in onconephrology could improve the care of these patients.
Through an exploratory and descriptive study, we identified current situation of kidney involvement in cancer patients. The objective of the present study is to establish the criteria for specific assistance in the field of onconephrology. For this, we have reviewed key aspects and analyzed the current situation in our country, through a survey addressed to all nephrologists through the Spanish Society of Nephrology, together with the experience of 2 Spanish centers. From this information, we have established some requirements and recommendations for the start-up of these consultations.
En los últimos años, estamos asistiendo en nefrología a un incremento de las necesidades asistenciales de los pacientes con enfermedad oncológica1,2. Por este motivo, tanto nefrólogos como oncólogos creemos necesaria la colaboración que permita optimizar la atención de estos pacientes. La onconefrología surge como un área de la medicina cada vez más complicada y de rápido crecimiento. Las razones se derivan de la gran prevalencia de complicaciones renales en los pacientes con cáncer y también de la prevalencia de cáncer en pacientes con enfermedad renal.
Dentro de la enfermedad renal asociada al cáncer es predominante la posibilidad de daño renal agudo (DRA), en ocasiones asociado a fármacos nefrotóxicos3–6, que aumenta drásticamente en presencia de una enfermedad renal crónica (ERC) preexistente. Algunos tumores o agentes antineoplásicos pueden tener además un efecto deletéreo sobre la estructura glomerular y producir proteinuria al dañar los podocitos7. La conexión entre cáncer y riñón se amplía con daño renal relacionado con la inmunoterapia, trastornos hidroelectrolíticos, problemas relacionados con las dosis y tiempos de quimioterapia en pacientes con ERC y en diálisis, nefrectomía parcial o total en pacientes con cáncer y ERC, así como aspectos relacionados con el trasplante renal (donantes y receptores con historia previa de cáncer)8.
La onconefrología es ya una subespecialidad iniciada en muchos centros. Muchas publicaciones y organismos internacionales, como la Kidney Disease Improving Global Outcomes ?KDIGO?, invitan a organizar esta atención en los centros de referencia de oncología y nefrología1,9–13. Sin embargo, en el momento actual no existe información amplia y contrastada sobre algunos aspectos como la frecuentación a este tipo de consultas.
Algunos estudios ya apuntan a que los pacientes con cáncer tienen un riesgo de DRA a uno y 5 años de 17,5 y 27%, respectivamente3, y una prevalencia de ERC en estadio 3 del 12%5. El impacto sobre la mortalidad es también reseñable. A menor filtrado glomerular, existe una mayor mortalidad entre los pacientes con enfermedad neoplásica14.
Por otro lado, algunos estudios han apuntado que a menor filtrado glomerular, el riesgo de aparición de cáncer aumenta. De manera general, un descenso de 10ml/min en el filtrado glomerular incrementa el riesgo de cáncer un 29%15. En pacientes en tratamiento renal sustitutivo en hemodiálisis, la incidencia acumulada de desarrollo de tumores a 5 años se ha estimado en un 9,5%16. Mención aparte, los pacientes sometidos a un trasplante renal tienen una probabilidad 2,1 veces mayor que la población general de desarrollar un cáncer17.
El riesgo de DRA en pacientes con enfermedad tumoral durante una hospitalización ha sido igualmente demostrado en varios estudios, observándose una mayor estancia hospitalaria y riesgo de complicaciones1,18.
La complejidad de la relación entre ambas afecciones (cáncer y enfermedad renal) es cada vez más evidente y frecuente, determinando que el abordaje multidisciplinar resulte esencial para un adecuado y óptimo manejo de la enfermedad, su prevención, su tratamiento y sus complicaciones. Asimismo, la formación de subespecialistas en onconefrología y la creación de consultas monográficas deben constituir el punto de apoyo inicial en la valoración precoz e integral de este grupo de pacientes, tanto para una prevención de complicaciones mayores e ingresos innecesarios como para el desarrollo de áreas de investigación entre las diferentes especialidades de oncohematonefrología.
En el presente trabajo revisamos los motivos de derivación de estos pacientes, las características del abordaje multidisciplinar, la evaluación del paciente onconefrológico y la situación de las consultas de onconefrología en España. Presentamos, además, la escasa experiencia que tenemos hasta ahora en nuestro país, con la finalidad de estimular el valor de esta práctica médica, identificándose algunos de los requisitos para la puesta en marcha.
Valor añadido de las consultas monográficasEn los últimos años, debido a la evolución de diversas especialidades y como respuesta a una creciente necesidad asistencial, se ha ido consolidando la creación de consultas monográficas. De forma general, su objetivo es mejorar los resultados en salud mediante, entre otros aspectos, el abordaje transversal de la enfermedad atendida, la disminución de la variabilidad clínica y una mayor calidad de la atención de enfermedades poco prevalentes o situaciones clínicas que en muchas ocasiones son de mayor complejidad.
Especialidades como cardiología, neumología y reumatología han ido implantando consultas de estas características para la atención a enfermedades concretas. La insuficiencia cardíaca, la enfermedad pulmonar obstructiva crónica, los pacientes con oxigenoterapia domiciliaria y la artritis son algunos ejemplos de consultas que han demostrado su utilidad en cuanto a una disminución del número de ingresos hospitalarios o de episodios de urgencias19–23.
Dentro de la propia nefrología, el desarrollo de las unidades de ERC avanzada, como ejemplo de consulta monográfica, ha ido cobrando cada vez mayor importancia en nuestros servicios. Desde la propia Sociedad Española de Nefrología, recientemente se presentó el proyecto ACERCA, como modelo de acreditación para la calidad de estas unidades24. Con base en la utilización de estándares comunes, podrían obtenerse resultados unificados. Hasta ahora, desafortunadamente, no disponemos de datos objetivos de este tipo de consultas, a pesar del tiempo de instauración en muchos de nuestros hospitales.
Existen, asimismo, dentro de la nefrología algunas otras experiencias multidisciplinares como en el caso de los pacientes con enfermedad cardíaca y renal. Se trata de pacientes complejos, en los que la coexistencia de insuficiencia cardíaca y ERC se beneficia del abordaje terapéutico conjunto entre cardiólogos y nefrólogos. Esta consulta puede ser además utilizada para el despistaje de enfermedad cardiológica de cara al trasplante renal, con beneficios reflejados en una menor mortalidad25.
La creación de las consultas de onconefrología podría suponer, por tanto, un claro beneficio para los pacientes en los que el abordaje de la enfermedad neoplásica y renal concomitante resulta complejo. La posibilidad del manejo de casos concretos o de contactar de manera eficaz y rápida con el equipo referente de onconefrología facilitaría la toma de decisiones en esta población y es valorado positivamente por las otras especialidades implicadas.
Aspectos clave en la creación de la consulta de onconefrologíaCriterios de derivaciónEn la tabla 1 se recogen los principales motivos de derivación a la consulta de onconefrología. El DRA es frecuente en los pacientes con cáncer26,27. Según un estudio danés realizado en 2011, en el que se analizaron 37.267 pacientes incidentes con cáncer, el riesgo de presentar un DRA fue del 17,5% a un año y del 27% a 5 años, mucho mayor que el observado en la población general3.
Principales motivos de derivación a la consulta de onconefrología
| Deterioro de la función renal (previo, durante o posterior al diagnóstico del cáncer/tratamiento antineoplásico) |
| HTA de reciente diagnóstico/mal control de la tensión arterial en paciente con HTA previa durante un tratamiento antineoplásico |
| Alteraciones hidroelectrolíticas |
| Proteinuria/alteraciones sedimento |
| Valoración del paciente con diagnóstico de cáncer renal |
| Planificación de la estrategia quirúrgica y tratamientos neo/adyuvantes en pacientes con ERC y cáncer renal |
| Evaluación del riesgo de ERCT en pacientes que van a ser sometidos a nefrectomía |
| Cáncer y trasplante renal |
| Valoración de inclusión en lista de trasplante de pacientes con antecedente tumoral |
| Cribado tumoral en paciente con trasplante renal |
| Manejo de inmunosupresión en pacientes con trasplante renal |
| Enfermedad hematológica y afectación renal |
| Mieloma de células plasmáticas |
| Amiloidosis |
| GMSR |
| Leucemia linfática crónica |
| Linfoma |
| Valoración TRS en pacientes con ERC |
| Inicio de TRS en paciente con enfermedad neoplásica activa |
| Interrupción de la TRS en paciente con enfermedad neoplásica avanzada |
ERC: enfermedad renal crónica; ERCT: enfermedad renal crónica terminal; GMSR: gammapatía monoclonal de significado renal; HTA: hipertensión arterial; TRS: tratamiento renal sustitutivo.
El DRA supone un gran impacto negativo en la morbimortalidad de estos pacientes: aumenta el riesgo de presentar toxicidad por la quimioterapia, pone en riesgo la continuidad de tratamientos efectivos, limita la participación de los pacientes en ensayos clínicos y obliga a disminuir la dosis de fármacos muy eficaces o a buscar alternativas terapéuticas menos efectivas4.
Con relativa frecuencia, el deterioro de la función renal será independiente del proceso tumoral y del tratamiento oncológico, aunque en muchas ocasiones pueda estar favorecido por los mismos, al ser esta población más susceptible a factores funcionales o a la toxicidad renal de fármacos de empleo habitual, como los diuréticos o los antiinflamatorios no esteroideos.
Sin embargo, estos pacientes pueden presentar también un daño renal directamente relacionado con la enfermedad neoplásica o el tratamiento recibido7,28,29. El nefrólogo debe estar familiarizado con el diagnóstico y el manejo de entidades tales como el síndrome de lisis tumoral o la nefropatía por cilindros (riñón de mieloma), así como con las toxicidades derivadas del arsenal terapéutico oncológico en continuo desarrollo. Ello requiere una constante actualización que permita una precoz identificación y un tratamiento adecuado. En la tabla 2 se resumen las principales causas de DRA en los pacientes con cáncer.
Daño renal agudo en el paciente oncológico
| Prerrenal | Baja ingesta, vómitos, diarrea, sepsis, anemiaHipercalcemiaFármacos (diuréticos, AINE, IECA/ARA II, inhibidores de la calcineurina) |
| Posrenal u obstructivo | Tumores urinariosCompresión extrínseca por adenopatías, tumores abdominopélvicosFibrosis retroperitoneal (antecedente de radioterapia previa) |
| Parenquimatoso | Túbulo intersticialNTA tóxica por contraste intravenosoNTA tóxica por otros fármacos (AINE, aminoglucósidos, anfotericina B, aciclovir, inhibidores de la calcineurina)Toxicidad tubular por platino o por cristales (metotrexato)NTIA por fármacos (AINE, antibióticos, IBP, alopurinol…)Nefritis intersticial inmunomediada por inhibidores de los checkpointSíndrome de lisis tumoralNefropatía por cilindros (riñón de mieloma)Infiltración tumoralSíndrome de obstrucción sinusoidal (enfermedad venooclusiva hepática) |
| GlomerularGlomerulonefritis paraneoplásicaDaño podocitario por fármacos (ITK, anti-VEGF, inhibidores del mTor, bifosfonatos, interferón)Glomerulonefritis inmunomediada por inhibidores de los checkpointGMSR (enfermedad por depósito de proteína monoclonal, amiloidosis AL, glomerulonefritis con patrón membranoproliferativo) | |
| VascularMAT paraneoplásica, EICH, nefropatía por radiación, por fármacos (anti-VEGF, ITK, gemcitabina, mitomicina-C, inhibidores de los checkpoint) |
AINE: antiinflamatorios no esteroideos; ARA II: antagonistas de los receptores de angiotensina ii; IBP: inhibidores de la bomba de protones; EICH: enfermedad injerto contra huésped; IECA: inhibidores de la enzima convertidora de angiotensina; ITK: inhibidores de la tirosina cinasa; MAT: microangiopatía trombótica; NTA: necrosis tubular aguda; NTIA: nefropatía tubulointersticial aguda; VEGF: factor de crecimiento endotelial vascular.
No hay que olvidar que los pacientes oncológicos son frecuentemente sometidos a exploraciones radiológicas con contraste intravenoso. Esto, asociado a situaciones de riesgo como son la depleción de volumen o la presencia de comorbilidades como diabetes mellitus o ERC, los convierte en pacientes especialmente vulnerables al desarrollo de lesión renal aguda poscontraste, así como a la pérdida progresiva de la reserva renal funcional30. Podrían ser útiles para minimizar el riesgo de la nefrotoxicidad por contraste, el uso de contrastes isoosmolares y la implementación de protocolos de prevención. El objetivo es asegurar una adecuada hidratación intravenosa y la suspensión de medicaciones con repercusión en la situación de volemia o en los mecanismos de regulación del flujo intrarrenal (bloqueo del sistema renina-angiotensina-aldosterona, antiinflamatorios no esteroideos o fibratos).
Otro de los motivos más frecuentes de consulta es la presencia de ERC, que tiene una alta prevalencia en la población con enfermedad neoplásica14,17. La estimación del filtrado glomerular resulta de vital importancia para un ajuste correcto de la dosis de fármacos que pueden ser nefrotóxicos y para continuar o no una terapia antineoplásica que puede condicionar la supervivencia del paciente. Si en la población general la búsqueda del mejor método de estimación del filtrado glomerular sigue siendo motivo de discusión, en los pacientes con cáncer existe aún mayor controversia31,32. La utilización de CKD-EPI ajustada a la superficie corporal parece demostrar una buena correlación con el filtrado real33. Otros estudios evidencian que las ecuaciones basadas en la cistatina pueden ofrecer un beneficio respecto a las que se basan en la creatinina34. La medición exacta mediante técnicas de medicina nuclear en centros con experiencia (gammagrafía con tecnecio 99m-DTPA) es la técnica gold standard. En ocasiones será necesaria la realización de otras pruebas funcionales (dentro del estudio de una uropatía obstructiva) y/o una biopsia renal para llegar a un diagnóstico definitivo. Ello puede en ocasiones ser de suma importancia, por ejemplo, por las implicaciones en la continuidad de una terapia antineoplásica eficaz.
Los trastornos hidroelectrolíticos, frecuentes también, al igual que ocurre con el DRA, pueden ser debidos a causas similares a las acontecidas en la población general (hiponatremia asociada al uso de tiazidas o hipopotasemia por pérdidas digestivas) o pueden estar asociados a la enfermedad tumoral (por ejemplo, el síndrome de secreción inadecuada de hormona antidiurética paraneoplásico) o al tratamiento quimioterápico (por ejemplo, la hipomagnesemia en pacientes tratados con platinos o cetuximab)35. En la tabla 3 se recogen las principales alteraciones hidroelectrolíticas en el paciente oncológico.
Alteraciones hidroelectrolíticas en el paciente oncológico
| Hiponatremia | Pérdidas digestivas, tiazidas, fluidoterapia inadecuadaICC, cirrosis, DRAHipotiroidismo, insuficiencia suprarrenalSIADH paraneoplásico (carcinoma microcítico de pulmón, tumores de cabeza y cuello, tumores cerebrales…)SIADH farmacológico (ciclofosfamida, vincristina, vinblastina, cisplatino)SIADH por dolor, náuseas/vómitos |
| Hipopotasemia | Diuréticos, pérdidas digestivas, poliuria postobstructivaCisplatino, ifosfamida, anfotericina B, aminoglucósidosSecreción ectópica de ACTH (tumores carcinoides bronquiales, carcinoma microcítico y adenocarcinoma de pulmón) |
| Hiperpotasemia | DRAInsuficiencia suprarrenalSíndrome de lisis tumoralInhibidores de la calcineurina, AINE, trimetoprima-sulfametoxazol |
| Hipofosfatemia | Caquexia, malnutrición, déficit de vitamina DPlatinosSíndrome de Fanconi (mieloma múltiple)Osteomalacia oncogénica (condrosarcoma, osteoblastoma, hemangiopericitoma)ITK |
| Hipercalcemia | Secreción de PTHrp por el tumor (carcinoma epidermoide de pulmón, cérvix y esófago)Osteólisis (mieloma múltiple, metástasis óseas de carcinoma de mama y de pulmón)Producción de 1,25-OH-vitamina D (linfomas)Hipovolemia |
| Hipomagnesemia | Platinos, cetuximab, panitumumabDiuréticos del asa, inhibidores de la bomba de protones |
ACTH: hormona adenocorticotropa; AINE: antiinflamatorios no esteroideos; DRA: daño renal agudo; ICC: insuficiencia cardíaca congestiva; ITK: inhibidores de la tirosina cinasa; PTHrp: proteína relacionada con la hormona paratiroidea; SIADH: síndrome de secreción inadecuada de hormona antidiurética.
La evaluación del paciente con enfermedad hematológica que presenta deterioro de la función renal o proteinuria forma parte relevante de la actividad que se realiza en las consultas de onconefrología. En el mieloma múltiple, la afectación renal en forma de nefropatía por cilindros requiere la producción de grandes cantidades de paraproteína (considerándose esta como un evento definitorio de mieloma múltiple). Sin embargo, en las otras 2 formas más frecuentes de afectación renal asociada a disproteinemias (amiloidosis AL y enfermedad por depósito de inmunoglobulina monoclonal tipo Randall) son las propiedades físico-químicas de la paraproteína y no su cuantía las que determinan la lesión renal. Por lo tanto, es infrecuente que estos pacientes cumplan criterios hematológicos de tratamiento quimioterápico, cuyo inicio estará determinado por la afectación renal36. Para su evaluación se solicitarán electroforesis e inmunofijación en sangre y orina, así como cadenas ligeras libres en sangre. En la mayoría de los casos se requerirá un diagnóstico histológico mediante la realización de una biopsia renal (incluyendo técnicas de inmunofluorescencia y microscopia electrónica) para determinar el tipo de lesión. De esta manera puede valorarse la forma de expresión dentro del término gammapatía monoclonal de significado renal, su severidad y la necesidad de tratamiento del proceso hematológico.
En la tabla 4 se recogen aspectos particulares en la evaluación del paciente onconefrológico, a realizar en la consulta para una aproximación integral.
Evaluación del paciente en la consulta de onconefrología
| Historia clínica | Antecedentes personales y familiares de enfermedad renalComorbilidades que se asocian a enfermedad renal (HTA, DM2…)Toma de fármacos nefrotóxicosExploraciones recientes con contraste intravenosoTipo y estadificación del tumorLíneas de tratamiento antineoplásico recibidasEstado actual de la enfermedad neoplásica, tratamiento activo, respuesta al tratamiento, pronóstico |
| Exploración física | Cifras de tensión arterialEstado de volemia |
| Pruebas analíticas | Bioquímica, hemograma, gasometría venosa, sistemático y sedimento de orina. Cociente proteínas/creatinina en orinaEvaluación del filtrado glomerular (CKD-EPI ajustado a SC, medicina nuclear)Electroforesis e inmunofijación en sangre y orina, cadenas ligeras libres en sangre (pacientes con gammapatía monoclonal) |
| Pruebas de imagen | |
| Otras | AMPA, MAPAPruebas funcionales |
| Biopsia renal |
AMPA: automedida de la presión arterial; CKD-EPI: Chronic Kidney Disease Epidemiology Collaboration; DM2: diabetes mellitus tipo 2; HTA: hipertensión arterial; MAPA: medición ambulatoria de la presión arterial; SC: superficie corporal.
La valoración inicial del paciente se continuará con frecuencia de un seguimiento a medio-largo plazo, debido a la presencia de una ERC o a la persistencia de factores de riesgo para desarrollarla. En otras ocasiones, el paciente será dado de alta tras la resolución del proceso agudo en caso de no existir relación con el cáncer ni con el tratamiento oncológico.
Abordaje multidisciplinarUn abordaje multidisciplinar permite ofrecer a los pacientes los mejores resultados clínicos con un impacto positivo en supervivencia y calidad de vida37. El cuidado multidisciplinar requiere una relación proactiva y bidireccional entre distintos especialistas9,38.
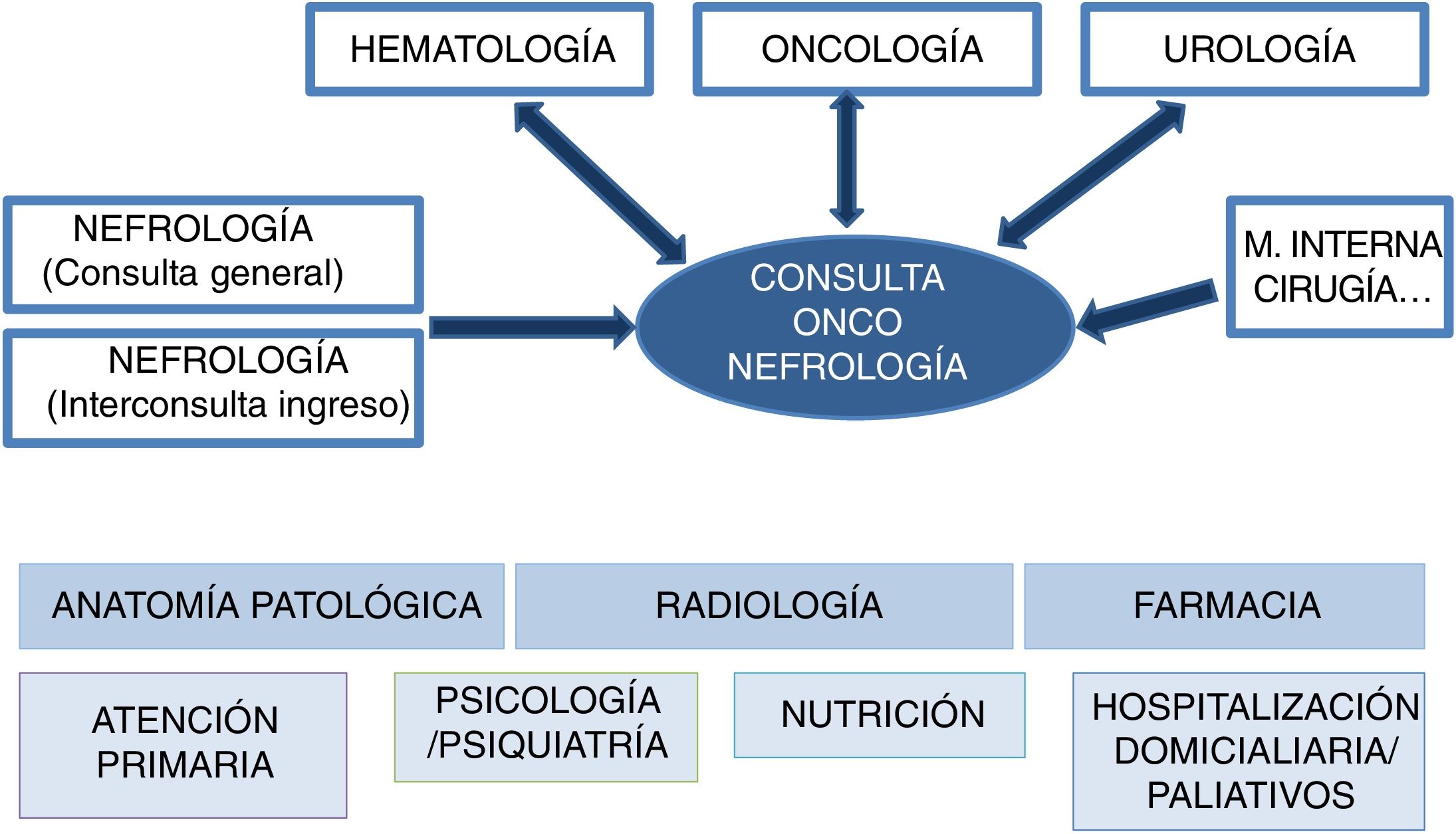
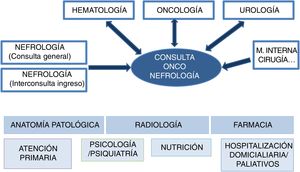
En el caso de la onconefrología, nefrólogos, oncólogos, hematólogos y urólogos serán el núcleo del equipo colaborativo. La participación de otros especialistas como atención primaria, cuidados paliativos, psicólogos/psiquiatras y nutricionistas resultará también fundamental en la atención y seguimiento de los pacientes en función de las necesidades. Por último, en la aproximación diagnóstica y terapéutica juegan también un papel relevante los especialistas de anatomía patológica, radiología y farmacia (fig. 1).
Relación con oncologíaLa comunicación con los oncólogos deberá ser permanente y estrecha, con el objetivo de facilitar la toma de decisiones y el seguimiento del paciente.
Las sesiones clínicas con participación multidisciplinar resultan de gran utilidad para valorar la relación riesgo-beneficio de terapias potencialmente nefrotóxicas en pacientes de alto riesgo para desarrollarla o con enfermedad renal previa. En este sentido, se deben establecer estrategias para evitar o minimizar la nefrotoxicidad asociada a fármacos y otros agentes (por ejemplo, el uso repetido y sin distancia temporal adecuada de contrastes radiológicos intravenosos).
Relación con urologíaLa colaboración entre nefrología y urología resulta fundamental para garantizar un adecuado manejo de los pacientes con cáncer renal que pueden presentar tanto insuficiencia renal aguda como ERC. El nefrólogo debe estar familiarizado con la biología del cáncer renal, su tratamiento y sus complicaciones, e implicado en el cuidado longitudinal de estos pacientes39,40. Su participación debe ser activa en la valoración preoperatoria en el momento de decidir una nefrectomía parcial o radical. Debe tenerse en cuenta si existe ERC previa o factores de riesgo para desarrollarla. El objetivo en estos pacientes es la preservación del máximo parénquima renal, sin renunciar a la curación con la resección tumoral, siempre que sea posible. Los pacientes con enfermedad metastásica, expuestos a terapias sistémicas con potencial toxicidad renal (anti-VEGF, inhibidores del mTor, inhibidores de los checkpoint), también se benefician de esta colaboración entre ambas especialidades.
No es infrecuente, además, que pacientes con otros tumores de la vía urinaria desarrollen enfermedad renal aguda o crónica como consecuencia de las intervenciones urológicas a las que se vean sometidos (derivaciones urinarias, cistectomías, etc.)41. Son también, por tanto, candidatos a un abordaje conjunto entre urología y nefrología.
Relación con hematologíaDe manera característica, la oncohematología constituye un área de especial importancia, dado que en muchos casos la afectación renal puede facilitar el diagnóstico de la enfermedad hematológica y con ello la indicación de su tratamiento. La evolución de la enfermedad renal se utiliza como indicador de respuesta a la terapia y un marcador de recidiva de la enfermedad.
En los últimos años ha cobrado una gran importancia el término de gammapatía monoclonal de significado renal. Se refiere a aquellos casos que no cumplen criterios de mieloma múltiple, siendo la afectación hematológica compatible con una gammapatía monoclonal de significado incierto, pero que asocian una importante morbilidad debido a la severidad de las lesiones renales ocasionadas por la paraproteína. En estos casos es crucial una colaboración estrecha entre nefrología y hematología, ya que el pronóstico renal y vital del paciente va a depender de un diagnóstico precoz y de la instauración de un adecuado tratamiento quimioterápico (aunque no existan criterios hematológicos de tratamiento), dirigido a suprimir la producción de la paraproteína patogénica36.
Relación con el equipo de trasplante renalOtro escenario en el que la valoración multidisciplinar resulta clave es en el trasplante renal. El desarrollo del proyecto PROMETEO en 2016, promovido por la Sociedad Española de Trasplante, manifiesta la importancia de este hecho42. La participación del oncólogo a la hora de incluir en lista de trasplante a un paciente con antecedente tumoral nos ofrecerá información precisa acerca del riesgo de recidiva del tumor. Ello nos permitirá decidir el momento adecuado para su inclusión, así como establecer el plan de inmunosupresión más beneficioso para el paciente. Dicha colaboración también será necesaria en el manejo del paciente trasplantado renal que desarrolla un tumor a lo largo de su evolución postrasplante43. Debe realizarse una evaluación pormenorizada de las opciones terapéuticas, teniendo en cuenta la supervivencia global del paciente, del injerto y su calidad de vida.
Cáncer y tratamiento renal sustitutivoEl abordaje multidisciplinar con participación del nefrólogo es también esencial en la toma de decisiones en terapia renal sustitutiva. Cobra especial relevancia el momento tanto de iniciar la diálisis en un paciente con una enfermedad neoplásica activa como el de interrumpirla. El proceso de toma de decisiones en onconefrología debe individualizarse e incorporar las trayectorias de ambas enfermedades, la oncológica y la renal. En este sentido, puede ser útil el modelo de toma de decisiones compartida44. Se evalúan los aspectos clínicos y el pronóstico general, y se integran en el contexto personal del paciente, con el objetivo de lograr una decisión informada. Para ello es importante una adecuada evaluación del pronóstico, utilizando escalas de estado funcional, nivel nutricional, comorbilidad y fragilidad, así como una comunicación empática y eficaz del mismo. Esto permitirá abordar las distintas opciones terapéuticas, con sus pros y contras, con una cuidadosa exploración de los objetivos personales del paciente. De esta manera, se podrá formular un plan de tratamiento informado de acuerdo con sus preferencias personales.
Onconefrología en EspañaLa creación del grupo de trabajo de Onconefrología (ONCONEFRO) en 2018 en el marco de la Sociedad Española de Nefrología45 supuso el reconocimiento de la importancia creciente de esta subespecialidad en España, con el compromiso de la puesta en marcha de proyectos y estudios en este ámbito.
Entre diciembre de 2018 y enero de 2019, el grupo ONCONEFRO llevó a cabo una encuesta para conocer la situación actual al respecto en nuestro país.
Se recibieron 168 respuestas y se identificaron 9 centros donde ya se disponía de consulta monográfica a fecha de enero de 2019: Hospital Clínico Universitario (Valencia), Hospital Universitario Virgen del Rocío (Sevilla), Hospital Universitario Virgen Macarena (Sevilla), Hospital Universitario Doce de Octubre (Madrid), Hospital Clínic (Barcelona), Hospital Universitario Nuestra Señora de Candelaria (Tenerife), Hospital Sant Joan de Déu (Barcelona), Clínica Universitaria (Navarra) y Hospital General (Alicante). Los 2 primeros centros son los de mayor tiempo de instauración. Otros 9 centros manifestaron asimismo su proyecto de puesta en marcha próxima de la consulta.
A pesar de que un 80% de los encuestados opinaba que la onconefrología es una subespecialidad en auge que requiere de la participación activa del nefrólogo, solo un 42% pensaba que era posible materializar el proyecto de la consulta monográfica por motivos logísticos y de plantilla.
Aunque se tiene constancia de la puesta marcha de estas consultas en otros países, no existen aún datos preliminares acerca de resultados. En Estados Unidos, centros como el MD Anderson Cancer Center de Houston, el Memorial Sloan Kettering Cancer de Nueva York y el Dana-Farber Cancer Institute de Boston adoptan cada vez más un modelo más multidisciplinar para la atención de la enfermedad neoplásica46.
Experiencia acumulada de la consulta monográfica de onconefrología en 2 centros españolesEn nuestro país, decidimos analizar los datos iniciales de una serie de 199 pacientes de 2 hospitales con consulta monográfica de onconefrología, valorados desde su puesta en marcha hasta octubre de 2019 (Hospital Universitario Virgen Macarena de Sevilla, 161 pacientes, apertura en octubre de 2017, y Hospital Universitario Doce de Octubre de Madrid, 38 pacientes, apertura en junio de 2018), con criterios de inclusión similares en ambos centros.
En las tablas 5 y 6 se describen las características basales de nuestra serie de pacientes, así como las características de la afectación renal.
Características principales de los pacientes derivados a la consulta de onconefrología
| Total pacientes (N=199) | |
|---|---|
| Edad (años), Md (RI) | 68 (59-76) |
| Sexo masculino, n (%) | 129 (65) |
| ERC previa, n (%) | 131 (66) |
| Tumor sólido/hematológico, n (%) | 112 (56)/87 (44) |
| Enfermedad metastásica, n (%) | 60 (35) |
| Tiempo desde el diagnóstico oncológico hasta la derivación a la consulta (meses), Md (RI) | 20 (8-50) |
| Línea de tratamiento, n (%) | |
| Primera línea | 69 (70) |
| Segunda línea | 18 (18) |
| Tercera línea o más | 11 (12) |
| Antineoplásico en el momento de la derivación, n (%) | |
| Quimioterapia | 48 (48) |
| Hormonoterapia | 8 (8) |
| Inmunomoduladora | 7 (7) |
| Terapias dirigidasb | 26 (26) |
| Inhibidores de checkpointc | 11 (11) |
| CAR T-cell | 1 (1) |
CAR T-cell: receptor de antígeno quimérico de células T; ERC: enfermedad renal crónica; Md: mediana; RI: rango intercuartílico.
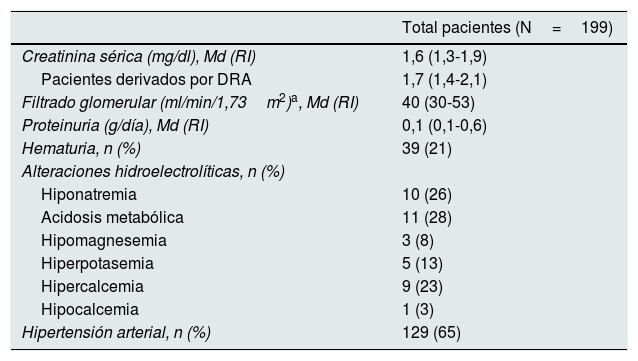
Características de la afectación renal
| Total pacientes (N=199) | |
|---|---|
| Creatinina sérica (mg/dl), Md (RI) | 1,6 (1,3-1,9) |
| Pacientes derivados por DRA | 1,7 (1,4-2,1) |
| Filtrado glomerular (ml/min/1,73m2)a, Md (RI) | 40 (30-53) |
| Proteinuria (g/día), Md (RI) | 0,1 (0,1-0,6) |
| Hematuria, n (%) | 39 (21) |
| Alteraciones hidroelectrolíticas, n (%) | |
| Hiponatremia | 10 (26) |
| Acidosis metabólica | 11 (28) |
| Hipomagnesemia | 3 (8) |
| Hiperpotasemia | 5 (13) |
| Hipercalcemia | 9 (23) |
| Hipocalcemia | 1 (3) |
| Hipertensión arterial, n (%) | 129 (65) |
DRA: daño renal agudo; Md: mediana; RI: rango intercuartílico.
Se aprecian algunas diferencias entre la población con tumor sólido (n=112) y aquella con enfermedad hematológica (n=87). Por ejemplo, respecto al motivo de derivación, la ERC fue el motivo principal en la población hematológica (67%), seguido del DRA (24%). En el caso de la población con tumor sólido, los porcentajes fueron similares (42% ERC vs. 43% DRA).
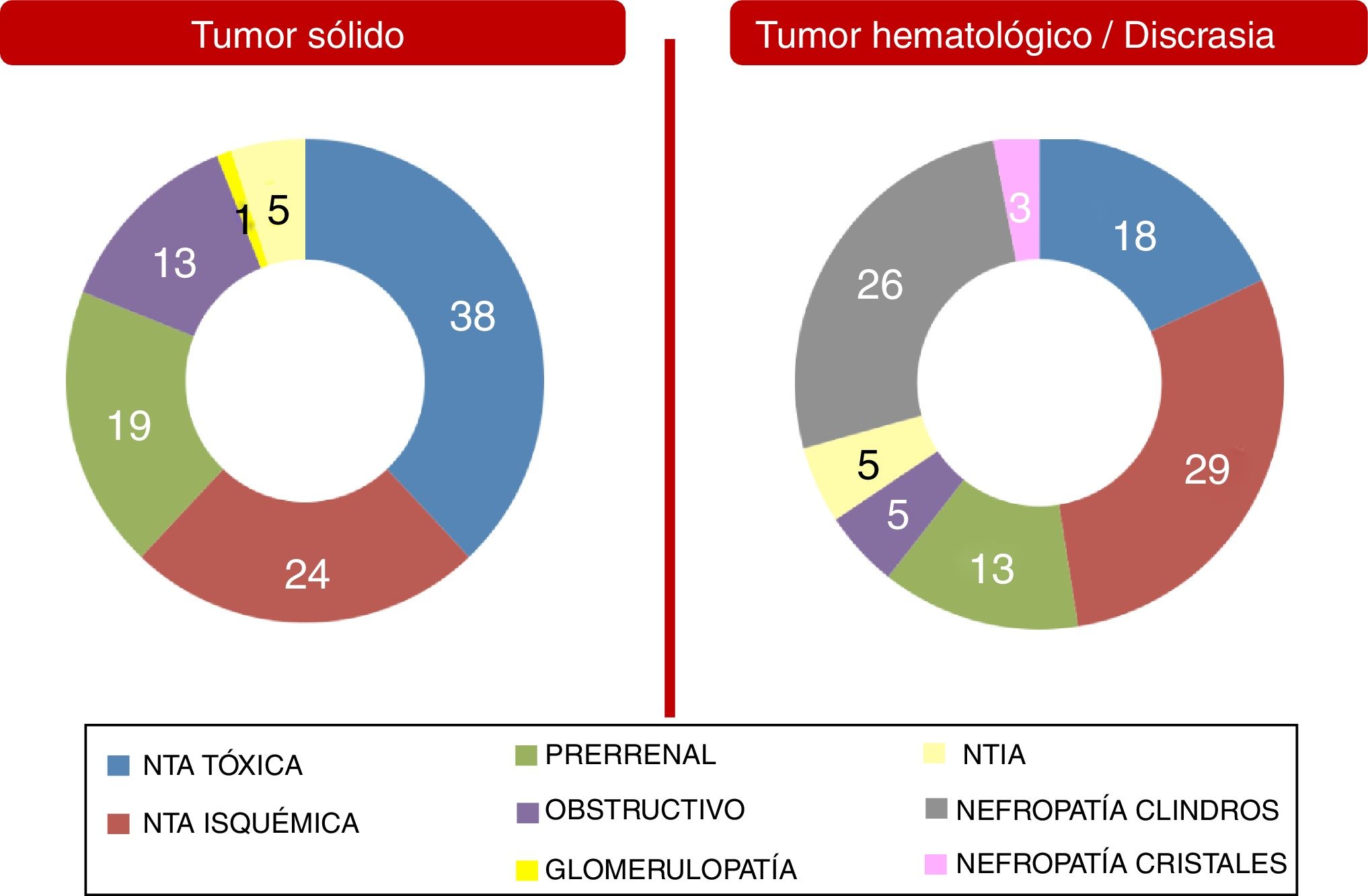
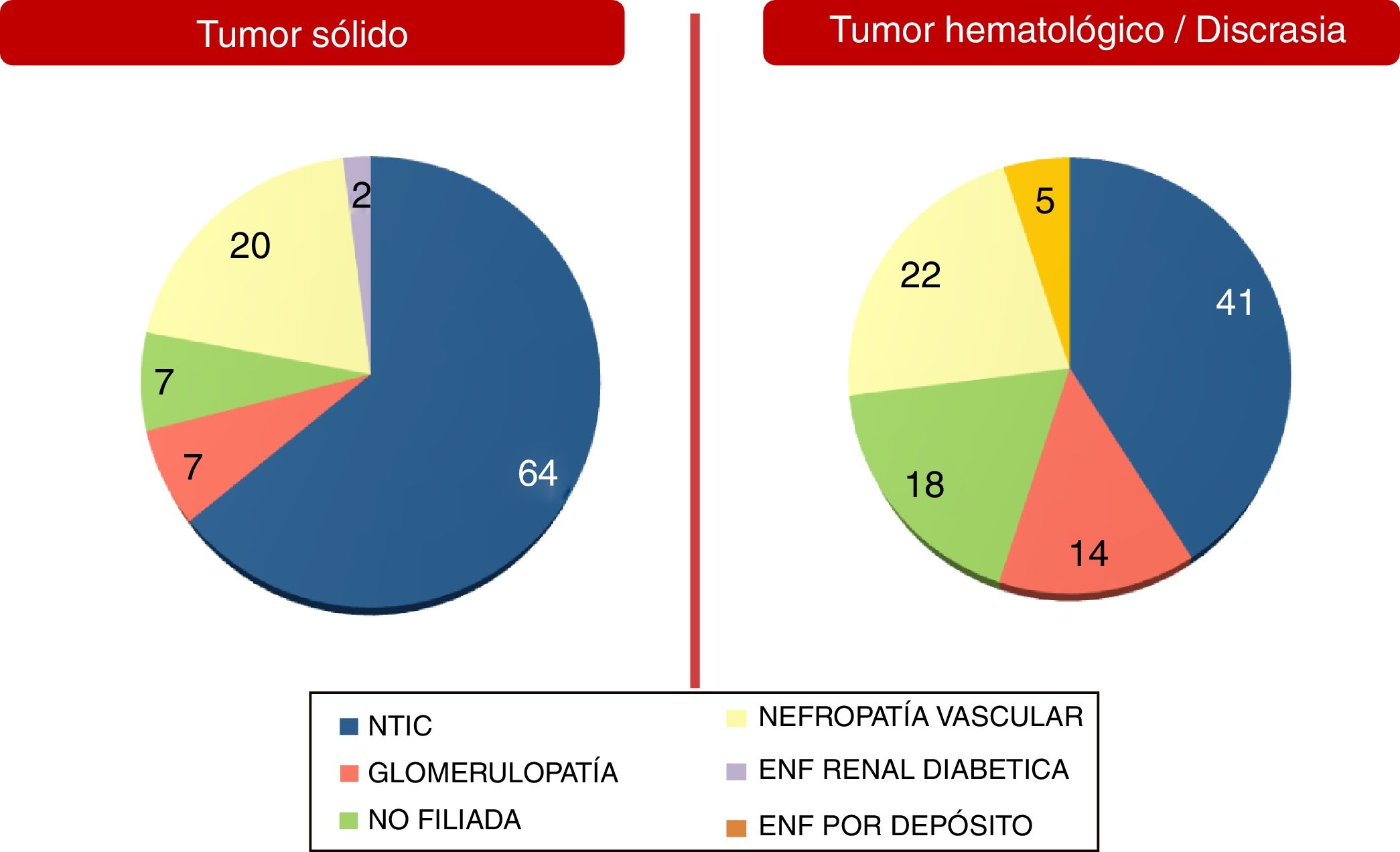
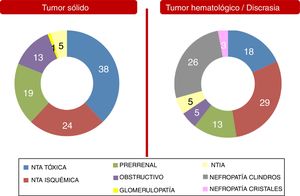
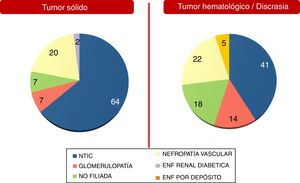
Estas diferencias entre ambos grupos poblacionales se mostraron más significativas al analizar por separado las etiologías de DRA y ERC. Se recogen en las figuras 2 y 3. Es destacable que la etiología de ERC por causa no filiada aumenta en el caso de la población con enfermedad hematológica (18% de los casos), probablemente por imposibilidad de realización de biopsia renal (comorbilidades, alto riesgo, edad más avanzada en muchos pacientes con gammapatía monoclonal de significado renal, riñones ecográficamente no aptos, etc.).
En relación con el tratamiento, cabe destacar que en el momento de la derivación del paciente a la consulta de onconefrología, la mitad de ellos (49%) se encontraban en tratamiento antineoplásico activo. De estos, 38 precisaron la suspensión temporal de dicho tratamiento por su asociación con la afectación renal, 10 requirieron la suspensión permanente sin reinicio de ninguna otra terapia y a 13 se les realizó cambio a otra línea de tratamiento. La mejoría parcial o completa de la afección renal en aquellos pacientes en los que se realizó alguna intervención por parte del nefrólogo se produjo en 86 pacientes (86%). Ello refleja la importancia de la valoración nefrológica en estos pacientes.
De los 199 pacientes, 25 fueron sometidos a la realización de una biopsia renal (13%). Los diagnósticos anatomopatológicos principales fueron: gammapatía monoclonal de significado renal en 7 pacientes (28%), enfermedad glomerular paraneoplásica en 6 (24%), nefritis intersticial aguda en 4 (16%) y tubulopatía por cisplatino en uno. En 2 casos no se llegó a aclarar el diagnóstico a pesar de la biopsia y en los 5 restantes (20%) el diagnóstico histológico no estaba relacionado con la enfermedad neoplásica/discrasia sanguínea o su tratamiento.
Desde un punto de vista clínico y de manera global, se estableció la posible relación entre la enfermedad renal y la neoplásica en las distintas poblaciones con tumor sólido y hematológico (tabla 7). Se consideró que no existía relación entre la enfermedad renal y la neoplásica en un 38% de los pacientes con tumor sólido y un 36% de los pacientes con enfermedad hematológica. La afección renal se relacionó más con la hematológica propiamente dicha en un 37% de los casos y con el tratamiento antineoplásico (bien médico, bien quirúrgico) en un 40% de la población con tumor sólido. Hubo un mayor porcentaje de relación sin aclarar en la población con tumor/discrasia hematológica (19%).
Finalmente, en torno a un 20% de los pacientes derivados a la consulta fallecieron durante su periodo de seguimiento. La causa principal de exitus fue la propia enfermedad neoplásica en el 80% de los casos. Las infecciones, la enfermedad cardiovascular o la insuficiencia renal crónica terminal correspondieron al 6, 6 y 3% del resto de las causas, respectivamente.
Con base en nuestra experiencia, no existen dificultades iniciales para la puesta en marcha de este tipo de consulta. Es importante la presentación del proyecto a las otras especialidades implicadas, para resaltar el valor del trabajo colaborativo y la presentación del «onconefrólogo» referente.
De manera general, la experiencia propia de los centros con la consulta es satisfactoria, tanto por parte de las otras especialidades implicadas como por los propios pacientes en sí.
Requisitos y recomendaciones para la apertura de una consulta monográfica de onconefrologíaGracias a la encuesta ONCONEFRO y la experiencia de los centros con consulta ya instaurada, se recogen algunos requisitos identificados en la tabla 8. Es necesaria un área poblacional suficiente para la puesta en marcha de la consulta, situada entre los 250.000 y los 500.000 habitantes, concordante con otras publicaciones anteriores38. Esto permitiría un flujo anual aproximado de 150 pacientes.
Requisitos recomendados para la apertura de una consulta de onconefrología
| Área poblacional hospitalaria de referencia: 250.000-500.000 habitantes |
| Presencia hospitalaria de las especialidades de oncología y hematología, con formación de grupos de trabajo multidisciplinares |
| Acceso común al sistema informático y datos compartidos de los pacientes |
| Flujo anual de pacientes recomendado (al menos 150 pacientes) |
| Tiempo disponible recomendado para las revisiones: 15-20min |
| Posibilidad de coordinar las distintas visitas hospitalarias del paciente |
| Posibilidad de respuesta precoz a las interconsultas preferentes/urgentes |
A medida que el volumen de la consulta aumente, puede ser necesario desdoblar esta en pacientes con tumores sólidos y con discrasias hematológicas, con el objetivo de facilitar la labor diaria.
Los centros con consulta ya disponible recomiendan, de igual manera, el contacto directo con las especialidades de hematología, oncología y urología. La creación de grupos de trabajo multidisciplinar para el abordaje de casos concretos es fundamental para agilizar el manejo y la toma de decisiones. Al tratarse de pacientes que pueden desarrollar un trastorno agudo en cualquier momento, se recomienda estructurar la agenda, de manera que se asegure la posibilidad de asistencia urgente en estos casos.
Es deseable que sean al menos 2 las personas responsables del programa de onconefrología en cada unidad. Esto permitiría repartir la atención clínica y las tareas. Los onconefrólogos deben mantener una actualización formativa constante, así como estar familiarizados con la terminología oncológica utilizada, lo que puede resultar una dificultad en nuestro día a día, debido a la elevada carga asistencial existente en nuestras unidades de nefrología. El contacto directo con el oncólogo es fundamental para conocer el pronóstico de la enfermedad neoplásica, lo cual también puede resultar una ardua tarea, dada la subespecialización por aparatos de la propia oncología.
Al iniciar la consulta, sería aconsejable comenzar un registro adecuado de la información a nivel local. La unificación de la recogida de datos a nivel nacional permitiría estudios sobre incidencia y prevalencia de estas complicaciones, clarificar las lesiones renales asociadas a terapias oncológicas, conocer su evolución y manejo, así como identificar áreas de mejora en la atención a estos pacientes.
Cobra vital importancia la realización de reuniones formativas multidisciplinares, que permitan la elaboración de circuitos y protocolos. Es deseable una formación «nefrológica» hacia las otras especialidades implicadas, que permita la utilización de un lenguaje común y la identificación precoz de enfermedad renal. La evaluación de los resultados obtenidos debe constituirse también como un objetivo prioritario.
Consideraciones finalesLa creación de consultas monográficas de onconefrología resulta en una mejor atención a los pacientes con enfermedad neoplásica que desarrollan cualquier alteración renal aguda o crónica, así como trastornos hidroelectrolíticos. Para su puesta en marcha son precisos, sin embargo, algunos requisitos y recomendaciones. La adaptación individualizada en cada centro será fundamental para el éxito y la continuidad de la consulta.
El abordaje multidisciplinar entre las distintas especialidades implicadas debe llevarse a cabo con el objetivo de optimizar la toma de decisiones y realizar un adecuado manejo del paciente de manera global. El pronóstico, la calidad de vida, las preferencias personales y los valores del propio paciente deben tenerse en cuenta durante todo el proceso, especialmente en las decisiones referentes a la terapia renal sustitutiva. Dentro de nuestra propia especialidad es necesario, en muchas ocasiones, un abordaje conjunto con el equipo de trasplante renal y de diálisis.
En la serie analizada de nuestras consultas se aprecia de manera global un alto porcentaje de pacientes con ERC y DRA como motivos de consulta.
Hemos observado un bajo número de biopsias renales realizadas. Como posible justificación a este hecho, en algunos casos se ha considerado innecesaria por ausencia de conexión entre la enfermedad tumoral y la renal justificada clínicamente, y por otro lado, en un porcentaje no desdeñable de pacientes, por imposibilidad técnica (comorbilidades o riñones no aptos).
Son manifiestas las diferencias evidenciadas en las etiologías de DRA y ERC entre los 2 grupos poblacionales de pacientes. En el caso de la población con tumor sólido, existe una mayor relación entre la enfermedad renal y las terapias antineoplásicas utilizadas (médicas o quirúrgicas), y en el caso de la población con discrasia, la afectación renal se relaciona más con la enfermedad hematológica propiamente dicha.
Es destacable la confirmación de que un alto porcentaje de pacientes con enfermedad renal asociada a neoplasia o discrasia sanguínea se beneficia de la valoración por nefrología en la consulta, permitiendo optimizar el tratamiento antineoplásico y mejorar la afección renal.
La creación de bases de datos unificadas y registros puede resultar útil para el análisis de los datos clínicos en la práctica clínica diaria, así como para la realización de estudios prospectivos multicéntricos. Las consultas de onconefrología deben ser el punto de partida para la consecución de este objetivo a nivel nacional y para el desarrollo creciente de esta subespecialidad en auge.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Agradecer a todos los coordinadores del grupo español de Onconefrología su apoyo a la realización de este trabajo (Patricia García, Isidro Torregrosa, Luis F Quintana y Eduardo Gutiérrez). Asimismo, nos gustaría también agradecer su colaboración en la encuesta realizada acerca de la consulta de Onco-nefrología, a Miguel Ángel Solís y Carmen Ramos, del Hospital Clínico Universitario de Valencia, a Virginia Cabello, del Hospital Universitario Virgen del Rocío, a Nuria García, de la Clínica Universitaria de Navarra, a Pedro Arango, del Hospital Sant Joan de Déu y a Miguel Perdiguero, del Hospital Clínico de o. de Alicante.