La enfermedad renal crónica (ERC) será la segunda causa de muerte en España en el año 2100. El Registro Español de Enfermos Renales (REER) recopila información sobre la incidencia, la prevalencia y la mortalidad de todos los pacientes en terapia renal sustitutiva (TRS) en España.
MétodosLos datos del REER proceden de los remitidos por las comunidades autónomas (CCAA) y las ciudades autónomas, así como los aportados por la Organización Nacional de Trasplantes. Se ha calculado la incidencia y la prevalencia de la TRS (atendiendo a la población española conforme a los datos anuales del Instituto Nacional de Estadística) y la mortalidad de los pacientes en TRS en nuestro país durante el periodo 2013-2022.
ResultadosLa tasa de incidencia de TRS creció un 21% entre 2013 y 2019, estabilizándose desde entonces y siendo de 152,2 personas por millón (pmp) en 2022, correspondiendo un 77,8% a hemodiálisis (HD), un 16,7% a diálisis peritoneal (DP) y un 5,5% a trasplante renal. La diabetes es la primera causa de ERC con necesidad de TRS (21,8%), seguida de miscelánea (21,6%). La tasa de incidencia de TRS fue dos veces mayor en hombres que en mujeres, con grandes diferencias entre CCAA (1,93 veces en hombres y 2,55 en mujeres entre aquellas con mayor y menor incidencia).
La tasa de prevalencia de TRS del año 2022 fue de 1.391,1pmp, con un ascenso progresivo en la última década, principalmente a expensas de un aumento en la población trasplantada renal (765,0pmp, 55,0%).
En el año 2022 se realizaron 3.404 trasplantes renales en España (71,7pmp), que mantiene el liderazgo mundial. La donación procede principalmente de la muerte encefálica (51,5%), seguida de la donación en asistolia (37%).
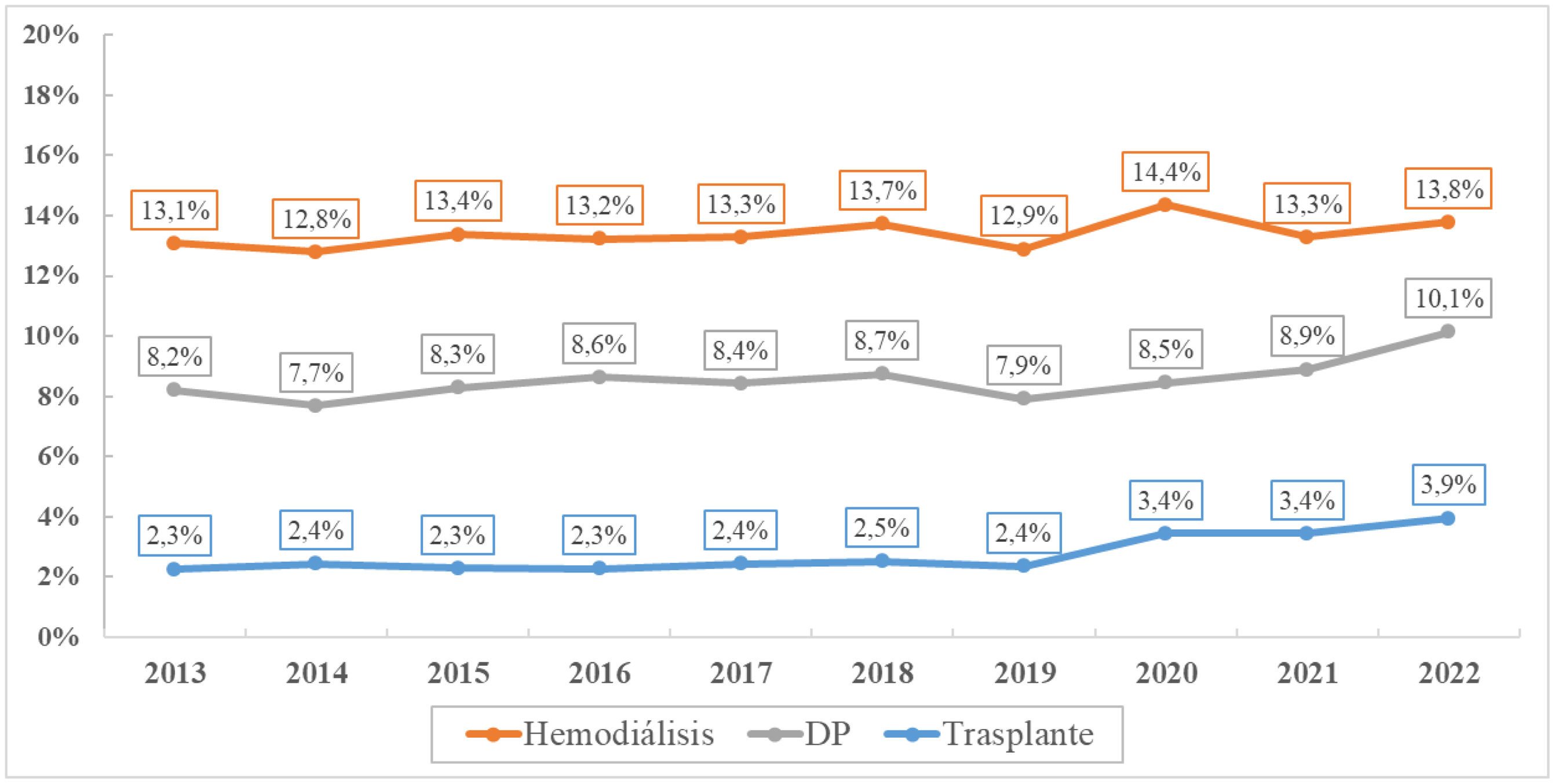
La mortalidad global de los pacientes en TRS fue del 8,4% anual (13,8% en HD, 10,1% en DP y 3,9% en trasplante).
ConclusionesA pesar de una cierta estabilización en los últimos años, la incidencia y la prevalencia de pacientes en TRS siguen en aumento en España, aunque con una amplia variabilidad entre CCAA. Es preceptivo adoptar medidas adicionales que permitan homogeneizar y optimizar la atención sanitaria a la ERC.
Chronic kidney disease (CKD) will be the second leading cause of death in Spain by 2100. The Spanish Renal Disease Registry (REER) records the incidence, prevalence and mortality of all patients requiring renal replacement therapy (RRT) in Spain.
MethodsData are provided by Spanish autonomous regions and cities and the Organización Nacional de Trasplantes. Incidence and prevalence rates of RRT have been calculated (considering the Spanish population according to annual data from the Instituto Nacional de Estadística), as well as mortality of patients on RRT in our country during the period 2013-2022.
ResultsThe incidence rate of RRT increased by 21% from 2013 to 2019, and stabilized thereafter, with a value of 152.2 cases per million population (pmp) in 2022, of which 77.8% were on haemodialysis (HD), 16.7% on peritoneal dialysis (PD) and 5.5% received a preemptive kidney transplant. Diabetes was the leading cause of CKD requiring RRT (21.8%), followed by other causes (21.6%). The incidence rate of RRT was 2-fold higher in men than in women, with large regional differences (1.93-fold for men and 2.55-fold for women in regions with the highest and lowest incidence rates).
The prevalence rate of RRT was 1,391.1pmp in 2022, showing a progressive increase over the last decade, mainly at the expense of an increase in the transplant population (765.0pmp, 55.0%).
In 2022, 3,404 kidney transplants were performed in Spain (71.7pmp), which situates it as a world leader. The most frequent donor type was the donor after the neurological determination of death (51.5%), followed by the donor after the circulatory determination of death (37%).
The overall annual mortality of RRT patients was 8.4% (13.8% for HD, 10.1% for PD and 3.9% for transplantation).
ConclusionsAlthough it has stabilized somewhat in recent years, the incidence and prevalence of RRT continues to rise in Spain. Additional measures must be adopted to harmonize and optimize kidney health care.
La enfermedad renal crónica será la segunda causa de muerte en el año 21001. El Registro Español de Enfermos Renales (REER) es una fuente de datos esencial para conocer la incidencia, la prevalencia y la mortalidad de los pacientes en terapia renal sustitutiva (TRS) en España. El REER es resultado de un esfuerzo colaborativo entre los Registros de Enfermedad Renal de las Comunidades Autónomas y las Ciudades Autónomas, la Sociedad Española de Nefrología (S.E.N) y la Organización Nacional de Trasplantes (ONT), quien se encarga de la gestión y el análisis de datos. Además de colaborar con la European Renal Association (ERA) y el registro United States Renal Data System (USRDS), la memoria del REER se presenta en el congreso anual de la S.E.N. desde 1996 y se pretende que, de ahora en adelante, se publique anualmente en la revista NEFROLOGÍA.
En los últimos años la nefrología ha avanzado en el manejo de la enfermedad renal crónica (ERC), con un amplio desarrollo y aprobación de nuevos tratamientos y técnicas diagnósticas2. A pesar de ello, cada año un mayor número de personas precisan TRS tanto en España como a nivel global3. En 2022, la incidencia de TRS en España fue la decimoquinta más alta de Europa (sobre un total de 34)3,4. En cuanto a la prevalencia de TRS en España, esta se situó en la tercera más alta de Europa (sobre un total de 29 países europeos que remiten sus datos)3,4. En comparación con Estados Unidos, la incidencia y la prevalencia fueron sensiblemente mejores en España: 410 pacientes por millón de población (pmp) y 2.436pmp, respectivamente5.
El objetivo del presente informe es actualizar los datos de prevalencia, incidencia y mortalidad de los pacientes en TRS en España relativos al año 2022, comparando evolutivamente la situación de los últimos 10años.
MétodosFuentes de datos y población a estudioEl presente estudio recogió los datos de los pacientes en TRS notificados al REER entre los años 2013 y 2022 y que proceden de los remitidos por las comunidades autónomas (CCAA) y ciudades autónomas de España a la ONT. Los datos de los pacientes portadores de un injerto renal se complementaron con los datos del sistema de información CORE de la ONT. La población de referencia nacional y de cada comunidad autónoma a 1 de enero del año en estudio se obtuvo del Instituto Nacional de Estadística6.
Los datos de incidencia y prevalencia fueron calculados sobre los datos agregados (las CCAA remiten estos datos de forma individualizada o agregada), mientras que el análisis de supervivencia se realizó sobre los datos de pacientes individuales de los registros autonómicos que los facilitaron (todas las CCAA, a excepción de Baleares, Ceuta y Melilla, lo que supone una cobertura poblacional del 97%).
VariablesSe recogieron datos epidemiológicos (edad, sexo), etiología de la enfermedad renal primaria (ERP), tipo de TRS y mortalidad. En cuanto a la etiología, la definición y la agrupación han ido variando a lo largo de la existencia del REER, adoptándose desde 2022 la propuesta por el registro de la ERA4, que incluye los grupos de enfermedad glomerular, tubulointersticial, diabetes mellitus, enfermedad vascular renal, otras enfermedades sistémicas, nefropatías familiares/hereditarias y miscelánea (entre las que se incluyen las no filiadas). Previamente, la clasificación utilizada agrupaba a los pacientes en las siguientes categorías7: glomerulonefritis, pielonefritis/intersticial, enfermedad poliquística, diabetes mellitus, vascular, sistémica, hereditaria, otras y no filiadas.
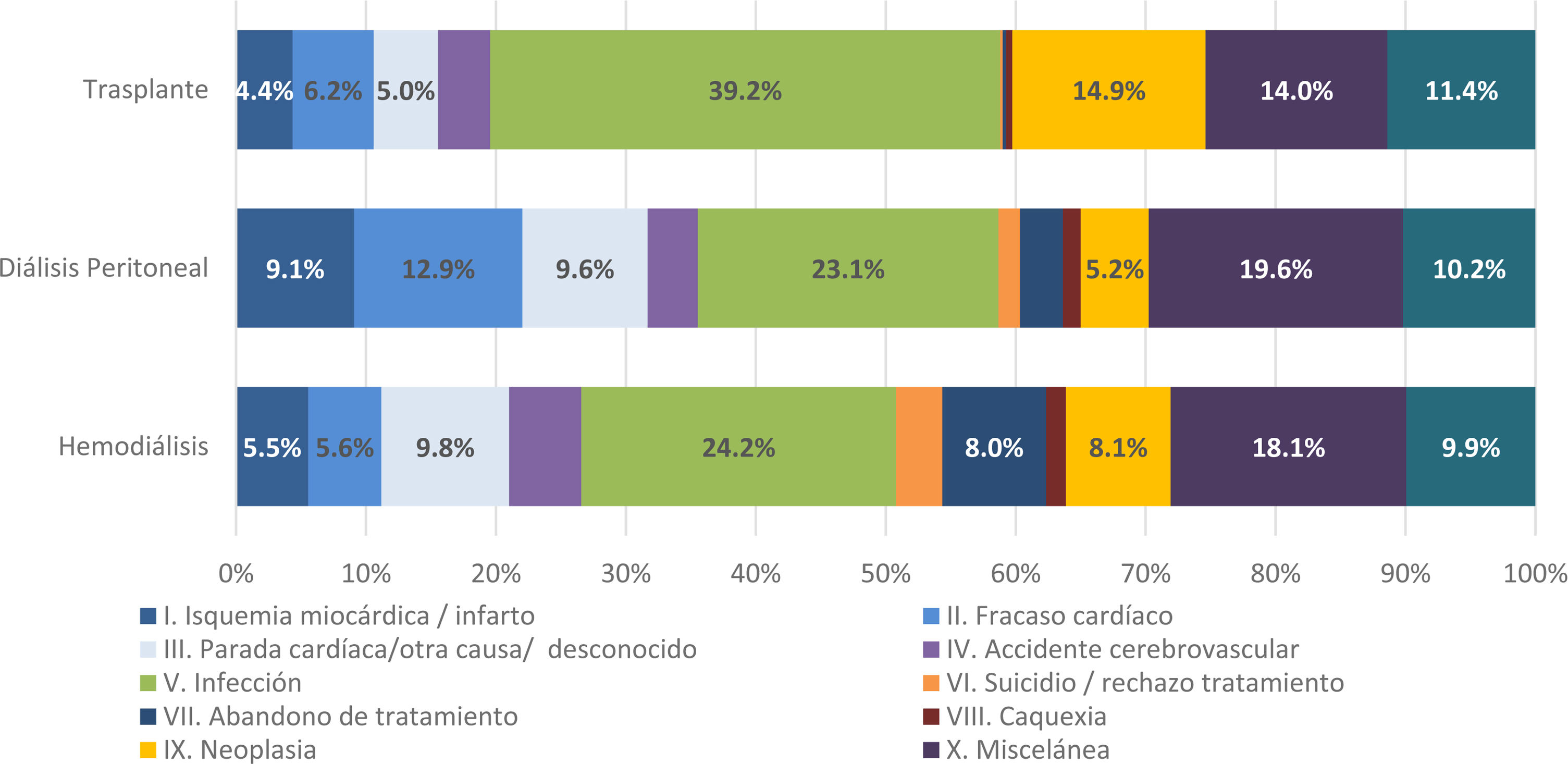
Las causas de muerte también han sufrido variaciones en su codificación. Hasta 2022 se agrupaban las causas de fallecimiento en origen cardíaco, vascular, muerte súbita, infecciosa, cáncer, hepática, gastrointestinal, psicológica/social, accidente, otras y no filiada. Desde 2022 se ha adoptado también la clasificación de la ERA-EDTA4, que las clasifica en: I.Isquemia miocárdica/infarto. II.Fracaso cardíaco. III.Parada cardíaca/otra causa/desconocido. IV.Accidente cerebrovascular. V.Infección. VI.Suicidio/rechazo de tratamiento. VII.Abandono de tratamiento. VIII.Caquexia. IX.Neoplasia. X.Miscelánea. XI.Desconocido/no disponible.
Métodos estadísticosLos datos se expresan como números absolutos y frecuencias (porcentajes), así como en tasas por millón de población (pmp). La incidencia se refiere al número de pacientes que inician TRS durante cada uno de los años del periodo de estudio, y la prevalencia, al número total de pacientes vivos en TRS a 31 de diciembre de cada año. La tasa de trasplante renal se calcula como el número de trasplantes realizados en un año sobre la población de referencia.
Para el cálculo de la supervivencia se han utilizado los datos de pacientes individuales de aquellas CCAA que los han facilitado y han autorizado su uso. Para poder fusionar todos los datos, previamente se ha realizado un proceso de depuración y conversión de los datos hasta obtener un formato común que permitiera su integración, con las variables y la información requeridas para el análisis. Se han incluido los pacientes incidentes desde al año 2004 de los que se dispone de información, mayores de 15años y con un seguimiento superior a 3meses. Se han excluido del análisis los pacientes con trasplante renal como primer TRS y los pacientes procedentes de otros registros. Se ha usado el método de Kaplan-Meier para calcular la probabilidad de supervivencia no ajustada y el test de LogRank para comparar las curvas de supervivencia entre grupos. Se ha desarrollado un modelo de Cox de riesgos proporcionales para estudiar los potenciales factores predictores de supervivencia utilizando como variables de ajuste la edad, el sexo, la modalidad de TRS, la nefropatía diabética como ERP y haber recibido al menos un trasplante. El fallecimiento ha sido considerado como evento, censurando la recuperación de la función renal, el traslado a otro registro y la pérdida de seguimiento.
De manera análoga, para el análisis de la supervivencia del primer trasplante se ha utilizado la misma metodología, censurando los pacientes que se pierden en el seguimiento y considerando como evento la muerte del paciente, el retrasplante o el fallo del injerto.
Para la comparación de los datos de supervivencia (global y del trasplante) entre España y el global de la ERA se ha utilizado el informe que facilita la ERA de forma individual a los registros participantes4. La metodología utilizada por este análisis es la aplicada por la ERA4.
El análisis se ha realizado por intención de tratamiento. El software utilizado ha sido Microsoft Excel 365 (v. 2404®) y SPSS v.25.0 para Windows.
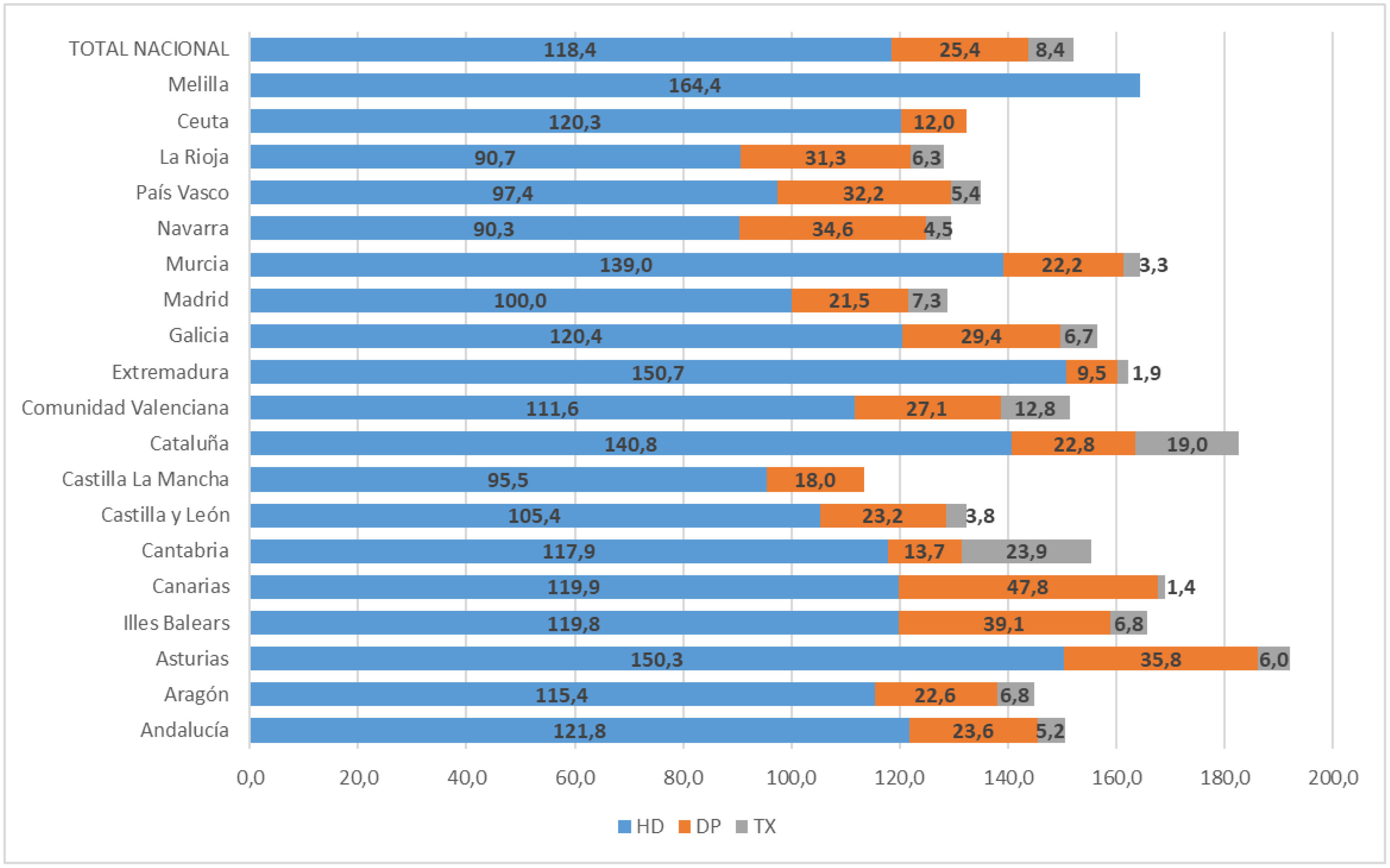
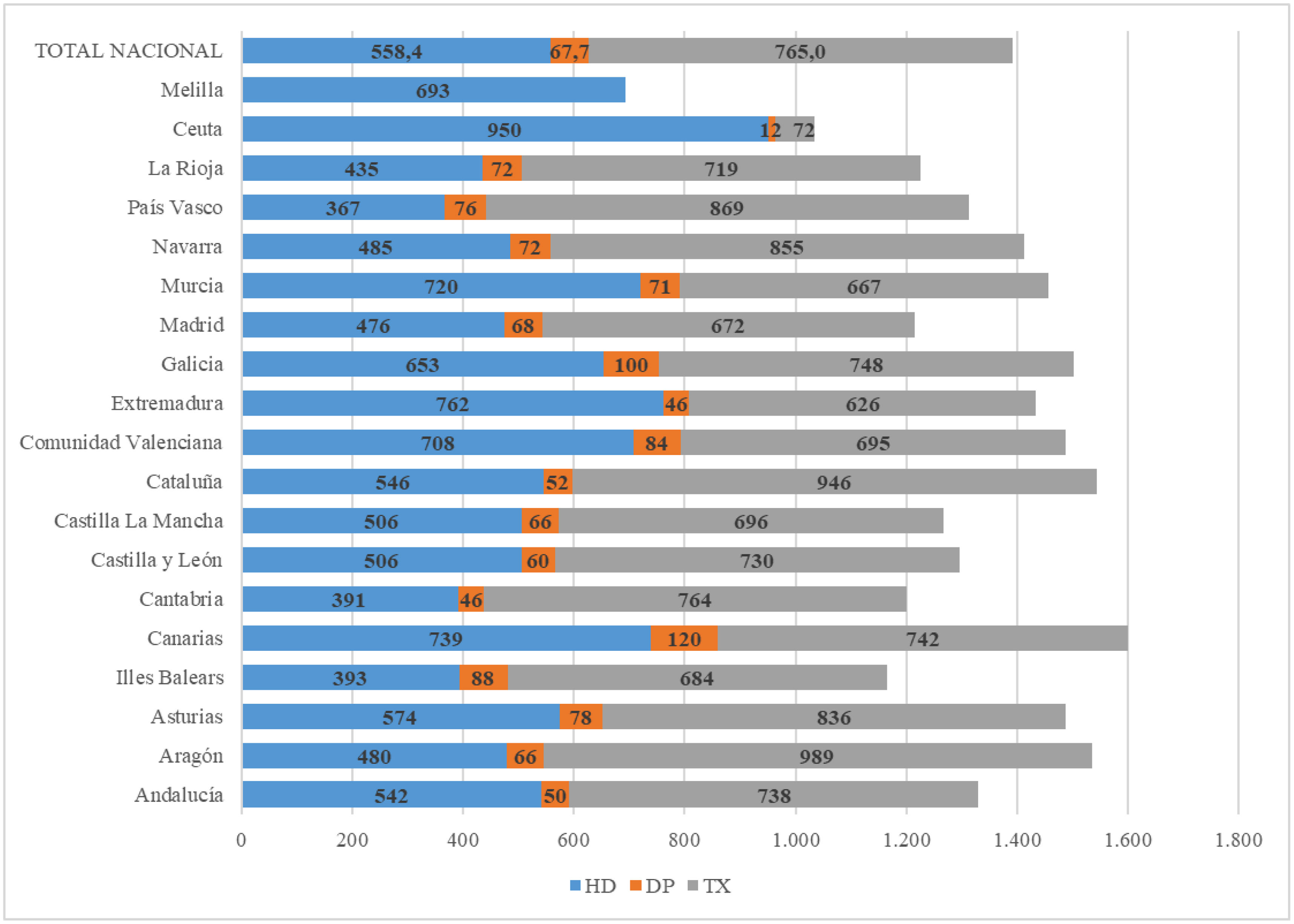
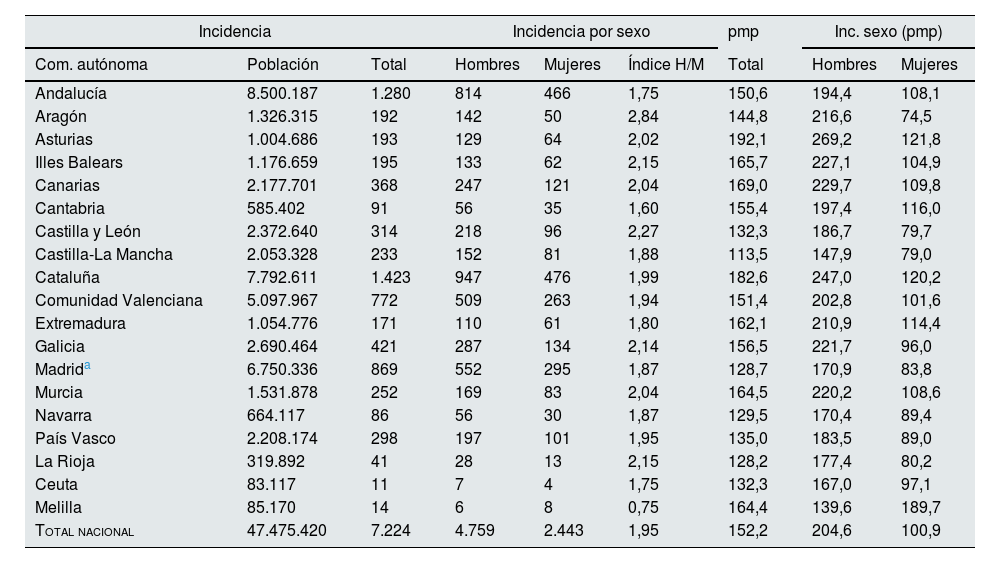
ResultadosIncidenciaDurante el año 2022, 7.224 pacientes iniciaron TRS, de los que 4.759 (66%) eran varones. La incidencia fue de 152,2pmp (204,6pmp en varones y 100,9pmp en mujeres) (tabla 1). En cuanto a la modalidad de TRS, 117,9pmp (78%) iniciaron TRS con hemodiálisis (HD), 24,7pmp (17%) con diálisis peritoneal (DP) y 7,7pmp (5%) recibieron un trasplante renal anticipado. En la figura 1 se muestra la incidencia por CCAA según la modalidad de TRS, objetivándose diferencias entre las regiones. Concretamente, la tasa de incidencia de TRS en fue 1,93 veces mayor en hombres entre Asturias y Melilla, y 2,55 mayor en mujeres entre Melilla y Aragón.
Incidencia de TRS global y por sexo en España y sus comunidades autónomas en 2022
| Incidencia | Incidencia por sexo | pmp | Inc. sexo (pmp) | |||||
|---|---|---|---|---|---|---|---|---|
| Com. autónoma | Población | Total | Hombres | Mujeres | Índice H/M | Total | Hombres | Mujeres |
| Andalucía | 8.500.187 | 1.280 | 814 | 466 | 1,75 | 150,6 | 194,4 | 108,1 |
| Aragón | 1.326.315 | 192 | 142 | 50 | 2,84 | 144,8 | 216,6 | 74,5 |
| Asturias | 1.004.686 | 193 | 129 | 64 | 2,02 | 192,1 | 269,2 | 121,8 |
| Illes Balears | 1.176.659 | 195 | 133 | 62 | 2,15 | 165,7 | 227,1 | 104,9 |
| Canarias | 2.177.701 | 368 | 247 | 121 | 2,04 | 169,0 | 229,7 | 109,8 |
| Cantabria | 585.402 | 91 | 56 | 35 | 1,60 | 155,4 | 197,4 | 116,0 |
| Castilla y León | 2.372.640 | 314 | 218 | 96 | 2,27 | 132,3 | 186,7 | 79,7 |
| Castilla-La Mancha | 2.053.328 | 233 | 152 | 81 | 1,88 | 113,5 | 147,9 | 79,0 |
| Cataluña | 7.792.611 | 1.423 | 947 | 476 | 1,99 | 182,6 | 247,0 | 120,2 |
| Comunidad Valenciana | 5.097.967 | 772 | 509 | 263 | 1,94 | 151,4 | 202,8 | 101,6 |
| Extremadura | 1.054.776 | 171 | 110 | 61 | 1,80 | 162,1 | 210,9 | 114,4 |
| Galicia | 2.690.464 | 421 | 287 | 134 | 2,14 | 156,5 | 221,7 | 96,0 |
| Madrida | 6.750.336 | 869 | 552 | 295 | 1,87 | 128,7 | 170,9 | 83,8 |
| Murcia | 1.531.878 | 252 | 169 | 83 | 2,04 | 164,5 | 220,2 | 108,6 |
| Navarra | 664.117 | 86 | 56 | 30 | 1,87 | 129,5 | 170,4 | 89,4 |
| País Vasco | 2.208.174 | 298 | 197 | 101 | 1,95 | 135,0 | 183,5 | 89,0 |
| La Rioja | 319.892 | 41 | 28 | 13 | 2,15 | 128,2 | 177,4 | 80,2 |
| Ceuta | 83.117 | 11 | 7 | 4 | 1,75 | 132,3 | 167,0 | 97,1 |
| Melilla | 85.170 | 14 | 6 | 8 | 0,75 | 164,4 | 139,6 | 189,7 |
| Total nacional | 47.475.420 | 7.224 | 4.759 | 2.443 | 1,95 | 152,2 | 204,6 | 100,9 |
pmp: personas por millón de población; TRS: terapia renal sustitutiva.
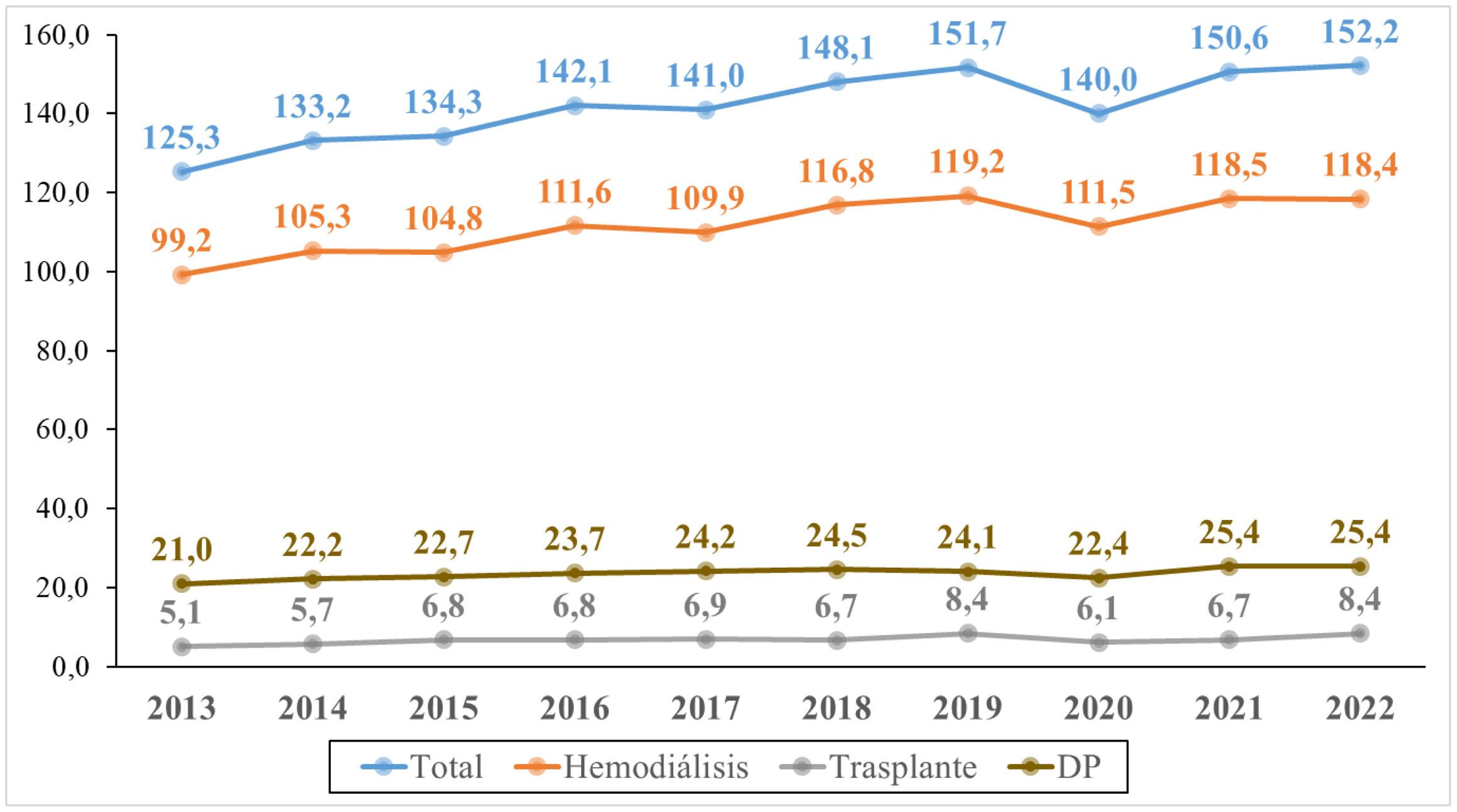
La tasa de incidencia de TRS creció un 21% entre 2013 y 2019 (151,7 vs 125,4pmp), estabilizándose desde entonces, con una depresión en 2020 probablemente relacionada con la pandemia de COVID-19 (fig. 2). En la década de estudio, la HD como TRS de inicio aumentó un 19,4%, la DP un 20,9% y el trasplante anticipado un 64,7% (fig. 2).
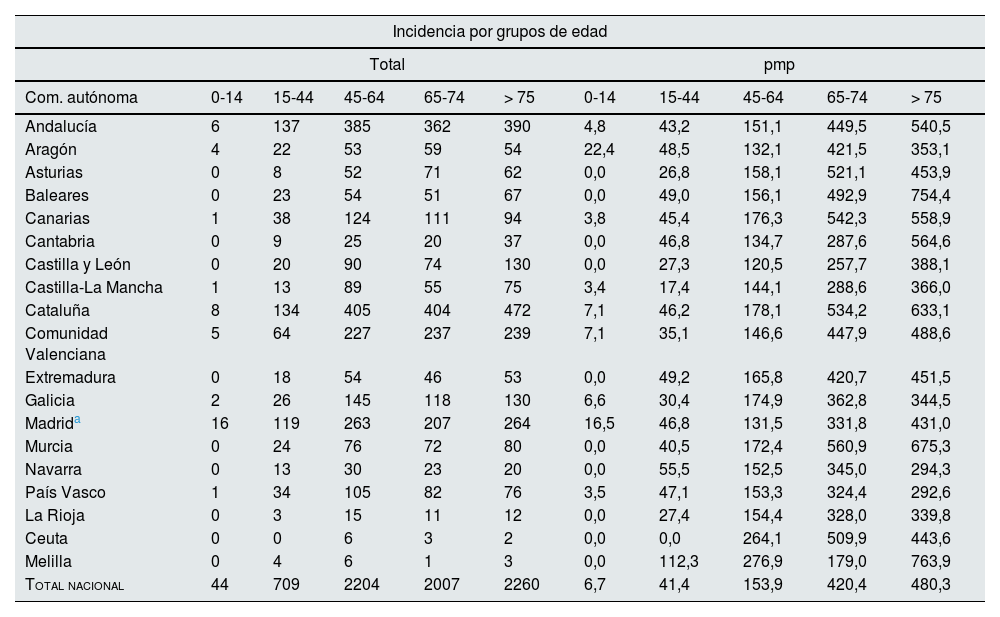
El grupo de edad con mayor incidencia fue el de mayores de 74años (480,3pmp), seguido del de 65-74años (420,4pmp), 45-64años (153,9pmp), 15-44años (41,4pmp) y menores de 15años (6,7pmp). En la tabla 2 se muestra la incidencia en los grupos de edad en cada una de las CCAA.
Incidencia de TRS por grupos de edad en los diferentes territorios en 2022
| Incidencia por grupos de edad | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| Total | pmp | |||||||||
| Com. autónoma | 0-14 | 15-44 | 45-64 | 65-74 | > 75 | 0-14 | 15-44 | 45-64 | 65-74 | > 75 |
| Andalucía | 6 | 137 | 385 | 362 | 390 | 4,8 | 43,2 | 151,1 | 449,5 | 540,5 |
| Aragón | 4 | 22 | 53 | 59 | 54 | 22,4 | 48,5 | 132,1 | 421,5 | 353,1 |
| Asturias | 0 | 8 | 52 | 71 | 62 | 0,0 | 26,8 | 158,1 | 521,1 | 453,9 |
| Baleares | 0 | 23 | 54 | 51 | 67 | 0,0 | 49,0 | 156,1 | 492,9 | 754,4 |
| Canarias | 1 | 38 | 124 | 111 | 94 | 3,8 | 45,4 | 176,3 | 542,3 | 558,9 |
| Cantabria | 0 | 9 | 25 | 20 | 37 | 0,0 | 46,8 | 134,7 | 287,6 | 564,6 |
| Castilla y León | 0 | 20 | 90 | 74 | 130 | 0,0 | 27,3 | 120,5 | 257,7 | 388,1 |
| Castilla-La Mancha | 1 | 13 | 89 | 55 | 75 | 3,4 | 17,4 | 144,1 | 288,6 | 366,0 |
| Cataluña | 8 | 134 | 405 | 404 | 472 | 7,1 | 46,2 | 178,1 | 534,2 | 633,1 |
| Comunidad Valenciana | 5 | 64 | 227 | 237 | 239 | 7,1 | 35,1 | 146,6 | 447,9 | 488,6 |
| Extremadura | 0 | 18 | 54 | 46 | 53 | 0,0 | 49,2 | 165,8 | 420,7 | 451,5 |
| Galicia | 2 | 26 | 145 | 118 | 130 | 6,6 | 30,4 | 174,9 | 362,8 | 344,5 |
| Madrida | 16 | 119 | 263 | 207 | 264 | 16,5 | 46,8 | 131,5 | 331,8 | 431,0 |
| Murcia | 0 | 24 | 76 | 72 | 80 | 0,0 | 40,5 | 172,4 | 560,9 | 675,3 |
| Navarra | 0 | 13 | 30 | 23 | 20 | 0,0 | 55,5 | 152,5 | 345,0 | 294,3 |
| País Vasco | 1 | 34 | 105 | 82 | 76 | 3,5 | 47,1 | 153,3 | 324,4 | 292,6 |
| La Rioja | 0 | 3 | 15 | 11 | 12 | 0,0 | 27,4 | 154,4 | 328,0 | 339,8 |
| Ceuta | 0 | 0 | 6 | 3 | 2 | 0,0 | 0,0 | 264,1 | 509,9 | 443,6 |
| Melilla | 0 | 4 | 6 | 1 | 3 | 0,0 | 112,3 | 276,9 | 179,0 | 763,9 |
| Total nacional | 44 | 709 | 2204 | 2007 | 2260 | 6,7 | 41,4 | 153,9 | 420,4 | 480,3 |
pmp: personas por millón de población; TRS: terapia renal sustitutiva.
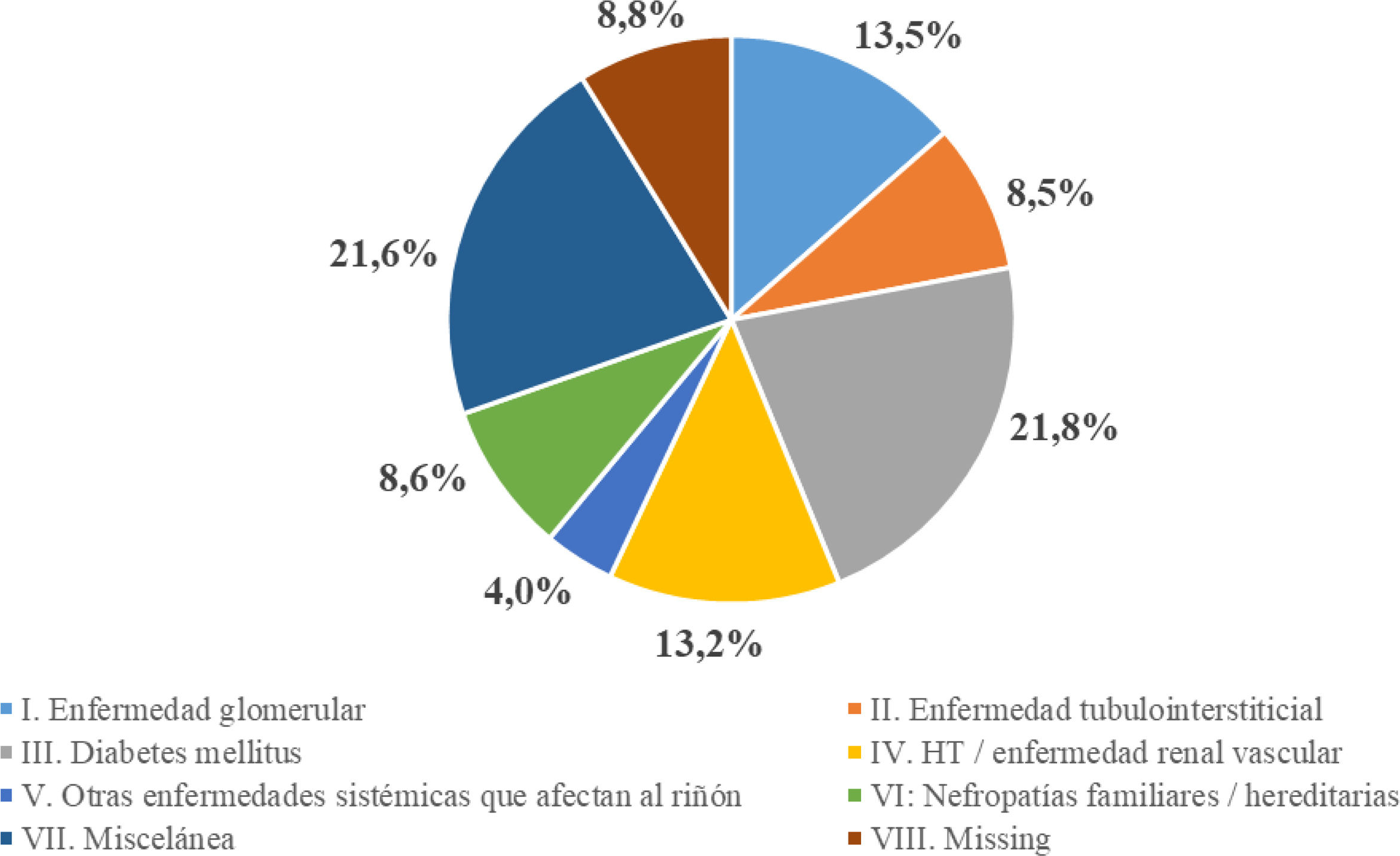
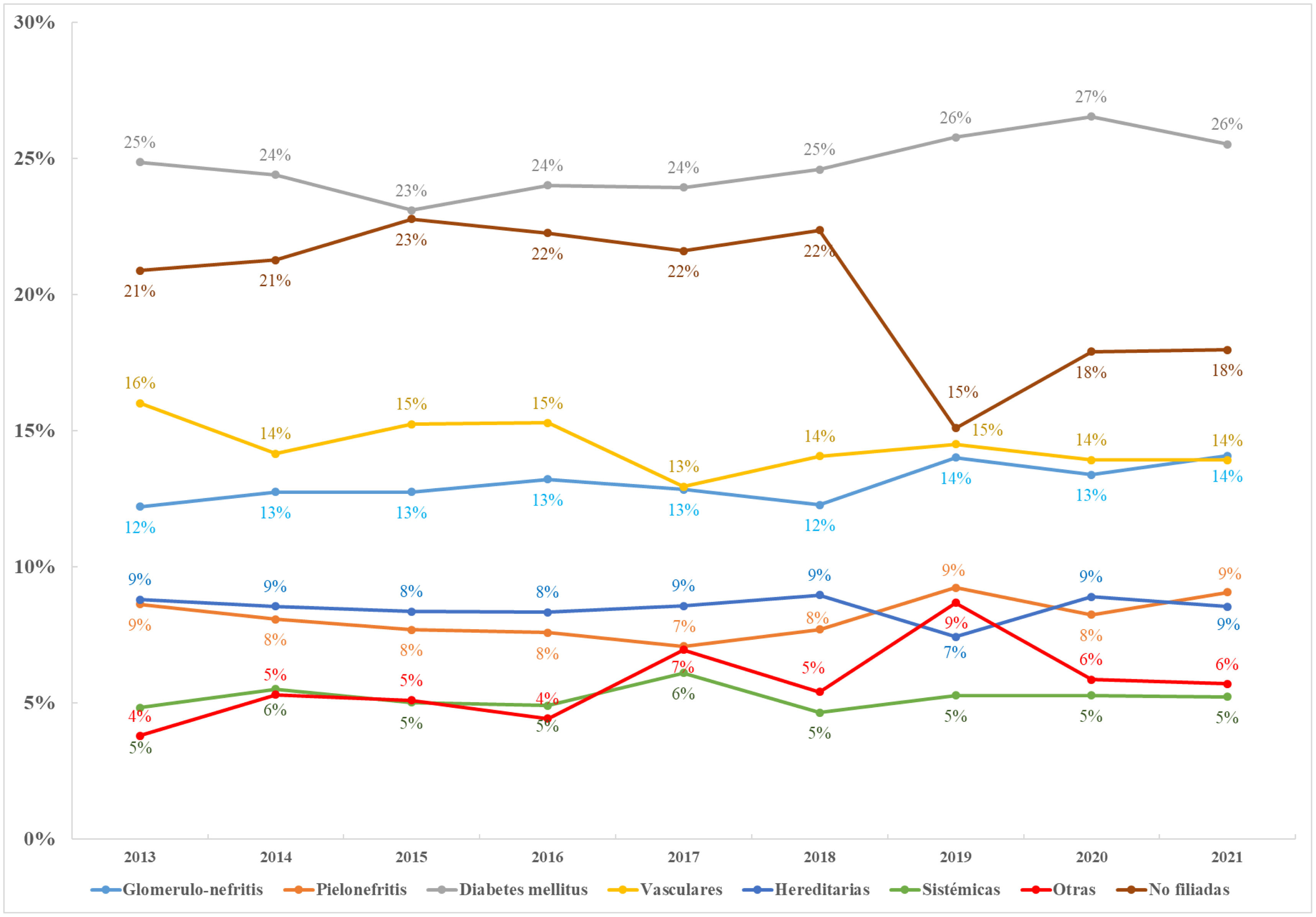
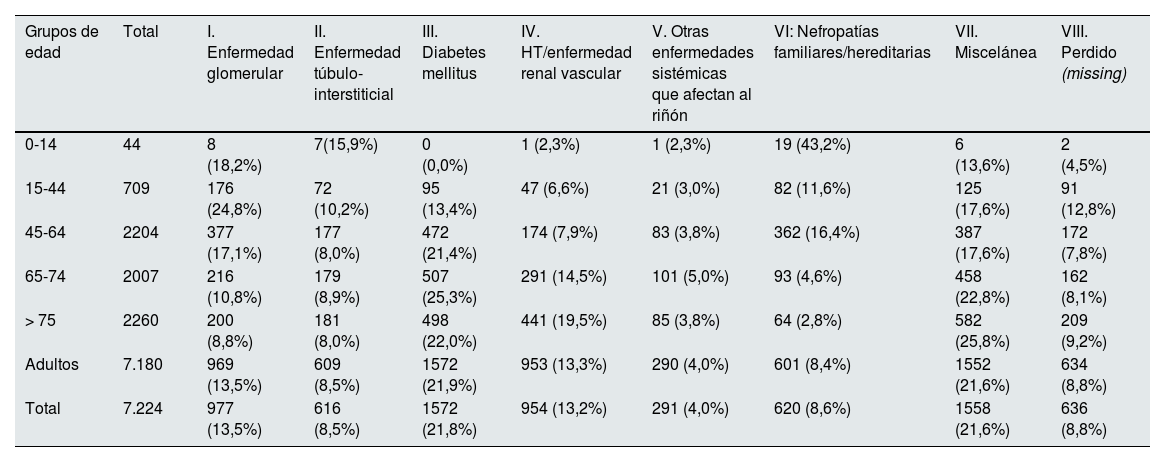
En cuanto a la etiología de la ERP, la más frecuente fue la diabetes mellitus (21,8%), seguida de miscelánea (21,6%) y la enfermedad glomerular (13,5%) (fig. 3). La etiología de la ERC muestra diferencias según el grupo de edad, como se muestra en la tabla 3. La evolución de la etiología en el periodo 2013-2021 (previo al cambio en la nomenclatura de la etiología) muestra que la diabetes ha sido la causa más frecuente de ERP durante todo el periodo de estudio en los pacientes incidentes, seguida de la no filiada, con una tendencia en ambas a la baja en los datos de 2022 (figs. 3 y 4).
Distribución de la etiología de la ERC en el TRS incidente en los diferentes grupos de edad en 2022
| Grupos de edad | Total | I. Enfermedad glomerular | II. Enfermedad túbulo-interstiticial | III. Diabetes mellitus | IV. HT/enfermedad renal vascular | V. Otras enfermedades sistémicas que afectan al riñón | VI: Nefropatías familiares/hereditarias | VII. Miscelánea | VIII. Perdido (missing) |
|---|---|---|---|---|---|---|---|---|---|
| 0-14 | 44 | 8 (18,2%) | 7(15,9%) | 0 (0,0%) | 1 (2,3%) | 1 (2,3%) | 19 (43,2%) | 6 (13,6%) | 2 (4,5%) |
| 15-44 | 709 | 176 (24,8%) | 72 (10,2%) | 95 (13,4%) | 47 (6,6%) | 21 (3,0%) | 82 (11,6%) | 125 (17,6%) | 91 (12,8%) |
| 45-64 | 2204 | 377 (17,1%) | 177 (8,0%) | 472 (21,4%) | 174 (7,9%) | 83 (3,8%) | 362 (16,4%) | 387 (17,6%) | 172 (7,8%) |
| 65-74 | 2007 | 216 (10,8%) | 179 (8,9%) | 507 (25,3%) | 291 (14,5%) | 101 (5,0%) | 93 (4,6%) | 458 (22,8%) | 162 (8,1%) |
| > 75 | 2260 | 200 (8,8%) | 181 (8,0%) | 498 (22,0%) | 441 (19,5%) | 85 (3,8%) | 64 (2,8%) | 582 (25,8%) | 209 (9,2%) |
| Adultos | 7.180 | 969 (13,5%) | 609 (8,5%) | 1572 (21,9%) | 953 (13,3%) | 290 (4,0%) | 601 (8,4%) | 1552 (21,6%) | 634 (8,8%) |
| Total | 7.224 | 977 (13,5%) | 616 (8,5%) | 1572 (21,8%) | 954 (13,2%) | 291 (4,0%) | 620 (8,6%) | 1558 (21,6%) | 636 (8,8%) |
ERC: enfermedad renal crónica; HT: hipertensión; TRS: terapia renal sustitutiva.
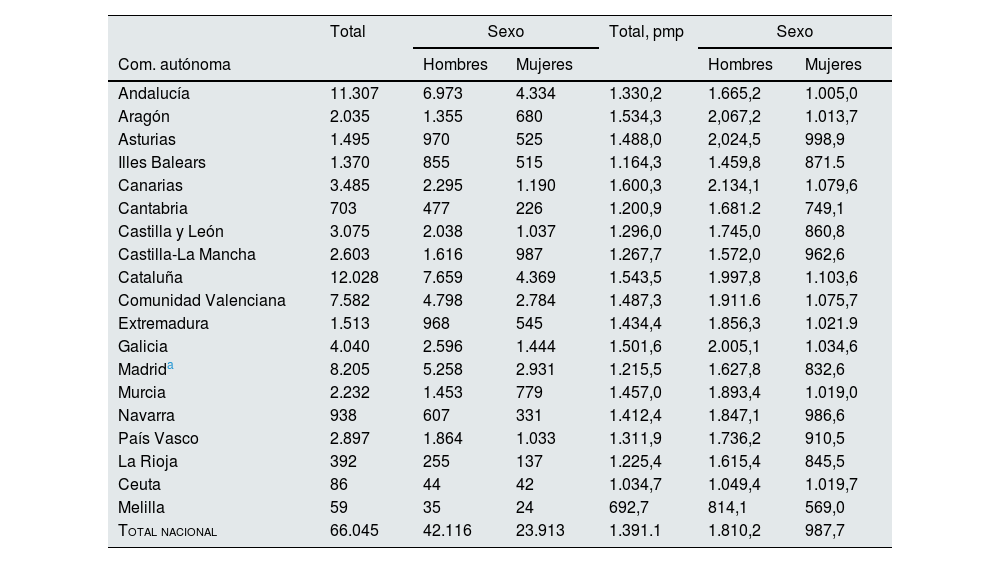
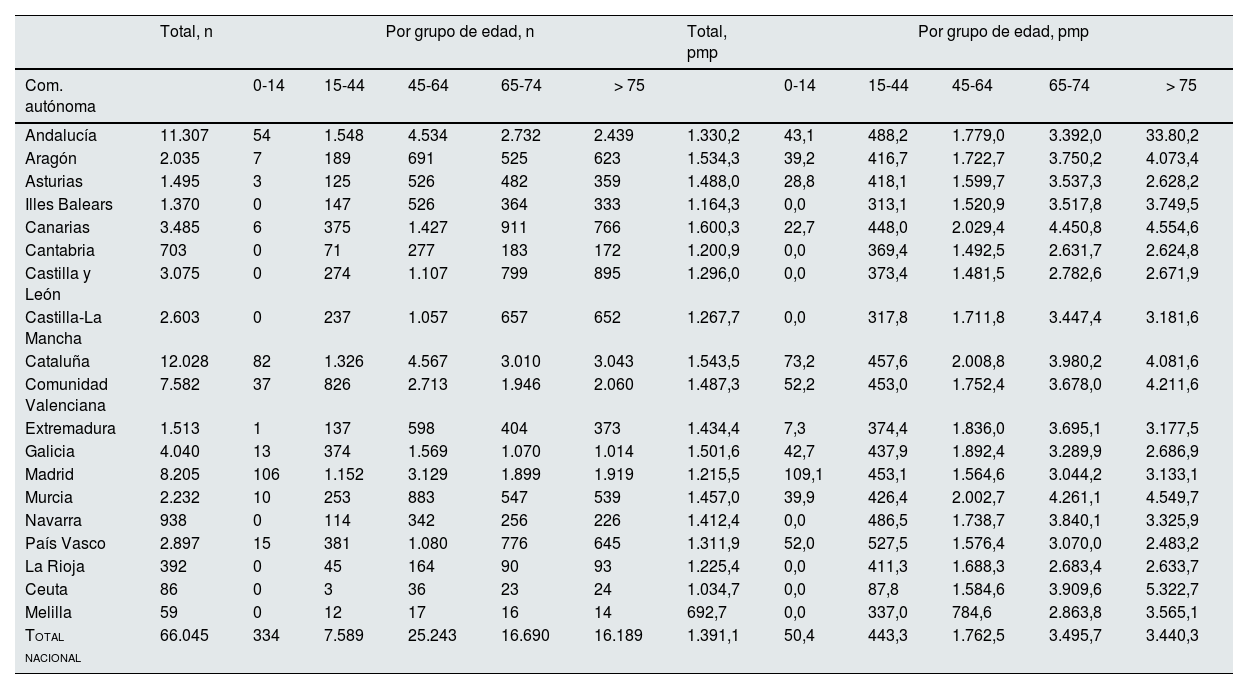
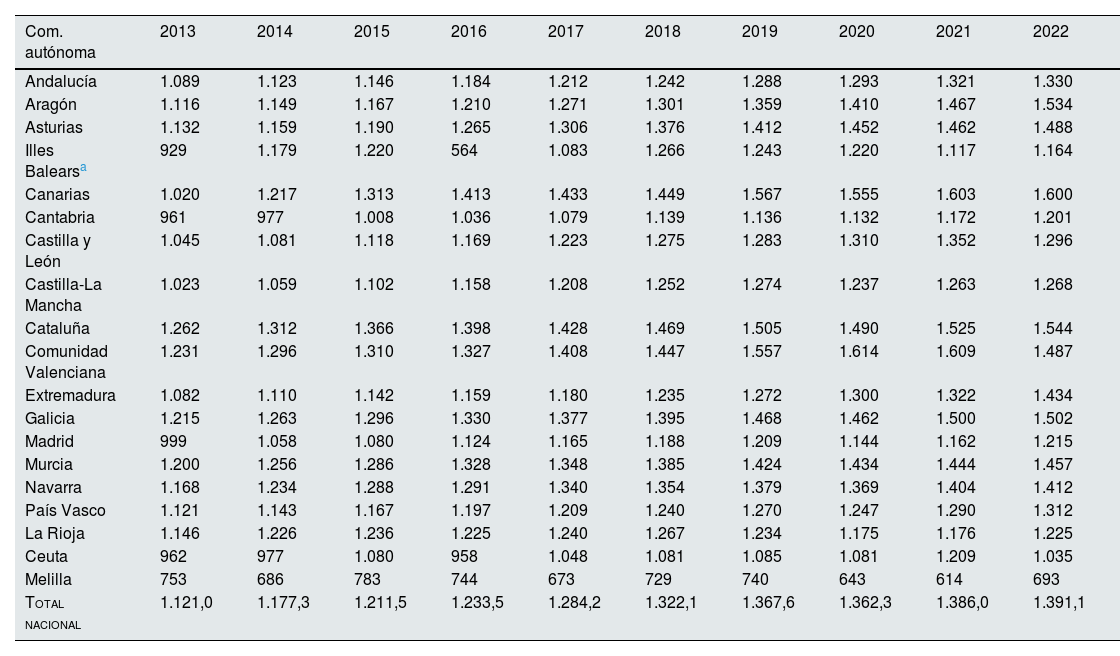
La prevalencia de TRS en España en 2022 fue de 66.045 personas, de las que 42.116 (63,8%) eran varones. La prevalencia global fue de 1.391,1pmp, siendo 1.810,2pmp en varones y 987,7pmp en mujeres, con heterogeneidad en los diferentes territorios (tabla 4). La prevalencia de TRS fue máxima en los pacientes mayores de 65años, con importantes diferencias entre los territorios (tabla 5). En la última década, la prevalencia de TRS en España ha aumentado un 24,1% (tabla 6).
Prevalencia de TRS en el año 2022 en las diferentes comunidades autónomas y su distribución por sexos
| Total | Sexo | Total, pmp | Sexo | |||
|---|---|---|---|---|---|---|
| Com. autónoma | Hombres | Mujeres | Hombres | Mujeres | ||
| Andalucía | 11.307 | 6.973 | 4.334 | 1.330,2 | 1.665,2 | 1.005,0 |
| Aragón | 2.035 | 1.355 | 680 | 1.534,3 | 2,067,2 | 1.013,7 |
| Asturias | 1.495 | 970 | 525 | 1.488,0 | 2,024,5 | 998,9 |
| Illes Balears | 1.370 | 855 | 515 | 1.164,3 | 1.459,8 | 871.5 |
| Canarias | 3.485 | 2.295 | 1.190 | 1.600,3 | 2.134,1 | 1.079,6 |
| Cantabria | 703 | 477 | 226 | 1.200,9 | 1.681.2 | 749,1 |
| Castilla y León | 3.075 | 2.038 | 1.037 | 1.296,0 | 1.745,0 | 860,8 |
| Castilla-La Mancha | 2.603 | 1.616 | 987 | 1.267,7 | 1.572,0 | 962,6 |
| Cataluña | 12.028 | 7.659 | 4.369 | 1.543,5 | 1.997,8 | 1.103,6 |
| Comunidad Valenciana | 7.582 | 4.798 | 2.784 | 1.487,3 | 1.911.6 | 1.075,7 |
| Extremadura | 1.513 | 968 | 545 | 1.434,4 | 1.856,3 | 1.021.9 |
| Galicia | 4.040 | 2.596 | 1.444 | 1.501,6 | 2.005,1 | 1.034,6 |
| Madrida | 8.205 | 5.258 | 2.931 | 1.215,5 | 1.627,8 | 832,6 |
| Murcia | 2.232 | 1.453 | 779 | 1.457,0 | 1.893,4 | 1.019,0 |
| Navarra | 938 | 607 | 331 | 1.412,4 | 1.847,1 | 986,6 |
| País Vasco | 2.897 | 1.864 | 1.033 | 1.311,9 | 1.736,2 | 910,5 |
| La Rioja | 392 | 255 | 137 | 1.225,4 | 1.615,4 | 845,5 |
| Ceuta | 86 | 44 | 42 | 1.034,7 | 1.049,4 | 1.019,7 |
| Melilla | 59 | 35 | 24 | 692,7 | 814,1 | 569,0 |
| Total nacional | 66.045 | 42.116 | 23.913 | 1.391.1 | 1.810,2 | 987,7 |
pmp: personas por millón de población; TRS: terapia renal sustitutiva.
Tasa de prevalencia (pmp) de pacientes en TRS por grupos de edad en las diferentes comunidades autónomas en 2022
| Total, n | Por grupo de edad, n | Total, pmp | Por grupo de edad, pmp | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Com. autónoma | 0-14 | 15-44 | 45-64 | 65-74 | > 75 | 0-14 | 15-44 | 45-64 | 65-74 | > 75 | ||
| Andalucía | 11.307 | 54 | 1.548 | 4.534 | 2.732 | 2.439 | 1.330,2 | 43,1 | 488,2 | 1.779,0 | 3.392,0 | 33.80,2 |
| Aragón | 2.035 | 7 | 189 | 691 | 525 | 623 | 1.534,3 | 39,2 | 416,7 | 1.722,7 | 3.750,2 | 4.073,4 |
| Asturias | 1.495 | 3 | 125 | 526 | 482 | 359 | 1.488,0 | 28,8 | 418,1 | 1.599,7 | 3.537,3 | 2.628,2 |
| Illes Balears | 1.370 | 0 | 147 | 526 | 364 | 333 | 1.164,3 | 0,0 | 313,1 | 1.520,9 | 3.517,8 | 3.749,5 |
| Canarias | 3.485 | 6 | 375 | 1.427 | 911 | 766 | 1.600,3 | 22,7 | 448,0 | 2.029,4 | 4.450,8 | 4.554,6 |
| Cantabria | 703 | 0 | 71 | 277 | 183 | 172 | 1.200,9 | 0,0 | 369,4 | 1.492,5 | 2.631,7 | 2.624,8 |
| Castilla y León | 3.075 | 0 | 274 | 1.107 | 799 | 895 | 1.296,0 | 0,0 | 373,4 | 1.481,5 | 2.782,6 | 2.671,9 |
| Castilla-La Mancha | 2.603 | 0 | 237 | 1.057 | 657 | 652 | 1.267,7 | 0,0 | 317,8 | 1.711,8 | 3.447,4 | 3.181,6 |
| Cataluña | 12.028 | 82 | 1.326 | 4.567 | 3.010 | 3.043 | 1.543,5 | 73,2 | 457,6 | 2.008,8 | 3.980,2 | 4.081,6 |
| Comunidad Valenciana | 7.582 | 37 | 826 | 2.713 | 1.946 | 2.060 | 1.487,3 | 52,2 | 453,0 | 1.752,4 | 3.678,0 | 4.211,6 |
| Extremadura | 1.513 | 1 | 137 | 598 | 404 | 373 | 1.434,4 | 7,3 | 374,4 | 1.836,0 | 3.695,1 | 3.177,5 |
| Galicia | 4.040 | 13 | 374 | 1.569 | 1.070 | 1.014 | 1.501,6 | 42,7 | 437,9 | 1.892,4 | 3.289,9 | 2.686,9 |
| Madrid | 8.205 | 106 | 1.152 | 3.129 | 1.899 | 1.919 | 1.215,5 | 109,1 | 453,1 | 1.564,6 | 3.044,2 | 3.133,1 |
| Murcia | 2.232 | 10 | 253 | 883 | 547 | 539 | 1.457,0 | 39,9 | 426,4 | 2.002,7 | 4.261,1 | 4.549,7 |
| Navarra | 938 | 0 | 114 | 342 | 256 | 226 | 1.412,4 | 0,0 | 486,5 | 1.738,7 | 3.840,1 | 3.325,9 |
| País Vasco | 2.897 | 15 | 381 | 1.080 | 776 | 645 | 1.311,9 | 52,0 | 527,5 | 1.576,4 | 3.070,0 | 2.483,2 |
| La Rioja | 392 | 0 | 45 | 164 | 90 | 93 | 1.225,4 | 0,0 | 411,3 | 1.688,3 | 2.683,4 | 2.633,7 |
| Ceuta | 86 | 0 | 3 | 36 | 23 | 24 | 1.034,7 | 0,0 | 87,8 | 1.584,6 | 3.909,6 | 5.322,7 |
| Melilla | 59 | 0 | 12 | 17 | 16 | 14 | 692,7 | 0,0 | 337,0 | 784,6 | 2.863,8 | 3.565,1 |
| Total nacional | 66.045 | 334 | 7.589 | 25.243 | 16.690 | 16.189 | 1.391,1 | 50,4 | 443,3 | 1.762,5 | 3.495,7 | 3.440,3 |
pmp: personas por millón de población; TRS: terapia renal sustitutiva.
Evolución de la tasa de prevalencia (pmp) de TRS en el periodo 2013-2022 en las diferentes comunidades autónomas
| Com. autónoma | 2013 | 2014 | 2015 | 2016 | 2017 | 2018 | 2019 | 2020 | 2021 | 2022 |
|---|---|---|---|---|---|---|---|---|---|---|
| Andalucía | 1.089 | 1.123 | 1.146 | 1.184 | 1.212 | 1.242 | 1.288 | 1.293 | 1.321 | 1.330 |
| Aragón | 1.116 | 1.149 | 1.167 | 1.210 | 1.271 | 1.301 | 1.359 | 1.410 | 1.467 | 1.534 |
| Asturias | 1.132 | 1.159 | 1.190 | 1.265 | 1.306 | 1.376 | 1.412 | 1.452 | 1.462 | 1.488 |
| Illes Balearsa | 929 | 1.179 | 1.220 | 564 | 1.083 | 1.266 | 1.243 | 1.220 | 1.117 | 1.164 |
| Canarias | 1.020 | 1.217 | 1.313 | 1.413 | 1.433 | 1.449 | 1.567 | 1.555 | 1.603 | 1.600 |
| Cantabria | 961 | 977 | 1.008 | 1.036 | 1.079 | 1.139 | 1.136 | 1.132 | 1.172 | 1.201 |
| Castilla y León | 1.045 | 1.081 | 1.118 | 1.169 | 1.223 | 1.275 | 1.283 | 1.310 | 1.352 | 1.296 |
| Castilla-La Mancha | 1.023 | 1.059 | 1.102 | 1.158 | 1.208 | 1.252 | 1.274 | 1.237 | 1.263 | 1.268 |
| Cataluña | 1.262 | 1.312 | 1.366 | 1.398 | 1.428 | 1.469 | 1.505 | 1.490 | 1.525 | 1.544 |
| Comunidad Valenciana | 1.231 | 1.296 | 1.310 | 1.327 | 1.408 | 1.447 | 1.557 | 1.614 | 1.609 | 1.487 |
| Extremadura | 1.082 | 1.110 | 1.142 | 1.159 | 1.180 | 1.235 | 1.272 | 1.300 | 1.322 | 1.434 |
| Galicia | 1.215 | 1.263 | 1.296 | 1.330 | 1.377 | 1.395 | 1.468 | 1.462 | 1.500 | 1.502 |
| Madrid | 999 | 1.058 | 1.080 | 1.124 | 1.165 | 1.188 | 1.209 | 1.144 | 1.162 | 1.215 |
| Murcia | 1.200 | 1.256 | 1.286 | 1.328 | 1.348 | 1.385 | 1.424 | 1.434 | 1.444 | 1.457 |
| Navarra | 1.168 | 1.234 | 1.288 | 1.291 | 1.340 | 1.354 | 1.379 | 1.369 | 1.404 | 1.412 |
| País Vasco | 1.121 | 1.143 | 1.167 | 1.197 | 1.209 | 1.240 | 1.270 | 1.247 | 1.290 | 1.312 |
| La Rioja | 1.146 | 1.226 | 1.236 | 1.225 | 1.240 | 1.267 | 1.234 | 1.175 | 1.176 | 1.225 |
| Ceuta | 962 | 977 | 1.080 | 958 | 1.048 | 1.081 | 1.085 | 1.081 | 1.209 | 1.035 |
| Melilla | 753 | 686 | 783 | 744 | 673 | 729 | 740 | 643 | 614 | 693 |
| Total nacional | 1.121,0 | 1.177,3 | 1.211,5 | 1.233,5 | 1.284,2 | 1.322,1 | 1.367,6 | 1.362,3 | 1.386,0 | 1.391,1 |
pmp: personas por millón de población; TRS: terapia renal sustitutiva.
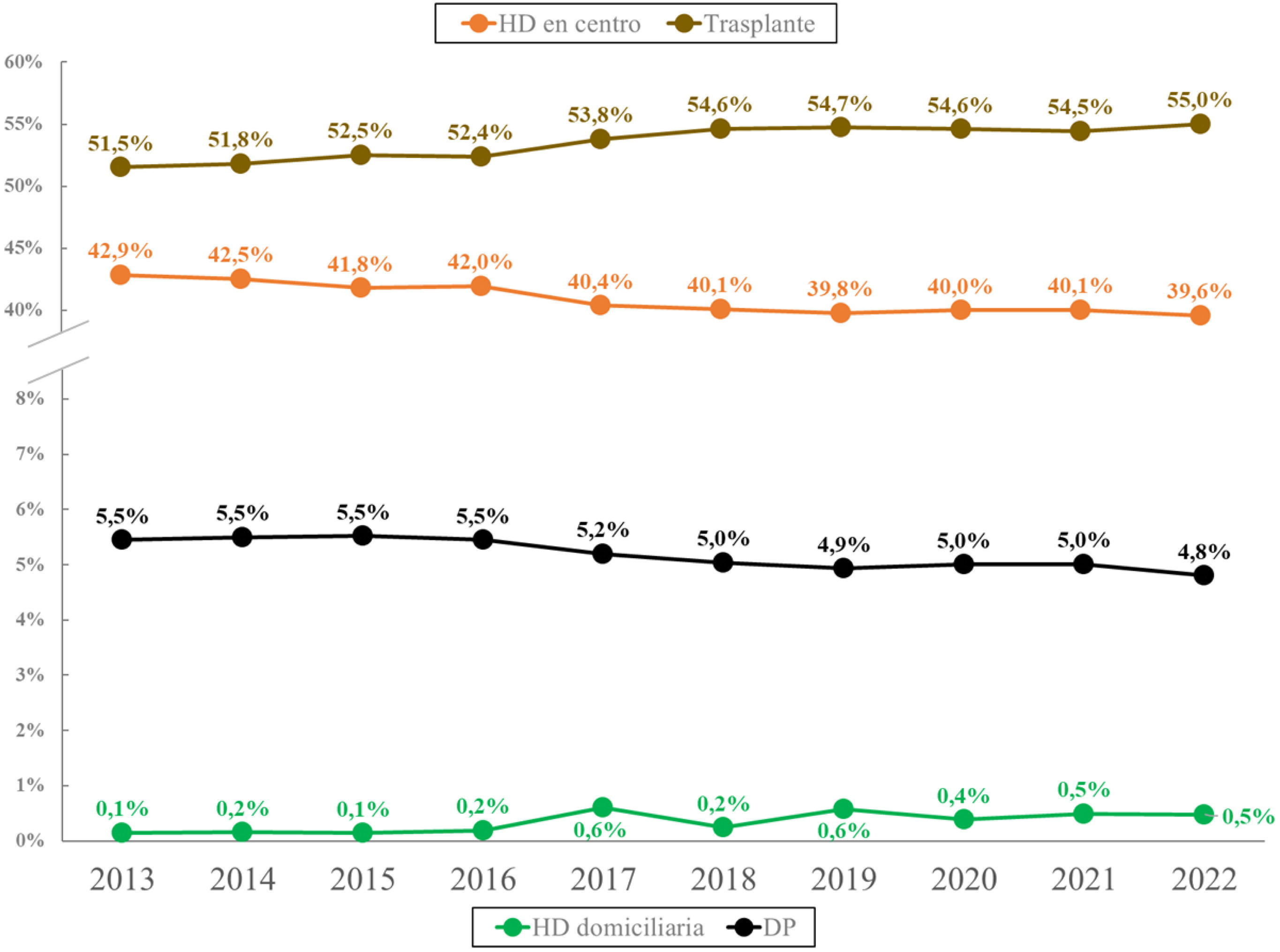
Del total de pacientes en TRS, 36.321 (55,0%) eran portadores de un injerto renal funcionante, 26.136 (39,6%) estaban en programa de HD en centro, 3.214 (4,9%) en DP y 374 (0,5%) en HD domiciliaria. La distribución por territorios se muestra en la figura 5. Los datos evolutivos de los últimos 10años muestran un incremento de la proporción de pacientes prevalentes portadores de injerto renal funcionante, un descenso del porcentaje de pacientes en HD en centro y una estabilidad de las técnicas domiciliarias (fig. 6).
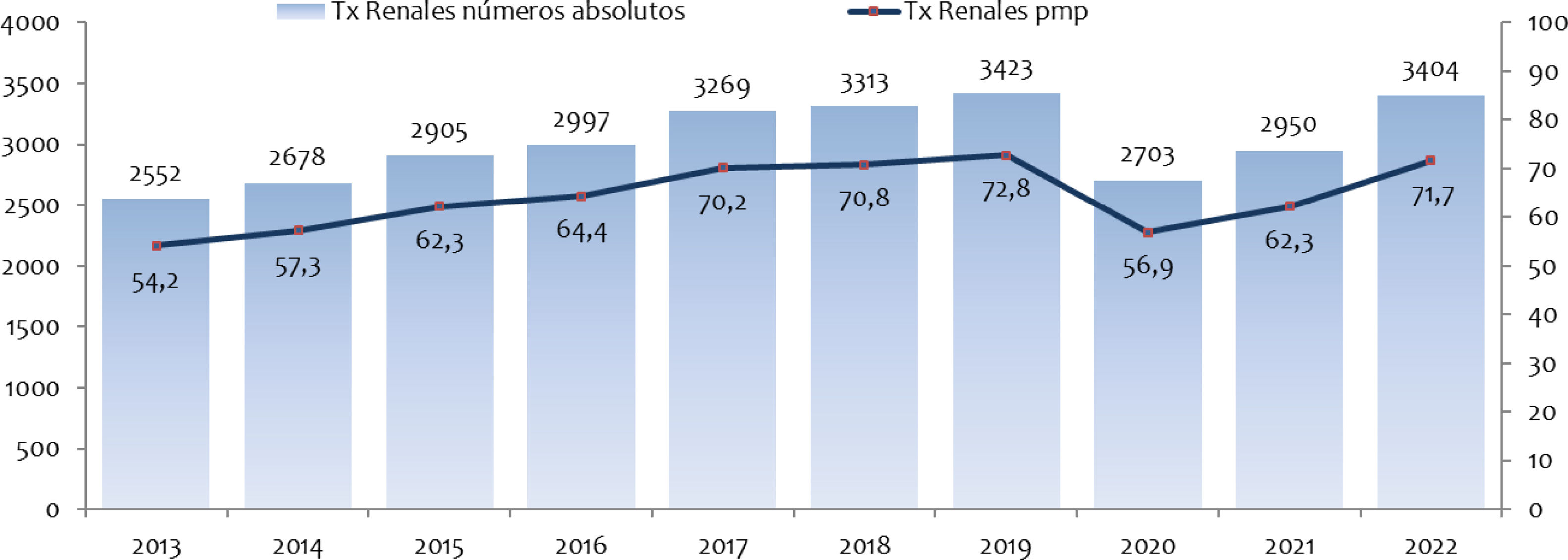
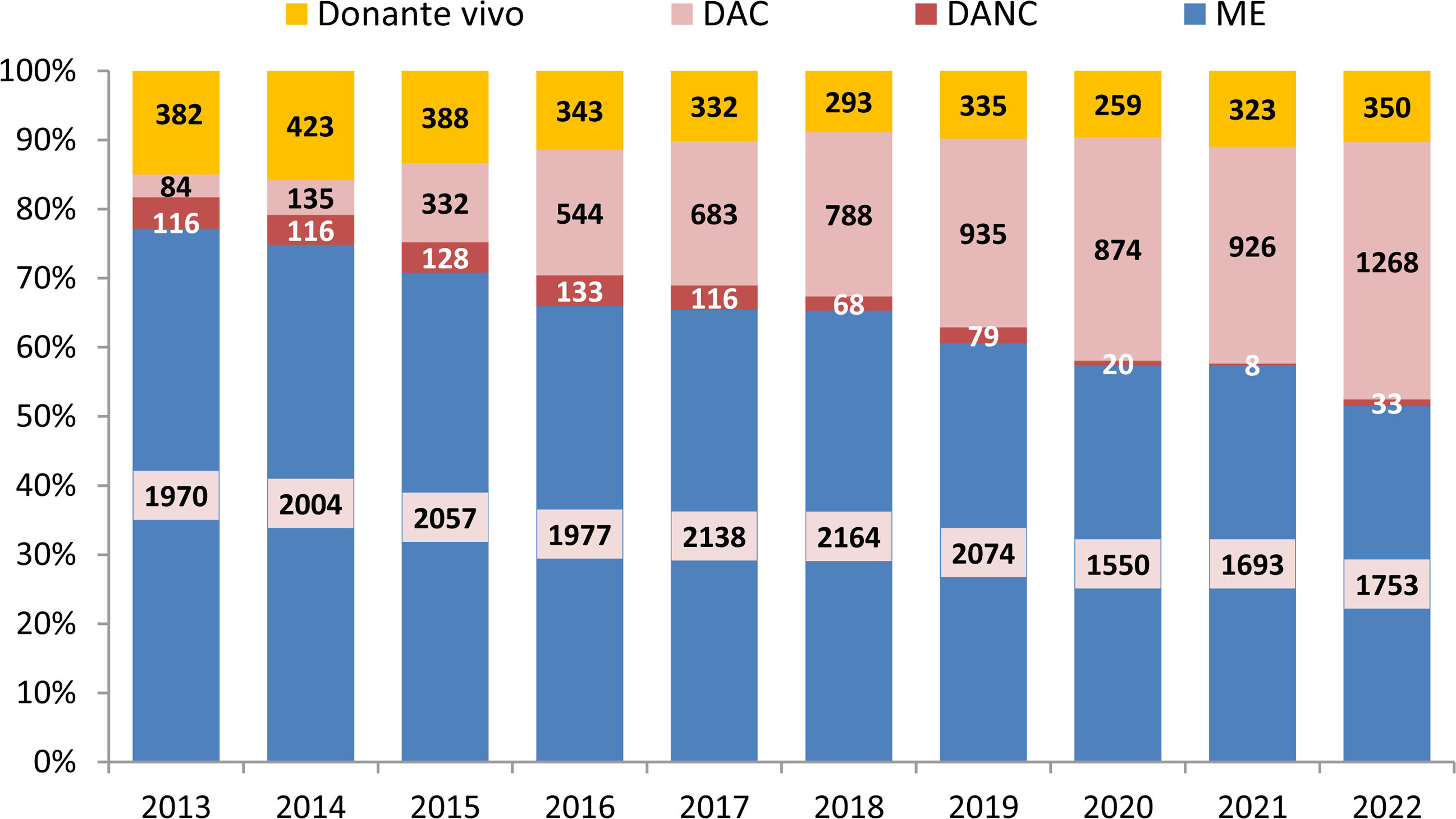
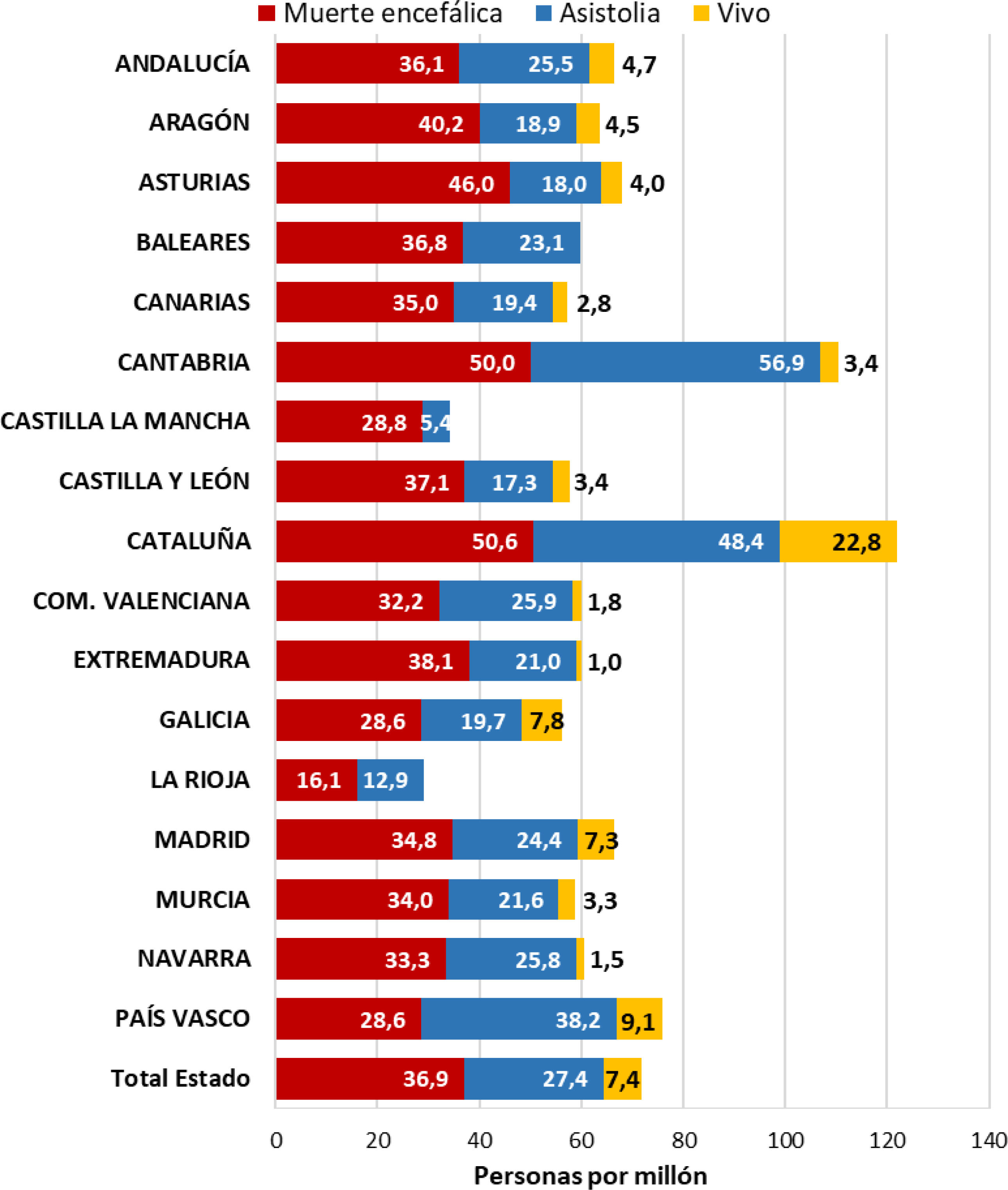
Durante el año 2022 se realizaron en España 3.404 trasplantes renales (71,7pmp). La actividad de trasplante renal ha ido aumentando paulatinamente desde el inicio del periodo de estudio, produciéndose una importante disminución en 2020, en coincidencia con la pandemia por COVID-19, que se recupera en los años siguientes (fig. 7). El trasplante renal de donante fallecido en situación de muerte encefálica es el predominante (1.753 procedimientos en 2022; 51,5%), pero se objetiva un aumento progresivo del trasplante renal de donantes en asistolia (1.301 trasplantes en 2022; 37%) con estabilidad en la modalidad del trasplante renal de donante vivo (350 trasplantes en 2022; 10,3%) (fig. 8). La proporción de los distintos tipos de trasplante renal entre los territorios de España es heterogénea, siendo mayor en Cataluña y en Cantabria (fig. 9). De los 26.549 pacientes prevalentes en HD en 2022, 731 (2,5%) tenían como causa la pérdida del injerto renal.
Evolución de la actividad de trasplante renal (fuente ONT)22.
pmp: personas por millón de población; Tx: trasplante.
Evolución de los diferentes tipos de trasplante renal realizados en el periodo 2013-2022 (fuente ONT)22.
DAC: donante en asistolia controlada; DANC: donante en asistolia no controlada; ME: muerte encefálica.
Distribución de los diferentes tipos de trasplante renal realizados en 2022 (personas por millón de población) en las diferentes comunidades autónomas en 2022 (fuente ONT)22.
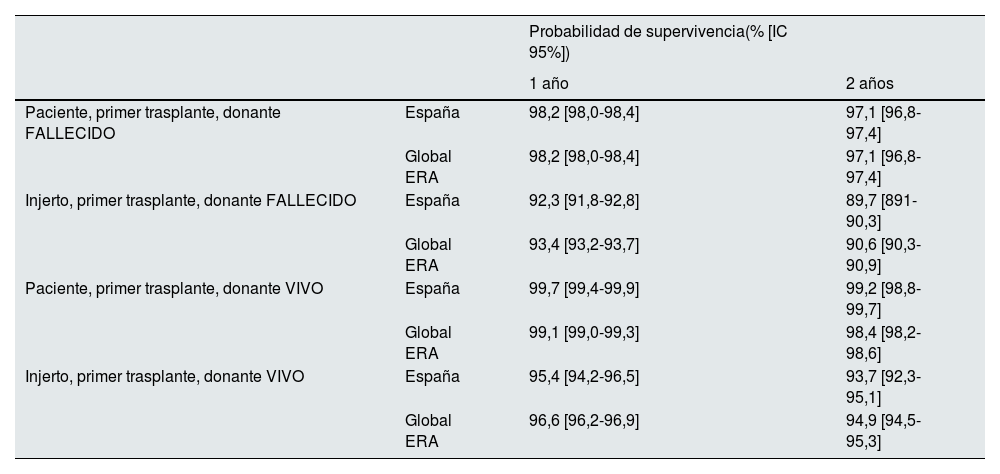
En cuanto a la supervivencia del injerto renal, en el análisis realizado por la ERA-EDTA a partir de los datos individuales proporcionados por las CCAA-ONT, los datos de la cohorte de 2016-2020 muestran una supervivencia ajustada por edad, ERP y sexo del 92,3% y del 89,7% para el primer y el segundo año, respectivamente, en lo que se refiere al donante fallecido, y del 95,4% y el 93,7% para el de vivo, sin diferencias destacables con los datos globales del registro ERA-EDTA (tabla 7)4.
Supervivencia del paciente y del injerto renal entre 2016-2020 y en comparación con los datos de la European Renal Association en el grupo de donante fallecido y de donante vivo4
| Probabilidad de supervivencia(% [IC 95%]) | |||
|---|---|---|---|
| 1 año | 2 años | ||
| Paciente, primer trasplante, donante FALLECIDO | España | 98,2 [98,0-98,4] | 97,1 [96,8-97,4] |
| Global ERA | 98,2 [98,0-98,4] | 97,1 [96,8-97,4] | |
| Injerto, primer trasplante, donante FALLECIDO | España | 92,3 [91,8-92,8] | 89,7 [891-90,3] |
| Global ERA | 93,4 [93,2-93,7] | 90,6 [90,3-90,9] | |
| Paciente, primer trasplante, donante VIVO | España | 99,7 [99,4-99,9] | 99,2 [98,8-99,7] |
| Global ERA | 99,1 [99,0-99,3] | 98,4 [98,2-98,6] | |
| Injerto, primer trasplante, donante VIVO | España | 95,4 [94,2-96,5] | 93,7 [92,3-95,1] |
| Global ERA | 96,6 [96,2-96,9] | 94,9 [94,5-95,3] |
ERA: European Renal Association.
Los cálculos están ajustados para edad, sexo y etiología de la enfermedad renal primaria.
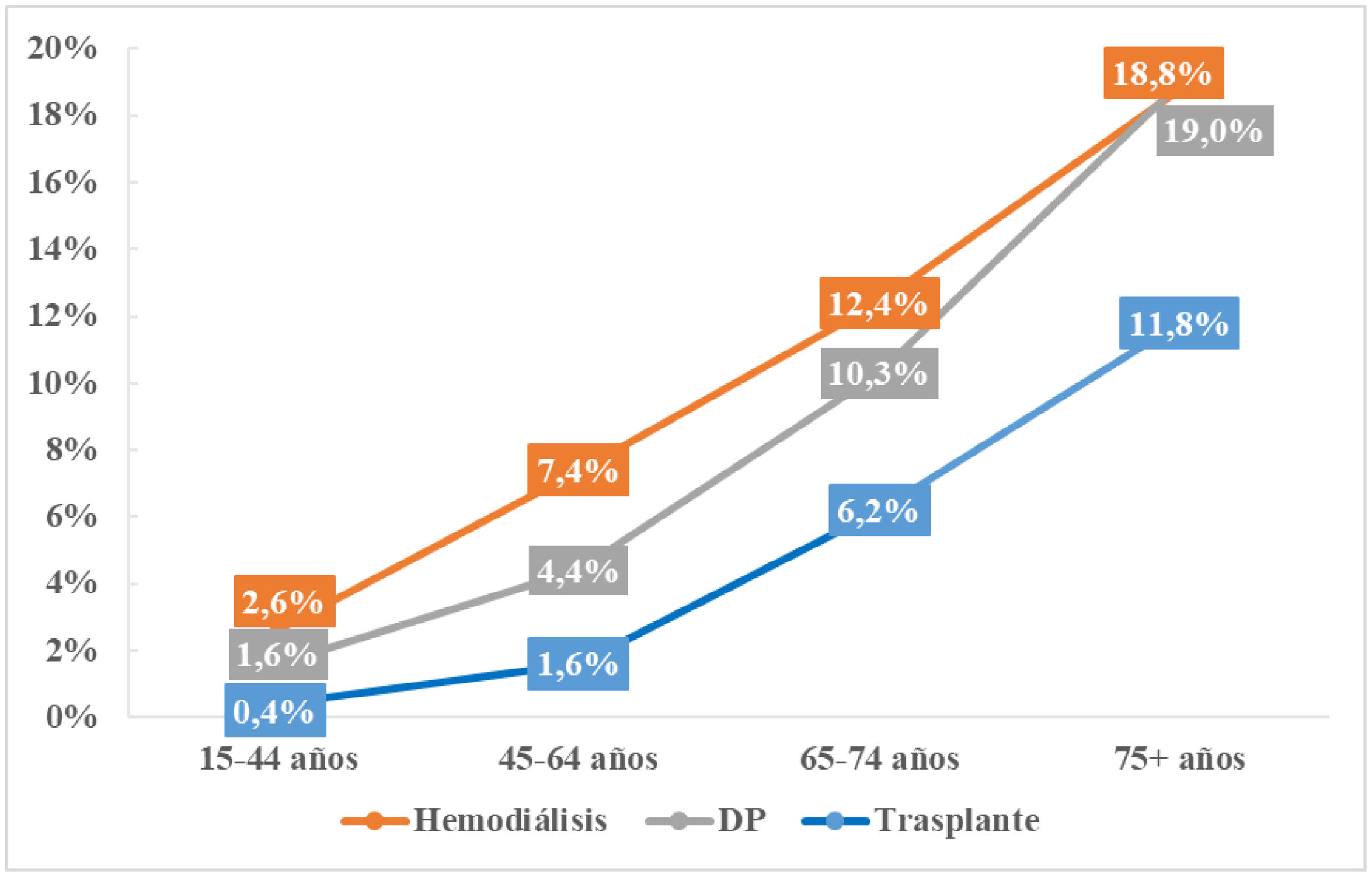
La mortalidad global de los pacientes en TRS en los últimos diez años (2013-2022) se ha mantenido estable, pasando de un 7,4% a un 8,4% (con un ligero repunte en 2020, probablemente en relación con la pandemia de COVID-19). Tal y como se muestra en la figura 10, la mortalidad presenta un mínimo ascenso en los pacientes en DP y en trasplantados renales. El análisis por grupos de edad muestra una asociación entre la modalidad de TRS y la mortalidad, siendo los portadores de un injerto renal los más protegidos en todos los grupos, seguidos de los pacientes en DP (con excepción del grupo >75años, donde la mortalidad se iguala a los pacientes en HD) (fig. 11).
De los 6.095 pacientes en TRS fallecidos en 2022, las causas de muerte más frecuentes fueron las infecciones (27,8%), miscelánea/otras causas (17,2%), isquemia miocárdica/fracaso cardiaco (11,7%), desconocida (10,3%), neoplasia (9,6%) y parada cardíaca (8,6%). La figura 12 muestra la distribución de las causas de mortalidad en función del tipo de TRS.
La estimación de la mediana de supervivencia global para todos los incidentes desde 2004 fue de 6,2años, con un intervalo de confianza del 95% entre 6,1 y 6,4.
La probabilidad no ajustada de supervivencia es del 91, del 81 y del 57% a 1, 2 y 5años, respectivamente.
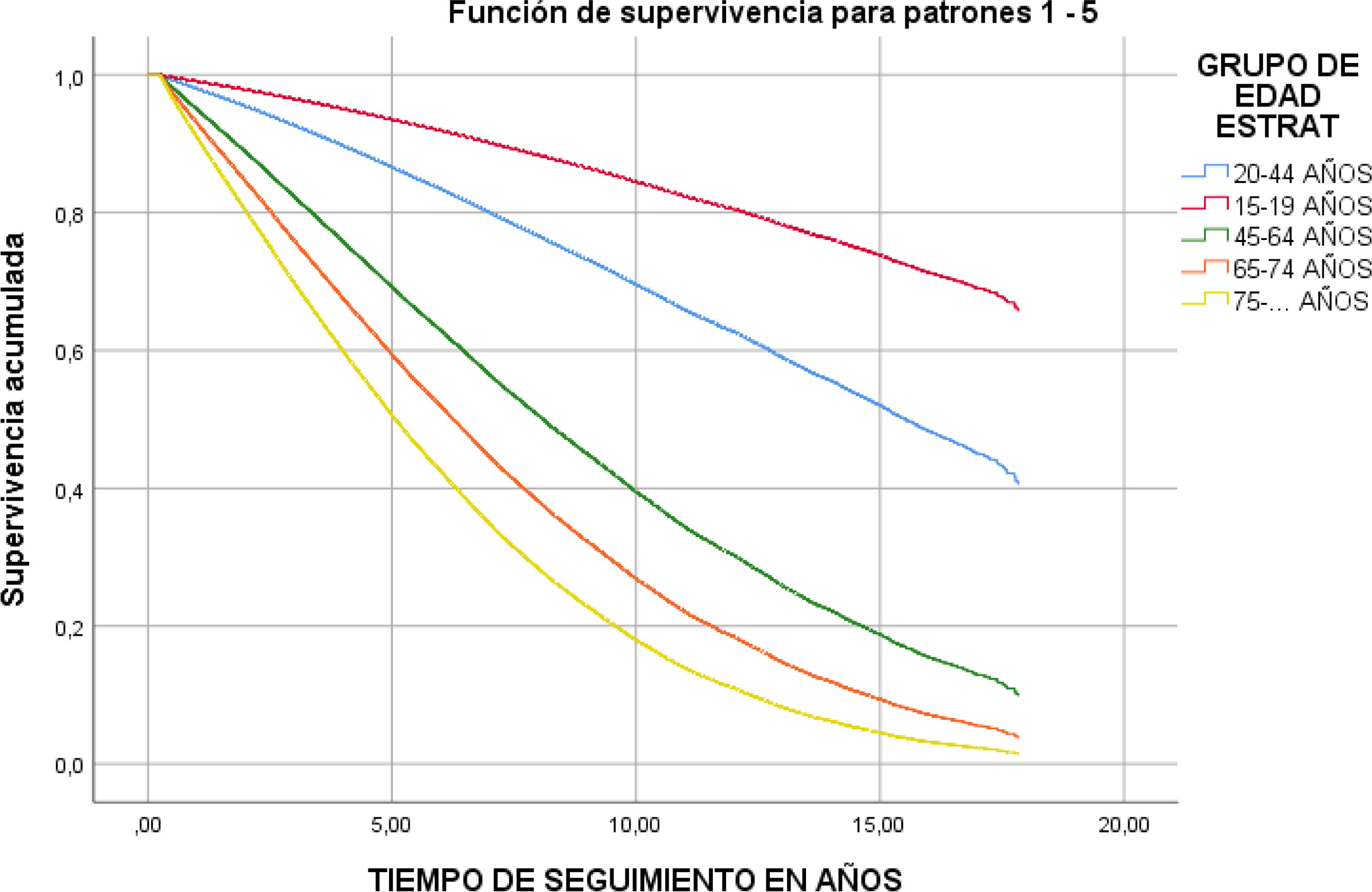
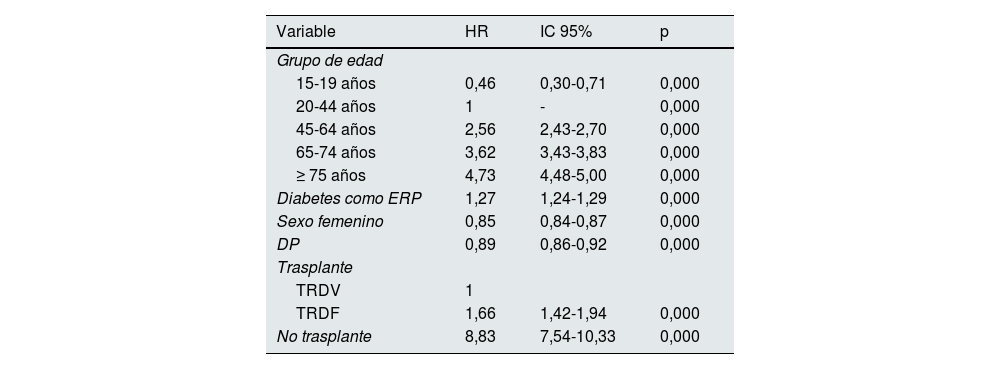
El análisis ajustado de supervivencia se presenta en la tabla 8. El modelo de Cox muestra como factores independientes de supervivencia la edad, la diabetes como ERP, el haber sido trasplantado, el sexo y la modalidad de TRS de inicio, siendo peor la supervivencia para hombres diabéticos, por encima de los 45años, que hayan iniciado TRS con HD y que no hayan sido trasplantados (tabla 8).
Modelo de Cox de supervivencia para pacientes con TRS
| Variable | HR | IC 95% | p |
|---|---|---|---|
| Grupo de edad | |||
| 15-19 años | 0,46 | 0,30-0,71 | 0,000 |
| 20-44 años | 1 | - | 0,000 |
| 45-64 años | 2,56 | 2,43-2,70 | 0,000 |
| 65-74 años | 3,62 | 3,43-3,83 | 0,000 |
| ≥ 75 años | 4,73 | 4,48-5,00 | 0,000 |
| Diabetes como ERP | 1,27 | 1,24-1,29 | 0,000 |
| Sexo femenino | 0,85 | 0,84-0,87 | 0,000 |
| DP | 0,89 | 0,86-0,92 | 0,000 |
| Trasplante | |||
| TRDV | 1 | ||
| TRDF | 1,66 | 1,42-1,94 | 0,000 |
| No trasplante | 8,83 | 7,54-10,33 | 0,000 |
DP: diálisis peritoneal; HR: hazard ratio; IC 95%: intervalo de confianza al 95%; ERP: enfermedad renal primaria; TRDV: trasplante renal de donante vivo; TRDF: trasplante renal de donante fallecido; TRS: terapia renal sustitutiva.
La figura 13 muestra las curvas de supervivencia de los pacientes incidentes en el período 2004-2022 en función del grupo de edad.
En cuanto a la supervivencia del paciente trasplantado renal, en el análisis efectuado por la ERA-EDTA a partir de los datos individuales de España vs el global de países participantes, los datos de la cohorte 2015-2020 muestran una supervivencia ajustada por edad, ERP y sexo del 98,2% y del 97,1% para el primer y el segundo año, respectivamente, para la donación de fallecido, y del 99,7% y del 99,2% para la donación de vivo (tabla 7)4.
DiscusiónLos datos del REER de la última década demuestran un crecimiento de la incidencia de TRS en España entre 2013 y 2019, con estabilización posterior. La actividad de trasplante renal sitúa a España como un líder mundial. Asimismo, la mortalidad se sitúa en un 8,4%, cifra que se mantiene estable en los últimos 10años, salvo en el año 2020, con un aumento achacable a la pandemia por COVID-19.
Enlentecer la progresión de la ERC es un reto médico, social, político y económico que precisa de medidas globales. La enorme prevalencia de ERC, estimada en más de un 15% en nuestro país8, podría alcanzar a una de cuatro personas a final de siglo1. Las causas de la estabilización de la incidencia de TRS en los últimos 4años deberían explorarse en profundidad. En 2020 se produjo un descenso, probablemente como consecuencia de la alta mortalidad de COVID-19 en pacientes con ERC9,10. Sin embargo, en 2021 y 2022 se mantuvo en cifras de 2019. Las principales posibles causas de esta estabilización a explorar son cambios en la actitud frente al tratamiento conservador del fallo renal y la eficacia de las nuevas herramientas terapéuticas, sin poder descartar otras. Si hubiera un impacto de los nuevos tratamientos, como es el caso de los inhibidores del co-transportador sodio-glucosa tipo2 (iSGLT2)11,12, serían de esperar futuras mejoras, ya que en 2020-2022 no se habían alcanzado todavía las tasas deseables de prescripción y que el efecto sobre la progresión es mayor en estadios menos avanzados, y, por tanto, su plena repercusión tardará unos años en llegar13. El diagnóstico y el tratamiento precoces de la insuficiencia renal, así como una remisión más temprana a las consultas de Nefrología, podrían paliar en parte esta problemática13-15.
En relación con la etiología de la ERC, la diabetes sigue siendo la causa principal de inicio de TRS en nuestro país. Aunque en el año 2022 este dato parece haber disminuido con respecto a la evolución de la última década, debemos analizarlo con cautela. En primer lugar, porque la etiología de la enfermedad renal no siempre obedece a criterios diagnósticos evidentes; en segundo lugar, porque el año 2022 es el primero en el que se ha adaptado el REER al registro de la ERA para que sean comparables y, por tanto, puede haber pacientes clasificados en otro grupo, y en tercer lugar, porque la nueva categoría «perdidos» ocupa un 6,8% que antes no formaba parte del contaje total (al ser un valor que podía dejarse en blanco). En cualquier caso, la aprobación de fármacos que enlentecen la progresión de la enfermedad renal diabética (iSGLT2, finerenona, arGLP-1) abre un futuro optimista en esta patología y en la ERC en general16. La segunda causa de ERC sigue siendo miscelánea, que incluye, en la nueva clasificación, a los pacientes cuya etiología no se ha filiado, a diferencia de la codificación anterior a 2022, donde se reportaba de manera separada. Aunque el porcentaje (21,7%) de casos sigue siendo inaceptable, es esperable que la integración de la genética en el algoritmo diagnóstico de la ERC reduzca este porcentaje en los siguientes informes17. Iniciativas como GENSEN, que identificó una probable causa genética en el 25% de pacientes jóvenes (<45años) con fallo renal de causa desconocida en España, sugieren que un uso más extenso del diagnóstico genético puede ayudar a disminuir el porcentaje de pacientes con ERC de causa desconocida18.
España es líder en trasplante renal, con una tasa de 71,7pmp, tan solo superado por Estados Unidos. A pesar de un ascenso en la modalidad de trasplante tras donación en asistolia, la donación en muerte encefálica sigue siendo la opción más frecuente, tal y como ocurre en el continente americano, Europa u Oceanía, que concretamente son los territorios que más trasplantes realizan a nivel global19. En comparación con los datos de la ERA, en su informe de 2022, la supervivencia del injerto renal en España es similar a la reportada en Europa en los dos primeros años y para la donación de vivo y de fallecido3,4. Un esfuerzo por incrementar la tasa de trasplante con donante vivo en España sería deseable dado el incremento significativo de la supervivencia (injerto y paciente) que ofrece esta modalidad con respecto al trasplante de donante fallecido.
En términos generales y obviando el impacto de la COVID-1920, la mortalidad de los pacientes en TRS se mantiene estable, sin disminuir, en parte como consecuencia de un envejecimiento de la población, pero también de la exclusión sistemática de dichos pacientes en los ensayos clínicos. Son pocos los estudios que permiten incluir a pacientes con filtrado glomerular estimado inferior a 30ml/min/1,73m2, por lo que la indicación de la práctica totalidad de fármacos pronósticos es muy limitada en población en HD y DP21. Si bien es cierto que el uso fuera de indicación está extendido en determinadas circunstancias, ni siquiera disponemos de datos en vida real que avalen la prescripción de fármacos como iSGLT2, antagonistas de la neprilisina, antagonistas del receptor mineralocorticoide o incluso bloqueantes del sistema renina angiotensina aldosterona. Una situación similar ocurre con los pacientes portadores de un injerto renal, raramente incluidos en ensayos clínicos.
Tal y como se muestra en la tabla 7, la supervivencia del injerto y del paciente trasplantado en España es superponible a la publicada por ERA. No obstante, resulta preocupante que el pico de mortalidad de 2020, claramente relacionado con la COVID-19, no ha retornado a valores previos, como ocurrió en los pacientes en HD, sino que persiste alto e incluso está aumentando. Una caracterización detallada de las causas de muerte en esta población en particular puede ayudar a invertir esta preocupante tendencia reciente10.
El presente informe presenta limitaciones. En primer lugar, de forma inherente los registros pueden dar lugar a pérdida de algunos datos no obligatorios. Sin embargo, la obligatoriedad en su cumplimentación hace que estas pérdidas no sean relevantes en el análisis global. Además, los datos de prevalencia e incidencia son reales, puesto que estos dos indicadores son de cumplimentación obligatoria. En segundo lugar, el cambio en la clasificación de la etiología hace difícilmente comparables los datos previos a 2022, especialmente en las categorías de pérdidas, otras y miscelánea. A este respecto, la etiología de la ERC puede tener algunos sesgos debido a la ausencia de criterios diagnósticos bien establecidos (por ejemplo, vascular o diabética). En tercer lugar, las tasas de incidencia y prevalencia no se han estandarizado por edad y sexo, lo que podría tener implicaciones cuando analizamos los datos por CCAA. Finalmente, las causas de mortalidad no son siempre muy evidentes, por lo que podrían existir algunos pacientes con diagnóstico erróneo.
ConclusionesEl análisis del REER de la última década demuestra que la incidencia de personas que requieren TRS en España ascendió hasta 2019 y parece haberse estabilizado desde entonces. Sin embargo, podrían persistir algunas diferencias entre CCAA, cuyas causas se deben estudiar en profundidad con objeto de optimizar el manejo de la enfermedad renal atendiendo a los diferentes factores sociodemográficos. La diabetes sigue siendo la primera causa de ERC con necesidad de TRS en España. La edad, la modalidad, el sexo y la diabetes son los predictores independientes de mortalidad en los pacientes que precisan TRS en España.
Nota de los autoresEl Registro Español de Enfermos Renales (REER) pasará a denominarse Registro Español de Diálisis y Trasplante (REDYT).
FinanciaciónLa investigación de AO, BQ, ES, AM, DH está financiada por el Instituto de Salud CarlosIII (ISCIII) FIS/Fondos FEDER RICORS program to RICORS2040 (RD21/0005/0001) funded by European Union-NextGeneration EU, Mecanismo para la Recuperación y la Resiliencia (MRR) y PREVENTCKD Consortium Project ID: 101101220 Programme: EU4H DG/Agency: HADEA. La investigación de MM está financiada por el Instituto de Salud CarlosIII (ISCIII) FIS PI23/01518
Conflicto de interesesBQ es el actual coordinador de registros de la Sociedad Española de Nefrología (S.E.N.) y ha recibido financiación/honorarios por parte de Sandoz, Novo Nordisk, Otsuka, AstraZeneca, Boehringer y CSL-Vifor.
AO ha recibido financiación de Sanofi y honorarios de consultoría o por conferencias o apoyo para viajes de Adviccene, Alexion, Astellas, AstraZeneca, Amicus, Amgen, Boehringer Ingelheim, Fresenius Medical Care, GSK, Bayer, Sanofi-Genzyme, Sobi, Menarini, Mundipharma, Kyowa Kirin, Lilly, Freeline, Idorsia, Chiesi, Otsuka, Novo Nordisk, Sysmex y Vifor Fresenius Medical Care Renal Pharma y Spafarma, y es Director de la cátedra UAM-AstraZeneca de enfermedad renal crónica y electrólitos. Tiene acciones en Telara Farma.
AM es miembro de la Junta Directiva de la Sociedad Española de Nefrología (S.E.N.) y ha recibido financiación/honorarios por parte de GSK, Sandoz, Astellas, Sanofi, Otsuka y AstraZeneca.
ES es el actual presidente de la Sociedad Española de Nefrología (S.E.N.) y ha recibido financiación/honorarios por parte de Novo Nordisk, AstraZeneca, Boehringer y CSL-Vifor.
MM es la actual presidente de la Sociedad Madrileña de Nefrología y miembro del Comité del Registro Madrileño de Pacientes Renales (REMER) y ha recibido honorarios por colaboración en docencia y formación y/o asesoría científica de Alexion, Amgen, AstraZeneca, Bayer, Boehringer Ingelheim, Lilly, CSL-Vifor, Esteve, GSK, Menarini y NovoNordisk.
ARB es presidente de la Sociedad Andaluza de Trasplante de Órganos y Tejidos. Ha recibido financiación/honorarios de Astellas Farma, Chiesi, GSK y Novo Nordisk.
MVM ha recibido financiación/honorarios por parte de Fresenius, Sandoz y Sanofi.
BMD, DH, STA, MCSP, OLRA, MFSR, IME, MRC, IMA, EBC, MABG, JDL, HGL, FEAM y GGM no tienen conflicto de intereses.
Agradecemos a todos los profesionales que con su esfuerzo nutren el REER.
Andalucía: Pablo Castro de la Nuez, Alberto Rodríguez Benot; Aragón: Federico E. Arribas Monzón; Asturias: José Ramón Quirós, Silvia Rivera Ariza; Baleares: Miguel Agudo García, Gonzalo Gómez Marqués; Canarias: Sara Trujillo Alemán, Domingo Marrero Miranda, César García Cantón; Cantabria: Juan Carlos Ruíz San Millán, María Valentín Muñoz, Oscar García; Cataluña: Jordi Comas i Farnes, Mercè Borràs; Castilla la Mancha: Carmen Román Ortiz, Inmaculada Moreno Alía, Rafael Díaz Tejeiro, Carmen Vozmediano Poyatos; Castilla León: Pablo Ucio, María Ángeles, Héctor García López, Mario Prieto; Extremadura: Juan Antonio Linares Dópido, Javier Deira Lorenzo; Galicia: Encarnación Bouzas Caamaño, Teresa García Falcón; Madrid: Almudena Escribá Bárcena, María Marqués Vidas, Alberto Ortiz; Murcia: Mª Carmen Santiuste de Pablos, Inmaculada Marín Sánchez, Juan Cabezuelo Romero; Navarra: Joaquín Manrique Escola, María Fernanda Slon Roblero; La Rioja: Emma Huarte Loza, Marta Artamendi Larrañaga, Hermann Hernández Vargas; País Vasco: Esther Corral, Ángela Magaz Lago, María Teresa Rodrigo de Tomás, Iñigo Moina Eguren; Comunidad Valenciana: Olga Lucía Rodríguez, Cayetano Merino Egea, Antonio Sarrión, Juan Carlos Alonso Gómez.
Ingesa: María Antonia Blanco Galán.
S.E.N.: J. Emilio Sánchez Álvarez (presidente), Borja Quiroga (Coordinador de Registros).
SENTRA: Auxiliadora Mazuecos.
SET: Domingo Hernández.
ONT: Agustín Carreño, Beatriz Mahillo.