Antecedentes: A finales del siglo pasado, evidencias científicas de nivel II apoyaban una mayor supervivencia en técnicas de hemodiálisis (HD) alternativas a la HD convencional, cuya expectativa de vida a cinco años, en Europa, era inferior al 40 %. Desde el año 2000 nuestros pacientes incidentes se adscribieron a una estrategia de HD no convencional con el objetivo de evaluar su influencia en la supervivencia. Método: Estudio de cohorte realizado en 183 incidentes en HD entre 2000 y 2010. Al inicio de la HD se evaluaron antecedentes de enfermedad cardiovascular (EFCV) e índice de Charlson (ICh). Desde el año 2000 iniciamos la estrategia de HD no convencional que contenía protocolos de HD biocompatible, de alto flujo, objetivo de peso seco, esquema de tres sesiones semanales de cinco horas (HD 5 h x 3) y desde 2003, coexistiendo con el anterior, se inicia el esquema de sesiones de HD de cuatro horas en días alternos sin descanso de fin de semana (every other day dialysis: EODD) para incidentes de mayor riesgo. Resultados: De los 183 pacientes incidentes en el programa de HD, 84 se dializaron en esquema HD 5 h x 3 y 99 en EODD. La edad media fue de 60,6 ± 13,8 años, el 31,7 % eran mayores de 70 años, diabéticos el 43 %, con EFCV el 58,5 % y el ICh medio era de 4,55. La supervivencia (%) del primero al quinto año fue de 92, 82, 75, 62 y 55, con mediana de 5,65 años (intervalo de confianza [IC] 4,18-7,11) y media de 5,4 (IC 4,75-6,1). Conclusiones: La estrategia de HD no convencional que aplicamos a los pacientes incidentes en la técnica proporciona un buen resultado de supervivencia.
Background: At the end of the last century, level II scientific evidence supported higher survival rates for alternative haemodialysis (HD) techniques when compared with conventional HD, whose five-year life expectancy in Europe was below 40%. Our incident patients participated in an unconventional HD strategy from the year 2000, with the aim of assessing its influence on survival. Method: A cohort study on 183 incident HD patients between 2000 and 2010. At the beginning of HD, we evaluated a history of cardiovascular disease (CVD) and Charlson index (ChI). In the year 2000, we began the unconventional HD strategy that included protocols of biocompatible high flux HD, dry weight target, a schedule of three weekly five hour sessions (HD 5h x 3) and from 2003, in combination with the foregoing, we began a schedule of four hour HD sessions on alternate days including weekends (every other day dialysis: EODD) for higher risk incident patients. Results: Of the 183 incident patients in the HD programme, 84 were dialysed in the 5hx3 HD schedule and 99 in EODD. The mean age was 60.6±13.8 years, 31.7% were older than 70, 43% were diabetic, with CVD sufferers at 58.5% and the mean ChI was 4.55. Survival (%) from the first to the fifth year was 92, 82, 75, 62 and 55, with a median of 5.65 years (confidence interval [CI] 4.18-7.11) and a mean of 5.4 (CI 4.75-6.1). Conclusions: The unconventional HD strategy that we applied to incident patients in the technique resulted in good survival.
INTRODUCCIÓN
Desde el final del siglo XX, asistimos a la universalización del tratamiento mediante hemodiálisis (HD) para una población de mayor edad con más incidencia de diabetes (DM) y con aumento de la comorbilidad cardiovascular, factores relacionados directamente con la mortalidad en HD. Desde el inicio de la técnica, se publicaron estudios1-6 que aportaban mejoras de supervivencia en relación con alguno de sus componentes, aunque no alcanzaban el máximo rango de evidencia científica. Sin embargo, en Occidente, se mantienen esquemas de HD convencional de bajo flujo con tres sesiones semanales de cuatro horas, con setenta y dos horas de fin de semana sin HD, sin reducción de la mortalidad7,8. En ese esquema convencional, el reciente estudio DOPPS (Dialysis Outcomes and Practice Pattern Study) registra para nuestro país una duración de las sesiones de HD igual a cuatro horas en menos del 50 % de los pacientes e inferior a cuatro horas en más del 50 %9.
Desde el año 2000, nuestra unidad inició una estrategia de HD no convencional que incorporó un conjunto de actuaciones en el tratamiento mediante HD relacionadas con la biocompatibilidad, uso de dializador con membrana sintética de alto flujo, sesiones con aumento de tiempo o frecuencia en función del nivel de riesgo del paciente y control del volumen extracelular (VEC), incorporando, además, nuevas tecnologías10. Estos protocolos se basaban en estudios previos con nivel II de evidencia que mostraban reducción de la mortalidad y cuya implantación estaba al alcance de la práctica clínica habitual.
El objetivo del estudio es evaluar la repercusión que tiene esta estrategia de HD no convencional sobre la supervivencia de los pacientes que iniciaron tratamiento en nuestra unidad de HD durante la década 2000-2010.
PACIENTES Y MÉTODOS
Población
Estudio de cohorte realizado en 183 pacientes con insuficiencia renal crónica, incidentes por cualquier causa en HD entre 2000 y 2010 en la unidad de HD del Hospital Universitario de Puerto Real, con permanencia mínima en la técnica superior a un mes y que aceptaron el protocolo de HD descrito posteriormente. Del resto de los pacientes incidentes en ese período, 61 no cumplían el mes de permanencia y 6 no aceptaron el protocolo de esquema de HD no convencional.
Al inicio se evaluaron sus antecedentes: enfermedad cardiovascular (EFCV) si presentaban antecedentes de arritmia o insuficiencia cardíaca o angina/infarto de miocardio o enfermedad vásculo-cerebral o vasculopatía periférica; índice de comorbilidad de Charlson (ICh): bajo si menor de 4, medio entre 4 y 6, alto si mayor de 6. Se consideró DM como diagnóstico previo y riesgo en ICh, independientemente de la causa de la nefropatía.
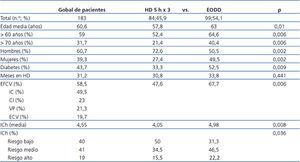
La edad media fue de 60,6 ± 13,8 años, el 57,4 % tenían más de 60 años y el 31,7 % eran mayores de 70 años. Las características basales se muestran en la tabla 1: predominaban los hombres (relación 1,5:1), con presencia de DM en el 43 % y de EFCV en el 58,5 % al inicio.
Estrategia de hemodiálisis no convencional
Los pacientes fueron tratados de acuerdo con los siguientes protocolos:
1. Esquemas de HD: en el año 2000 se inicia el esquema de tres sesiones semanales de cinco horas (HD 5 h x 3) con descanso de 72 horas en el fin de semana11. En el año 2003, y coexistiendo con el anterior, se inicia el esquema de sesiones de cuatro horas en días alternos (EODD), cada 48 horas4 (lunes-miércoles-viernes-domingo-martes-jueves-sábado-lunes).
Criterios para la asignación de pacientes al esquema:
Al esquema HD 5 h x 3: 2000-2002: todos los incidentes durante ese período. 2003-2010: pacientes incidentes sin EFCV con ICh bajo o que no aceptaron el esquema de EODD. Si la superficie corporal era inferior a 1,5 m2 y durante su evolución alcanzaban sobradamente los objetivos de dosis y control del VEC, el tiempo pasaba a cuatro horas y media, siempre que mantuvieran los objetivos de dosis y peso.
Al esquema EODD: 2003-2010: pacientes incidentes con EFCV o ICh medio-alto. Pacientes que iniciaron HD en HD 5 h x 3 (2000-2002) y que reunían alguno de los criterios para EODD, o con ganancias de peso > 4 % sobre el peso seco12 tras el fin de semana que no permitían alcanzar su peso con tasa de ultrafiltración (UF) adecuada en HD 5 h x 3. Estos pacientes quedaron registrados en EODD si permanecían en él más de seis meses.
2. Acceso vascular: se priorizó la fístula arteriovenosa nativa como primer objetivo; desde 2004 se implantó catéter tunelizado de doble luz de forma transitoria siempre que la necesidad se prolongase más de tres semanas13 y, desde 2009, protocolo de profilaxis de infecciones relacionadas con catéter mediante relleno con gentamicina y heparina de cualquier tipo de catéter14.
3. Técnica de HD de alto flujo: líquido de HD constituido a partir de agua ultrapura15 con flujo de 500 ml/min, tampón bicarbonato y perfil constante de sodio y UF. Monitores de HD con control de UF. Esterilización del circuito extracorpóreo y dializador sin óxido de etileno. Dializadores con membranas sintéticas con coeficientes de UF > 50 ml/h/mmHg (poliamida o poliacrilonitrilo o polisulfona), y superficies 1,7 y 2,1 m2, indicados según la superficie corporal. Flujo sanguíneo > 300 ml/min. No se emplearon técnicas convectivas.
4. Control del VEC: dieta baja en sal (< 4 g/día). En cada paciente, al inicio de la HD se buscó el objetivo de peso seco retirando, progresivamente, la medicación antihipertensiva (MHTA)16,17 y asociando las tasas de UF necesarias para conseguir descensos de 0,5 kg a 1 kg respecto del peso previo sin superar, en términos generales, pérdidas superiores al 3 % del peso al inicio de la HD18.
El objetivo de peso seco era evaluado tras cada sesión de HD, durante el tiempo requerido para su estabilización con retirada de la MHTA; una vez conseguido, se revaluaba semanalmente en cada paciente.
5. Los objetivos de presión arterial sistólica (PAS) se definieron individualmente según la edad y la comorbilidad.
El perfil ideal fue: PAS inicial ≤ 180 mmHg y final ≥ 120 mmHg19 con objetivo de que la media de presión arterial pre y post-HD no superara la cifra de 150, y en general, aquella PAS más baja que es bien tolerada durante la sesión20,21. Desde 2007 se limitó la UF a 10 ml/kg peso/hora22. Desde 2006 se registró la variación del volumen sanguíneo23on-line por hemoglobinometría de absorción óptica en cada sesión con objetivo de reducción horaria inferior al 5 %24.
6. Dosis de HD. 2000-2005. Estándar Kt/V ≥ 2. Desde 2006, Kt por dialisancia iónica25 en cada sesión, con seguimiento on-line y objetivo mínimo según la superficie corporal26, con media de 47 para HD 5 h x 3 y 41 (47 x 13/15) para EODD27. El tiempo de las sesiones se cumplía independientemente del logro anticipado del objetivo mínimo.
7. El programa contenía el protocolo de seguimiento analítico, de control de anemia con eritropoyetina alfa/beta intravenosa y hierro intravenoso, control de calcio, fósforo, hormona paratiroidea, mediante quelantes de fósforo, análogos de la vitamina D y, desde 2007, con cinacalcet.
Toda la información se registró en las bases de datos informáticas de la unidad de HD. Se recogieron variables demográficas, como sexo, edad al inicio de la HD, antecedentes de EFCV, ICh, permanencia en HD, estado final y causa del fallecimiento, así como parámetros de las sesiones, indicadores clínicos y analíticos. Para analizar los resultados de la aplicación de la estrategia de HD no convencional en nuestra población, aplicamos el método estadístico para medidas de tendencia central y dispersión (medias ± desviación estándar) para variables cuantitativas y frecuencias para variables cualitativas. Significación estadística para valores de p < 0,05. Para estadística inferencial, comparación de datos mediante test de Χ2 y t-Student según tipos de variables, determinación de riesgos e intervalos de confianzas (IC) al 95 %, curvas de supervivencia de Kaplan-Meyer y test de log-rank para comparación de curvas.
RESULTADOS
Del total de los 183 pacientes, 84 se dializaron en esquema HD 5 h x 3 y 99 en esquema EODD.
En la tabla 1 se reflejan los datos basales de los pacientes asignados a los dos esquemas. La edad y la comorbilidad (DM, EFCV, ICh) de los pacientes en EODD eran superiores, con diferencias significativas, respecto de los pacientes en HD 5 h x 3, conforme a los criterios de riesgo para la asignación a uno u otro esquema no convencional.
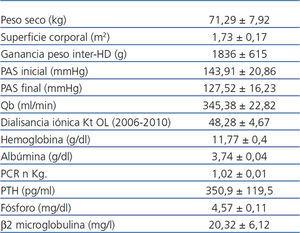
La tabla 2 muestra parámetros clínicos y analíticos del conjunto de pacientes. Solo un paciente requirió cirugía paratiroidea por adenoma refractario; ningún paciente presentó sintomatología de síndrome del túnel carpiano.
Al iniciar la HD, 135 de los 183 pacientes tomaban MHTA (74 %), que se pudo retirar en 126 (93 %) durante el período de seguimiento. En 8 pacientes no se alcanzó un peso seco estable por exceso de ingesta hidrosalina, aunque se redujo el número de fármacos, y un paciente presentaba elevación de la PAS no dependiente de volumen.
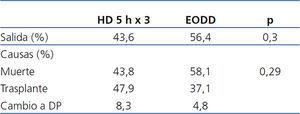
Las causas principales de salida fueron la muerte y el trasplante renal (51,8 % y 41,8 %, respectivamente). El resto (6,4 %) cambió a diálisis peritoneal. Entre las causas de muerte, la principal fue cardiovascular (42,9 %), seguida de infecciosas (21,4 %), cáncer (17,9 %) y otras/no determinadas (17,9 %). La tabla 3 muestra la comparación de las causas de salida entre los dos esquemas. No existen diferencias significativas. La mortalidad de causa cardiovascular fue similar en los dos esquemas de HD.
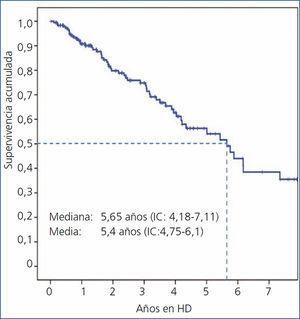
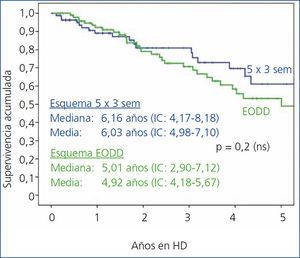
La curva de supervivencia global de los pacientes se muestra en la figura 1. Presenta una mediana de 5,6 años (IC 4,18-7,11) y una media de 5,4 (IC 4,75-6,1). Esta supervivencia resultado de la estrategia de HD no convencional era independiente de cuál de los dos esquema se utilizó (figura 2), ya que en ambos se mantiene este pronóstico para la vida del paciente (HD 5 h x 3: mediana 6,16 años: IC 4,17-8,18; media 6,03: IC 4,98-7,10. EODD: mediana 5,01 años: IC 2,9-7,12; media 4,92: IC 4,18-5,67), aunque las características basales eran distintas, como los criterios de asignación para uno u otro esquema dentro del protocolo.
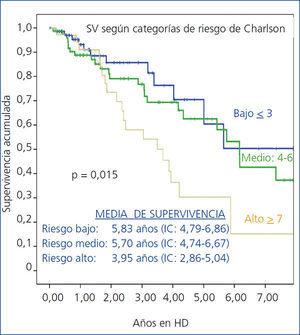
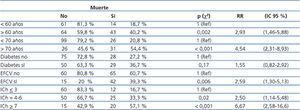
El análisis de los factores de riesgo para muerte (tabla 4), mediante tablas de contingencia, Χ2 y riesgos relativos (con IC al 95 %), muestra que los principales riesgos para la supervivencia al inicio de la HD fueron: edad mayor de la media, ser mayor de 70 años, presencia de EFCV y categorías de riesgo medio (IC = 4-6) o alto (IC ≥ 7) del ICh. La presencia de DM al inicio no alcanzó significación (p = 0,17). Los factores significativos en el análisis de riesgos también lo eran en el análisis inferencial efectuado comparando las curvas de supervivencia (test de log-rank): destacamos la comparación de las categorías del ICh al inicio (figura 3).
DISCUSIÓN
Las características demográficas y de comorbilidad de nuestra población son similares a las registradas en nuestro entorno occidental28-30, mostrando una población incidente en HD cada vez más anciana, con mayor proporción de DM y más riesgo cardiovascular, factores todos ellos relacionados inversamente con la supervivencia en HD. Desde el año 2000, aplicamos en nuestros pacientes incidentes una estrategia de HD no convencional mediante procedimientos avalados por estudios previos con nivel de evidencia media y con incorporación de innovaciones tecnológicas, ya referenciadas en el método, con el objetivo de mejorar la supervivencia de nuestra población.
Nuestro estudio coincide con la mayoría en la causa de muerte cardiovascular como la más frecuente y en los principales riesgos al inicio de la técnica: edad mayor de la media, ser mayor de 70 años, antecedente de EFCV y categorías de riesgo medio o alto del ICh. La supervivencia en ambos esquemas no presentó diferencia significativa pese a que el grupo en EODD presentaba riesgos basales significativamente superiores.
Comparamos estos resultados con los de estudios recientes en poblaciones homologables en demografía y factores de riesgo (tabla 5). En España, el estudio con datos del Registro de Canarias de pacientes incidentes en HD, en el período 2006-2009, muestra que la supervivencia es inferior en un 17 % al cuarto año28 con respecto a nuestros resultados. En comparación con los datos (1997-2006) del último Registro Europeo, este tiene resultados inferiores en un 19 % a cinco años para el período 1997-2001, y un 13 % y 16 % inferior en los dos primeros años para el período 2001-200629. Los datos del Registro de Estados Unidos del período 2002-2004 también muestran una supervivencia inferior: 92 % frente a 78 % al primer año, 82 % frente a 63 % a los dos años y 55 % frente a 35 % a los cinco años30. También comparamos nuestros resultados con los de HD corta diaria (HD no convencional con una media de 13 horas semanales), estudio que muestra la supervivencia de 415 pacientes desde 1982 a 200531. En los 265 pacientes que seguían este protocolo en domicilio, la supervivencia a los cinco años era del 78 %, resultado excelente pero consecuencia de un sistema de difícil acceso para la población general en HD. Sin embargo, en relación con los 150 pacientes del grupo con sesiones en centro, nuestro resultado de supervivencia es ligeramente superior (55 % frente a 50 % al quinto año), pese a que nuestros pacientes presentaban peores indicadores de riesgo, con una edad media diez años mayor, y duplicaban la frecuencia de DM.
Nuestros resultados de supervivencia son inferiores a los de otras experiencias anteriores de HD no convencional a causa, principalmente, de las diferencias existentes en las características de los grupos de pacientes. El grupo de Tassin1 comunicaba, hace más de veinte años, los resultados de una estrategia que combinaba un excelente control del VEC y dosis de diálisis, mediante un esquema de tres sesiones semanales de 8 horas con dializador de celulosa y con un seguimiento estricto del control del peso seco y la PAS sin necesidad de MHTA. El resultado de supervivencia fue del 80 % a los cinco años y del 75 % a los diez años. Sin embargo, la presencia de factores de riesgo de los pacientes que iniciaban esa técnica eran muy diferentes de las poblaciones incidentes en HD en los estudios del siglo XXI: edad media de 48 años, con otros factores de riesgo en solo el 20 %. Otras experiencias de HD no convencional, como la HD larga nocturna diaria, presentan excelentes resultados3, pero por la selección de sus poblaciones, menor edad, factores de riesgo y escasas posibilidades de implantación general no son comparables.
El esquema EODD empleado en nuestros pacientes de riesgo medio/alto se basa en el trabajo publicado en 1998 por Mastrangelo et al.4 (utilizado como variante de su otro esquema de cuatro sesiones semanales) en sus pacientes con superficie corporal inferior a 1,55 m2, si bien nosotros no ajustamos para superficie corporal y mantuvimos cuatro horas de sesión aunque se alcanzara el objetivo mínimo de dosis. La HD no convencional de Lecce obtuvo una excelente supervivencia del 75 % a los cinco años, pero sobre una población de incidentes en HD muy diferente a la actual en factores de riesgo: edad media de 48 años, 22 % de mayores de 60 años, 6 % de mayores de 70 años y 37,5 % con riesgo alto. Posteriormente el esquema EODD ha sido aplicado en Estados Unidos con base en su buen control del VEC32.
Nuestra estrategia de HD contiene protocolos con sistemas de mayor biocompatibilidad, HD de alto flujo, aumento del 25 % del tiempo de las sesiones, objetivo de peso seco tras retirar MHTA y perfil de PAS individualizado. Posteriormente, desde 2003, implantamos el esquema alternativo de EODD en pacientes de riesgo medio y alto. La introducción de biosensores on-line permitió cambiar el método para evaluar la dosis y mejorar la tolerancia hemodinámica. Analizamos el papel que estos protocolos pueden representar en nuestros resultados.
Aumento de la frecuencia y el tiempo de las sesiones. Control del volumen extracelular y dosis de hemodiálisis
La comunicación en 1999 del aumento significativo de la mortalidad en HD tras el fin de semana33 ha sido reforzada recientemente para todas las causas de muerte y especialmente la cardíaca34 en pacientes con esquema de HD convencional. El esquema EODD anula el período «no fisiológico» de 72 horas35 de expansión del VEC, permite tasas de UF adecuadas, control de las cifras de PAS36 y mejora la tolerancia de las sesiones37. La aplicación de este protocolo en nuestro grupo de pacientes con EFCV o ICh medio-alto asignado a EODD puede justificar un grado importante de sus resultados de supervivencia, confirmando la influencia negativa de permanecer 72 horas sin HD en pacientes con riesgo elevado y EFCV en régimen de HD convencional. Aunque el esquema de HD 5 h x 3 mantuvo el fin de semana sin HD para el grupo con menor riesgo, el aumento del tiempo por sesión permitía mantener el peso seco al final de la semana y su recuperación al inicio de la siguiente, asegurando la estabilidad del VEC.
El estudio DOPPS del año 2006 señala una reducción del 7 % en el riesgo relativo de muerte (RR) por cada 30 minutos de aumento del tiempo de la sesión, una asociación protectora entre tiempo más dosis, y mayor riesgo de muerte cuando se emplean tasas de UF > 10 ml/hora/kg peso22. Esta necesidad de adecuar la UF a la capacidad de relleno vascular del paciente ha sido confirmada para UF > 12 ml/hora/kg peso38. Los datos del año 2006 del Registro de Australia y Nueva Zelanda corroboran la disminución de mortalidad para sesiones de 4,5 a 5 horas39. Con respecto al esquema convencional de HD, aumentamos el tiempo de las sesiones, un 20 % en HD 5 h x 3 y un 17 % a la semana en EODD con un doble efecto sobre la depuración de moléculas y la reducción de la tasa de UF. Esto ha facilitado conseguir el objetivo de peso seco con buena tolerancia hemodinámica: el 93 % de nuestros pacientes alcanzaron el peso seco suspendiendo la MHTA; además mantuvieron un perfil de presión arterial adecuado al objetivo individual, sin ajustarse a las recomendaciones de la K/DOQI, cuyos objetivos de PAS se cuestionan por su relación inversa con la supervivencia40. Los resultados del estudio de Myers confirman la relevancia de este objetivo en mantener cifras de PAS adecuadas en pacientes en HD de mayor edad41.
A mitad de la década cambiamos el referente de dosis de diálisis basado en estándar Kt/V, abandonando el volumen de distribución de urea para referir el objetivo de Kt a la superficie corporal con seguimiento on-line26. El Kt medio obtenido por sesión (48,3) se corresponde al recomendado para la media de superficie corporal que presentaron nuestros pacientes (1,73 m2), aunque nunca se fijó dosis mínima para el fin de la sesión. Este cambio, además de beneficiar a los pacientes de menor superficie corporal, permitió seguir y analizar la dosis on-line en cada sesión, en lugar de una vez al mes, posibilitando correcciones inmediatas para mejorarla con un balance muy positivo en el control de su evolución.
Biocompatibilidad y hemodiálisis de alto flujo
Todos nuestros pacientes iniciaron en 2000 HD biocompatible con membranas de alto flujo para depurar Beta-2-microglobulina (β2-m), aunque, como ya ha sido señalado, resulta difícil establecer el grado de mejora en morbilidad o supervivencia que se pueda atribuir a cada variable42. Estudios posteriores al año 2000 las relacionan con mayor supervivencia respecto a la HD convencional. En la comunicación inicial del estudio Hemo43, la HD de alto flujo solo mejoraba ligeramente, sin significación estadística, la mortalidad respecto a la HD de bajo flujo, aunque los análisis secundarios mostraban una reducción significativa en los pacientes con permanencia en HD superior a 3,7 años y de la mortalidad de causa cardíaca44; además, reflejaba el valor predictivo de RR de muerte de los niveles de β2-m, así como la asociación de sus niveles más bajos con la HD de alto flujo45. Nuestros pacientes presentaban un nivel medio pre-HD de β2-m de 20,32 mg/l, inferior al nivel del grupo de alto flujo del estudio de Cheung et al. En la agrupación de nuestros pacientes prevalentes en 2010, según los grupos de riesgo de muerte en función de los niveles de β2-m, el 93 % de ellos se encuadraban en el grupo con nivel de menor riesgo (< 27,5 mg/l); esto podría explicarse porque nuestra población inició y permaneció todo el período en HD de alto flujo, con alto aclaramiento de β2-m y, además, con aumento del tiempo y la frecuencia de sesiones respecto al esquema convencional del estudio Hemo; apoya este argumento la nula incidencia del síndrome del túnel carpiano secundario a amiloidosis de HD en nuestros pacientes durante la década del estudio. Posteriormente, el estudio MPO (Membrane Permeability Outcome study), realizado sobre pacientes incidentes46, muestra la correlación positiva, con nivel alto de evidencia, entre supervivencia y HD de alto flujo en pacientes con nivel de albúmina sérica menor de 4 g/dl y, en análisis secundario, en DM. En consecuencia la Guía EDTA, en 2010, modificó el nivel de recomendación para la indicación de HD de alto flujo, elevándolo al grado máximo en pacientes con albúmina menor de 4 g/dl y de grado B para DM47, recomendando su uso generalizado en pacientes por razones de coste/eficiencia.
En nuestros pacientes hemos considerado la DM como diagnóstico previo y factor de riesgo real en ICh, independientemente de la causa de la nefropatía. En contraposición a muchos estudios, la presencia de DM como factor de comorbilidad al inicio de la HD, fuera o no causa de la nefropatía, no alcanzó diferencia significativa respecto a la no existencia de DM como factor de riesgo de muerte. Una posible explicación sería atribuirlo al efecto positivo y de sinergia que aporta la HD de alto flujo en DM asociado con prolongadas permanencias en esta técnica y sesiones de más duración.
Durante el período 2000-2010, diversos estudios han reforzado el nivel inicial de evidencia de cada actuación en que se basó nuestro sistema, aunque nuestro estudio tiene la limitación de que, al aplicarse conjuntamente, es difícil atribuir el grado de aportación de cada medida al resultado de supervivencia.
En conclusión, los sistemas de HD no convencional que aplicamos constituyen una alternativa viable de HD en centro y, aunque tienen un coste económico adicional, generan un ahorro importante en MHTA, hospitalización y en la práctica desaparición de sesiones de HD urgentes no programadas generadas por sobrehidratación. Nuestra estrategia de HD consiguió una buena supervivencia en nuestra población incidente y este resultado se relaciona, posiblemente, con la influencia conjunta y sinérgica de los protocolos aplicados dentro de la estrategia no convencional de HD.
Agradecimientos
Agradecemos al profesor Evaristo Fernández Ruiz su estímulo y apoyo a la innovación en diálisis desde 1975.
Conflictos de interés
Los autores declaran que no tienen conflictos de interés potenciales relacionados con los contenidos de este artículo.
Figura 1. Supervivencia global
Figura 2. Supervivencia según esquema de hemodiálisis
Figura 3. Supervivencia según índice de Charlson
Tabla 2. Datos clínicos y analíticos durante el período del total de pacientes: media ± desviación estándar
Tabla 1. Datos demográficos y clínicos del total de pacientes incidentes y su agrupación según esquema de hemodiálisis
Tabla 3. Causas de salida y muerte según esquema de hemodiálisis
Tabla 4. Análisis de los factores de riesgo para la muerte: número y porcentaje
Tabla 5. Supervivencia global (%)