La leucemia mieloide crónica (LMC) es una enfermedad mieloproliferativa caracterizada por la expansión clonal de células mieloides que expresan la proteína de fusión BCR-ABL, responsable de los efectos oncogénicos de la LMC. La terapia actual en el tratamiento de LMC es el inhibidor de la BCR-ABL tirosín-kinasa, imatinib. Aunque este fármaco ha demostrado mejorar la supervivencia en pacientes con LMC, su papel en el contexto del trasplante renal no ha sido ampliamente descrito en la literatura. Presentamos un caso de remisión molecular de LMC en un varón de 55 años con un segundo trasplante renal, hepatitis C y con riesgos cardiovasculares e inmunológicos asociados.
INTRODUCCIÓN
La leucemia mieloide crónica (LMC) es una enfermedad mieloproliferativa caracterizada por la expansión clonal de células mieloides1. La anomalía citogenética patognomónica de la LMC es el cromosoma de Filadelfia2 que se produce por la translocación recíproca de los brazos largos de los cromosomas 9 y 223. Esta translocación genera la proteína de fusión BCR-ABL, responsable de los efectos oncogénicos en la LMC.
En la literatura se ha descrito el uso de imatinib (Gleevec, Novartis), un inhibidor de la BCR-ABL tirosín-kinasa en el tratamiento de LMC, en el trasplante renal en sólo dos ocasiones4,5, pero en ningún caso en un paciente con un segundo trasplante, con hepatitis C y con alto riesgo cardiovascular e inmunológico.
CASO CLÍNICO
Varón de 55 años que desarrolla LMC en fase crónica tras su segundo trasplante renal. El paciente entra en hemodiálisis debido a una glomerulonefritis mesangiocapilar en 1976, a los 24 años, y recibe un trasplante renal de donante vivo en 1983. La inmunosupresión consiste de azatioprina y esteroides. En 1989, seis años después de su primer trasplante, sufre un infarto agudo de miocardio. Dos años después, vuelve a entrar en hemodiálisis por rechazo crónico del injerto.
En 1994, a los 42 años, el paciente recibe un segundo trasplante renal de una donante de 44 años. La donante y receptor comparten tres alelos HLA (HLA A3, B8 y DR3). El panel de anticuerpos reactivos (PRA) es del 29%, probablemente con relación a varias transfusiones sanguíneas durante el curso intraoperatorio del primer trasplante y el injerto en sí. La inmunosupresión inicial tras el segundo trasplante consiste en esteroides (0,5 mg/kg/día), azatioprina (2 mg/kg/día) y ciclosporina (CyA) (10 mg/día).
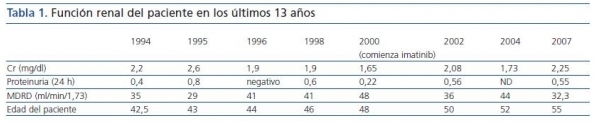
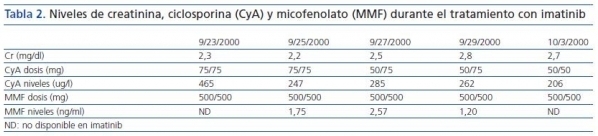
Postrasplante, el paciente desarrolla necrosis tubular aguda posisquémica, requiriendo dos intervenciones quirúrgicas posteriores un mes después de su trasplante para corregir una fístula urinaria. En el momento de la intervención quirúrgica, se realiza una biopsia renal que objetiva un rechazo agudo grado 1 que se trata con terapia de rescate con esteroides (1 g en cuatro dosis). Dos años después, debido al empeoramiento de la función renal con CyA, el tratamiento con azatioprina se sustituye por micofenolato (tabla 1 y tabla 2).
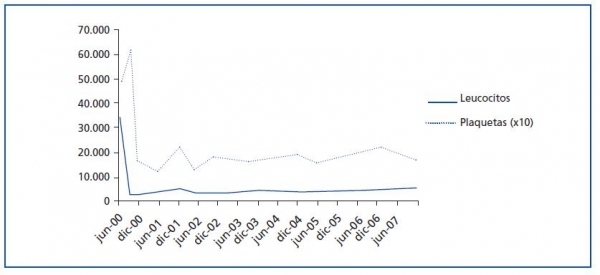
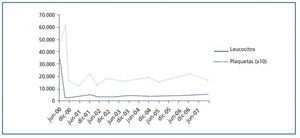
El seguimiento del paciente es satisfactorio hasta junio de 2000, cuando se descubre en una analítica de control una importante leucocitosis (34,5 x 109/l) y trombocitosis (487 x 109/l) (figura 1). El paciente refiere dolor bilateral de cadera, pero por lo demás está asintomático. La exploración es normal y el paciente no tiene esplenomegalia ni hepatomegalia.
La resonancia magnética de la cadera objetivó afectación difusa de la médula ósea de prácticamente todos los huesos. La aspiración y el trepanado de médula ósea confirman hiperplasia granulocítica y megacariocítica compatible con LMC. No se describe fibrosis en la médula ósea y el paciente se clasifica como de bajo riesgo en el índice de Sokal.
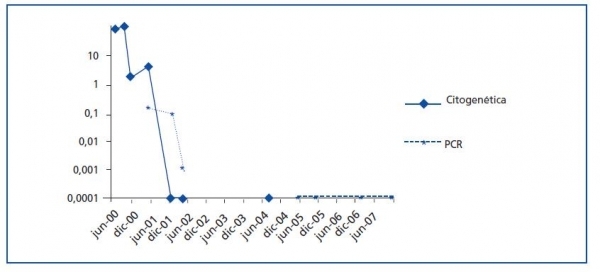
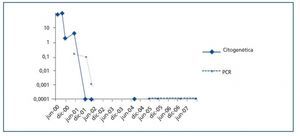
La presencia del cromosoma de Filadelfia (46XY t[9;22][q34;q11]) se detectó por análisis de cariotipo de la médula ósea. Posteriores estudios moleculares citogenéticos con hibridación in situ fluorescente (FISH) demostraron la presencia del gen de fusión BCR-ABL en el 90% de los núcleos. La RT-PCR confirmó la presencia típica del reordenamiento de p210 BCRABL con el transcrito de fusión b2a2. Durante dos meses, se trató al paciente con hidroxiurea, sin ningún beneficio. En septiembre de ese año, el paciente entra en el ensayo clínico de Novartis STI571-0113, y recibe 400 mg diarios de imatinib con buena tolerancia al fármaco, sin ningún efecto adverso. Obtiene remisión hematológica completa, remisión citogenética completa, y remisión molecular mantenida a los dos, seis y nueve meses, respectivamente, que persiste al día de hoy (figura 2). Catorce años después de su segundo trasplante, el paciente mantiene una función renal aceptable (estadio III de enfermedad renal crónica) y no ha experimentado rechazo agudo, empeoramiento de la función hepática o nuevos eventos cardiovasculares (tabla 1).
DISCUSIÓN
Este caso demuestra que el imatinib es un fármaco seguro y eficaz en el tratamiento de LMC en el paciente trasplantado renal.Nuestro paciente respondió de una forma rápida al tratamiento, con normalización en sangre periférica y médula ósea en los dos primeros meses y remisión citogenética y molecular durante el primer año de tratamiento. Estos resultados concuerdan con los del estudio IRIS1, que demostró una respuesta citogenética completa en el 89% de los pacientes con un índice de Sokal bajo, y una supervivencia del 83%. Finalmente, este estudio, al igual que en el caso de nuestro paciente, demuestra que una respuesta citogenética y molecular temprana está asociada con una mejor evolución a largo plazo y un menor riesgo de progresión a la fase acelerada o crisis blástica6.
El uso de imatinib en este paciente puede que también haya tenido un efecto inmunosupresor benéfico en el injerto renal, tal como sugieren recientes estudios in vitro y en modelos animales que han demostrado que este fármaco puede tener efectos inmunomoduladores. Appel et al. demostraron que el imatinib puede inhibir la diferenciación de células progenitoras CD34+ en sangre periférica en células dendríticas (CD). Además, la activación de células T se puede ver inhibida, ya que la secreción de citocinas y quimiocinas por CD disminuye7. El imatinib también inhibe el desarrollo de monocitos y macrófagos de progenitores de médula ósea8. Finalmente, Dietz et al. demostraron que el imatinib puede inhibir la proliferación de células T deteniendo la proliferación de linfocitos en la fase G09.
Algunos estudios sugieren que el imatinib puede causar fallo renal por necrosis tubular aguda en presencia de ciclosporina10,11. A pesar de recibir ambos fármacos, la función renal de nuestro paciente permaneció estable desde el momento de inicio de la terapia con imatinib. La creatinina osciló entre 1,75 y 2,4 mg/dl con niveles bajos de proteinuria (proteinuria máxima fue de 0,56 g/dl) (tabla 1).
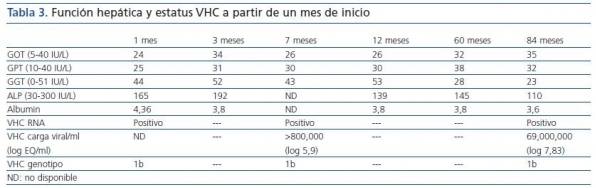
También se han descrito efectos hepáticos secundarios graves, incluyendo fallo hepático fulminante asociado al tratamiento con imatinib12-15. Nuestro paciente, que era VHC positivo, no tuvo ningún tipo de alteración en su función hepática durante el tratamiento. Ésta siempre estuvo dentro de los rangos de normalidad, a pesar de tener RNA VHC detectable en suero, como suele ocurrir con la mayoría de los pacientes con VHC tras un trasplante16 (tabla 3).
El imatinib, según el fabricante, puede tener efectos adversos en pacientes cardíacos por el riesgo de insuficiencia cardíaca. Nuestro paciente, que sufrió un infarto de miocardio con 37 años, no ha tenido ningún efecto adverso y este año ha tenido una prueba de esfuerzo cardíaco normal.
En conclusión, el imatinib es un tratamiento seguro y eficaz en pacientes trasplantados renales con LMC. Además, estudios in vitro y en animales sugieren que el fármaco puede tener efectos inmunomoduladores que pueden ser beneficiosos en el contexto de un trasplante.
Figura 1.
Figura 2.
Tabla 1.
Tabla 2.
Tabla 3.