El efecto renoprotector de los fármacos inhibidores del sistema renina-angiotensina (ISRA) ha sido cuestionado en la enfermedad renal crónica (ERC) avanzada. La combinación de tratamiento ISRA (doble bloqueo) puede, además, acelerar el deterioro de la función renal en algunas poblaciones de riesgo. Sin embargo, se desconoce si este efecto adverso está relacionado con la dosis total prescrita de ISRA o más específicamente con una interacción farmacológica.
ObjetivoInvestigar si la tasa de reducción de función renal en la ERC avanzada se asocia a la dosis total de ISRA, y si el doble bloqueo SRA deteriora la función renal independientemente de los principales factores de confusión.
Material y métodosEstudio retrospectivo de observación en una cohorte de pacientes adultos con ERC estadios 4-5 prediálisis, tratados con ISRA desde al menos 3 meses antes de la inclusión en el estudio. Otros criterios de inclusión fueron: tener al menos 3 medidas consecutivas de filtrado glomerular durante un periodo superior a 3 meses. Las dosis equipotentes de ISRA fueron normalizadas (DEN-ISRA) a un peso corporal de 70kg o a una superficie corporal de 1,73m2. La asociación de DEN-ISRA o doble bloqueo con la progresión de ERC fue analizada mediante modelos de regresión lineal uni- y multivariante, tomando en cuenta las principales variables de confusión.
ResultadosSe incluyeron 813 pacientes (edad media: 64±14 años; 430 hombres) con un filtrado glomerular medio de 14,9±4,2ml/min/1,73m2; 729 pacientes eran tratados con ISRA monoterapia y 84 pacientes con doble bloqueo. La mediana de la DEN-ISRA en el grupo total de estudio fue de 0,91 (rangos IQ: 0,69-1,20). Los pacientes con doble bloqueo tenían una DEN-ISRA significativamente mayor que el resto (1,52±0,49 vs. 0,93±0,44; p<0,0001). Mediante regresión lineal univariable, DEN-ISRA se correlacionó significativamente con la tasa de progresión de la ERC (R=−0,149; p<0,0001). Los pacientes con doble bloqueo mostraron un deterioro más acelerado de la función renal que el resto (−6,19±5,57 vs. −3,04±5,37ml/min/1,73m2/año, p<0,0001). Mediante regresión lineal multivariante, el tratamiento con doble bloqueo SRA mantuvo la asociación significativa e independiente con el deterioro de la función renal (beta=−0,094; p=0,005), mientras que la DEN-ISRA no alcanzó significación estadística.
ConclusiónLa DEN-ISRA se asocia de forma significativa con la tasa de progresión en pacientes con ERC avanzada. Sin embargo, el efecto negativo del doble bloqueo SRA sobre la progresión de la ERC parece independiente de la DEN-ISRA y de otros factores relevantes de confusión.
The renoprotective effect of renin-angiotensin (RAS) blockers (angiotensin converting enzyme inhibitors and angiotensin receptor blockers) has been questioned in patients with advanced chronic kidney disease (CKD). Moreover, combination therapy (dual RAS blockade) can further accelerate renal function decline in some populations at risk. However, it is unknown whether this adverse outcome is due to a dose-dependent effect or if it can be attributed more specifically to a drug interaction.
Aim This study aims to investigate if the rate of renal function decline in advanced CKD patients is associated to the doses of RAS blockers, and if dual RAS blockade worsens renal function independently of major confounding factors.
Material and methodsRetrospective, observational study in an incident cohort of adult patients with CKD stage 4 or 5 not on dialysis, treated with RAS blockers for at least 3 months prior to the study inclusion. Inclusion criteria were: having at least three consecutive measurements of estimated glomerular filtration rate (eGFR) in a follow-up period >3 months. Decline in renal function was estimated as the slope of the individual linear regression line of eGFR over follow-up time. Equipotent doses of RAS blockers were normalised for a body weight of 70kg or a body surface area of 1.73m2 (END-RASI). Associations of END-RASI or dual RAS blockade with the rate of renal function decline were analysed by uni- or multivariate linear regression models, accounting for major confounding variables.
ResultsThe study group consisted of 813 patients (mean age 64±14 years, 430 males) with a mean eGFR 14.9±4.2ml/min/1.73m2; 729 patients were on RAS blockade monotherapy and 84 on dual RAS blockade. Median END-RASI in the whole group was 0.91 (I.Q. ranges: 0.69-1.20). Patients on dual RAS blockade had significantly higher END-RASI than the rest of study patients (1.52±0.49 vs. 0.93±0.44; p<0.0001). In univariate linear regression, END-RASI were significantly correlated with eGFR decline (R=−0.149; p<0.0001). Patients on dual RAS blockade showed a significantly faster decline of renal function than the rest of the study patients (−6.19±5.57 vs. −3.04±5.37ml/min/1.73m2/year, p<0.0001). By multivariate linear regression, while dual RAS blockade remained independent and significantly associated with faster renal function decline (beta=−0.094; p=0.005), END-RASI (normalised either for body weight or surface area) did not reach statistical significance.
ConclusionEND-RASI are significantly associated with the rate of renal function decline in advanced CKD patients. However, the detrimental effect of dual RAS blockade on CKD progression seems to be independent of END-RASI and other major confounding factors.
Los fármacos inhibidores del sistema renina-angiotensina (ISRA) han sido durante las últimas décadas el principal recurso terapéutico para intentar frenar o enlentecer la progresión de la enfermedad renal crónica (ERC) de diversas etiologías1-4. Tanto a los inhibidores del enzima de conversión de la angiotensina (IECA) como a los antagonistas de los receptores de la angiotensina II (ARA), además del efecto sobre el control de la presión arterial, también se les han atribuido otros beneficios: hemodinámicos, antiproteinúricos, pleiotrópicos (antifibrogénicos, etc.) que podrían justificar el calificativo de «renoprotectores»1-5.
Estos efectos favorables sobre la progresión de la ERC han sido demostrados basándose en rigurosos estudios en animales de experimentación y en numerosos ensayos clínicos, bien resumidos en la revisión de Čertíková Chábová y Červenka6. Tales resultados apoyaban de forma tan firme el control sobre el sistema renina-angiotensina (SRA) que durante la primera década del presente siglo se propuso elevar al máximo las dosis de estos fármacos e incluso combinarlos (doble bloqueo SRA con IECA más ARA), persiguiendo objetivos terapéuticos más allá del estricto control de la presión arterial, como por ejemplo la reducción de la proteinuria5.
Aunque unas dosis elevadas de ISRA e incluso el doble bloqueo han demostrado ser beneficiosos en la evolución y supervivencia de algunas enfermedades cardiovasculares3,7-9, la frecuente asociación con deterioros acelerados de la función renal y desarrollo de otros efectos adversos han ido cuestionando la idoneidad de esta estrategia de tratamiento en la ERC, y especialmente en algunas nefropatías como la diabética, o en pacientes con ERC avanzada6,10-14. Así, han surgido numerosas opiniones contrarias al uso generalizado de estos fármacos en la ERC15-22, creándose una controversia clínico-terapéutica que merece ser investigada.
Nosotros hemos observado en pacientes con ERC avanzada que el doble bloqueo SRA se asocia con una progresión más acelerada de la insuficiencia renal23. Otro dato importante de estas observaciones previas es la gran heterogeneidad en las dosis que se prescriben de los ISRA ajustadas a peso o superficie corporal. Así, las cuestiones que estos datos nos estimularon a plantear son: ¿existe una asociación entre la dosis total ajustada de ISRA y la progresión de la ERC avanzada?, y ¿el efecto negativo del doble bloqueo SRA sobre la progresión de la ERC podría estar justificado por una dosis total elevada de ISRA o es independiente de esta y de otros factores importantes de confusión?
Con el objetivo de analizar estas cuestiones se realizó el presente estudio de observación en una cohorte de pacientes con ERC avanzada tratados con ISRA.
Material y métodosEstudio retrospectivo de observación longitudinal en una cohorte de pacientes adultos diagnosticados de ERC estadios 4-5 no en diálisis, seguidos en la consulta de ERC avanzada (ERCA) durante el periodo comprendido entre enero de 2000 y diciembre de 2016. Los criterios de selección fueron: haber sido seguidos en la consulta ERCA durante un periodo superior a 3 meses; haber realizado durante este tiempo al menos 3 mediciones de la función renal; y estar siendo tratado con ISRA durante un mínimo de 3 meses antes de su inclusión en el estudio.
Todos los pacientes fueron remitidos a la consulta ERCA por deterioro progresivo de la función renal. Los datos demográficos, clínicos, y medicación prescrita se obtuvieron de las historias clínicas, exploración física y anamnesis. La comorbilidad fue evaluada en el momento de la inclusión, utilizando el índice de Davies24, y los pacientes fueron categorizados en 3 grupos: sin comorbilidad, leve-moderada, o grave.
Todos las muestras y análisis bioquímicos se extrajeron y realizaron en un mismo laboratorio central (Servicio de Análisis Clínicos del Hospital Infanta Cristina) por métodos convencionales (Autoanalizador Advia Chemistry, Siemens Healthcare Diagnostics, Nueva York, EE.UU.), en muestras frescas (no almacenadas), y tanto las calibraciones como la trazabilidad de la creatinina se realizaron conforme a las recomendaciones de estándares internacionales NKDEP25. El filtrado glomerular fue estimado mediante la fórmula abreviada MDRD26.
Los pacientes fueron seguidos de forma ininterrumpida con revisiones cada 30 a 90 días. Para determinar la velocidad de progresión de la ERC se realizó en cada paciente una regresión lineal entre el filtrado glomerular estimado en cada control y el tiempo transcurrido desde la primera cita, con una precisión de días. La pendiente resultante de esta ecuación lineal se expresó en ±ml/min/1,73m2/año, teniendo los valores negativos o positivos de este parámetro los significados de progresión de la insuficiencia renal o recuperación de la función renal basal, respectivamente.
La valoración de la potencia comparada de ISRA (dosis equipotente) de cada uno de los fármacos utilizados en estos pacientes se estimó siguiendo las recomendaciones de prescripción de los laboratorios fabricantes sobre dosis diaria para el control de la presión arterial en adultos y recogida en los boletines de la Agencia Española del Medicamento y Productos Sanitarios (AEMPS) según se detalla en la tabla 1.
Dosis diaria equipotente de los inhibidores del sistema renina-angiotensina utilizados en este estudio. Cada una de estas dosis se tomó como unidad terapéutica antes de ajustarse al peso o a la superficie corporal
| Inhibidores enzima conversión angiotensina | Dosis/24h (mg) | Antagonistas receptores angiotensina II | Dosis/24h (mg) |
|---|---|---|---|
| Captopril | 150 | Losartán | 100 |
| Enalapril | 20 | Valsartán | 160 |
| Fosinopril | 20 | Candesartán | 16 |
| Quinapril | 40 | Olmesartán | 40 |
| Trandolapril | 4 | Telmisartán | 80 |
| Ramipril | 10 | Irbesartán | 300 |
| Lisinopril | 20 | Eprosartán | 600 |
| Perindopril | 8 |
Cada una de estas dosis diarias se consideró como unidad terapéutica de potencia similar (equipotente), que se sumó en tratamientos combinados, y se normalizó a un peso corporal de 70kg o una superficie corporal de 1,73m2, estableciendo el parámetro dosis equipotente normalizada (DEN). Por ejemplo, un paciente con un peso corporal de 70kg que tomaba 20mg de enalapril o 160mg de valsartán o 16mg de candesartán diario tenía una DEN de 1. Si estas mismas dosis se prescribieron a un paciente con un peso de 100kg, la DEN resultante fue de 0,7; y si se prescribieron a un paciente con 50kg, la DEN resultante fue de 1,4. Si se combinaron tratamientos (doble bloqueo), por ejemplo 20mg de enalapril y 16mg de candesartán en un paciente de 70kg, la DEN resultante fue de 2, y así sucesivamente.
Diseño del estudio y métodos estadísticosEstudio retrospectivo de observación longitudinal.
Se compararon las características demográficas, clínicas y bioquímicas de los pacientes tratados con monoterapia ISRA y doble bloqueo.
Se analizó el grado de correlación entre las dosis normalizadas de ISRA (DEN-ISRA) y la progresión de la ERC mediante correlación lineal uni- y multivariante, incluyendo como variables independientes, además de la DEN-ISRA: doble bloqueo ISRA, edad, sexo, índice de comorbilidad, índice de masa corporal, tabaquismo, diabetes mellitus, función renal inicial (basal), presión arterial (toma basal en consulta), proteinuria en orina de 24h, bicarbonato sérico, y tratamiento concomitante con diuréticos, betabloqueantes, y antagonistas de los canales de calcio. Para la selección de las variables con los mejores modelos de predicción se utilizó el proceso automático de eliminación progresiva condicional.
Para la comparación descriptiva de las variables continuas y dependiendo de sus características se utilizaron pruebas paramétricas o no paramétricas, y para las variables categóricas se utilizó la prueba chi-cuadrado.
Los datos estadísticos descriptivos se presentan como media y desviación estándar, o como mediana y rangos intercuartiles para las variables continuas, y como porcentajes para las variables categóricas. Una p<0,05 se consideró estadísticamente significativa, y todos los valores de p que se muestran son bilaterales. Los análisis estadísticos se realizaron con el software IBM SPSS Statistics 24.0 (IBM Corp. Armonk, EE.UU.).
ResultadosDurante el periodo de inclusión del estudio se atendieron un total de 1.580 pacientes incidentes en la consulta ERCA. Se incluyeron en el estudio 1.079 pacientes que cumplieron los criterios de tiempo de seguimiento. De estos, 813 cumplieron los criterios de estar en tratamiento con ISRA más de 3 meses antes de la inclusión, y fueron los que finalmente conformaron el grupo de estudio.
Las características demográficas, clínicas y bioquímicas del grupo total de estudio se muestran en la tabla 2.
Características demográficas, clínicas y bioquímicas en el grupo total de pacientes y según estuvieran siendo tratados con ISRA en monoterapia o con doble bloqueo
| Variable | Total | Monoterapia ISRA | Doble bloqueo ISRA | p |
|---|---|---|---|---|
| N pacientes, (%) | 813 | 729 (90) | 84 (10) | |
| Edad, años | 64 (14) | 64 (14) | 60 (14) | 0,008 |
| Sexo, hombre / mujer | 428 / 385 | 381 / 348 | 47 / 37 | 0,521 |
| Índice masa corporal, kg/m2 | 30,1 (5,9) | 29,9 (5,9) | 30,9 (5,9) | 0,166 |
| Índice comorbilidad Davies, (ausente / leve-moderado / grave) | 314 / 407 / 92 | 284 / 362 / 83 | 30 / 45 / 9 | 0,792 |
| Fumadores, (%) | 138 (17) | 121 (17) | 17 (20) | 0,400 |
| Diabetes mellitus, (%) | 327 (40) | 286 (39) | 41 (49) | 0,090 |
| Tiempo de seguimiento, meses | 15,7 [8,2-26,7] | 15,8 [8,3-27,3] | 13,3 [7,2-24,7] | 0,092 |
| Número determinaciones | 7 [5-12] | 8 [5-12] | 6 [4-9] | 0,002 |
| Filtrado glomerular basal (MDRD), ml/min/1,73m2 | 14,9 (4,2) | 14,9 (4,1) | 15,5 (4,7) | 0,207 |
| Presión arterial sistólica, mmHg | 160 (27) | 159 (26) | 168 (30) | 0,003 |
| Presión arterial diastólica, mmHg | 88 (14) | 88 (14) | 91 (16) | 0,063 |
| Proteinuria, g/g creatinina | 1,489 [0,563-3,024] | 1,323 [0,513-2,774) | 2,930 [1,666-4,319] | 0,000 |
| Pendiente filtrado glomerular, ml/min/1,73m2/año | −3,36 (5,48) | −3,03 (5,37) | −6,19 (5,57) | 0,000 |
| Dosis equipotente ISRA | 1,08 (0,53) | 1,01 (0,48) | 1,73 (0,46) | 0,000 |
| DEN-ISRA, normalizada peso corporal 70kg | 0,99 (0,48) | 0,93 (0,44) | 1,52 (0,49) | 0,000 |
| DEN-ISRA normalizada superficie corporal 1,73m2 | 1,03 (0,49) | 0,96 (0,44) | 1,61 (0,45) | 0,000 |
| Tratamiento diuréticos, (%) | 544 (67) | 485 (67) | 59 (70) | 0,494 |
| Tratamiento con betabloqueantes, (%) | 209 (26) | 189 (26) | 20 (24) | 0,674 |
| Tratamiento con antagonistas canales de calcio, (%) | 392 (48) | 343 (47) | 49 (58) | 0,050 |
Se muestran las desviaciones estándar de las variables continuas entre paréntesis, excepto tiempo de seguimiento, número de determinaciones y proteinuria (mediana y rangos intercuartiles).
DEN-ISRA: dosis equipotente normalizada de inhibidor sistema renina-angiotensina; ISRA: inhibidor sistema renina-angiotensina.
La edad media del grupo era de 64 años, con ligero predominio de hombres (53%) y una alta prevalencia de diabetes mellitus (40%). Otra de las características clínicas destacadas de este grupo era la presencia de nefropatías con proteinuria y presión arterial elevadas.
Un 90% de los pacientes tenían prescrito el ISRA en monoterapia, y la DEN a un peso de 70kg o a una superficie corporal de 1,73m2 fueron de 0,99 y 1,03, respectivamente.
Se observó una diferencia muy significativa en la tasa de progresión de la ERC entre los pacientes que recibían ISRA en monoterapia y los que tenían prescrito doble bloqueo ISRA (−3,03±5,37 vs. −6,19±5,57ml/min/1,73m2/año, p<0,0001).
Entre estos 2 subgrupos también existían algunas diferencias en las características clínicas, como la menor edad media, cifras más altas de presión arterial sistólica, y mayor proteinuria en el subgrupo tratado con doble bloqueo ISRA con respecto a los tratados con monoterapia (tabla 2).
Como era esperable, la DEN-ISRA del subgrupo tratado con doble bloqueo fue significativamente mayor que la de los tratados con monoterapia (1,52 ± 0,49 vs. 0,93 ± 0,44; p < 0,0001).
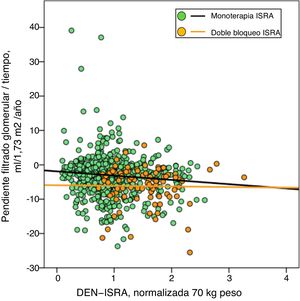
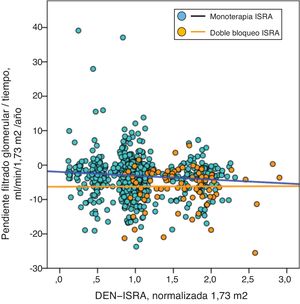
Se observó una correlación lineal significativa entre las DEN-ISRA y la pendiente de la relación filtrado glomerular/tiempo (progresión de la ERC), tanto si la normalización se realizó al peso corporal (fig. 1) como si fue a la superficie corporal (fig. 2).
Regresión lineal entre la pendiente de la relación filtrado glomerular (FG)/tiempo y la dosis equipotente normalizada (DEN) de inhibidores del sistema renina-angiotensina (ISRA) ajustada a peso de 70kg. Las rectas de regresión que aparecen en la figura son las correspondientes a los subgrupos con doble bloqueo y monoterapia, respectivamente.
La ecuación de regresión lineal conjunta fue: Pendiente FG (ml/min/1,73m2/año)=−1,672−(1,71×DEN-ISRA); R=−0,149; p<0,0001.
Para los pacientes en monoterapia: Pendiente FG/tiempo=−1,88−(1,24×DEN-ISRA); R=0,101; p=0,006.
Para los pacientes con doble bloqueo: Pendiente FG/tiempo=−5,93−(0,17×DEN-ISRA); R=0,015; p=0,89.
Regresión lineal entre la pendiente de la relación filtrado glomerular (FG)/tiempo y la dosis equipotente normalizada (DEN) de inhibidores del sistema renina-angiotensina (ISRA) ajustada a superficie corporal de 1,73m2. Las rectas de regresión que aparecen en la figura son las correspondientes a cada subgrupo con doble bloqueo y monoterapia, respectivamente.
La ecuación de regresión lineal conjunta fue: Pendiente FG (ml/min/1,73 m2/año)=−1,685−(1,659×DEN-ISRA); R=−0,145; p<0,0001.
Para los pacientes en monoterapia: Pendiente FG/tiempo=−1,959−(1,120×DEN-ISRA); R=0,093; p=0,012.
Para los pacientes con doble bloqueo: Pendiente FG/tiempo=−6,279−(0,053×DEN-ISRA); R=0,004; p=0,969.
También se observó que a igual DEN-ISRA, los pacientes tratados con doble bloqueo tenían una progresión más acelerada (figs. 1 y 2).
En el análisis multivariante de regresión lineal sobre las variables asociadas a la progresión de la ERC, el doble bloqueo ISRA seguía estando asociado independiente y significativamente con la variable de resultado (pendiente relación filtrado glomerular/tiempo), pero no así la DEN-ISRA, que perdió la significación estadística cuando esta relación se ajustó al resto de las variables independientes (tabla 3).
Análisis de regresión lineal multivariante sobre los factores asociados a la progresión de la enfermedad renal crónica (pendiente de la relación filtrado glomerular/tiempo)
| Univariable | Multivariante | |||||
|---|---|---|---|---|---|---|
| Variable | Coeficiente B (IC 95%) | Coeficiente beta | p | Coeficiente B (IC 95%) | Coeficiente beta | p |
| Edad, años | 0,025 (−0,005; 0,055) | 0,063 | 0,106 | 0,039 (0,012; 0,065) | 0,098 | 0,004 |
| Índice comorbilidad (0,1,2) | 0,252 (−0,467; 0,972) | 0,030 | 0,491 | |||
| Fumador, (0,1) | 0,308 (−0,668; 1,283) | 0,021 | 0,536 | |||
| Diabetes, (0,1) | −0,343 (−1,292; 0,605) | −0,031 | 0,477 | |||
| Índice masa corporal, kg/m2 | 0,038 (−0,028; 0,104) | 0,042 | 0,254 | |||
| Presión arterial sistólica, cmHg | −0,113 (−0,288; 0,063) | −0,055 | 0,208 | −0,218 (−0,356; −0,084) | −0,107 | 0,002 |
| Presión arterial diastólica, cmHg | −0,192 (−0,518; 0,134) | −0,055 | 0,207 | |||
| Filtrado glomerular basal, ml/min/1,73m2 | −0,095 (−0,182; −0,007) | −0,073 | 0,034 | −0,104 (−0,190; −0,018) | −0,080 | 0,018 |
| Proteinuria, g/g creatinina | −0,700 (−0,852; −0,548) | −0,315 | 0,0001 | −0,688 (−0,835; −0,541) | −0,310 | 0,0001 |
| Bicarbonato sérico basal, mEq/l | 0,167 (0,064; 0,270) | 0,109 | 0,001 | 0,164 (0,062; 0,265) | 0,107 | 0,002 |
| DEN-ISRA, normalizado 70kg peso corporal | −0,592 (−1,418; 0,234) | −0,052 | 0,160 | |||
| Doble bloqueo ISRA, (0,1) | −1,411 (−2,681; −0,141) | −0,078 | 0,029 | −1,699 (−2,878; −0,519) | −0,094 | 0,005 |
| Diuréticos, (0,1) | 0,374 (−0,409; 1,157) | 0,032 | 0,348 | |||
| Betabloqueantes, (0,1) | −0,838 (−1,679; 0,003) | −0,067 | 0,051 | |||
| Antagonistas canales de calcio (0,1) | −0,500 (−1,231; 0,230) | −0,046 | 0,179 | |||
| Constante | −2,206 (−6,251; 1,839) | −2,620 (−5,752; 0,512) | ||||
DEN-ISRA: dosis equipotente normalizada de inhibidor sistema renina-angiotensina; IC: intervalo de confianza; ISRA: inhibidor sistema renina-angiotensina.
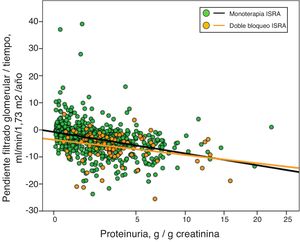
En la figura 3 se muestra la asociación entre proteinuria y progresión de la ERC, con las rectas de regresión correspondientes al subgrupo tratado con monoterapia o con doble bloqueo. Las diferencias más significativas entre los subgrupos se observaron en pacientes con proteinurias inferiores a 5g/día.
Regresión lineal entre la pendiente de la relación filtrado glomerular (FG)/tiempo y proteinuria. Las rectas de regresión que aparecen en la figura son las correspondientes a cada subgrupo con doble bloqueo y monoterapia, respectivamente. El eje Y está representado con una escala exponencial 0,5.
La ecuación de regresión lineal conjunta fue: Pendiente FG (ml/min/1,73m2/año)=−1,720−(0,739×proteinuria en g/g creatinina); R=0,332; p<0,0001.
Para los pacientes en monoterapia: Pendiente FG/tiempo=−1,532−(0,727×proteinuria en g/g creatinina); R=0,315; p<0,0001.
Para los pacientes con doble bloqueo: Pendiente FG/tiempo=−4,409−(0,495×proteinuria en g/g creatinina); R=0,275; p<0,011.
Los resultados de este estudio muestran que existe una asociación significativa entre la DEN de los ISRA y la rapidez con que progresa la insuficiencia renal en sus estadios más avanzados. Esta progresión de la ERC es mucho más acelerada cuando se combinan IECA y ARA (doble bloqueo), y además es independiente de la DEN y de otros factores relevantes que podrían compartir el riesgo de progresión con el motivo de su prescripción (p.ej., gravedad de la hipertensión arterial, proteinuria, diabetes).
Aunque los ISRA han sido considerados como tratamiento de elección para detener o enlentecer la progresión de la ERC de diversas etiologías1-4, en los últimos años han surgido corrientes de opinión que ponen en duda su utilidad si se prescriben de forma conjunta (doble bloqueo) o incluso en monoterapia en la ERC avanzada15-22. Además de los estudios de observación y ensayos clínicos que alertaban sobre el efecto negativo del doble bloqueo sobre la progresión de la ERC, hay algún ensayo clínico en curso que intenta analizar de qué manera influye la suspensión de los ISRA en la progresión de la ERC avanzada27.
La DEN media de ISRA en nuestros pacientes se aproximaba a la unidad, pero es reseñable el amplio rango de dosis prescritas. Aunque sí se observó una regresión lineal significativa entre las DEN y la progresión de la ERC, el ajuste del modelo multivariante añadiendo otras variables importantes de confusión descartó una asociación significativa entre estos 2 parámetros, revelando este hallazgo la posibilidad de la influencia de un sesgo por indicación. Sin embargo, el doble bloqueo ISRA sí mantuvo la asociación independiente con la progresión en modelos ajustados, incluyendo las DEN, como se ilustra de una manera más gráfica en las figuras 1 y 2.
El doble bloqueo ISRA ha demostrado un efecto renoprotector en algunos modelos experimentales de insuficiencia renal en ratas6, pero sin embargo son numerosos los ensayos clínicos que no han podido demostrar este beneficio en humanos10-14.
Este efecto negativo del doble bloqueo sobre la progresión de la ERC avanzada podría deberse a la eficacia anti-SRA que se logra con la combinación de estos fármacos, y que podría ser inapropiada para las condiciones fisiopatológicas de la ERC avanzada por excesivo control de la presión arterial sistémica y/o de la presión de filtrado, exponiendo estos cambios hemodinámicos a un mayor riesgo de isquemia tubulointersticial.
Aunque la administración experimental de doble bloqueo a ratas hipertensas tiene un efecto muy positivo sobre objetivos subrogados, tales como presión arterial, proteinuria e hipertrofia ventricular izquierda, paradójicamente esta asociación de fármacos disminuye la función renal e incrementa las lesiones de glomerulosclerosis y fibrosis intersticial28,29. Se sospecha que este efecto adverso es debido a la incapacidad de regular el flujo sanguíneo renal como consecuencia de una hipotensión «relativa» y bloqueo de la acción de la angiotensina II en el mecanismo de retroalimentación glomérulo-tubular, y como consecuencia de esta desregulación se produciría daño isquémico y fibrosis29.
Cambios bruscos del filtrado glomerular, de hasta un 30% de descenso, son frecuentes cuando se inicia un tratamiento con ISRA, pero suelen revertir en menos de 2 meses4. En el presente estudio, todos los pacientes estaban siendo tratados con ISRA más de 3 meses antes de su inclusión, descartándose por tanto que los cambios de función renal observados pudieran deberse a esta peculiaridad del tratamiento.
Este estudio tiene limitaciones. Debido al diseño retrospectivo, no se pueden establecer relaciones causales firmes, y dado que se realizó en un solo centro con unos determinados criterios de tratamiento, los resultados podrían no ser generalizables.
Otra limitación importante fue la falta de control sobre el cumplimiento de tratamiento, y de la cantidad efectiva de principio activo de cada prescripción debido a la dispensación masiva de genéricos, que como es bien sabido y admitido legalmente pueden variar este contenido hasta en un 20%. Tampoco se tuvo en cuenta las peculiaridades farmacocinéticas de cada uno de los fármacos utilizados para calcular la potencia terapéutica comparada. La mayoría de los ISRA se eliminan en una alta proporción por vía renal, y en estadios avanzados de ERC se recomienda un ajuste proporcional de la dosis, que es muy similar en la mayoría de ellos30,31.
En conclusión, DEN elevadas de ISRA se asocian a un deterioro más acelerado de la función renal en pacientes con ERC avanzada, pero esta relación pierde significación cuando se ajusta a otras variables de confusión. Sin embargo, el doble bloqueo ISRA sí se asocia de forma independiente con un deterioro más acelerado de la función renal que no puede justificarse por unas DEN más elevadas.
Según estos resultados, las recomendaciones más prudentes en pacientes con ERC avanzada serían las de evitar el doble bloqueo ISRA y ajustar las dosis en monoterapia, pero hasta que no conozcamos los resultados de los ensayos en curso que aporten evidencias más sólidas, se debe evitar la suspensión total de los ISRA, ya que en estos pacientes no solo es importante la progresión de la ERC sino también mantener el potencial efecto cardioprotector que tienen estos fármacos9.
Conflicto de interesesLos autores declaran no tener conflictos de interés relacionados con la publicación de este artículo.