Sr. Director:
El actual avance de la nefrología y su correlación con otras áreas del conocimiento médico aconseja que el nefrólogo desarrolle capacidades técnicas no presentes en la formación clásica de éste. Presentamos un caso ilustrativo al respecto.
El paciente en cuestión es un varón de 83 años en programa de hemodiálisis (HD) convencional con enfermedad renal crónica secundaria a nefropatía diabética. Los antecedentes más relevantes incluyen: diabetes mellitus tipo 2 con síndrome metadiabético, hipertensión arterial y dolor torácico atípico sin evidencia de cardiopatía isquémica.
Inicia HD en febrero de 2010 mediante catéter tunelizado con buena tolerancia hemodinámica y satisfactoria adecuación. Se realiza fístula arteriovenosa (FAV) humerocefálica izquierda un mes después. Tras un período de maduración de 30 días se inicia venopunción de la FAV objetivándose una maduración subóptima, difícil interpretación anatómica, colapso venoso, frecuentes extravasaciones e imposibilidad de alcanzar un flujo sanguíneo (Qb) superior a 250 ml/min.
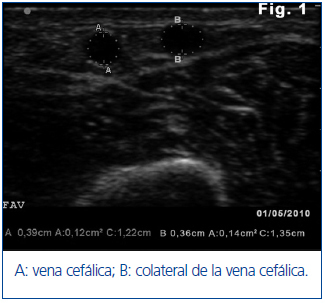
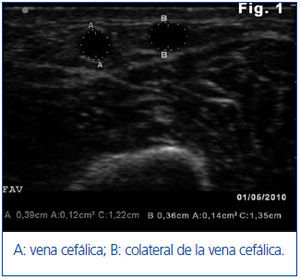
Ante estos hallazgos se realiza ecografía del acceso vascular (AV) portátil (EcoAVP) en la sala de HD (figura 1) y se observa ausencia de estenosis en la unión arteriovenosa, doble sistema venoso con colateral que nace a 3 cm de la anastomosis arterial y grosor equiparable de las dos venas (diámetro: 0,39 vs. 0,36 cm, área: 0,12 vs. 0,14 cm2). Se detectan dos estenosis en la porción proximal de la vena cefálica.
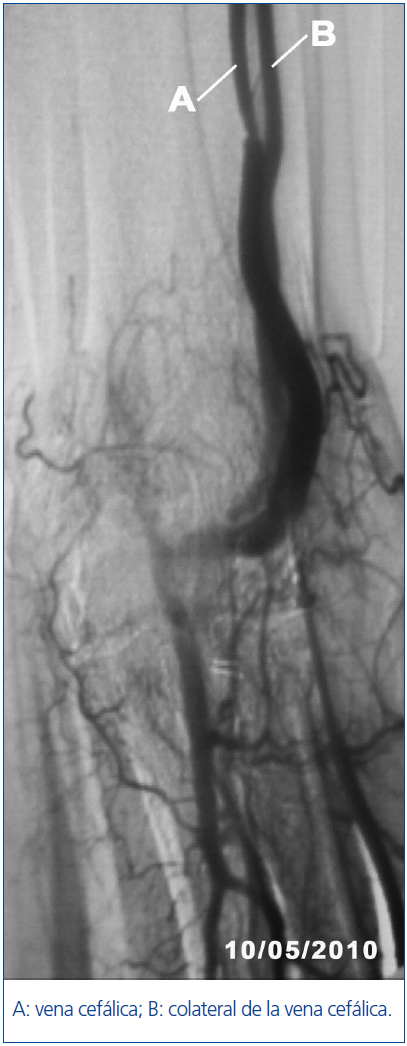
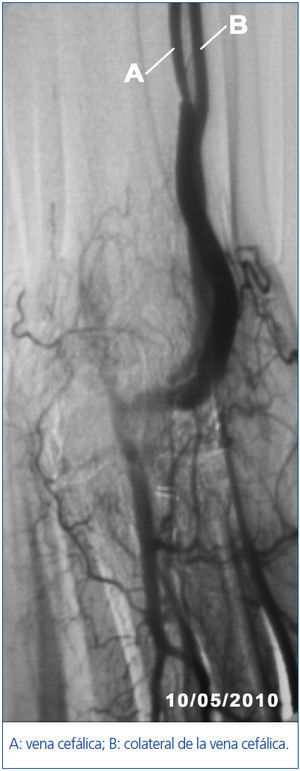
La fistulografía (figura 2) confirma los hallazgos ecográficos y pone de manifiesto una estenosis hemodinámicamente significativa del 80% a 10 cm de la unión arteriovenosa y otra de menor grado en tercio proximal de la vena cefálica. Se realiza angioplastia percutánea sobre las dos estenosis con buen resultado angiográfico. No se realiza tratamiento alguno de la colateral evidenciada.
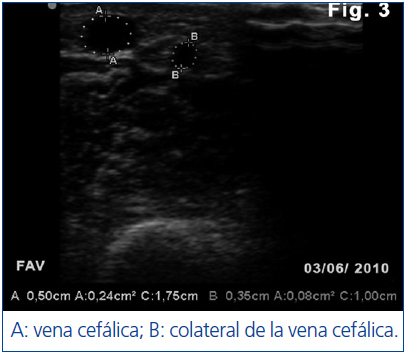
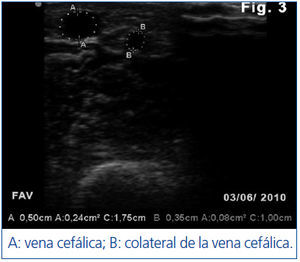
Un mes después la FAV presenta buen desarrollo que permite canalización sin extravasaciones y Qb adecuado. Una segunda EcoAVP (figura 3) confirma el aumento del diámetro y el área transversal de la vena principal (diámetro: 0,5 cm, área: 0,24 cm2) con disminución del calibre de la colateral (diámetro: 0,35, área: 0,08 cm2).
Un año después la FAV funciona correctamente, con Qb de 350 ml/min y presión venosa habitual de 140 mmHg.
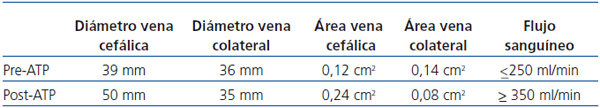
La tabla 1 muestra los cambios en algunos parámetros clínicos y ecográficos objetivados tras el tratamiento con angioplastia percutánea.
El uso de EcoAVP no es un procedimiento habitual en la práctica diaria, pese a su utilidad para la planificación, el seguimiento y el diagnóstico de las complicaciones de la FAV1. La ecografía proporciona información morfológica y funcional con rapidez, fiabilidad y de forma no invasiva, que ayuda a decidir la realización de tratamiento percutáneo o quirúrgico2. La EcoAVP permite combinar la exploración en modo B, que estima el calibre venoso, la presencia de hematomas, calcificaciones parietales, trombos intraluminales, existencia de colaterales y estenosis, y el modo Doppler Color que estima flujo sanguíneo, velocidad pico-sistólica, presencia de turbulencias y la morfología de la onda de pulso con los correspondientes índices de resistencia3. Los resultados de la ecografía siempre deben interpretarse en conjunto con los hallazgos clínicos3.
Una visión más amplia de la participación del nefrólogo en la toma de decisiones incluiría la valoración ecográfica del árbol vascular (mapping) con utilidad demostrada respecto al éxito de la intervención quirúrgica4,5,6,7 y la elastografía venosa estimada como factor con valor predictivo para el funcionamiento de la FAV (evidencia limitada en el momento actual)5.
Actualmente las guías no establecen criterios estrictos de valoración periódica mediante ecografía del AV ni determinan el momento de iniciar el seguimiento ecográfico. En algunos estudios las complicaciones implicadas en el fallo del AV, detectables mediante EcoAVP, están presentes en FAV todavía normofuncionantes8. Por otro lado, la disfunción temprana con fallo primario elevado de las FAV radiocefálicas y el frecuente retraso en la maduración en pacientes diabéticos hace pensar que el uso de EcoAVP como método de seguimiento debería tener una aplicación universal en los pacientes de diálisis4. Teniendo en cuenta el aumento de la edad media de los pacientes en las unidades de diálisis y los datos del elevado número de complicaciones a cualquier nivel y cualquier tipo de AV en los pacientes mayores4,9, podemos afirmar que el entrenamiento en exploraciones ecográficas debería incluirse en la formación de los nefrólogos. La participación activa de los nefrólogos en el diagnóstico y tratamiento de las complicaciones del AV puede reducir el número y la duración de los ingresos hospitalarios relacionados con éste, reducir el uso de catéteres venosos, acortar el tiempo de espera para realización de una FAV, reducir los costes derivados de procedimientos diagnóstico-terapéuticos y, en general, optimizar la prevención de complicaciones10.
A pesar de cierta dependencia de especialidades como cirugía vascular o radiología intervencionista en este campo, es responsabilidad final del nefrólogo asegurar el buen funcionamiento del AV. Esta responsabilidad implica un seguimiento estricto y tratamiento precoz de las complicaciones del AV en un campo multidisciplinar con frecuentes obstáculos administrativos. Un entrenamiento adecuado en exploraciones ecográficas permitiría una mayor agilidad en la toma de decisiones terapéuticas donde la rapidez de acción determina el éxito final de ésta.
Conflictos de interés
Los autores declaran que no tienen conflictos de interés potenciales relacionados con los contenidos de este artículo.
Figura 2. Imagen de la fistulografía realizada posteriormente a la angioplastia percutánea sobre las dos estenosis.
Figura 1. Primera ecografía en modo B del acceso vascular donde se observan dos venas de calibre equiparable
Figura 3. Segunda ecografía en modo B de la fístula arteriovenosa con aumento del calibre de la vena cefálica y reducción del grosor de la colateral
Tabla 1. Cambios de algunos parámetros estudiados tras angioplastia transluminal percutánea de la fístula arteriovenosa