Los recambios plasmáticos terapéuticos (RPT) están indicados como tratamiento coadyuvante en los casos de lesión renal aguda (LRA) grave secundaria a vasculitis1–7. Su beneficio se ha objetivado tanto en la fase aguda de estas enfermedades como durante el primer año, reduciendo la tasa de dependencia dialítica del 60 al 40%3,5. A pesar del beneficio demostrado en diversas patologías, las técnicas de aféresis terapéutica han tenido una aplicación limitada durante años. Esto podría explicarse, entre otras razones, por la dificultad técnica del procedimiento, la rápida recurrencia de algunas de las enfermedades en las cuales se emplean, así como a la escasez de estudios controlados aleatorizados y metaanálisis que avalen su utilidad; en cambio existen una serie de artículos publicados con conceptos no actualizados sobre su eficacia, seguridad y costes. Comentamos a continuación los resultados de un estudio unicéntrico, descriptivo, longitudinal y de una base prospectiva, de pacientes con LRA secundaria a vasculitis, tratados mediante RPT en el Servicio de Hematología y Hemoterapia del Hospital Miguel Servet de Zaragoza. La gravedad de la lesión renal aguda se clasificó según la escala Acute Kidney Injury Network (AKIN) y los criterios Risk, Injury, Failure, Loss y End Stage Kidney Disease risk, Injury (RIFLE).
Se analizaron 13 casos, 7 eran mujeres, con una mediana de edad de 67,7 años. El 92,3% tenía una comorbilidad alta (Índice de Charlson > 4). Más del 60% de los casos correspondían a indicaciones tipo I o II de las guías de la Sociedad Americana de Aféresis2. Todos los casos precisaron soporte con diálisis pero solo en 4 se realizó de manera urgente y antes del inicio de los RPT (estos 4 presentaban valores séricos de creatinina > 6,8mg/dl). Las demás características de la serie se exponen en la tabla 1.
Características generales de la serie
| n (%) | |
|---|---|
| Diagnósticos | |
| Brote de GNRP asociada a ANCA | n = 4 (30,8) |
| Poliangeítis granulomatosa | n = 3 (23,1) |
| Enfermedad por Ac anti-MBG | n = 2 (15,4) |
| Brote de GN no asociada a ANCA | n = 2 (15,4) |
| Nefropatía Schonlein-Henoch | n = 1 (7,7) |
| Crioglobulinemia esencial | n = 1 (7,7) |
| Indicación según guías ASFA | |
| Indicación I | |
| GNRP asociada a ANCA con DD (1A) | n = 3 (23,1) |
| Poliangeítis granulomatosa con DD (1A) | n = 2 (15,4) |
| Poliangeítis granulomatosa con HAD (1C) | n = 1 (7,7) |
| Enfermedad por Ac anti-MBG con HAD (1C) | n = 1 (7,7) |
| Indicación II | |
| Crioglobulinemia esencial grave (2A) | n = 1 (7,7) |
| Indicación III | |
| Enfermedad por Ac anti-MBG con DD (2B) | n = 1 (7,7) |
| Nefropatía Schonlein-Henoch (2C) | n = 1 (7,7) |
| GNRP asociada a ANCA con ID (2C) | n = 1 (7,7) |
| Fuera de indicación | |
| GN no asociada a ANCA | n = 2 (15,4) |
| Hallazgos histológicos en la biopsia renal | |
| Presencia de semilunas | n = 8 (61,5) |
| Atrofia tubular | n = 6 (46,2) |
| Fibrosis | n = 6 (46,2) |
| No disponible (otro centro) | n = 2 (15,4) |
| Clasificación AKIN | |
| LRA I | n = 0 |
| LRA II | n = 1 (7,7) |
| LRA III | n = 12 (92,3) |
| Clasificación RIFLE | |
| Risk | n = 0 |
| Injury | n = 1 (7,7) |
| Failure | n = 12 (92,3) |
| Loss | n = 0 |
| End stage Kidney Disease | n = 0 |
| Tratamiento previo a RPT | |
| Pulsos de MTPa | n = 4 |
| Pulsos de MTPa y Cy | n = 7 |
| Prednisona oralb | n = 2 |
| Tratamiento concomitante con RPT | |
| Bolus de Cyc + MTP | n = 7 |
| Bolus de Cyc + prednisona | n = 6 |
| Tratamiento posterior a RPT | |
| Cy + prednisona | n = 12 |
| Rituximabd | n = 1 |
Ac: anticuerpos; ANCA: anticuerpos anticitoplasma de neutrófilos; AKIN: Acute Kidney Injury Network; Cy: ciclofosfamida; DD: dependencia dialítica; FA: fuera de indicación; GN: glomerulonefritis; GNRP: glomerulonefritis rápidamente progresiva; HAD: hemorragia alveolar difusa; ID: independencia dialítica; MBG: membrana basal glomerular; MTP: metilprednisolona; RIFLE: Risk, Injury, Failure, Loss y End Stage Kidney Disease risk, Injury; RPT: recambios plasmáticos terapéuticos.
La tasa de respuesta al mes de haber finalizado los RPT fue del 38,5%. Los valores de creatinina sérica menores a 5,8mg/dl se relacionaron con mejores respuestas (p = 0,032, RR: 0,16; IC95% [0,02-1,03]), coincidiendo con bibliografía publicada de series mayores2–6.
A nivel analítico, se objetivaron descensos significativos en los valores de creatinina sérica (p = 0,005), filtrado glomerular (p = 0,003) y proteinuria en muestra simple de orina (p = 0,045). También se objetivó descenso de los valores de plaquetas (p = 0,022) y fibrinógeno (p = 0,037), sin embargo, estos últimos hallazgos analíticos no se relacionaron con manifestaciones hemorrágicas.
En cuanto a la técnica de recambio plasmático, durante el procedimiento realizamos profilaxis de la hipocalcemia con gluconato cálcico intravenoso, cuya administración se repite ante la aparición de síntomas. Y al final del mismo, y con el fin de prevenir la coagulopatía dilucional se administra de manera profiláctica vitamina K intravenosa. Los dispositivos utilizados son separadores celulares de flujo continuo (Cobe Spectra® u Optia Spectra®, Terumo) con adenina-citrato-dextrosa formula A (ACD-A) como anticoagulante. Los accesos venosos centrales de los pacientes fueron catéter hickman (n = 9), shaldon (n = 2) y femoral (n = 2).
La mediana de días entre la sospecha clínica y el inicio de los RPT fue 10 (0-28). Se realizaron 6 sesiones (4-17) por paciente, con un volumen intercambiado de 3.371 (2.333-4.759) mL, correspondiendo a 1-1,5 volemias. La reposición se hizo de manera estándar con albúmina 5%.
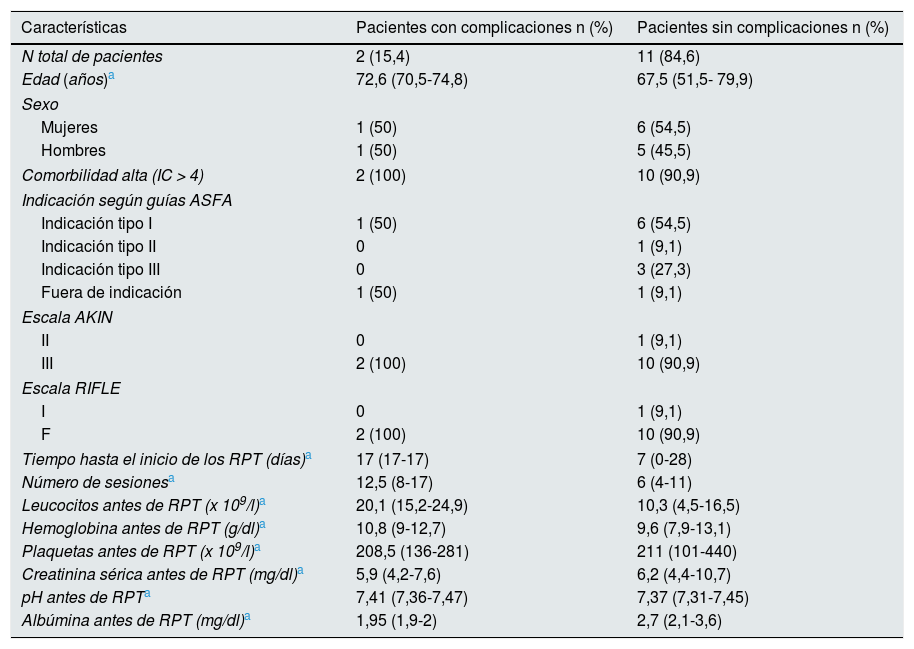
De las 96 sesiones realizadas en total, hubo una (1,04%) con baja presión de acceso y 4 (4,1%) con complicaciones clínicas (prurito en 3 y en una fiebre), correspondiendo todas ellas a 2 pacientes (tabla 2). Ninguna de ellas fue grave y únicamente hubo que suspender una sesión ante la presencia de fiebre. Los pacientes que desarrollaron más complicaciones (clínicas y técnicas) tenían una cifra mayor de leucocitos previo al inicio de los RPT (p = 0,04) y se les había realizado un mayor número de sesiones de RPT (p = 0,010), consultar tabla 2. También se objetivó una mayor tasa de complicaciones en los RPT realizados antes del año 2010 (28,6 vs. 0%), sin significado estadístico.
Características de los pacientes con y sin complicaciones
| Características | Pacientes con complicaciones n (%) | Pacientes sin complicaciones n (%) |
|---|---|---|
| N total de pacientes | 2 (15,4) | 11 (84,6) |
| Edad (años)a | 72,6 (70,5-74,8) | 67,5 (51,5- 79,9) |
| Sexo | ||
| Mujeres | 1 (50) | 6 (54,5) |
| Hombres | 1 (50) | 5 (45,5) |
| Comorbilidad alta (IC > 4) | 2 (100) | 10 (90,9) |
| Indicación según guías ASFA | ||
| Indicación tipo I | 1 (50) | 6 (54,5) |
| Indicación tipo II | 0 | 1 (9,1) |
| Indicación tipo III | 0 | 3 (27,3) |
| Fuera de indicación | 1 (50) | 1 (9,1) |
| Escala AKIN | ||
| II | 0 | 1 (9,1) |
| III | 2 (100) | 10 (90,9) |
| Escala RIFLE | ||
| I | 0 | 1 (9,1) |
| F | 2 (100) | 10 (90,9) |
| Tiempo hasta el inicio de los RPT (días)a | 17 (17-17) | 7 (0-28) |
| Número de sesionesa | 12,5 (8-17) | 6 (4-11) |
| Leucocitos antes de RPT (x 109/l)a | 20,1 (15,2-24,9) | 10,3 (4,5-16,5) |
| Hemoglobina antes de RPT (g/dl)a | 10,8 (9-12,7) | 9,6 (7,9-13,1) |
| Plaquetas antes de RPT (x 109/l)a | 208,5 (136-281) | 211 (101-440) |
| Creatinina sérica antes de RPT (mg/dl)a | 5,9 (4,2-7,6) | 6,2 (4,4-10,7) |
| pH antes de RPTa | 7,41 (7,36-7,47) | 7,37 (7,31-7,45) |
| Albúmina antes de RPT (mg/dl)a | 1,95 (1,9-2) | 2,7 (2,1-3,6) |
AKIN: Acute Kidney Injury Network; ASFA: Asociación Americana de Aféresis; HD: hemodiálisis; IC: Índice de Charlson; RPT: recambios plasmáticos terapéuticos; RIFLE: del acrónimo Risk, Injury, Failure, Loss y End Stage Kidney Disease risk, Injury.
Es lógico pensar que a mayor número de sesiones, habrá un mayor número de eventos adversos relacionados con la técnica. Aun así, la frecuencia global de complicaciones en nuestra serie fue menor a la publicada en otros trabajos8–10. El hallazgo de una mayor cifra de leucocitos iniciales en los pacientes con más complicaciones, se podría deber a una dosis inicial más alta de corticoesteroides, no obstante este dato no se pudo confirmar. Su relación con el desarrollo de complicaciones deberá estudiarse en series de mayor casuística.
El hecho de que nuestra tasa de complicaciones sea menor a la publicada, nos permite concluir que los RPT son una estrategia terapéutica segura en nuestro centro y nos anima a continuar con la realización de los mismos. Podríamos postular que las maniobras profilácticas que usamos son las que están evitando su aparición.