Sr. Director:
La nefropatía diabética (ND) es la principal causa de enfermedad renal crónica terminal (ERCT) en los países desarrollados1. Su incidencia y su prevalencia continúan aumentando. Describimos el resultado final en el riñón de la evolución natural de una diabetes mellitus (DM) de años de evolución (sin tratamientos renoprotectores previos y con mal control metabólico).
CASO CLÍNICO
Hombre de 60 años con antecedentes personales de DM tipo 2 de más de 20 años de evolución, inicialmente en tratamiento con antidiabéticos y en los últimos 5 años con insulina, con mal control metabólico. Retinopatía diabética no proliferativa. Ex-fumador de 30 cigarrillos/día hasta hace 5 años.
El paciente acude a urgencias refiriendo edemas generalizados de un mes de evolución, disnea de medianos esfuerzos y nicturia de 2-3 veces. En la exploración física, el paciente tenía buen estado general, estaba consciente y orientado. La presión arterial era de 160/110 mmHg, la frecuencia cardíaca de 80 lat/min. Ingurgitación yugular. Auscultación cardíaca rítmica. En la auscultación pulmonar presentaba mínimos crepitantes en bases. Edemas con fóvea hasta rodilla; el resto de la exploración fue normal.
La analítica en sangre reveló glucosa 200 mg/dl; urea 52 mg/dl; creatinina 1,2 mg/dl; ácido úrico 5,3 mg/dl; colesterol 313 mg/dl; triglicéridos 144 mg/dl; albúmina 1,9 g/dl; proteínas totales 4,4 g/dl; calcio 7,6 mg/dl; fósforo 3,2 mg/dl; hierro 41 µg/dl, y ferritina 155 ng/ml. La hemoglobina fue de 11,6 g/dl, el hematocrito del 34,3%, y el resto del hemograma y de las pruebas de coagulación fueron normales. Las hormonas tiroideas, serología de virus (VIH, virus de las hepatitis B y C), y el PSA fueron normales. La hemoglobina A1c era del 8,3%. El estudio inmunológico, incluyendo inmunoglobulinas, complemento, factor reumatoide, ASLO, ANA, anti-ADN, ANCA y proteína C reactiva, también fue normal.
El sistemático de orina mostró proteínas +++, sangre +, glucosa ++, nitritos negativos. La proteinuria en orina recogida de 24 horas fue de 10 g. En la electroforesis en orina la proteinuria era no selectiva, siendo la proteinuria de Bence-Jones negativa.
En la radiografía de tórax se objetivaron cardiomegalia y signos radiológicos de hipertensión venocapilar grado II. En la ecografía abdominal se encontró un riñón derecho de 12 cm, de morfología normal; el riñón izquierdo era de 15 cm, con dilatación del sistema excretor.
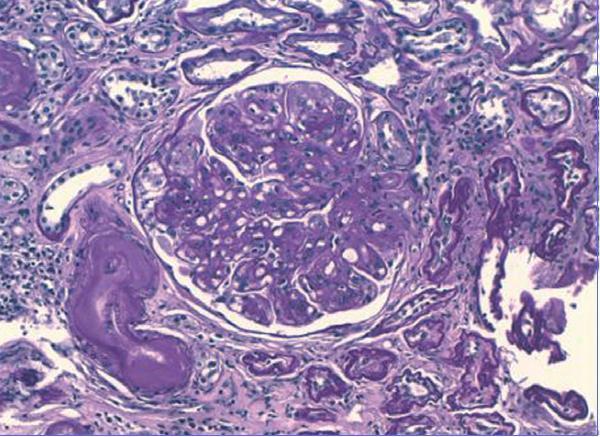
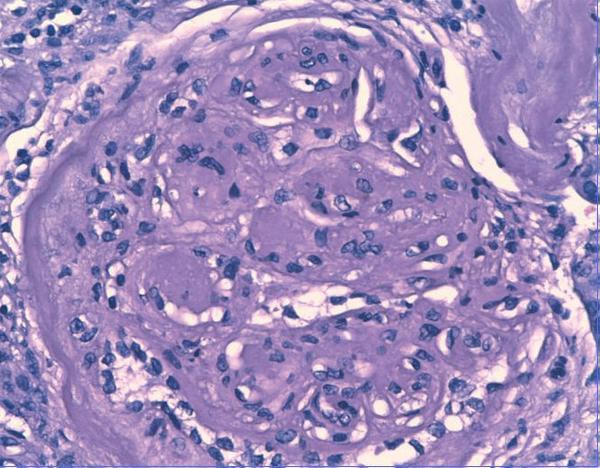
Se inició tratamiento depletivo con diuréticos, inhibidores de la enzima de conversión de la angiotensina (IECA) y antagonistas de los receptores de angiotensina II (ARAII), estatinas, heparina de bajo peso molecular, y se recomendó mejorar el control glucémico. Debido a la hidronefrosis del riñón izquierdo provocada por un síndrome de la unión pieloureteral se realizó pieloplastia y se colocó una nefrostomía percutánea en el riñón izquierdo. A pesar de estas medidas el paciente requirió nuevos ingresos hospitalarios por descompensación del síndrome nefrótico, con incremento de la creatinina plasmática a 2,5-3 mg/dl y persistencia de la proteinuria nefrótica, motivo por el que se decide iniciar programa de hemodiálisis. Aunque la sospecha inicial fue de ND, estando el paciente en hemodiálisis persistió el mal control volumétrico y con parámetros bioquímicos de actividad del síndrome nefrótico decidimos realizar una biopsia renal para descartar una glomerulopatía asociada. Los hallazgos de biopsia fueron: 12 glomérulos por plano de corte, cinco de ellos completamente esclerosados. Todos los glomérulos estudiados mostraban una expansión mesangial con formación de nódulos acelulares (Kinmelstein-Wilson). La inmunofluorescencia fue negativa. En el intersticio se observó una fibrosis moderada con focos de atrofia tubular asociada. El componente vascular mostró una llamativa hialinosis de su pared, siendo el diagnostico anatomopatológico final compatible con una glomeruloesclerosis difusa (figura 1) y nodular (figura 2), con sustrato morfológico de enfermedad diabética.
DISCUSIÓN
En la patogenia de la ND se han implicado factores metabólicos y hemodinámicos2. La angiotensina II desempeña un papel primordial en la patogenia y en la progresión de la ND, y su inhibición confiere renoprotección en pacientes con diabetes3. Un retraso en el inicio de los tratamientos con IECA o con ARAII en pacientes con DM2, con proteinuria e insuficiencia renal, hace que sean menos efectivos, de ahí la importancia de instaurar un tratamiento precoz3. En el caso que presentamos, a pesar de haber comenzado la terapia durante el primer ingreso con inhibidores del sistema renina-angiotensina-aldosterona (SRAA), el síndrome nefrótico siguió descontrolado, precisando el paciente nuevos ingresos por descompensación hidrópica. Esta nula respuesta al tratamiento puede justificarse, en primer lugar, por tratarse de una ND de muchos años de evolución con mal control metabólico; en segundo lugar, por la presencia de una proteinuria severa cuando se estudió por vez primera al paciente y la ausencia de terapia previa con fármacos antiproteinúricos y, en tercer lugar, por los hallazgos histológicos de la biopsia renal.
Con los tratamientos actuales se mantiene la progresión de la ND a ERCT, por lo que la inhibición del SRAA puede no ser suficiente. Recientemente se han descrito nuevos agentes terapéuticos que pueden tener un papel en tratar de retrasar la progresión de la ND4: se ha visto que los receptores de hormonas desempeñan un papel protector en enfermedades cardiovasculares, inflamatorias y metabólicas. Así, su modulación podrá suponer nuevas «dianas» para su tratamiento. En el caso de la DM, los receptores más estudiados han sido los de estrógenos, PPAR-gamma y vitamina D5.
La hiperglucemia crónica promueve la generación de productos avanzados de la glicosilación (advanced glycation end products [AGE])2. Así, se han descrito inhibidores de los AGE (aminoguanidina, ALT-946, piridoxamina, tiamina) y antagonistas de los receptores de AGE (RAGE)4.
Otro de los agentes potenciales (por sus propiedades reológicas y antiinflamatorias) es la pentoxifilina6; en estudios animales se ha observado que tiene efectos renoprotectores y antiproteinúricos7. Además, en un reciente metanálisis de revisión de ensayos aleatorizados controlados, la pentoxifilina ha demostrado ser eficaz como antiproteinúrico en pacientes con enfermedad renal diabética8.
También existen evidencias de que la activación de la proteína C kinasa (PCK) causa insuficiencia renal (hiperfiltración, daño en membrana basal y glomeruloesclerosis). Entre los inhibidores de la PCK, la ruboxistaurina ha demostrado poseer un efector prometedor en la prevención de las complicaciones vasculares diabéticas4.
Por último, varios factores de crecimiento se expresan en el riñón normal y han sido implicados en la patogenia de la ND, y los inhibidores de TGF-beta, CTGF y VEGF son potenciales agentes terapéuticos9.
En definitiva, en la era de la inhibición del SRAA todavía es posible detectar a pacientes con un curso natural de la ND. El retraso en el inicio del tratamiento hace que la respuesta posterior sea discreta. En los próximos años se comprobará si los nuevos agentes terapéuticos ayudarán a impedir la aparición de la ND y/o a tratarla de forma que se retrase la progresión a ERCT.
Figura 1. Técnica de PAS (x20 aumentos): glomeruloesclerosis difusa con hialinosis de la arteriola eferente e intensa hialinosis de vasos de mediano calibre.
Figura 2. Técnica de hematoxilina-eosina (x40 aumentos): glomeruloesclerosis nodular típica.