El fracaso renal agudo (FRA) es una complicación frecuente e importante en pacientes con insuficiencia hepática (IH)1. El FRA relacionado con el incremento de la bilirrubina es conocido desde principios del siglo xx. Esta entidad ha recibido diferentes nombres, nefropatía colestásica, nefropatía relacionada con la ictericia, nefropatía por cilindros biliares y nefropatía biliar1-4.
Presentamos un caso inusual de FRA debido a hiperbilirrubinemia grave secundaria al uso de esteroides anabolizantes (EA) utilizados para culturismo. Es un varón de 40 años, sin antecedentes de interés, que solicitó valoración por cuadro de ictericia, hipocolia, coluria, prurito y astenia. El paciente no presentaba hábitos tóxicos y refería que había estado tomando durante el mes previo suplementos vitamínicos Animal-Pak® y EA Havoc®.
En el examen físico únicamente destacaba marcada ictericia mucocutánea. En los análisis al ingreso se evidenció bilirrubina de 30mg/dl, GPT: 226U/l, GOT: 89U/l y fosfatasa alcalina y gamma-GT normales. No presentó coagulopatía y la función renal fue normal. Se realizaron serologías víricas, alfa-1-antitripsina, ceruloplasmina, cobre, anticuerpos, inmunoglobulinas y complemento que fueron normales, al igual que la ecografía abdominal.
En su evolución se objetivó incremento progresivo de la bilirrubina hasta máxima de 39,9mg/dl, motivo por el cual se realizó una biopsia hepática, identificándose áreas de hepatitis periportal, colestasis canalicular y parenquimatosa y fibrosis perisinusoidal; hallazgos compatibles con hepatitis de origen medicamentoso. La bilirrubina fue mejorando paulatinamente presentando una bilirrubina de 30mg/dl en el momento del alta.
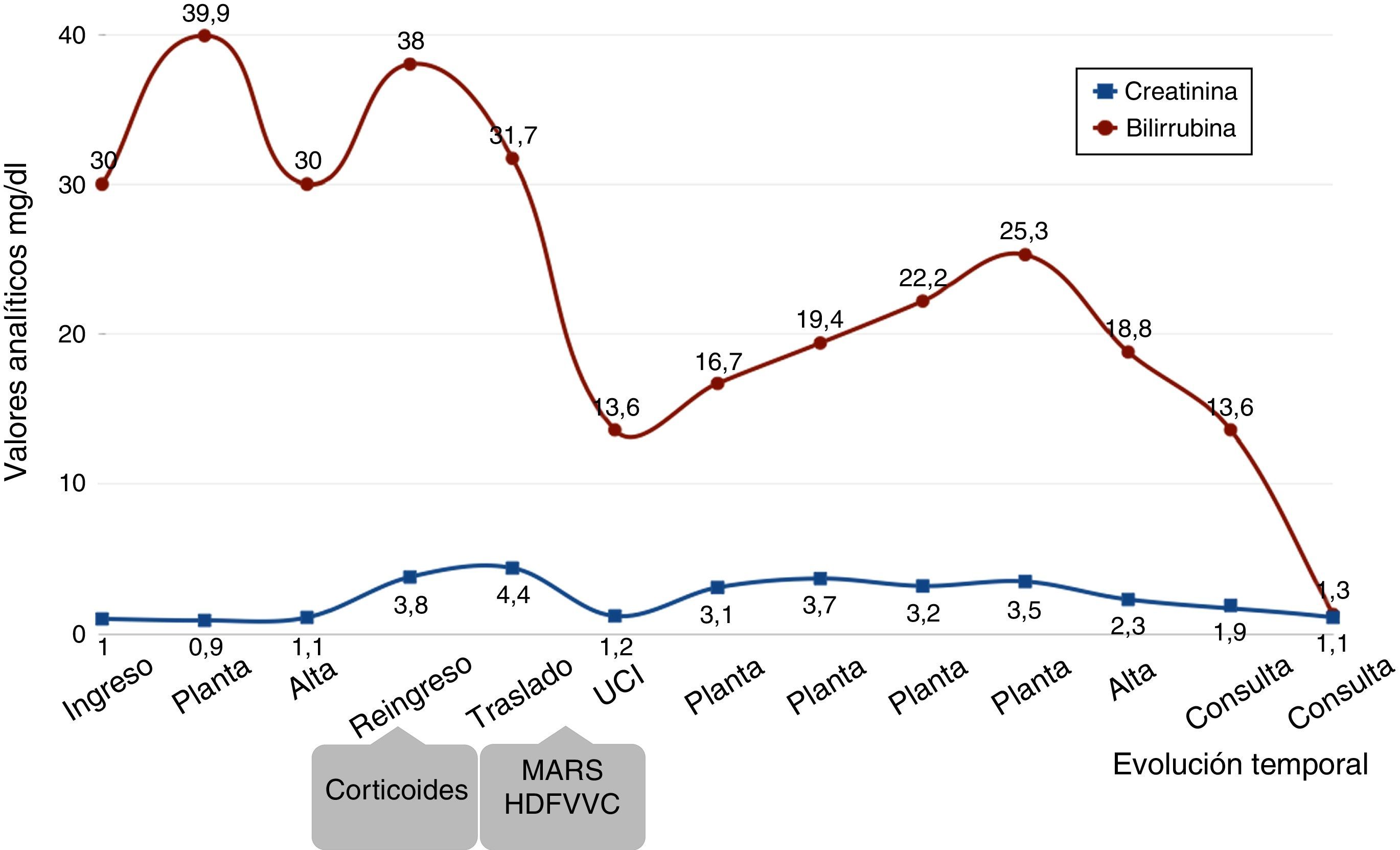
A la semana del alta el paciente ingresó por FRA con creatinina sérica (Crs) de 4,5mg/dl e incremento de las cifras de bilirrubina hasta 38mg/dl (fig. 1). Tras estos hallazgos se inició tratamiento con sueroterapia, ácido ursodesoxicólico, resincolestiramina y corticoides (1mg/kg) con disminución de la bilirrubina hasta 30mg/dl, pero persistiendo con FRA por lo que se inició hemodiálisis y posteriormente terapia Molecular Adsorbents Recirculation System (MARS) y hemodiafiltración veno-venosa continua (HDFVVC).
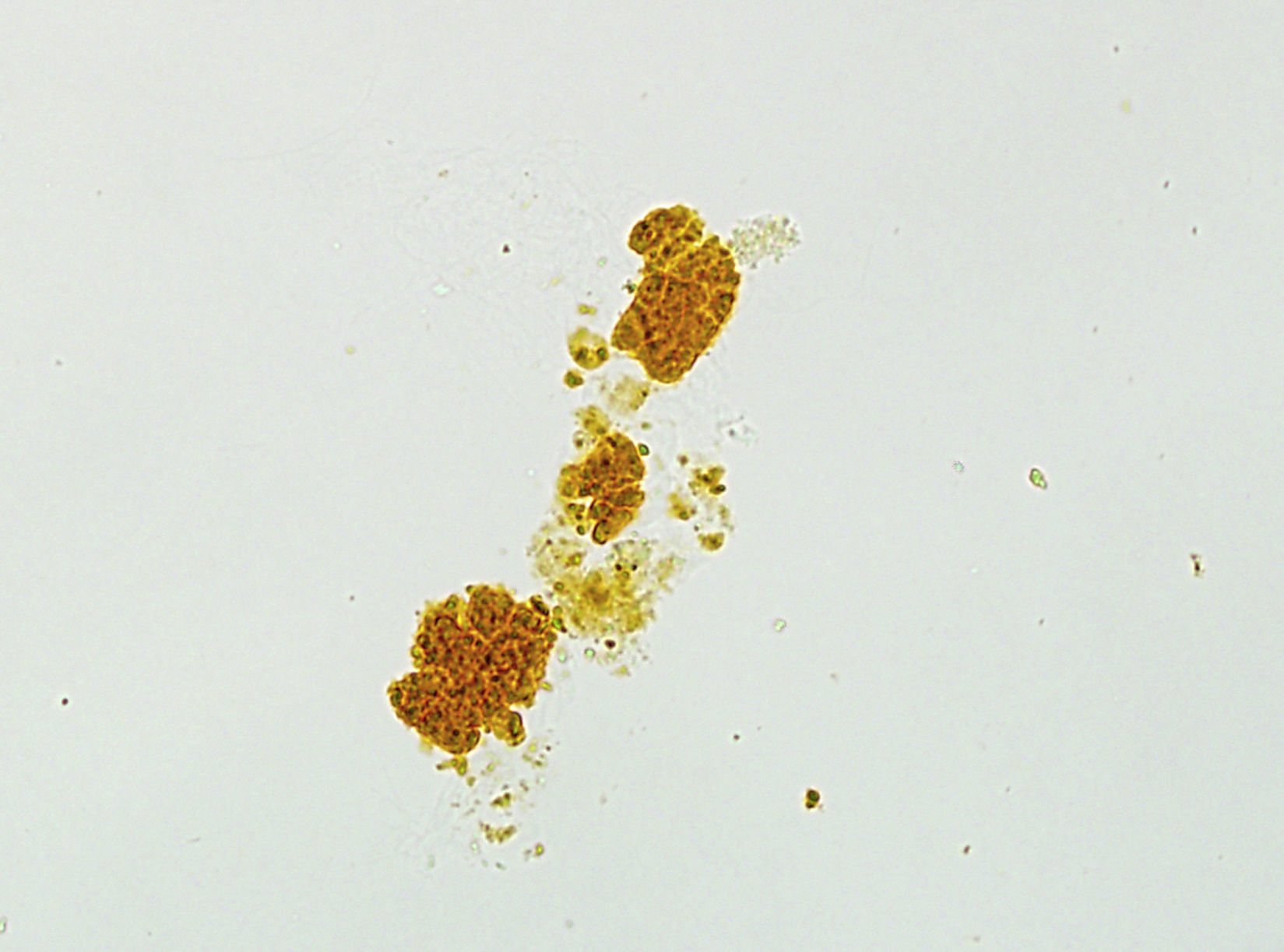
Se realizó estudio renal completo en el que se objetivó únicamente la presencia de abundantes cilindros de bilirrubina en el sedimento (fig. 2). En su evolución posterior la bilirrubina fue mejorando progresivamente hasta cifras de 18,8mg/dl en paralelo al tratamiento y disminución gradual de los corticoesteroides, lo que permitió la retirada del MARS y la HDFVVC. La función renal mejoró hasta una Crs de 2,4mg/dl en el momento del alta por lo que se decidió no realizar biopsia renal. A los 4 meses del inicio del cuadro el enfermo alcanzó una Crs de 1,1mg/dl con una bilirrubina de 1,3mg/dl suspendiéndose los esteroides a los 2 meses de su inicio.
Los EA son derivados sintéticos de la testosterona y pueden causar toxicidad hepática (colestasis, hiperplasia nodular regenerativa, neoplasias…) puesto que alteran la excreción canicular de la bilirrubina conjugada y su captación sinusal provocando su acumulación2,5. El paciente había estado tomando Havoc® que contiene metilepitiostanol, que es una prohormona que se metaboliza dando lugar al compuesto desoximetiltestosterona que puede producir colestasis hepática, uno de los motivos por los que se ha prohibido su venta6.
Desde una perspectiva renal se ha descrito proteinuria asociada a glomeruloesclerosis focal y segmentaria y FRA2,5. Robles-Díaz et al. reportaron una serie de 25 pacientes con hepatotoxicidad por EA de los cuales un 31% desarrollaron FRA con recuperación completa de la función renal tras la resolución del daño hepático sin necesidad de realizar biopsia renal7.
La bilirrubina se incrementa en el seno de IH pudiendo ocasionar daño tubular directo, y por ende FRA. Es sabido que el riesgo de lesión tubular aumenta cuando los niveles de bilirrubina son superiores a 20mg/dl1,2,5,8,9. En el túbulo proximal se realiza el transporte de la bilirrubina, cuando se satura da lugar a la formación de cilindros que originan el daño tubular, bien por la toxicidad directa de la bilirrubina bien por la obstrucción intratubular de los cilindros1,8. Los mecanismos responsables del daño tubular son el desacoplamiento de la fosforilación mitocondrial disminuyendo la actividad ATPasa, el daño oxidativo de la membrana celular tubular, así como la inhibición de las bombas Na+-H+, Na+-Cl− y Na+-K+2,10.
Para el diagnóstico es preciso la sospecha clínica y la realización de un sedimento urinario que suele ser muy característico por la presencia de cilindros de bilirrubina y células epiteliales que contienen bilirrubina9. En la biopsia renal es habitual el hallazgo de túbulos llenos de células epiteliales degeneradas y cilindros de pigmentos biliares junto con dilatación de la luz y vacuolización citoplasmática con indemnidad glomerular3,4. En el estudio con microscopia electrónica es característico el hallazgo de crestas mitocondriales dilatadas y acumulación de ácidos biliares dentro de los lisosomas8.
El tratamiento no es específico y es básicamente de sostén. La terapia de reemplazo renal no tiene ningún papel específico salvo para el tratamiento del FRA mientras que la plasmaféresis puede ser de utilidad en la reducción de sustancias proinflamatorias9. Otras opciones destinadas a reducir citoquinas inflamatorias y bilirrubina son el MARS, el Coupled Plasma Filtration Adsorption (CPFA) y la diálisis de adsorción y filtración de plasma. Los esteroides, la colestiramina, el ácido ursodesoxicólico y la lactulosa han demostrado un beneficio mínimo8. Los EA pueden provocar este cuadro, por lo que los atletas aficionados deben ser informados sobre sus efectos secundarios.