La enfermedad renal crónica (ERC) constituye un auténtico problema de salud pública. Se estima que, para el año 2040, aproximadamente uno de cada 5 adultos tenga ERC, y para 2050 será la tercera causa de muerte en España. Sin embargo, la ERC se encuentra claramente infradiagnosticada, con cifras bajas de cribado en la población de riesgo, retrasando muchas veces su identificación a fases avanzadas de la enfermedad, lo que empeora el pronóstico de los pacientes y los costes asociados. Además, en la actualidad se dispone de fármacos que han demostrado reducir la progresión de la ERC y el riesgo de desarrollar complicaciones vasculares. En este contexto, la detección precoz, el diagnóstico y el manejo inicial de la ERC por parte de las organizaciones sanitarias debe convertirse en una prioridad, ya que disminuiría la carga de la enfermedad de manera sustancial. Al ser esta patología oligo o paucisintomática en estadios precoces, se exige del profesional sanitario una actitud proactiva, para detectar, diagnosticar y tratar precozmente esta patología. Diversas publicaciones han mostrado que hasta ahora tanto la detección de la ERC como su manejo inicial no son óptimos. El proyecto IntERKit surge con el objetivo de mejorar la detección precoz, el diagnóstico y el manejo inicial de la ERC promoviendo la colaboración con las organizaciones sanitarias, mediante herramientas fácilmente implementables por dichas organizaciones. El proyecto IntERKit proporciona a las organizaciones sanitarias un marco estructurado para optimizar el abordaje temprano de la ERC de manera eficiente, logrando un impacto real, medible, sostenible y escalable, que pueda evolucionar en función de los resultados obtenidos.
Chronic kidney disease (CKD) is a real public health problem. It is estimated that by 2040, approximately one in 5 adults will develop CKD, and by 2050 it will be the third cause of death in Spain. However, CKD is clearly underdiagnosed, with low screening figures in the population at risk, often delaying its identification to advanced stages of the disease, which worsens the prognosis of patients and increases the associated costs. In addition, drugs are now available that have been shown to reduce the progression of CKD and the risk of developing vascular complications. In this context, the early detection, diagnosis and initial management of CKD by health organizations should become a priority, as it would reduce the burden of the disease substantially. The IntERKit project arises with the aim of improving the early detection, diagnosis and initial management of CKD by promoting collaboration with health organizations, through tools easily implemented by these organizations. Since this pathology is oligo or paucisymptomatic in early stages, a proactive attitude is required from the health professional to detect, diagnose and treat this pathology early. Several publications have shown that, to date, both the detection of CKD and its initial management are not optimal. The IntERKit project provides healthcare organizations with a structured framework to optimize the early approach of CKD efficiently, achieving a real, measurable, sustainable and scalable impact, which can evolve depending on the results obtained.
La enfermedad renal crónica (ERC) constituye un auténtico problema de salud pública. De hecho, se estima que a nivel mundial la ERC pasará de ser la décima causa de muerte en 2022 a la quinta en el 20251. En España, el estudio ENRICA, estudio epidemiológico de base poblacional, mostró una prevalencia de ERC en la población adulta del 15,1%2. En el estudio EPIRCE, la prevalencia de ERC estadios 3-5 en sujetos de al menos 20años fue del 6,8%, cifra que ascendió del 3,3% en aquellos individuos de 40-64años al 21,4% en los mayores de 64años3. En el estudio IBERICAN, la prevalencia de pacientes atendidos en las consultas de atención primaria fue del 14,4% (16,1% en varones y 12,9% en mujeres)4. En un estudio poblacional realizado en España en 2021, la incidencia de ERC fue de 2,1 por 1.000 pacientes-año5. Además, como consecuencia del envejecimiento de la población y de una mayor prevalencia de factores de riesgo para el desarrollo de ERC, principalmente hipertensión arterial y diabetes6, se espera que estas cifras aumenten en España, llegando a una prevalencia superior al 18% en el año 20407.
Estos datos son muy relevantes, ya que la ERC no solo aumenta el riesgo de progresión hacia las fases finales de la ERC, incluyendo la necesidad de tratamiento renal sustitutivo, sino que aumenta de manera marcada el riesgo de presentar complicaciones vasculares, envejecimiento biológico acelerado y de muerte prematura por cualquier causa; además, hace que el paciente sufra una peor calidad de vida, mayor grado de discapacidad y pérdida de trabajo8-12. Esto hace que el consumo de recursos y los costes asociados a la ERC sean muy elevados13,14.
Aunque se han realizado esfuerzos a nivel institucional15, lo cierto es que la ERC se encuentra claramente infradiagnosticada16, en parte porque el paciente está asintomático hasta fases avanzadas de la enfermedad, pero también debido a que el proceso asistencial no se encuentra optimizado y porque todavía existe cierto desconocimiento sobre la importancia y el impacto de la ERC7. De hecho, el último Plan Estratégico Nacional para el abordaje de la ERC en el Sistema Nacional de Salud data de 2015 y requiere una clara actualización15, y aunque en 2021 se publicó la estrategia para el abordaje de la cronicidad, con mención a las limitaciones para ERC y abordaje desde las comunidades autónomas17, y en 2022 hasta diez sociedades científicas —Sociedad Española de Nefrología (SEN), Sociedad Española de Hipertensión-Liga Española para la Lucha contra la Hipertensión Arterial (SEH-LELHA), Sociedad Española de Medicina Interna (SEMI), Sociedad Española de Endocrinología y Nutrición (SEEN), Sociedad Española de Cardiología (SEC), Sociedad Española de Médicos Generales y de Familia (SEMG), Sociedad Española de Médicos de Atención Primaria (SEMERGEN), Sociedad Española de Medicina de Laboratorio (SEQC(ML)), Sociedad Española de Medicina de Familia y Comunitaria (SEMFyC) y Sociedad Española de Diabetes (SED)— firmaron un importante documento sobre la detección y el manejo de la ERC10, que ha sido la actualización de otras dos versiones previas del documento, la realidad es que su difusión y su implementación en la práctica clínica en las diferentes comunidades autónomas en España ha sido limitada18, incluso después de que en 2023 se ampliara el documento con otro enfatizando el papel clave de medir la albuminuria en el diagnóstico precoz de la ERC y en la prevención de la enfermedad cardiovascular, con el apoyo de 14 sociedades científicas19.
Esto explicaría que un porcentaje significativo de pacientes con ERC, sobre todo en sus estadios más iniciales, no estén recibiendo el tratamiento adecuado para reducir la progresión de la ERC5. Y esto es particularmente importante, ya que en la actualidad existen tratamientos que en ensayos clínicos específicos han demostrado disminuir no solo la evolución de la ERC hacia los estadios finales, sino también el riesgo de presentar complicaciones vasculares mayores, principalmente los bloqueadores del sistema renina angiotensina20,21, los inhibidores del cotransportador de sodio-glucosa tipo222,23, algunos agonistas del receptor del péptido similar al glucagón tipo124, y en pacientes con ERC asociada a diabetes tipo2, la finerenona, un antagonista no esteroideo del receptor mineralocorticoide25,26.
Proyecto IntERCedeLa detección y el abordaje precoz de la ERC suponen una estrategia fundamental en esta patología, y constituyen una prioridad sanitaria de primer orden en España. En consecuencia, se deben establecer estrategias específicas desarrolladas con el objetivo de disminuir el riesgo de progresión de la ERC hacia estadios más avanzados, así como desarrollar complicaciones vasculares, para de esta forma mitigar la carga de la enfermedad y los costes asociados. En este contexto, el proyecto IntERCede surge como un programa multidisciplinar que trata de describir y comprender el modelo asistencial existente y de atención a los pacientes con ERC, identificando las áreas de mejora, con el fin de optimizar la atención de estos pacientes, centrándose en la prevención primaria y secundaria de la ERC a través del desarrollo de estrategias específicas de prevención, detección precoz y retraso de la progresión de la enfermedad. En concreto, como objetivos principales se incluyen la identificación de mejoras y la optimización del proceso asistencial, la identificación de puntos de descoordinación o gaps de asistencia, la mejora y la personalización de los servicios y el desarrollo de una visión holística de las necesidades que tiene el paciente como persona, siendo la atención primaria el pilar fundamental sobre el que se sustenta la atención al paciente con ERC, sobre todo en cuanto a la detección precoz, el abordaje de los factores de progresión y el manejo de los estadios iniciales de la ERC27.
En el seno de este proyecto se ha publicado recientemente un consenso multidisciplinar sobre los retos y factores clave para un modelo óptimo de atención en ERC que contó con un panel multidisciplinar de profesionales con experiencia en el ámbito de la ERC, integrado por un comité asesor de 15 expertos y un panel adicional de 44 especialistas. Se identificaron diferentes factores clave para poder optimizar el modelo de atención al paciente con ERC, que se centraban en cuatro aspectos: 1)desarrollo de modelos de gestión de la ERC y aumento de la visibilidad de la enfermedad; 2)prevención, cribado, diagnóstico precoz y registro de la ERC; 3)seguimiento integral, multidisciplinar y coordinado, para una mayor optimización del tratamiento y mejora de la continuidad asistencial, y 4)intensificación de la formación en ERC tanto en los profesionales sanitarios como en los pacientes28.
Dentro de estos factores clave, y considerado como altamente prioritario, se encuentran la detección precoz, el diagnóstico y el manejo inicial de la ERC por parte de las organizaciones sanitarias. Con este objetivo nace el proyecto IntERKit. El presente manuscrito se centra en presentar la metodología del proyecto IntERKit, esto es, describir las bases y el marco conceptual del proyecto, proporcionando una base sólida que sirva como primer paso para su difusión y desarrollo.
Proyecto IntERKitA pesar de las recomendaciones nacionales e internacionales acerca de la detección adecuada de la ERC, y la facilidad de realización de las pruebas diagnósticas necesarias, la realidad es que el cribado de la ERC no se realiza hasta en el 50% de los pacientes con alto riesgo de desarrollar ERC7,9,16,29. Esto tiene consecuencias muy relevantes, ya que la falta de detección temprana de la ERC retrasa el tratamiento, empeorando el pronóstico y aumentando los costes sanitarios5,8. En España, esto se debe a varios motivos, entre los que se incluyen la sobrecarga asistencial, particularmente importante en atención primaria, una falta de concienciación real sobre la importancia de la ERC en los profesionales sanitarios, administraciones y población en general, la falta de coordinación entre los niveles asistenciales, la falta de síntomas específicos de la ERC hasta las fases más avanzadas de la enfermedad, la falta de orden en la demanda (ordenar la demanda existente para alcanzar mayor eficiencia y eficacia) y la falta de cultura para el trabajo proactivo27,28. En consecuencia, la detección precoz de la ERC debería ser una estrategia prioritaria dentro del sistema nacional de salud, ya que ofrece importantes ventajas a múltiples niveles (tabla 1)7,30-32.
Ventajas de la detección precoz de la enfermedad renal crónica
| • Prevención/retraso de la progresión de la enfermedad renal, retrasando o disminuyendo la necesidad de tratamiento sustitutivo de la función renal• Reducción de complicaciones asociadas vasculares y no vasculares• Mejoría de la calidad de vida del paciente• Educación y empoderamiento del paciente• Reducción de costes asociados (directos e indirectos)• Optimización del uso de recursos sanitarios |
Fuente: tabla realizada con datos de las referencias7,30-32.
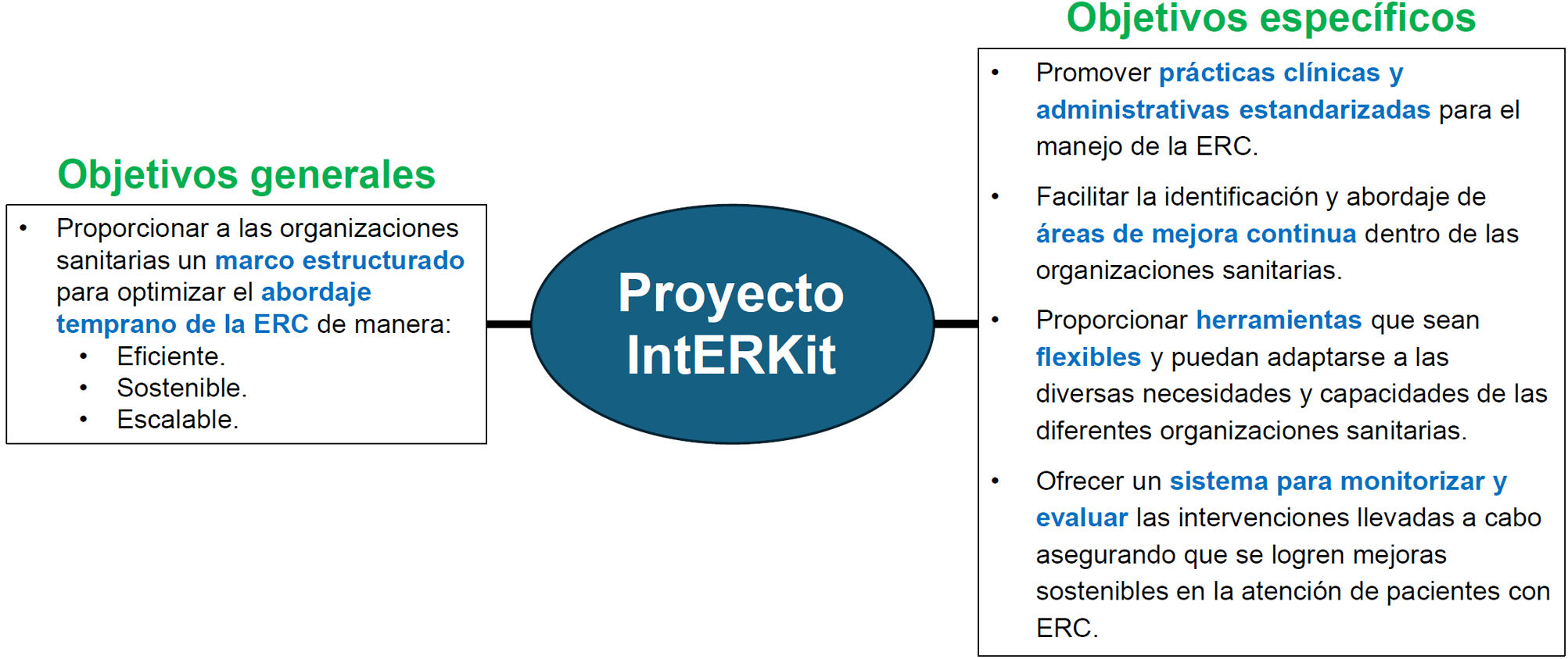
IntERKit es una iniciativa que se enmarca dentro del proyecto IntERCede con el objetivo de mejorar la detección precoz, el diagnóstico y el manejo inicial de la ERC promoviendo la colaboración con las organizaciones sanitarias, mediante herramientas fácilmente implementables por dichas organizaciones. Esto es, proporcionar a las organizaciones sanitarias un marco estructurado para optimizar el abordaje temprano de la ERC de manera eficiente, logrando un impacto real, medible y sostenible, que pueda evolucionar en función de los cambios y de las mejoras obtenidas de acuerdo con unos indicadores específicos, y que sea escalable, facilitando la replicación y la extensión del modelo en el conjunto del sistema sanitario español (fig. 1).
Para la consecución de dichos objetivos se aplican diversas herramientas que permiten mejorar el diagnóstico desde las actuaciones propias de atención primaria y hospitalaria, puesto que se detectan áreas de mejora y, a continuación, se proporcionan herramientas claras que se puedan implementar, junto con un sistema de monitorización y prácticas clínicas estandarizadas para el manejo de la ERC. Ahora bien, dado que IntERKit aborda el manejo temprano de la ERC, se espera que atención primaria sea el eje central de las intervenciones que se lleven a cabo, constituyendo los centros de salud el marco específico de implementación. Y es que, en la ERC, el rol de atención primaria es fundamental por su promoción de salud, detección de riesgos y, por supuesto, realización de pruebas de cribado para el diagnóstico precoz. Por otra parte, se espera que IntERKit tenga un impacto directo en todo el proceso asistencial, ya que el proyecto se ha desarrollado para que su implementación sea liderada desde la dirección asistencial de las organizaciones sanitarias y cuente con la participación no solo de profesionales de atención primaria sino también de atención hospitalaria.
Para la obtención de las herramientas resultantes del proyecto IntERKit se ha contado con un comité científico multidisciplinar, compuesto por expertos a nivel nacional en la atención a la ERC y gestores, tanto en el ámbito de atención primaria como de atención hospitalaria, así como por representantes de otros agentes clave que también intervienen, directa o indirectamente, en el desarrollo óptimo del proceso de detección, diagnóstico y tratamiento temprano de la ERC, como profesionales de laboratorio y de sistemas de información. Este comité científico ha estado compuesto por especialistas en Medicina Familiar y Comunitaria, Nefrología, Cardiología, Endocrinología, Análisis Clínicos, Enfermería especialista Familiar y Comunitaria y Farmacia de Atención Primaria, gestores sanitarios, expertos en salud digital y representantes de asociaciones de pacientes. A partir de distintas reuniones del comité científico y entrevistas personales se consensuaron los puntos críticos y áreas de mejora para el desarrollo del proyecto, así como la creación de las distintas herramientas (toolkit) para la implementación efectiva de IntERKit.
Además, el proyecto IntERKit cuenta con el aval científico de las principales sociedades científicas y de gestión, en concreto SEN, SEMERGEN, SEMG, SEMFYC, SEC, SEEN, SEMI, SEQC-ML, Sociedad Española de Directivos de Atención Primaria (SEDAP), Red de Grupos de Estudio de la Diabetes en Atención Primaria de la Salud (redGDPS), Sociedad Española de Directivos de la Salud (SEDISA) y Sociedad Española Informática de la Salud (SEIS), así como asociaciones de pacientes (Federación ALCER).
En definitiva, el proyecto IntERKit ha dado lugar al diseño de un conjunto de herramientas que facilitan a las organizaciones sanitarias el abordaje de las áreas de mejora identificadas. Dichas áreas incluyen, principalmente:
- 1.
Aumento de la concienciación entre los profesionales sanitarios sobre el impacto que tiene la ERC.
- 2.
Mejora del conocimiento que tienen los profesionales sanitarios sobre la ERC, incluyendo los criterios de diagnóstico, clasificación y tratamiento.
- 3.
Inclusión de pruebas de función renal en las peticiones de análisis clínicos rutinarios, para facilitar la capacidad de detección temprana de la enfermedad.
- 4.
Generación automática de sistemas de alerta que notifique a los profesionales sanitarios de manera temprana y efectiva sobre la presencia de ERC.
- 5.
Traslación de los resultados anormales de laboratorio en el registro de diagnósticos y acciones concretas en la historia clínica electrónica.
- 6.
Desarrollo del papel de enfermería en la detección temprana, manejo inicial y educación del paciente sobre la ERC.
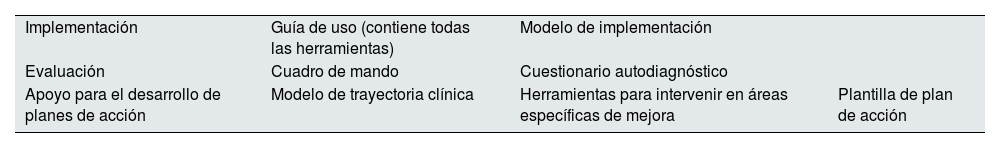
Las herramientas diseñadas para actuar sobre las áreas de mejora indicadas se agrupan en tres grupos: herramientas de implementación, herramientas de evaluación y herramientas de apoyo para el desarrollo de planes de acción (tabla 2).
- •
Herramientas de implementación. Tienen como objetivo detallar los requisitos necesarios, la organización y las actuaciones a desarrollar para llevar a cabo adecuadamente el despliegue del toolkit en las organizaciones sanitarias. Estas herramientas son:
- ∘
La guía de uso, que constituye la herramienta de implementación fundamental de IntERKit, y contiene la presentación del toolkit, describiendo las herramientas que lo componen, explicando los beneficios de su implementación, así como los requisitos que las organizaciones sanitarias deben cumplir para el despliegue del toolkit, definiendo su modelo de implantación.
- ∘
El modelo de implementación de IntERKit, que tiene como elemento base la formación de dos grupos integrados por profesionales de la organización sanitaria: el Comité de Dirección, encargado del liderazgo y planteamiento global, y el Equipo de Implementación.
- ∘
- •
Herramientas de evaluación. Son fundamentales para definir tanto la situación de partida como para evaluar el impacto y la efectividad de las intervenciones. Se han definido dos herramientas de evaluación:
- ∘
Cuadro de mando: incluye un conjunto de 9 indicadores fácilmente explotables desde los sistemas de información de atención primaria, utilizando datos disponibles y accesibles, así como las fórmulas para su medición y la tendencia esperada en su evolución temporal.
- ∘
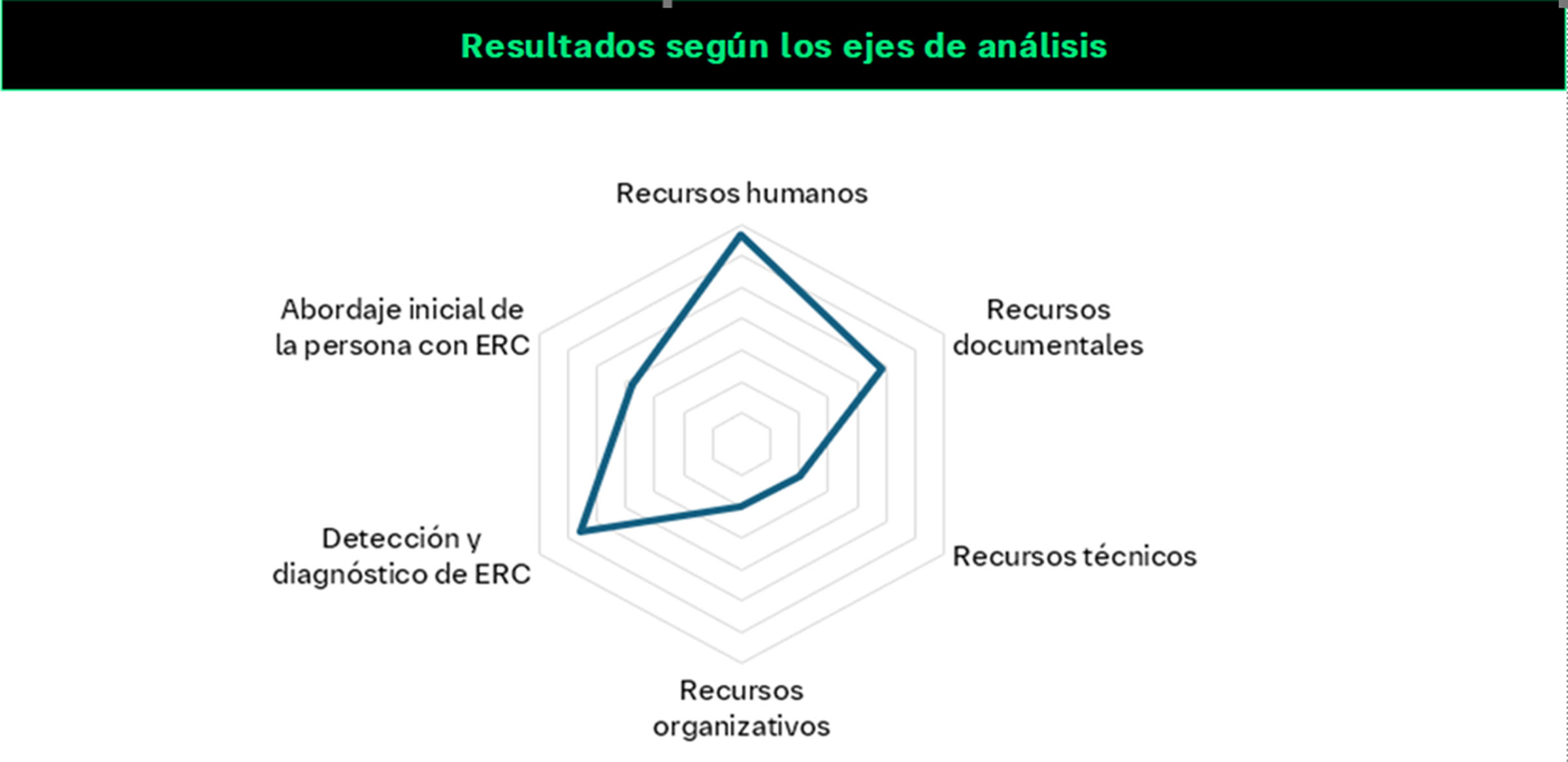
Cuestionario de autodiagnóstico sobre el abordaje inicial de la detección, diagnóstico y tratamiento temprano de la ERC, permitiendo identificar áreas de mejora, así como la generación automática de recomendaciones relativas a las áreas identificadas como de mayor desarrollo potencial (fig. 2).
- ∘
- •
Herramientas de apoyo para el desarrollo de planes de acción. Están diseñadas para estructurar y guiar la implementación de estrategias específicas destinadas a mejorar la detección, el diagnóstico y el tratamiento temprano de la ERC. Estas herramientas incluyen:
- ∘
Modelo de trayectoria clínica que ofrece una secuencia detallada de las acciones que los profesionales sanitarios deben seguir para lograr un abordaje óptimo tanto de la detección precoz de la ERC como del manejo de la enfermedad en sus primeras etapas.
- ∘
Herramientas para intervenir en áreas específicas de mejora, que incluyen una variedad de recursos diseñados para mejorar la detección, el diagnóstico y el tratamiento temprano de la ERC.
- ∘
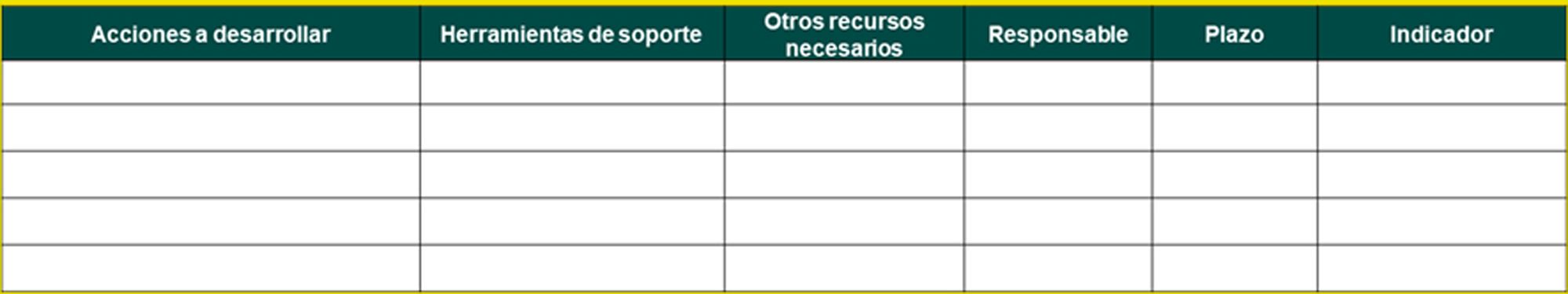
Plantilla de plan de acción, que es una herramienta diseñada para facilitar la planificación, el seguimiento y la ejecución de los mismos en las diferentes áreas de mejora identificadas (fig. 3).
- ∘
Herramientas del proyecto IntERKit
| Implementación | Guía de uso (contiene todas las herramientas) | Modelo de implementación | |
| Evaluación | Cuadro de mando | Cuestionario autodiagnóstico | |
| Apoyo para el desarrollo de planes de acción | Modelo de trayectoria clínica | Herramientas para intervenir en áreas específicas de mejora | Plantilla de plan de acción |
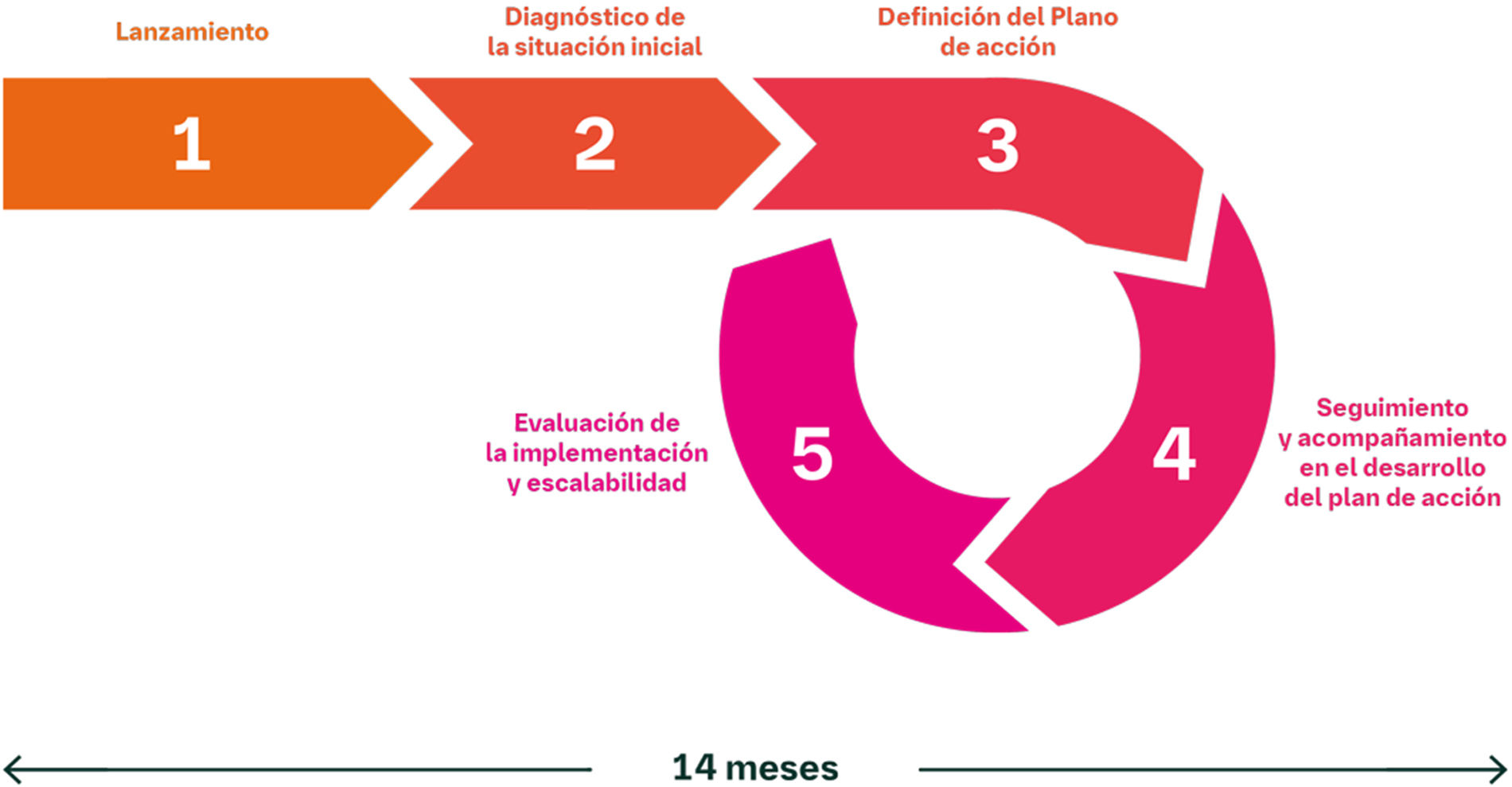
El modelo de implementación de IntERKit se estructura en 5 fases de desarrollo (fig. 4):
- 1.
Lanzamiento del proyecto.
- 2.
Diagnóstico de la situación inicial, mediante herramientas de evaluación, cuadro de mando y cuestionario de autodiagnóstico, que permiten a cada organización identificar el punto de partida, tanto a nivel cuantitativo como cualitativo, y las áreas de mejora.
- 3.
Definición y puesta en marcha del plan de acción, con soluciones concretas que permitan mejorar el diagnóstico temprano de la ERC. Para ello se utiliza una plantilla de plan de acción, que es una herramienta diseñada para facilitar la planificación, el seguimiento y la ejecución de los planes de acción para el abordaje de áreas de mejora identificadas, que incluyan acciones a desarrollar en áreas específicas, recursos necesarios, responsabilidades, plazos e indicadores de seguimiento.
- 4.
Seguimiento y acompañamiento en el desarrollo del plan de acción, a través del equipo de implementación que evalúa mediante reuniones periódicas cómo se está desarrollando el plan de acción. Con esta información, junto con los indicadores, el Comité de Dirección actualiza el plan de acción de manera continua.
- 5.
Evaluación de la implementación y la escalabilidad, mediante indicadores críticos, que serán analizados y permitirán determinar su éxito, encontrando nuevos puntos de mejora, limitaciones, permitiendo cambios y ajustes de actuación.
Tras un período inicial de implantación de 14 meses, se reinicia el proceso desde la fase3, de tal forma que se promueve la mejora continua de la atención a las personas con ERC mediante el desarrollo de sucesivos planes de acción, fomentando la sostenibilidad a largo plazo de los resultados alcanzados.
Desde un punto de vista práctico, se están realizando gestiones con el fin de ponerse en contacto con diferentes organizaciones sanitarias a nivel nacional, para explicar de manera pormenorizada el proyecto IntERKit y permitir la implementación del mismo. Posteriormente, se realizará el análisis para evaluar los efectos de dicha implementación y se publicarán los resultados.
ConclusionesIntERKit ofrece un modelo de implantación sencillo, entendible y accesible que facilita el diagnóstico temprano, sostenible y escalable de la ERC en España, mediante la implementación de planes específicos para la mejora del diagnóstico en las organizaciones sanitarias, con especial foco en atención primaria.
FinanciaciónEl proyecto intERKit ha sido financiado por Boehringer Ingelheim.
El desarrollo del proyecto intERKit fue realizado con la consultora CROWE, financiado por Boehringer Ingelheim.
Content Ed Net proporcionó asistencia de redacción médica y asistencia editorial para la confección de este manuscrito trabajando con los autores, financiado por Boehringer Ingelheim. Boehringer Ingelheim tuvo la oportunidad de revisar el manuscrito para verificar su precisión médica y científica en lo que se refiere a fármacos de Boehringer Ingelheim, así como consideraciones de propiedad intelectual.
La actividad investigadora de AO sobre el tema está financiada por Comunidad de Madrid en Biomedicina P2022/BMD-7223, CIFRA_COR-CM. Instituto de Salud CarlosIII (ISCIII) RICORS program to RICORS2040 (RD21/0005/0001) co-funded by European Union and SPACKDc PMP21/00109, FEDER funds, COST Action PERMEDIK CA21165, supported by COST (European Cooperation in Science and Technology); PREVENTCKD Consortium Project ID: 101101220 Programme: EU4H DG/Agency: HADEA. KitNewCare, Project ID: 101137054, Call: HORIZON-HLTH-2023-CARE-04, Programme: HORIZON. DG/Agency: HADEA.
Contribución de los autoresLos autores cumplen los criterios de autoría recomendados por el Comité Internacional de Editores de Revistas Médicas (ICMJE). Todos los autores han contribuido significativamente al trabajo presentado en este artículo, contribuyendo en la concepción, diseño o adquisición de información, o en el análisis e interpretación de datos. Todos los autores han participado en la redacción y/o revisión del manuscrito y aceptan su publicación.
Conflicto de interesesLos autores no han recibido honorarios relacionados con el desarrollo del manuscrito.
José Luis Górriz declara financiación para realizar ensayos clínicos de AstraZeneca, Bayer, Boehringer Ingelheim y Novo Nordisk (todos al Instituto de Investigación INCLIVA); honorarios de consultoría de AstraZeneca, Bayer, Boehringer-Ingelheim y Novo Nordisk; pago de honorarios por conferencias de AstraZeneca, Novo Nordisk, Bayer, Menarini, Boehringer-Ingelheim y Eli Lilly.
Fran Adán Gil no declara conflicto de intereses.
Manuel A. Botana López ha recibido honorarios por consultoría de AstraZeneca, Boehringer Ingelheim, Daiichi Sankyo, Esteve, Roche, Sanofi. Por ponencias, trabajos o informes, ha recibido honorarios de AstraZeneca, Almirall, Boehringer Ingelheim, Daiichi-Sankyo, Novo Nordisk, Novartis, Lilly, Sanofi, Servier. En concepto de invitaciones a congresos, cursos o actos educativos organizados por la industria farmacéutica ha recibido colaboraciones de AstraZeneca, Boehringer Ingelheim, Lilly, Novo Nordisk, Novartis, Menarini, Sanofi.
Antonio Buño Soto no declara conflicto de intereses.
Francisco José Campos Cabrera ha participado en labores de consultoría para Boehringer-Ingelheim.
Ángeles Cisneros no declara conflicto de intereses.
Silvia Cobo Guerrero ha recibido honorarios por conferencias de AstraZeneca, GlaxoSmithKline y Chiesi. Por asistencia a congresos, jornadas y actividades de formación de Boehringer-Ingelheim, AstraZeneca, GlaxoSmithKline, Lundbeck y Chiesi. Participación en documentos de consenso con el soporte de Boehringer-Ingelheim y AstraZeneca sin recibir honorarios.
María Dolores Conejos declara asistencia financiada a congresos, jornadas y actividades de formación por parte de Boehringer-Ingelheim y Novo Nordisk. Honorarios por participación en mesas de congresos por parte de Boehringer-Ingelheim.
Isabel Egocheaga Cabello declara haber percibido honorarios de consultoría de Bayer, Boehringer-Ingelheim y Viatris; pago de honorarios por actividades formativas de AstraZeneca, Rovi, Boehringer-Ingelheim y Eli Lilly.
M. Concepción Fernández Planelles no declara conflicto de intereses.
Lisardo García-Matarín ha recibido honorarios por conferencias AstraZeneca, Boehringer-Ingelheim, Lilly, Chiesi, GlaxoSmithKline, Bial, Menarini, Teva, Novartis, Pfizer, Sanofi Aventis, FAES, Novo Nordisk y Vifor Pharma. Ha participado en advisory boards de Boehringer-Ingelheim, AstraZeneca, Daiichi Sankyo y GlaxoSmithKline.
Natalia Jiménez es empleada de Boehringer Ingelheim España.
Juan Carlos Julián Mauro declara que su entidad (ALCER) recibe becas no relacionadas con este proyecto, por su participación en advisory boards o para proyectos de educación sociosanitaria de las compañías: Astellas, AstraZeneca, Baxter, BMS, Boehringer-Ingelheim, CSL Vifor, Diaverum, Fresenius, GSK, Hansa Biopharma, Ipsen, MSD, Novartis, Novonordisk y Pfizer.
David León Jiménez ha recibido honorarios como ponente de AstraZeneca Pharmaceuticals LP, Boehringer Ingelheim Pharmaceuticals Inc., Eli Lilly and Company, Janssen Pharmaceuticals Inc., Mundipharma, Sanofi, Esteve, Novo Nordisk, Mylan (Viatris), Bayer, Novartis, Rovi, Amgen. Asesoría: Sanofi, Boehringer Ingelheim Pharmaceuticals Inc., Eli Lilly and Company.
Daniel Martínez Gamote ha recibido honorarios por labores de consultoría para Boehringer-Ingelheim.
Pilar Mazón Ramos declara participación en congresos/Asesorías de AZ, Esteve, Boehringer-Ingelheim, Bayer, BMS-Pfizer, Daichii-Sankyo, Servier, Ferrer, Novo-Nordisk.
Alberto Ortiz ha recibido becas de Sanofi. Ha recibido honorarios por asesoramiento, ponencias y soporte para viajes de Adviccene, Alexion, Astellas, AstraZeneca, Amicus, Amgen, Bioporto, Boehringer Ingelheim, Esteve, Fresenius Medical Care, GSK, Bayer, Sanofi-Genzyme, Sobi, Menarini, Mundipharma, Kyowa Kirin, Lilly, Freeline, Idorsia, Chiesi, Otsuka, Novo-Nordisk, Sysmex and Vifor Fresenius Medical Care Renal Pharma y Spafarma, y es Director de la Cátedra UAM-AstraZeneca de enfermedad renal crónica y electrólitos. Posee acciones de Telara Farma.
Gemma Palau es empleada de Boehringer Ingelheim España.
Julia Quevedo Rivera ha participado en el documento de consenso por parte de Boehringer-Ingelheim.
Emilio Sánchez-Álvarez no declara conflicto de intereses.
Rita Tristancho Ajamilha ha participado en el documento de consenso por parte de Boehringer-Ingelheim.
Cristina Varga no declara conflicto de intereses.
Roser Vallés Fernández declara asistencia financiada a congresos, jornadas y actividades de formación por Pfizer, Daiichi-Sankyo y GSK. Honorarios por conferencia de GSK y participación documento de consenso por parte de Boehringer-Ingelheim.