La hipercalcemia postrasplante debida a la persistencia del hiperparatiroidismo (HPT) secundario tiene una prevalencia elevada en los primeros 3 meses postrasplante, que va disminuyendo a lo largo del primer año, aunque en torno al 5-10 % de los trasplantados renales persiste en el tiempo. La mayor resorción ósea y la mayor reabsorción tubular de calcio debido a la acción de la hormona paratiroidea (PTH) parecen ser los mecanismos principalmente implicados en la hipercalcemia. La PTH en el momento del trasplante renal (TR) es el factor que determina el desarrollo de hipercalcemia pos-TR, aunque a veces se encuentre enmascarada en los pacientes bien controlados con tratamiento médico. Cada vez más los pacientes en diálisis reciben cinacalcet como tratamiento del HPT secundario. La retirada del calcimimético en el momento del trasplante renal da lugar a una mayor prevalencia de hipercalcemia e hiperparatiroidismo en estos pacientes. En los pacientes con PTH bien controlada con cinacalcet antes del trasplante, existe una relación directa entre la dosis y el desarrollo posterior de hipercalcemia, probablemente porque indica la presencia de un HPT secundario más severo. La hipercalcemia puede tener efectos deletéreos sobre el injerto renal dando lugar a calcificación tubulointersticial. La hipercalcemia persistente es una marcador de aumento del riesgo de empeoramiento de la patología ósea de estos pacientes. Hoy en día, la primera opción de tratamiento la constituye el cinacalcet, y ante la ausencia de respuesta se valorará la realización de una paratiroidectomía. En esta revisión proponemos un algoritmo de manejo de la hipercalcemia pos-TR.
Post-transplant hypercalcemia due to persistent secondary hyperparathyroidism (HPT) has a high prevalence in the first 3 months after surgery and decreases during the first year, but it persists over time in around 5-10% of renal transplant patients. The increased bone resorption and tubular reabsorption of calcium due to the action of the parathyroid hormone (PTH) appear to be the main mechanisms involved in hypercalcemia. At the time of the renal transplantation (RT), PTH is the factor that determines the development of post-RT hypercalcemia, although it is sometimes masked in patients who are well controlled with medical treatment. The number of dialysis patients receiving treatment with cinacalcet for secondary HPT is increasing. The withdrawal of the calcimimetic at the time of renal transplantation results in a higher prevalence of hypercalcaemia and hyperparathyroidism in these patients. In patients with PTH well controlled with cinacalcet before transplantation, there is a direct relationship between the dose and the subsequent development of hypercalcemia, probably because it indicates the presence of a more severe secondary HPT. Hypercalcemia may have deleterious effects on the renal graft, resulting in tubulointerstitial calcification. Persistent hypercalcemia is a marker of an increased risk of bone disease deterioration in these patients. Nowadays, the first treatment option is cinacalcet and if there is no response, we consider performing a parathyroidectomy. In this review, we propose an algorithm for management of post-RT hypercalcemia.
INTRODUCCIÓN
La hipercalcemia es un hallazgo frecuente en los pacientes con trasplante renal (TR) funcionante, con una prevalencia que oscila entre el 5 y el 66 % según las series1-4, si bien la hipercalcemia severa (calcio total > 12 mg/dl) es bastante excepcional.
Estas diferencias de prevalencia se deben a varios factores, como el hecho de considerar distintos valores de corte como diagnósticos de hipercalcemia o el que se considere el valor sérico de calcio iónico o de calcio total, corregido o no por albúmina.
Otro factor a tener en cuenta es el período de tiempo considerado, ya que la prevalencia de la hipercalcemia va disminuyendo a medida que pasa el tiempo desde el TR. Por lo general, la prevalencia de la hipercalcemia se ha descrito como mucho más elevada durante los tres primeros meses después del TR, descendiendo de forma progresiva hasta el primer año para más adelante permanecer prácticamente estable en torno al 5-10 %2-5.
Hasta la aparición, en el año 2003, de las guías de manejo de las alteraciones del metabolismo mineral óseo en los pacientes con enfermedad renal crónica6, las series de pacientes recogidas mostraban una mayor incidencia y prevalencia de hipercalcemia pos-TR. De hecho, ya en el año 1973 se describió una prevalencia de hipercalcemia al año del TR superior al 30 %, que persistía prácticamente sin cambios a los 2 y 5 años del trasplante5.
Tras la aparición de las guías6 y su aplicación en la clínica, parece producirse un punto de inflexión en la prevalencia de hipercalcemia postrasplante. Así se pudo constatar al comparar pacientes estudiados entre 2004 y 2006 con un grupo control histórico de pacientes estudiados entre 1989 y 20021,2, en los que se observó una prevalencia de hipercalcemia del 41 % en el grupo histórico, mientras que en el grupo más actual se reducía al 14 %.
No obstante, la mayor parte de los estudios que han investigado el metabolismo de calcio después del TR se han realizado previamente a la introducción del cinacalcet en el tratamiento del hiperparatiroidismo (HPT) secundario de los pacientes en diálisis.
El cinacalcet fue aprobado por la United States Food and Drug Administration en 2004 y por la Agencia Europea del Medicamento en 2005 para el tratamiento del HPT secundario de los pacientes en diálisis, y posteriormente para el tratamiento del carcinoma de paratiroides y el HPT primario. La eficacia del cinacalcet en el control de la hormona paratiroidea (PTH) de los pacientes en diálisis ha sido ampliamente demostrada7-10.
El mejor control del HPT secundario en los pacientes en diálisis a partir de la introducción del cinacalcet probablemente condiciona un cambio en el escenario de las alteraciones del metabolismo mineral óseo después del TR, aunque esta situación todavía ha sido poco estudiada.
CAUSAS DE LA HIPERCALCEMIA
Los estudios de la era previa a la introducción del cinacalcet mostraban que los valores séricos elevados de PTH eran el predictor más importante de hipercalcemia postrasplante1.
La introducción del cinacalcet ha conllevado un mejor control del HPT secundario, con lo que ha disminuido considerablemente el porcentaje de pacientes que llegan al TR con valores séricos elevados de PTH. Sin embargo, la retirada del cinacalcet desde el momento del TR condiciona la presencia de niveles elevados de PTH en el postrasplante inmediato, y consecuentemente hipercalcemia en un elevado número de pacientes11.
Un reciente estudio, aunque con un número reducido de pacientes, ha constatado también este hecho, y los pacientes en tratamiento con cinacalcet antes del trasplante a los que se suspendió el tratamiento el día de la cirugía presentaban, al tercer mes postrasplante, una incidencia de hipercalcemia (Ca corregido > 10,3 mg/dl) superior frente a los pacientes que no habían recibido cinacalcet (42,9 % vs. 11,4 %)12.
En nuestra experiencia, al comparar pacientes que recibían cinacalcet en el momento del TR frente los que no lo recibían, encontramos una proporción de hipercalcemia (Ca corregido > 10,3 mg/dl) de 26,3 % al mes 3 postrasplante frente a 0 % de hipercalcemia en el grupo control (p = 0,01), a pesar de presentar ambos grupos valores de PTH y calcemia similares en el momento del trasplante13.
Los estudios posteriores a la introducción del cinacalcet muestran que la PTH pretrasplante influye en los valores de Ca postrasplante solo en los pacientes que no estaban en tratamiento con cinacalcet, mientras que, en aquellos pacientes que recibían cinacalcet previamente al TR, era la dosis de cinacalcet la que predecía el desarrollo posterior de HPT e hipercalcemia al actuar como un probable indicador de la severidad del HPT secundario de estos pacientes11,12.
FISIOPATOLOGÍA
Los mecanismos fisiopatológicos sugeridos como responsables de la hipercalcemia postrasplante son:
-Una mayor reabsorción tubular de calcio, debida a la acción de la PTH. Los resultados de diferentes estudios son dispares; mientras algunos muestran un disminución de la fracción de excreción de calcio1, otros refieren mayor excreción urinaria de calcio3. Parece que el efecto de la PTH aumentando la reabsorción tubular de calcio sería más manifiesto a largo plazo y menos manifiesto en el postrasplante inmediato1,3.
- Una mayor absorción intestinal de calcio, debida a un aumento de los valores séricos de calcitriol provocados por el aumento de su síntesis debido al estímulo de la PTH. Los valores séricos de calcitriol se recuperan de manera paulatina en la mayor parte de los pacientes tras el TR y nosotros hemos observado que ello está en relación con la rápida y progresiva disminución de los valores séricos de FGF23 (factor de crecimiento fibroblástico)13. Sin embargo, no ha habido ningún estudio que haya mostrado diferencias en los valores de calcitriol entre los pacientes con hipercalcemia y normocalcemia1,2.
- Una mayor resorción ósea de calcio, mediada por la PTH. Este parece ser el mecanismo implicado sobre todo en el TR reciente. En los pacientes con hipercalcemia se observan valores séricos de fosfatasa alcalina significativamente más elevados que en los pacientes con normocalcemia, lo que sugiere un aumento del turnover óseo1.
CONSECUENCIAS DE LA HIPERCALCEMIA
- Efecto sobre el injerto renal. La hipercalcemia, a través de un mecanismo de vasoconstricción, puede deteriorar el funcionalismo del injerto renal, tanto de manera aguda5 como crónica3,14. También puede provocar calcificaciones tubulointersticiales que podrían influir negativamente en la supervivencia del injerto a largo plazo15.
- Otros efectos. Se han descrito casos de pancreatitis en trasplantados renales con hipercalcemia por HPT16, y también se ha demostrado que incrementa el riesgo de calcificaciones en tejidos blandos y del desarrollo de calcificación vascular17.
Por otro lado, la hipercalcemia es fundamentalmente consecuencia del aumento del remodelado óseo con aumento de la resorción de calcio, por lo que la persistencia de hipercalcemia nos estará indicando que existe un incremento del riesgo de empeoramiento de la patología ósea de estos pacientes16,18.
MANEJO DE LA HIPERCALCEMIA POSTRASPLANTE
Para manejar la hipercalcemia debida a la persistencia del HPT después del TR, las alternativas son:
a) Conducta expectante. La actitud inicial, en caso de hipercalcemia moderada, puede ser el monitorizar los valores séricos de calcio y PTH a la espera de que estos se vayan normalizando con el paso del tiempo. No obstante, ante hipercalcemia importante (> 11 mg/dl) y/o persistente en el tiempo (> 1 año), o sintomática, deberíamos adoptar una actitud más proactiva.
En nuestra opinión, al igual que otros grupos19, creemos que, de no existir sintomatología o hipercalcemia importante, parece prudente esperar al menos un año con vistas a una resolución espontánea, si bien algunos autores abogan por esperar solamente entre 3-6 meses después del TR para decidir la paratiroidectomía20.
b) Paratiroidectomía. Clásicamente ha sido la única alternativa para controlar la hipercalcemia en estos pacientes y sigue siendo la opción que mejor corrige la hipercalcemia si la comparamos con el tratamiento con calcimiméticos21. Pero, por el contrario, muestra un mayor riesgo de hipocalcemia aguda y sostenida en el tiempo22, así como una elevada tasa de persistencia o recurrencia del HPT, dependiendo de la técnica empleada.
La paratiroidectomía no está exenta de riesgos:
- Síndrome del hueso hambriento, que conlleva una severa hipocalcemia después de la cirugía, con sintomatología que va desde parestesias a tetania franca, que a veces es difícil de controlar, requiriendo altas dosis de suplementos de calcio y vitamina D.
- Complicaciones quirúrgicas locales: infecciones de la herida quirúrgica, parálisis del nervio recurrente (descrito en el 1 % de las intervenciones y con recuperación progresiva posterior).
- Deterioro de función renal. Algunos estudios han observado un empeoramiento de la función renal tras la paratiroidectomía21,23-26, mientras que otros no lo han objetivado19,22. El deterioro de función renal es independiente del tipo de paratiroidectomía y parece que los pacientes en los que se deteriora la función renal ya presentaban deterioro previamente a la paratiroidectomía27.
Las opciones quirúrgicas son:
- Paratiroidectomía total con autotrasplante en antebrazo. La paratiroidectomía total con autotrasplante en el antebrazo conlleva una corrección más rápida de la calcemia; sin embargo, da lugar a un mayor riesgo de hipocalcemia.
En pacientes con TR funcionante, el índice de recidiva parece similar entre esta técnica y la paratiroidectomía subtotal28.
En caso de recidiva/persistencia, a veces es difícil discernir si ello es debido a una hiperplasia del autotrasplante o del posible tejido residual en el área cervical. En este caso, la gammagrafía MIBI nos puede ser de ayuda29.
La glándula autotrasplantada en antebrazo en caso de recidiva parece ser más accesible30, aunque también, en caso de hiperplasia importante (también denominada paratiromatosis), esta se suele diseminar por al área de implante y ser muy difícil de resecar.
- Paratiroidectomía subtotal. Consiste en la exéresis de todas las paratiroides, excepto un resto de glándula bien vascularizado del tamaño de una glándula normal. El resto de la glándula que se deja debería tener un aspecto macroscópico normal o el de una hiperplasia difusa simple. Muchos autores abogan por ella al considerarla la técnica menos agresiva28.
- Paratiroidectomía total sin autotrasplante. Es una alternativa eficaz en términos de mejoría del dolor óseo y, probablemente, es con la que se observa menor número de recurrencia/recidivas del HPT31-34.
En contraposición, la mayoría de estos pacientes suelen requerir suplementación con calcio y vitamina D de forma indefinida para evitar hipocalcemia y osteomalacia, respectivamente.
- Paratiroidectomía selectiva. Consiste en realizar la paratiroidectomía de solo una o dos glándulas paratiroideas. Si con la exploración ecográfica cervical y/o gammagrafía MIBI se demuestra que existen una o dos glándulas adenomatosas, algunos autores abogan por extirpar solo esas glándulas patológicas (aumentadas de tamaño y/o hipercaptantes).
Con esta técnica, el porcentaje de hipocalcemia aguda es menor que con las anteriores técnicas y el porcentaje de hipocalcemia persistente es casi nulo16,35. Por el contrario, parece aumentar el riesgo de persistencia/recurrencia del HPT28,36, aunque también hay series que muestran una buena evolución y baja incidencia de recidiva16,35,37
c) Calcimiméticos. Desde el año 2006, los calcimiméticos se han empleado como tratamiento alternativo de la hipercalcemia secundaria a la persistencia del HPT secundario (también denominado HPT terciario) en pacientes con TR funcionante38-46.
En todos los estudios publicados se confirma el adecuado control de la calcemia con mejoría de valores séricos de PTH y de la fosfatemia.
En la mayoría de ellos, no se han descrito efectos sobre la función renal, aunque en algún caso excepcional se ha descrito deterioro leve de la función renal a los tres meses44 o tras un año de tratamiento con cinacalcet41, si bien en este último trabajo se incluyeron pacientes con deterioro de función renal previo al inicio de cinacalcet que fue reversible en todos los casos tras el cese de la medicación41.
Aunque no queda claro a qué se debe este deterioro de función renal que se produce en algunas ocasiones, se ha sugerido que podría estar en relación con el descenso de los valores de PTH, al igual que ocurre tras la paratiroidectomía23,47. Esto ya se había descrito en estudios experimentales previos que sugerían que la PTH juega un papel en la regulación de la perfusión renal y en la función de las células mesangiales48,49.
Otra posibilidad que se ha sugerido es que el deterioro de la función renal estuviese relacionado con la posible hipercalciuria secundaria a la disminución de la PTH; sin embargo, en la mayoría de los estudios de pacientes en tratamiento con cinacalcet no se ha observado hipercalciuria relevante, y en ningún caso desarrollo de calcificación tubular renal50.
Recientemente un estudio retrospectivo que comparaba el uso de calcimiméticos frente a la paratiroidectomía y frente a la observación médica sin intervención alguna en trasplantados renales con función renal estable e HPT terciario ha observado una mayor tasa de fracaso renal agudo y de deterioro del injerto renal en el grupo de pacientes que no recibían tratamiento para su HPT terciario22.
El cinacalcet es una opción terapéutica segura para el tratamiento de la hipercalcemia en los pacientes receptores de TR; sin embargo, se observa recidiva del HPT tras la retirada de los calcimiméticos38,43.
Actualmente no conocemos ningún marcador que nos pueda indicar el tiempo que se ha de mantener el tratamiento con calcimiméticos.
Considerando que se trata de un grupo de pacientes en muchas ocasiones polimedicados y que el hecho de mantener esta medicación de manera indefinida tiene un coste económico elevado, es necesario realizar estudios que nos permitan encontrar algún marcador que nos ayude a conocer en qué momento podríamos retirar el tratamiento con calcimiméticos sin riesgo de recidiva del HPT y consecuente desarrollo de hipercalcemia.
En cualquier caso, en nuestra opinión, se debería ensayar el tratamiento con calcimiméticos para el manejo de la hipercalcemia postrasplante renal antes de practicar una paratiroidectomía.
PROPUESTA DE MANEJO DE LA HIPERCALCEMIA POSTRASPLANTE
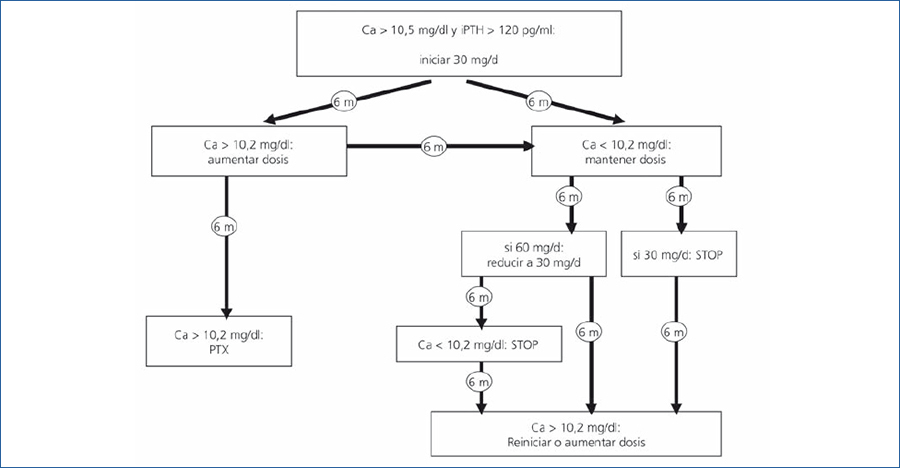
Con la revisión de la literatura y teniendo en cuenta la experiencia clínica acumulada, mostramos una propuesta de manejo de la hipercalcemia postrasplante renal, reflejada de manera esquemática en forma de algoritmo (figura 1).
Proponemos iniciar tratamiento con cinacalcet en todos los pacientes con Cac > 11 mg/dl y en los que presenten Cac entre 10,5-11 mg/dl durante más de 6 meses, en todos los casos con PTH > 120 pg/ml. La dosis de inicio será de 30 mg/día de cinacalcet, que se mantendrá durante 6 meses.
En caso de que el paciente responda a la dosis inicial de 30 mg/día (Cac < 10,2 mg/dl a los 6 meses de tratamiento), proponemos mantener la misma dosis 6 meses más (total 1 año) y, si persiste buen control, suspender la medicación, con un nuevo control a los 6 meses, de manera que si la calcemia aumentase nuevamente por encima de 10,2 mg/dl reiniciaríamos el tratamiento con cinacalcet.
Si, por el contrario, con la dosis inicial de 30 mg/día la calcemia persiste elevada (Cac > 10,2 mg/dl a los 6 meses), incrementaremos la dosis a 60 mg/dl. Si con el aumento de dosis consiguiésemos controlar la calcemia, se podría plantear disminuir nuevamente la dosis a 30 mg/día a los 6 meses y mantener esta pauta al menos otros 6 meses más. Si con ello se controla la calcemia, podemos plantearnos la retirada del fármaco.
En caso de que el paciente persista durante más de 12 meses con Cac > 10,5 mg/dl a pesar de haber incrementado las dosis de cinacalcet, probablemente lo más conveniente sería plantear la realización de una paratiroidectomía.
Conflictos de interés
Los autores declaran que no tienen conflictos de interés potenciales relacionados con los contenidos de este artículo.
Figura 1. Manejo orientativo de la hipercalcemia postrasplante renal