Los compuestos que contienen magnesio constituyen una aportación muy prometedora como captores del fósforo en el control de la hiperfosfatemia en el paciente con enfermedad renal crónica (ERC). Sin embargo, el efecto del magnesio en pacientes con ERC no está aún claro. Este artículo tiene como objetivo mejorar el conocimiento acerca del papel fisiológico del magnesio en la población general y en el paciente con ERC en particular. La prevalencia de la hipomagnesemia es elevada en la población general y especialmente en los pacientes ingresados en las Unidades de Cuidados Intensivos, y en muchos casos pasa inadvertida. El déficit de magnesio aumenta el riesgo de sufrir algunas enfermedades, como la diabetes tipo 2, la hipertensión y la arteriosclerosis. Por otra parte, la hipermagnesemia moderada parece tener efectos beneficiosos sobre la calcificación vascular y la mortalidad en pacientes con ERC. Además, se ha observado que la hipermagnesemia se asocia a niveles más bajos de hormona paratiroidea en estos pacientes, aunque los resultados sobre el hueso son controvertidos. Asimismo, la reducción del magnesio sérico se asocia a bajos índices de volumen óseo, osteoporosis y calcificación vascular. En los pacientes en diálisis, los niveles séricos de magnesio dependen principalmente de la concentración en el líquido de diálisis. A largo plazo, la administración de magnesio a los pacientes en diálisis podría retrasar la calcificación arterial y mejorar la supervivencia, pero se necesitan estudios prospectivos aleatorizados potentes para confirmar estos efectos. Puesto que hay un estudio aleatorizado prospectivo reciente que demuestra que un captor del fósforo que combina carbonato de magnesio y acetato cálcico fue igual de efectivo que el compuesto polimérico sevelamer ClH con similar perfil de tolerancia, procede examinar y poner al dia el papel del magnesio en los pacientes con ERC.
Magnesium containing compounds present promising oral phosphate binders for the treatment of hyperphosphataemia in patients with chronic kidney disease (CKD). However, the impact of magnesium in CKD patients still remains unclear in clinical routine practice. Therefore, this publication provides a practicable overview of knowledge about the physiological role of magnesium in general and in particular in CKD patients. Prevalence of hypomagnesaemia is high in the general population and especially in intensive care unit patients, but often not being detected. Magnesium deficiency increases the risk for several diseases, like diabetes mellitus type 2, hypertension and atherosclerosis. Moderate hypermagnesaemia, however, seems to have beneficial effects on vascular calcification and mortality rates in CKD patients. On the other hand, higher serum magnesium levels are reported to be linked to lower PTH levels and results on the effects on bone are controversial. In addition, low magnesium levels are associated with low bone mass, osteoporosis and vascular calcification. In dialysis patients serum magnesium levels are dependent mainly on the dialysate magnesium concentration. To confirm the potential delay of arterial calcification and improved survival outcomes by long-term intervention with magnesium powered randomized studies are required in dialysis patients. Since a recent trial revealed that a phosphate binder containing a combination of magnesium carbonate and calcium acetate was as effective as the polymer-based agent sevelamer hydrochloride and had an equally good tolerability profile, it is time for a re-examination of the role of magnesium in CKD patients.
INTRODUCCIÓN
El magnesio es el cuarto catión corporal más abundante y cumple importantes funciones en numerosas reacciones enzimáticas, procesos de transporte y síntesis de proteínas, ADN y ARN. A pesar de su importancia fisiológica, su importancia clínica está con frecuencia subestimada. De hecho los trastornos del magnesio se mencionan muy escasamente en la mayoría de los libros de medicina. Además, las concentraciones séricas de magnesio no se miden de forma rutinaria en el paciente hospitalizado y, por lo tanto, la mayoría de las alteraciones del magnesio no son detectadas1. Durante los últimos 20 años, ha habido un incremento en el conocimiento acerca del magnesio, abriéndose nuevas expectativas para los pacientes. Nuestro objetivo es presentar un panorama general acerca del metabolismo del magnesio y de los trastornos en el balance de magnesio, especialmente en los pacientes con enfermedad renal crónica (ERC). Es importante analizar el papel de los captores de fósforo que contiene magnesio en la ERC, ya que el uso de estos compuestos ofrece un nuevo camino para resolver algunos problemas asociados con otros captores de fósforo. Esta revisión está basada en una reciente publicación acerca del magnesio en la salud y en la enfermedad2.
METABOLISMO DEL MAGNESIO Y FISIOLOGÍA
El magnesio cumple varias funciones intracelulares. Estabiliza los enzimas en muchas reacciones que generan ATP, antagoniza el calcio en la contracción muscular, modula la señal de transducción y proliferación celular de la insulina y es importante para la adhesión celular y el transporte de membrana3. Cerca del 99 % del magnesio total se localiza en el hueso, músculos y tejidos blandos no musculares. El magnesio extracelular supone cerca del 1 % y se encuentra fundamentalmente en el suero y en los hematíes4.
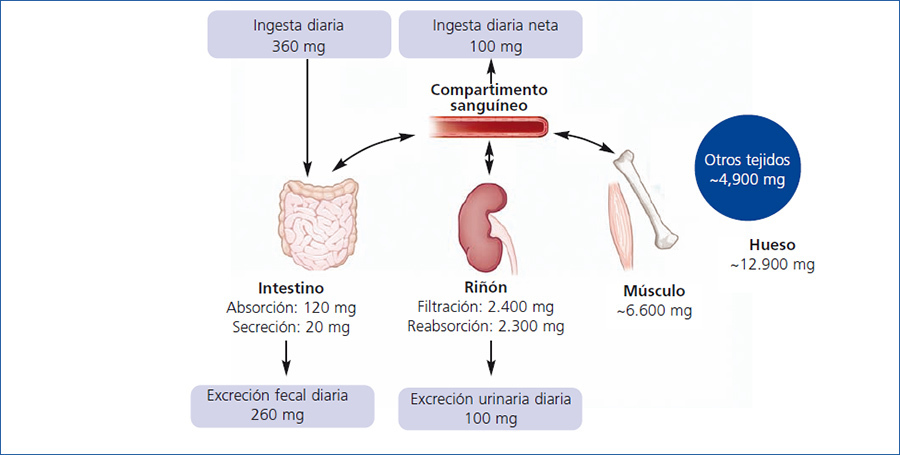
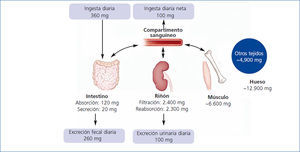
Los seres humanos tienen que consumir magnesio de forma regular para prevenir su deficiencia. Se recomienda 310-316 mg y 400-420 mg para mujeres y hombres adultos, respectivamente. El intestino, el hueso y los riñones mantienen la homeostasis del magnesio (figura 1): el magnesio es absorbido en el intestino, almacenado en el hueso y músculo y excretado por los riñones. La absorción intestinal depende del estado del magnesio y, así, los niveles de magnesio descendidos aumentan la absorción intestinal. Sin embargo, la regulación de la captación de magnesio intestinal es muy compleja y todavía no se comprende perfectamente. La mayoría del magnesio se absorbe de una forma pasiva con un mecanismo paracelular pasivo que está dirigido por el gradiente electroquímico3. Una menor pero importante fracción de magnesio se transporta activamente a través de dos canales transcelulares5. Además de la absorción intestinal, la excreción renal es crucial en el mantenimiento del balance de magnesio. Los riñones regulan la excreción de magnesio y la reabsorción dentro de unos márgenes muy amplios. La excreción renal de la carga filtrada puede variar del 0,5 al 79 %. En estadios 1-3 con moderada ERC, la pérdida de la función renal se compensa por un aumento en la excreción fraccional de magnesio, mientras que este mecanismo falla en la ERC avanzada, resultando hipermagnesemia. En los pacientes en diálisis, el magnesio sérico depende fundamentalmente del magnesio del líquido de diálisis y de la ingesta.
El test más común para ver cuál es la situación del estado del magnesio es la medida de los niveles de magnesio sérico, prueba muy sencilla y muy barata. Sin embargo, hemos de considerar que los niveles de magnesio sérico no reflejan el estado del contenido total del cuerpo de magnesio.
Los valores de referencia para el magnesio sérico son 0,65-1,05 mmol/litro (1,5-3,6 mg/dl) para magnesio total y 0,55-0,75 mmol/litro (1,3-1,8 mg/dl) para magnesio ionizado en suero de pacientes adultos6,7. La prevalencia de hipomagnesemia en pacientes hospitalizados es elevada: 9-65 %8, especialmente en pacientes en las Unidades de Cuidados Intensivos posoperatorios9. En la población general, la hipomagnesemia ocurre con frecuencia en pacientes con diabetes, enfermedad crónica gastrointestinal, alcoholismo o relacionada con el consumo de ciertas drogas. Hay un pequeño grupo de pacientes que presentan hipomagnesemia familiar asociada a mutaciones genéticas, particularmente de genes que codifican el transporte de iones en el túbulo contorneado distal, siendo las más frecuentes las mutaciones en el canal de magnesio TRPM65. La hipermagnesemia se ve generalmente asociada a una alteración renal no detectada o a una excesiva administración oral de sustancias que contienen magnesio (por ejemplo, laxantes o antiácidos) o en casos de avanzada ERC3,10. Los signos clínicos de hipo e hipermagnesemia no son específicos y pueden ser similares o incluso estar ausentes. Los signos incluyen pérdida de apetito, fatiga y debilidad y más tarde, a medida que la deficiencia de magnesio empeora, parestesias, calambres e incluso convulsiones, cambios de la personalidad, arritmias y espasmos coronarios. La hipermagnesemia severa puede llevar a una situación de depresión o pérdida de los reflejos tendinosos profundos, hipotensión, parálisis intestinal y cambios electrocardiográficos. En situaciones extremas, con magnesio sérico muy alto o muy bajo, se pueden presentar problemas de disfunción severa neuromuscular, hipotonía e incluso pseudoparálisis, depresión respiratoria, arreflexia y coma.
MAGNESIO SÉRICO Y RIESGO DE ENFERMEDAD
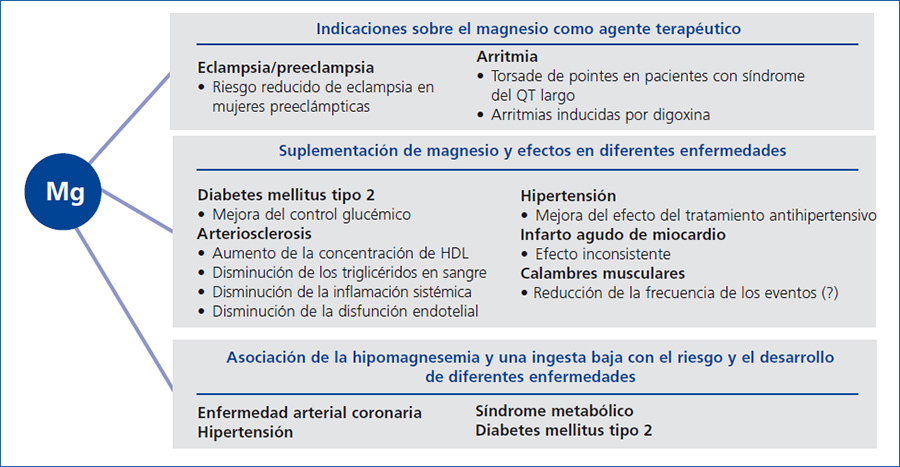
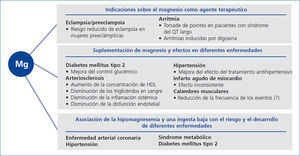
Varios estudios epidemiológicos han demostrado asociaciones entre los niveles bajos de magnesio y un aumento en el riesgo del síndrome metabólico, diabetes mellitus tipo 2, hipertensión y arterioesclerosis11. Sin embargo, el uso de magnesio como un agente terapéutico solamente está indicado en la preeclampsia y en algunas formas específicas de arritmias (figura 2). La enfermedad cardiovascular y la diabetes tipo II son comorbilidades muy frecuentes en la ERC y el papel del magnesio en estas enfermedades merece más información. En entre el 14 y el 48 % de los diabéticos tipo 2 se encontró hipomagnesemia en comparación con el grupo control, donde osciló del 3 al 15 %, y por ello ha sido implicada esta hipomagnesemia en algunas de las complicaciones de la diabetes12. Un estudio retrospectivo con 550 diabéticos tipo 2 sin enfermedad renal conocida demostró que los niveles bajos de magnesio se asociaban con un deterioro posterior de la función renal. Los pacientes con niveles elevados de magnesio, entre 0,82 y 1,3 mmol/litro, tenían una progresión más lenta y un mejor control de la glicemia. Por tanto, esos niveles séricos se sugirieron como niveles diana para los paciente diabéticos13. En un metaanálisis de 7 estudios (n = 286.668), se encontró que el aumento en la ingesta de magnesio de 100 mg al día se asociaba inversamente con la incidencia de diabetes tipo 214. Los autores sugirieron que una alimentación rica en magnesio podría reducir el riesgo de diabetes tipo 2. Si los pacientes diagnosticados ya de diabetes tipo 2 se benefician o no de un suplemento de magnesio adicional, fue estudiado en un metaanálisis de 9 estudios aleatorizados que incluían 370 diabéticos tipo 215. Aunque la dosificación y los criterios de inclusión variaron y los números de pacientes en estudios aislados fueron relativamente pequeños, se encontró que el suplemento de magnesio (dosis mediana de 15 mmol/día) usado como tratamiento adicional durante 4 a 16 semanas disminuía significativamente los niveles de glucosa en ayunas15. Por tanto, el suplemento diario de magnesio parece tener un efecto beneficioso en personas prediabéticas y en pacientes con diabetes tipo 2.
También hay muchos trastornos cardiovasculares que se asocian con niveles bajos de magnesio. En un reciente estudio epidemiológico (n = 212.157), se encontró que los niveles bajos de magnesio predecían la mortalidad cardiovascular y de todas las causas16. También mostraron que las concentraciones bajas de magnesio (a pesar de otros factores de riesgo) se asociaban con un aumento de la masa ventricular izquierda, que es un predictor de eventos cardiovasculares adversos.
La hipomagnesemia también se ha asociado a la elevación de la presión arterial. En el Estudio ARIC (n = 15.248), los niveles de magnesio sérico se relacionaron inversamente con la presión arterial sistólica17. Además, en un metaanálisis de 20 estudios aleatorizados (n = 1200) se encontró que el suplemento de magnesio se asociaba con reducciones en la presión arterial significativas relacionadas con la dosis18. Sin embargo, otros ensayos más recientes no han demostrado que el suplemento de magnesio reduzca directamente, pero sí sugieren que puede facilitar la acción de los medicamentos antihipertensivos19,20.
La arterioesclerosis es un factor de riesgo cardiovascular bien conocido y potencialmente responsable del infarto de miocardio y del accidente cerebrovascular. La patogénesis de la arterioesclerosis es compleja y, lo mismo que la disfunción endotelial y la hiperlipidemia, la hipomagnesemia ha sido identificada como un importante factor de riesgo. Según el seguimiento del Estudio ARIC (n = 13.922), los pacientes con el magnesio sérico más bajo tuvieron mayor riesgo de enfermedad coronaria21. Ascherio et al.22 encontraron una asociación negativa entre la ingesta de magnesio y el riesgo de ictus en un estudio prospectivo con 43.738 pacientes. Estas asociaciones inversas fueron más importantes en varones hipertensos que en normotensos, y no se modificaron después de ajustar por la presión arterial.
La hipomagnesemia ha sido también relacionada con la patogénesis de la cardiopatía isquémica alterando la composición de las lipoproteínas y modificando la arritmia posinfarto de miocardio. Por esta razón, el tratamiento con magnesio se ha estudiado extensamente en el contexto del infarto agudo de miocardio en varios ensayos clínicos11,23. Sin embargo, la conclusión después de los últimos ensayos clínicos24 fue que el sulfato de magnesio no podía ser recomendado de forma general para la administración rutinaria después del infarto agudo de miocardio.
MAGNESIO EN LA ENFERMEDAD RENAL CRÓNICA
Aunque la excreción de magnesio a través del riñón se adapta muy fácilmente, esta capacidad se deteriora cuando la función renal disminuye de forma significativa25. En situaciones de ERC moderada (estadios 1-3), se produce una compensación a esa pérdida de la función renal a través de un aumento en la excreción fraccional de magnesio, por lo que los niveles de magnesio sérico se mantienen dentro de lo normal26. Es interesante constatar que en estas circunstancias hay diferencias entre los diabéticos y los no diabéticos, pues se ha encontrado que en no diabéticos existe una correlación significativa entre un aclaramiento de creatinina bajo y niveles séricos altos de magnesio, mientras que en los pacientes diabéticos no se ha encontrado esta correlación; en estos pacientes los niveles de magnesio sérico fueron significativamente más bajos, a pesar de una disminución del aclaramiento de creatinina27.
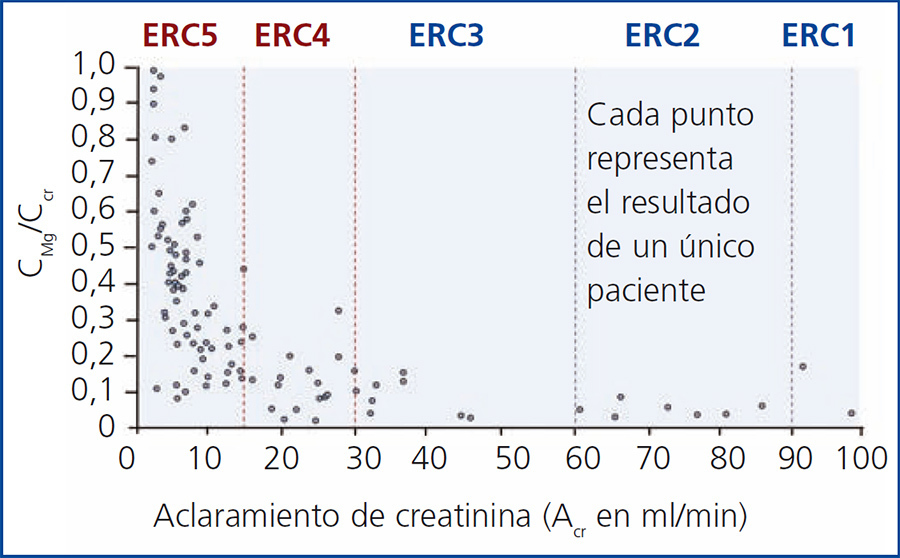
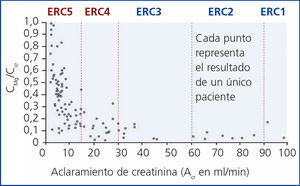
En estadios más avanzados de ERC (estadios 4-5), los mecanismos de compensación renal no son suficientes. Con frecuencia se desarrolla hipermagnesemia en pacientes con aclaramientos inferiores a 10 ml/minuto (figura 3). En pacientes en diálisis, las concentraciones de magnesio dependen fundamentalmente de la concentración de magnesio en el líquido de diálisis. El magnesio atraviesa con mucha facilidad la membrana de diálisis y la membrana peritoneal. Se han estudiado las diferentes concentraciones de magnesio en el líquido de diálisis en pacientes en hemodiálisis y en diálisis peritoneal (tabla 1). Las concentraciones de magnesio en el dializado de 0,75 mmol/litro pueden causar ligera hipermagnesemia, mientras que una concentración de 0,25 mmol/litro la mayoría de las veces causa hipomagnesemia. Los resultados para una concentración de magnesio en el líquido de diálisis de 0,5 mmol/litro son menos consistentes, pero, en líneas generales, las concentraciones de magnesio sérico están dentro del rango de lo normal. Resultados inconsistentes de diversos estudios sugieren que hay otros factores, tales como la nutrición, los suplementos de magnesio (por ejemplo antiácidos), que también pueden jugar un papel importante en los niveles séricos de magnesio en pacientes en diálisis.
Un aspecto importante del magnesio en pacientes con ERC es su relación con la actividad paratiroidea. Existen múltiples alteraciones que contribuyen al desarrollo de hiperparatiroidismo secundario, que se observa en casi todos los enfermos con ERC. Calcio sérico, valcitriol, factor de crecimiento fibroblástico (FGF-23) y fosfato sérico juegan un papel importante en la regulación de la síntesis y secreción de la hormona paratiroidea25. El calcio es el activador dominante del receptor del calcio, pero el magnesio también activa este receptor del calcio, aunque con una potencia 2 o 3 veces inferior. En cualquier caso, los niveles de magnesio sérico pueden tener un efecto regulador en la secreción de hormona paratiroidea. La relación entre el magnesio sérico y los niveles de hormona paratiroidea en pacientes en hemodiálisis o en diálisis peritoneal ha sido investigada en varios estudios25. Navarro et al.30,33 encontraron una relación significativa inversa entre el magnesio sérico y los niveles de hormona paratiroidea (p < 0,001) en 110 pacientes en hemodiálisis y también en 51 pacientes con diálisis peritoneal, usando concentraciones de magnesio en el dializado de 0,5 mmol/litro y 0,75 mmol/litro, respectivamente. Sin embargo, la mayoría de los otros estudios han usado cambios de las concentraciones de calcio y magnesio en el líquido de dializado de forma concomitante34, por lo que los resultados resultan difíciles de interpretar y son necesarios más estudios para cuantificar con precisión el grado de influencia que tiene el magnesio sérico sobre los niveles de hormona paratiroidea independiente del cambio en los valores de calcio.
El 55 % del contenido de magnesio del cuerpo se encuentra en el hueso, que es el depósito más importante del cuerpo humano. Pero el magnesio solo representa una proporción muy pequeña, menos del 1 % del total del contenido mineral del hueso, que principalmente consiste en calcio y fosfato en forma de hidroxiapatita. Los estudios realizados acerca de la contenido de magnesio en el hueso, en pacientes con ERC, presentan resultados muy diferentes, indicando que puede haber muchos factores que influencian el metabolismo del hueso urémico. El papel del magnesio en la patogénesis de la enfermedad renal ósea ha sido estudiado recientemente. El magnesio parece ser muy importante en la regulación de la actividad osteoblástica y osteoclástica y en el remodelado óseo. La deficiencia del magnesio en la rata produce una alteración del crecimiento óseo, osteopenia y fragilidad esquelética35. Los estudios epidemiológicos han asociado una deficiencia de magnesio en la dieta con una baja masa ósea y osteoporosis36. Sin embargo, hay otros muchos factores, como la vitamina D, el nivel de hormona paratiroidea, las concentraciones de calcio y fosfato y la acidosis metabólica, que también contribuyen al metabolismo óseo, por lo que la responsabilidad exacta de magnesio necesita una investigación con mayor profundidad.
MAGNESIO Y CALCIFICACIÓN VASCULAR EN LA ENFERMEDAD RENAL CRÓNICA
La enfermedad cardiovascular es la causa de muerte más reciente tanto en pacientes con ERC como en aquellos que se encuentran en hemodiálisis o diálisis peritoneal37. Los pacientes que se encuentran en diálisis tienen de dos a cinco veces más calcificación arterial coronaria que aquellos correspondientes a su edad. Las calcificaciones de la íntima y de la media son los causantes directos o indirectos más importantes de enfermedad cardiovascular y de la mortalidad de los pacientes con ERC.
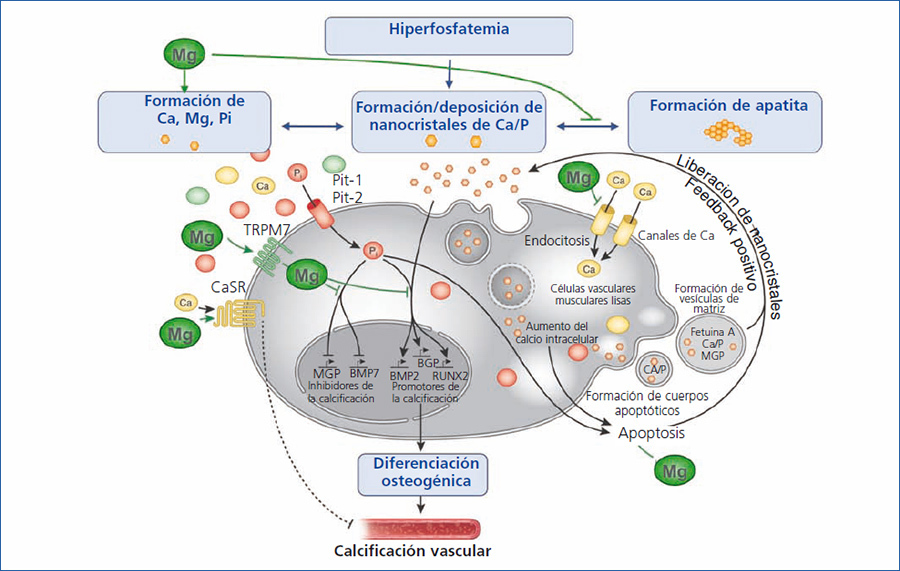
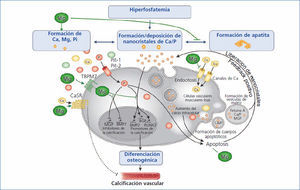
La pérdida progresiva de la función renal se acompaña de una elevación de los niveles de FGF-23, una disminución en la excreción de fósforo y una alteración en el metabolismo óseo. Las alteraciones minerales que ocurren durante la ERC ciertamente producen calcificación vascular. La patogénesis de esta calcificación vascular es un proceso activamente regulado y mediado por células que se asemejan bastante a la formación del tejido óseo normal38. Un papel central lo juegan las células musculares lisas que componen la capa media de la pared vascular y que se convierten en unas células parecidas a los osteoblastos, un fenotipo que normalmente se encuentra en los vasos calcificados. Las alteraciones en el metabolismo mineral, concretamente la hiperfosfatemia y la pérdida de inhibidores de la mineralización, llevan inicialmente a la formación de nanocristales de fosfato cálcico, que pueden transformarse en una forma más estable y organizada, en cristales de apatita. Puede ser que los nanocristales sean captados por las células lisas musculares vía endocitosis e inicien la transdiferenciación a células similares a los osteoblastos, resultando finalmente en la calcificación vascular.
Varios estudios, tanto in vitro como en animales, han sugerido un efecto protector del magnesio en la calcificación vascular a través de múltiples mecanismos (figura 4). En primer lugar, el magnesio inhibe la formación de cristales de apatita y produce unos depósitos menores y más solubles39. En segundo lugar, por determinadas funciones del magnesio como antagonista del calcio e inhibiendo la entrada de calcio en las células40. En tercer lugar, el magnesio restaura el balance entre la expresión de los promotores de calcificación y de los inhibidores41. Finalmente, el magnesio actúa sobre el receptor del calcio y la activación del receptor del calcio por los calcimiméticos ha demostrado que inhibe también la calcificación de las fibras musculares lisas vasculares42.
Los estudios clínicos demuestran la evidencia de este efecto protector del magnesio sobre la calcificación vascular. Hay estudios en los que se ha observado que la calcificación de la válvula mitral y el engrosamiento de la media íntima carotídea se asocian con niveles bajos de magnesio en pacientes en hemodiálisis43,44. El suplemento a largo plazo con magnesio redujo el grosor de la íntima media carotídea retardando la calcificación arterial en pacientes con ERC45. Además, estudios epidemiológicos realizados en pacientes en hemodiálisis revelaron que los niveles elevados de magnesio se asociaban con mayor supervivencia, mientras que los niveles bajos de magnesio fueron factores predictores independientes de muerte46. Pero, por encima de todo, los niveles elevados de magnesio y/o la suplementación con magnesio pueden retardar la calcificación arterial y llevar a una mejoría en la supervivencia de los pacientes en diálisis. Es evidente que se necesitan estudios prospectivos aleatorizados suficientemente potentes para confirmar estos resultados.
MAGNESIO COMO CAPTOR DEL FÓSFORO
La pérdida de la función renal se asocia con un aumento en los nieles de fósforo y la mayoría de los pacientes a partir de ERC estadio 4 desarrollan hiperfosfatemia. Para controlar la hiperfosfatemia, muy frecuentemente se precisan captores del fósforo, de manera que puedan evitarse las alteraciones en el metabolismo óseo y mineral, la enfermedad cardiovascular y el hiperparatiroidismo secundario. Estos quelantes o captores del fósforo han sido usados durante muchos años, pero el captor ideal en términos de eficacia, adherencia del paciente, seguridad y costos no se ha encontrado47. Los captores que contienen aluminio o calcio han dado lugar a algunos problemas clínicos, como por ejemplo la toxicidad por el aluminio o el aumento en la carga de calcio que produce hipercalcemia y asociaciones con las calcificaciones vasculares. Los nuevos agentes que evitan el calcio, por otra parte, son muy caros. Los quelantes del fósforo que contienen magnesio ofrecen la posibilidad de evitar algunos de los problemas asociados con otros agentes.
Hace ya años, en 1980, algunos estudios reemplazaron el aluminio por hidróxido de magnesio para evitar esa toxicidad. Este hidróxido de magnesio fue efectivo en el descenso de los niveles de fósforo y de hormona paratiroidea, pero se asociaba a una tolerancia gastrointestinal muy pobre. Estudios más recientes usando carbonato de magnesio combinado con carbonato cálcico o acetato cálcico han mejorado la tolerabilidad. Nos referiremos a algunos de los estudios más importantes recientemente realizados.
Eficacia del carbonato de magnesio en combinación con carbonato cálcico o acetato cálcico
Un estudio aleatorizado comparó la eficacia de la asociación carbonato de magnesio y acetato cálcico con relación a la monoterapia con carbonato cálcico en 50 pacientes en hemodiálisis48. El tratamiento con la combinación carbonato de magnesio y acetato cálcico resultó en unos niveles significativamente más bajos de fósforo, calcio y hormona paratiroidea comparados con la monoterapia (p < 0,05 cada uno). Las concentraciones de magnesio sérico en el grupo de combinación aumentaron significativamente, pero permanecieron dentro del rango de lo normal48.
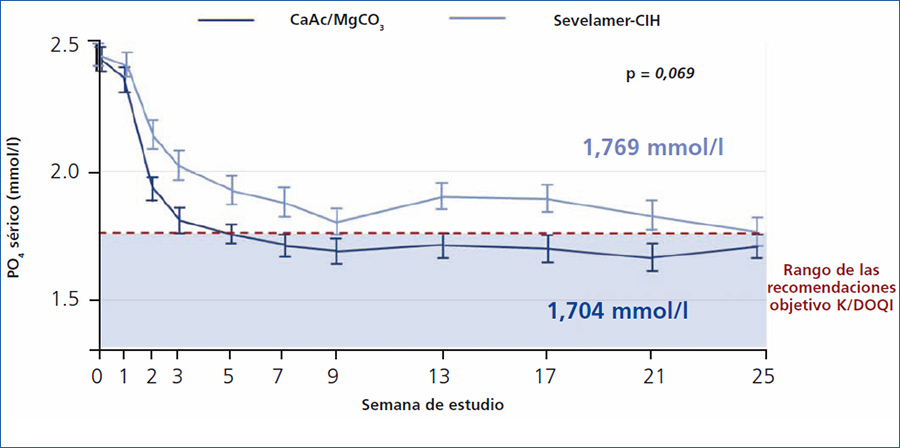
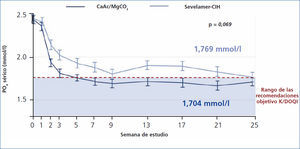
El estudio Calmag es un estudio aleatorizado multicéntrico que comparó la eficacia del acetato cálcico/carbonato de magnesio con sevelamer ClH en 255 pacientes en hemodiálisis49. El objetivo primario fue demostrar una no inferioridad del acetato cálcico-carbonato de magnesio comparado con el sevelamer ClH en el descenso de los niveles de fósforo por debajo de las recomendaciones KDOQI después de 24 semanas de tratamiento. Se cumplió completamente ese objetivo y no hubo diferencias significativas entre los grupos en relación con los niveles de fósforo sérico reducidos al final del estudio (p = 0,069) (figura 5). El área bajo la curva para el fósforo sérico (p = 0,0042) y el número de visitas por encima de las recomendaciones objetivo K/DOQI (≤ 1,78 mmol/l, p = 0,0198) y KDIGO (≤ 1,45 mmol/l, p = 0,0067) fueron significativamente más bajos con la asociación acetato cálcico-carbonato de magnesio comparado con sevelamer ClH.
Seguridad del carbonato de magnesio en combinación con carbonato cálcico o acetato cálcico
La tolerabilidad, hipermagnesemia y carga de calcio son parámetros de seguridad relevantes de los captores de fósforo que contienen magnesio. La tolerabilidad se demostró en diferentes estudios. La combinación magnesio/carbonato cálcico se comparó a la monoterapia con carbonato cálcico en un estudio aleatorizado cruzado de dos años en 29 pacientes en hemodiálisis50. Los niveles de calcio sérico, fósforo y magnesio fueron similares en ambas fases, pero la ingestión de calcio fue significativamente inferior en el grupo con terapia combinada (p = 0,001). A pesar de la ingesta elevada de magnesio de 465 ± 52 mg/día, el tratamiento combinado generalmente fue bien tolerado. Ningún paciente reportó síntomas intestinales incluyendo diarrea o meteorismo.
Un estudio piloto investigó la carga de calcio en el combinado magnesio/carbonato cálcico comparándolo con la monoterapia con acetato cálcico51. Treinta pacientes en hemodiálisis fueron aleatorizados a recibir o la combinación (n = 20) o la monoterapia (n = 10) durante 12 semanas. El control de fósforo del tratamiento combinado fue al menos tan bueno como el del acetato cálcico exclusivamente, pero el consumo de calcio fue significativamente inferior en el tratamiento combinado de magnesio/carbonato cálcico (908 ± 24 vs. 1743 ± 37 mg/día, p < 0,001), resultando en niveles de calcio significativamente inferiores (p < 0,003). Ambos regímenes fueron generalmente bien tolerados y con una incidencia similar de síntomas gastrointestinales.
El estudio CALMAG comparó los parámetros de seguridad del acetato cálcico/carbonato de magnesio con el sevelamer ClH49. Ambos regímenes fueron igualmente bien tolerados, con similar número de efectos adversos. No se observó hipermagnesemia sintomática. Se observó un pequeño aumento en el magnesio sérico en el grupo con acetato cálcico/carbonato de magnesio, pero las concentraciones medias (1,29 ± 0,25 mmol/l) estuvieron muy por debajo de los valores séricos que producen sintomatología (> 2,0 mmol/l).
Spiegel et al.52 estudiaron los efectos de la calcificación de la arteria coronaria y la densidad ósea mineral del magnesio y carbonato cálcico durante 18 meses en 7 pacientes en hemodiálisis. No encontraron progresión del score de calcificación coronaria ni cambios significativos en la densidad ósea mineral, lo que sugiere que el magnesio podría tener un efecto favorable en esos parámetros, aunque el tamaño del estudio no alcanza a permitir ningún tipo de conclusión.
Costo- efectividad
Los costos derivados en los tratamientos son cada vez factores más importantes. Los quelantes de fósforo que contienen magnesio son mucho más baratos comparados con los productos como sevelamer o lantano. Los costos calculados para el tratamiento con carbonato de magnesio y acetato cálcico fueron aproximadamente cerca de un 80 % más bajos que los del sevelamer ClH49. Si bien los compuestos de magnesio y calcio han probado su eficacia y seguridad, todavía hay alguna preocupación acerca de la hipermagnesemia y de la monitorización sérica del magnesio. Generalmente los niveles séricos de magnesio no son una medida que se utilice rutinariamente en muchas clínicas de diálisis. Algunos pueden argumentar que no es necesaria una monitorización rutinaria, ya que el margen de seguridad parece ser muy amplio, pero no es lo que satisface la preocupación de los nefrólogos. El costo de introducir la monitorización de magnesio podría, sin embargo, ser contrarrestado precisamente por un costo mucho menor cuando se compara con el sevelamer o el lantano y, además, por otra parte, los analizadores multicanales actuales pueden reportar los niveles de magnesio sin grandes implicaciones en el costo (es el mismo precio que el calcio sérico: como ejemplos, 2,3 euros en Alemania, 1,9 euros en Francia dependiendo de las técnicas).
CONCLUSIÓN
A pesar de la importancia fisiológica, el papel clínico del magnesio en términos de beneficio y daño (de niveles elevados o descendidos) particularmente en pacientes con ERC ha sido muy poco concretado en los últimos años. Los trastornos del balance de magnesio, especialmente la hipomagnesemia, son comunes, pero raramente son identificados en la rutina clínica diaria. Además, la deficiencia de magnesio se ha demostrado que es un factor de riesgo asociado a diferentes enfermedades metabólicas comunes, mientras que la suplementación de magnesio y la ligera hipermagnesemia podrían tener un efecto beneficioso en pacientes con ERC con respecto a la calcificación y la mortalidad. Por otra parte, el mejor conocimiento de los efectos de la hiperfosfatemia ha hecho que se necesiten cada vez más eficientes y mejor tolerados quelantes del fósforo. La combinación acetato cálcico y carbonato de magnesio es un quelante del fósforo, al menos tan efectivo como el sevelamer, igualmente bien tolerado, pero con un ahorro del 80 % de los costos del tratamiento. Los niveles de magnesio solo son ligeramente elevados y no hubo diferencias en la tolerabilidad gastrointestinal comparada con la del sevelamer ClH. Si fuera necesaria la monitorización rutinaria de magnesio, se puede realizar sin mayores implicaciones en el costo. Los posibles efectos beneficiosos del magnesio con relación a la calcificación, los niveles de hormona paratiroidea y la supervivencia en pacientes con ERC, por una parte, y los resultados prometedores acerca de la eficacia, tolerabilidad y coste de efectividad, por otra parte, son ventajas potenciales que pueden hacer considerar que los quelantes que contienen magnesio pueden ser una opción muy atractiva en la práctica clínica rutinaria. Sin embargo, necesitamos mucha más investigación clínica para confirmar y comprender los efectos clínicos de la administración del magnesio.
Agradecimientos
Este trabajo está basado en el número especial de Clinical Kidney Journal: «Magnesium – a versatile and often overlooked element: New Perspectives with a focus on chronic kidney disease» (vol. 5, S1, febrero 2012). Queremos agradecer la contribución de los siguientes autores: Friedrich C. Luft, Wilhelm Jahnen-Dechent, Markus Ketteler, Jeroen H.F. de Baaij, Joost G.J. Hoenderop, René J.M. Bindels, Helmut Geiger, Christoph Wanner, John Cunningham, Piergiorgio Messa, Ziad A. Massy, Tilman B. Drüeke, Alastair Hutchinson, Martin Wilkie.
Asimismo, nuestro agradecimiento a Jutta Passlick-Deetjen, Kristina Gundlach, Mirjam Peter, Nora Burkard y Sonja Steppan por su importante contribución en la organización y desarrollo de esta actualización.
CONCEPTOS CLAVE
1. La prevalencia de la hipomagnesemia es elevada y está asociada a varias enfermedades. Sin embargo, con frecuencia pasa inadvertida.
2. La hipermagnesemia moderada parece tener efectos beneficiosos sobre la calcificación vascular y las tasas de mortalidad.
3. En los pacientes en diálisis, los niveles séricos de magnesio están altamente influidos por la concentración de magnesio en el líquido de diálisis.
4. La combinación de carbonato de magnesio/acetato cálcico es un captor de fósforo eficaz, seguro y rentable.
Conflictos de interés
Los autores declaran conflictos de interés potenciales.
Becas: Abbott, Amgen, Fresenius.
Honorarios por ponencias: Abbott, Amgen, Fresenius, Shire.
Honorarios como consultores: Amgen, Fresenius, Vifor, Shire.
Bolsas de viaje o financiación para viajar: Abbott, Amgen, Fresenius, Vifor, Sanofi, Shire.
Figura 1. Regulación de la homeostasis del magnesio
Figura 2. Papel del magnesio en diferentes enfermedades
Figura 3. Relación entre la excreción fraccional de magnesio y el aclaramiento endógeno de creatinina en pacientes con enfermedad renal crónica
Figura 4. Presuntos efectos protectores del magnesio en el curso de la calcificación vascular
Figura 5. Eficacia del acetato cálcico&
Tabla 1. Influencia de la concentración de magnesio en el líquido de diálisis en los niveles séricos de magnesio en pacientes en hemodiálisis y diálisis peritoneal