La poliquistosis renal autosómica dominante (PQRAD) es la causa del 6-10% de los pacientes en tratamiento renal sustitutivo. Inicialmente, aparecen quistes renales que van creciendo y sustituyendo al parénquima renal, aunque la función renal permanece normal hasta la tercera década de la vida1. Los principales factores de progresión implicados en el descenso del filtrado glomerular (FG) son: el tipo de mutación, el volumen renal y la hipertensión arterial (HTA)2. La mutación PKD1 tiene peor pronóstico, sobre todo la tipo truncante, como se describe en el modelo predictivo PRO-PKD3. El aumento del volumen renal medido por RMN permite clasificar a los pacientes en progresadores rápidos si pertenecen a las clases 1C, 1D y 1E del modelo de la Clínica Mayo4.
La HTA, que aparece precozmente, aumenta la morbimortalidad cardiovascular, que es la primera causa de muerte en estos enfermos. El principal determinante de la HTA es la activación del sistema renina angiotensina (SRA), siendo los inhibidores del SRA los antihipertensivos de elección que, además, disminuyen la proteinuria consiguiendo enlentecer la progresión de la enfermedad renal crónica (ERC). Tal y como demuestra el estudio HALT, el grado de HTA influye en la evolución de la enfermedad, siendo útil la monitorización ambulatoria de la presión arterial para detectar de forma precisa las cifras de presión arterial y siendo necesario un control más estricto de las cifras de presión arterial que en la población general (PA 95-110/60-75mmHg en pacientes menores de 50 años)5,6.
El objetivo de nuestro estudio fue comprobar si el número de antihipertensivos, como un indicador sencillo de la gravedad de HTA, podría ser también un factor de progresión de la ERC en la PQRAD.
Se analizaron 123 pacientes con diagnóstico ecográfico y/o genético de PQRAD seguidos en consulta de nefropatías hereditarias (hasta el 31 de mayo de 2019). Se excluyeron los pacientes con FG<15mL/min. Las principales características clínicas fueron: edad media de 37,29±15,04 años, 48,8% varones, FG medio de 84,58±41,22mL/min, 56,1% hipertensos, 26,8% tomaba más de un antihipertensivo, 56,1% con estudio genético (40,7% PKD1 y 15,4% PKD2), 65% con riñones grandes (longitud renal por ecografía>13,5cm), 39,8% quistes hepáticos, 26% algún episodio de hematuria, colesterol 167,22±35,81mg/dL y urato de 5,34±1,72mg/dL. La distribución del tipo de antihipertensivo fue: IECA 50,72%, ARA-II 47,83%, antagonistas del calcio 40,58%, doxazosina 21,74%, betabloqueante 10,14% y diuréticos 7,25%.
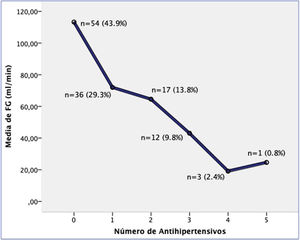
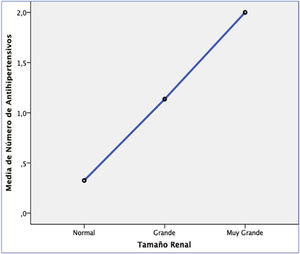
Se observó un menor FG en hipertensos (62,12±36,06 vs. 113,28±27,31, p=0,000) y en pacientes con más antihipertensivos (r=−0,642, p=0,000), destacando un mayor descenso del FG al aumentar el número de antihipertensivos (fig. 1). Además, se encontró una asociación estadísticamente significativa entre la HTA y la toma de un mayor número de antihipertensivos con un mayor volumen renal, ya que los pacientes hipertensos tuvieron riñones grandes en comparación con los no hipertensos (73,75% vs. 23,26%, p=0,000). En la figura 2 observamos como el número medio de antihipertensivos se asoció significativamente con mayor tamaño renal: 0,33±0,68 en riñones normales (<13,5cm), 1,14±1,12 en grandes (13,5-16,5cm) y 2,0±1,18 en muy grandes (>16,5cm).
En la PQRAD es fundamental identificar los factores de mal pronóstico que determinan la evolución de la ERC. En la mayoría de los centros hay limitada disponibilidad para realizar estudio genético (solo está indicado en determinadas situaciones)2 y para medir la tasa de crecimiento del volumen renal por RMN periódicas (como establecen las guías y la últimos estudios publicados)7. Sin embargo, la HTA es un factor accesible y que debemos controlar para frenar la progresión de la enfermedad8. Con nuestra experiencia hemos observado que el mayor número de antihipertensivos es otro importante factor de progresión a tener en cuenta en la enfermedad, no recogido por la mayoría de artículos publicados ni en los modelos predictivos.
En resumen, coincidimos con el resto de autores en que la HTA es un factor de primer orden en el deterioro del FG en la PQRAD, pero queremos destacar el número de antihipertensivos9 como indicador sencillo de la gravedad de HTA y también como factor de mal pronóstico de la enfermedad, útil y accesible en todos los servicios, a diferencia de otros como el estudio genético o la RMN.
FinanciaciónLa presente investigación no ha recibido ayudas específicas provenientes de agencias del sector público, sector comercial o entidades sin ánimo de lucro.
Conflicto de interesesTodos los autores de este artículo declaran no tener ningún conflicto de interés.