La información sobre la incidencia de insuficiencia renal aguda (IRA) intrahospitalaria relacionada con medicamentos y las características de los pacientes es escasa.
ObjetivoEstimar la incidencia de IRA relacionada con medicamentos en pacientes hospitalizados y comparar sus características con las de los pacientes con IRA relacionada con otras causas.
MétodosCohorte prospectiva de pacientes con IRA intrahospitalaria (julio de 2010-julio de 2011). Se recogió información sobre características y antecedentes de los pacientes, factores de riesgo y gravedad de la IRA según la clasificación RIFLE, y medicación durante la hospitalización. El análisis de la imputabilidad de los fármacos y la evaluación de la relación causal se realizó siguiendo los métodos y el algoritmo del Sistema Español de Farmacovigilancia.
ResultadosUn total de 194 casos presentaron un episodio de IRA intrahospitalaria. La edad mediana de los pacientes fue de 72 años (RI 20); el 60% eran hombres. La incidencia de IRA intrahospitalaria fue de 9,6 por cada 1.000 ingresos. Un 77,8% de los casos presentaron riesgo o daño renal según la clasificación RIFLE. En 105 (54,1%) casos, la IRA se relacionó con medicamentos; principalmente diuréticos, medicamentos que actúan sobre el sistema renina-angiotensina, inmunosupresores, bloqueadores β-adrenérgicos, bloqueantes de los canales de calcio, medios de contraste y antiinflamatorios no esteroideos. La morbilidad cardiovascular fue mayor y la frecuencia de factores de riesgo de IRA y la mortalidad menores en los pacientes con IRA relacionada con medicamentos.
ConclusionesLa mitad de los episodios de IRA intrahospitalaria se relacionaron con medicamentos. Los pacientes con IRA relacionada con medicamentos presentaron más antecedentes patológicos cardiovasculares, pero menos factores de riesgo de IRA y una menor mortalidad.
The information available on the incidence and the characteristics of patients with acute renal failure (ARF) related to drugs is scarce.
ObjectivesTo estimate the incidence of drug-related ARF in hospitalised patients and to compare their characteristics with those of patients with ARF due to other causes.
Material and methodsWe selected a prospective cohort of patients with ARF during hospital admission (July 2010-July 2011). Information on patients’ demographics, medical antecedents, ARF risk factors, ARF severity according to the RIFLE classification and hospital drug administration was collected. We analysed the relationship of drugs with the ARF episodes using Spanish Pharmacovigilance System methods and algorithm.
ResultsA total of 194 cases had an episode of hospital-acquired ARF. The median age of patients was 72 years [IQR 20]; 60% were men. The ARF incidence during hospitalization was 9.6 per 1,000 admissions. According to the RIFLE classification, a risk of kidney damage or kidney injury was present in 77.8% of cases. In 105 (54.1%) cases, ARF was drug-related; the drugs most frequently involved were diuretics, agents acting on the renin-angiotensin system, immunosuppressants, β-blocking agents, calcium channel blockers, contrast media and non-steroid anti-inflammatory drugs. Patients with drug-related ARF had more multi-morbidity, fewer ARF risk factors and lower mortality.
ConclusionsHalf of ARF episodes during hospitalisation were drug related. Patients with drug-related ARF had higher cardiovascular morbidity than those with ARF related to other causes, but they had a lower frequency of ARF risk factors and mortality.
La insuficiencia renal aguda (IRA) es una complicación frecuente y grave durante la hospitalización. Se ha descrito que puede afectar a entre un 5 y un 7% de los pacientes hospitalizados y que, a pesar del tratamiento, tiene una mortalidad del 20 al 70%1. No obstante, la incidencia depende de la definición que se utilice y de la población estudiada2,3.
Entre los factores de riesgo asociados a IRA durante la hospitalización se han descrito la edad avanzada, el sexo masculino, las infecciones, el antecedente de enfermedad cardiovascular y la insuficiencia renal crónica (IRC)4,5. Además de la mortalidad, la IRA incrementa el riesgo de acidosis metabólica, hiperpotasemia, arritmias cardíacas, sangrado gastrointestinal y también el riesgo de alteraciones neurológicas por el desequilibrio electrolítico4. Dependiendo del estudio y la definición de IRA, entre el 11 y el 40% de los pacientes con IRA durante la hospitalización necesitan diálisis4. Además, a mayor grado de disfunción renal se ha descrito una estancia hospitalaria más prolongada6.
Teniendo en cuenta tanto los episodios adquiridos en la comunidad como los originados en los hospitales, se ha descrito una frecuencia de IRA relacionada con medicamentos de un 18 a un 27% sobre el total de casos de IRA7. Sin embargo, en pacientes mayores de 60 años, los medicamentos han sido causa de IRA intrahospitalaria hasta en un 66% de los casos8. Algunos de los medicamentos implicados con mayor frecuencia en los casos de IRA intrahospitalarios han sido los aminoglucósidos, los antiinflamatorios no esteroideos (AINE), la piperacilina-tazobactam, anfotericina B, las combinaciones de trimetoprima con sulfonamidas, la ciclosporina y los inhibidores de la enzima conversora de la angiotensina (IECA)5.
Distintos estudios han descrito la frecuencia de IRA en pacientes hospitalizados en servicios médicos y quirúrgicos5,8–16 y la atribuible a medicamentos5,8–13, pero en ninguno se han comparado las características y la morbimortalidad de los pacientes con IRA relacionada con medicamentos con las de los pacientes con IRA por otras causas.
El objetivo principal del presente estudio fue determinar la incidencia de IRA relacionada con medicamentos en pacientes hospitalizados. Y describir los medicamentos más frecuentemente implicados, los factores de riesgo, la morbimortalidad y comparar estas características con las de los pacientes con IRA no relacionada con medicamentos.
MétodosSe realizó un estudio observacional prospectivo de pacientes que presentaron IRA durante el ingreso en un hospital terciario de Barcelona, entre el 19 de julio de 2010 y el 31 de julio de 2011. Los pacientes se siguieron hasta el alta hospitalaria.
Criterios de inclusión: pacientes adultos que durante la hospitalización en servicios médicos o servicios quirúrgicos presentaran en 2 analíticas consecutivas un aumento de la concentración de la creatinina sérica≥0,5mg/dl, si su concentración basal era ≤2,5mg/dl o un aumento >20% de la concentración de creatinina sérica si la concentración basal era >2,5mg/dl1,2. Se incluyó a los pacientes que presentaron un episodio de IRA en ingresos distintos.
Criterios de exclusión: pacientes para los que no se dispuso de al menos una determinación de la concentración de creatinina plasmática durante la hospitalización previa a la detección de la alteración de la función renal, los ingresados por IRA o IRC reagudizada o por trasplante renal, pacientes en diálisis crónica, los que participaban en ensayos clínicos y los que no otorgaron su consentimiento. También se excluyó a los pacientes ingresados en los servicios de traumatología y ginecología u obstetricia y los episodios de IRA de los pacientes ingresados en unidades de críticos (cuidados intensivos, quemados y sangrantes) o en el área de reanimación postintervención quirúrgica.
La concentración de creatinina plasmática basal se definió como la media de los valores de creatinina desde la admisión en el hospital hasta la creatinina previa a cumplir los criterios de inclusión. Los pacientes con IRC previa al ingreso fueron incluidos si la concentración de creatinina plasmática permanecía estable en el momento de la admisión en el hospital. Los pacientes se identificaron mediante un programa informático que, a partir de los datos de laboratorio, generaba un listado diario de los que cumplían los criterios de inclusión. Cada caso fue validado por los nefrólogos.
A partir de la historia clínica informatizada se recogió información sobre las características demográficas de los pacientes (edad y sexo), servicio de ingreso, estancia hospitalaria y los antecedentes patológicos. También se recogió información sobre los factores de riesgo de IRA durante el ingreso (insuficiencia cardíaca descompensada o evidencia clínica de insuficiencia cardíaca, hipotensión o presión arterial menor de 90/60mmHg, hemorragia o alguna causa de depleción de volumen según constase en la historia clínica).
A partir de la hoja de prescripción médica informatizada se recogió información de los fármacos administrados durante la hospitalización (principios activos, dosis y duración del tratamiento). Los medicamentos se clasificaron según el Sistema de Clasificación Anatómica, Terapéutica, Química (ATC)17.
Además, se recogió información sobre las complicaciones de la IRA durante la hospitalización y el desenlace al alta (recuperación de la función renal completa, parcial, no recuperación y la necesidad de tratamiento renal sustitutivo). La gravedad de la IRA se valoró según la clasificación RIFLE (riesgo, daño, fallo, pérdida prolongada de función renal y fallo final e irreversible de la función renal)3. También se recogió información sobre los diagnósticos al alta que fueron codificados según la Clasificación Internacional de Enfermedades, 9.ª revisión, Modificación clínica (CIE-9-MC)18.
El análisis de la imputabilidad de los fármacos y la evaluación de la relación causal entre los medicamentos y la IRA se realizó siguiendo los métodos y el algoritmo del Sistema Español de Farmacovigilancia (SEFV)19,20. Estos métodos fueron aplicados y consensuados por 2 farmacólogos clínicos conocedores y habituados a su uso. En la evaluación de la relación de causalidad se tuvo en cuenta la secuencia temporal entre el inicio del tratamiento y el inicio de la IRA, el conocimiento previo de la asociación causal entre el medicamento y la IRA, el efecto de la retirada y de la reexposición al medicamento sospechoso y la existencia de otras causas alternativas de IRA. La imputabilidad de los casos se determinó en función del resultado del algoritmo de causalidad y la existencia de factores de riesgo de IRA, categorizándose en improbable, condicional, posible, probable o definida19,20. Para el análisis se consideraron casos de IRA de causa medicamentosa aquellos que presentaron al menos un medicamento con imputabilidad definida, probable o posible. Los casos de IRA en los que todos los medicamentos prescritos durante la hospitalización resultaron con imputabilidad condicional o improbable se consideraron de causa no medicamentosa, y, en estos, la etiología de la IRA se clasificó en prerrenal, renal o posrenal según los criterios que constan en la guía de la Sociedad Española de Nefrología21.
Para el cálculo del tamaño de la muestra se tuvo en cuenta la incidencia de IRA intrahospitalaria descrita (5-7%)1 y el número de ingresos en el hospital durante un año. Se calculó que para detectar un 20%7 de casos de IRA relacionada con medicamentos durante el ingreso, con un intervalo de confianza (IC) del 95% y una precisión del ±5%, se deberían incluir 232 pacientes con IRA durante la hospitalización.
El estudio se realizó de acuerdo con las directivas nacionales para los estudios postautorización, y fue aprobado por el Comité Ético de Investigación Clínica del hospital.
La incidencia (IC del 95%) de IRA en pacientes hospitalizados en los servicios incluidos se estimó a partir de los casos de IRA por cualquier causa y el número total de ingresos en estos servicios durante el periodo de estudio. Para el cálculo de la incidencia total también se tuvo en cuenta a los pacientes que cumplían los criterios de inclusión pero que no otorgaron el consentimiento. La incidencia (IC del 95%) de IRA relacionada con medicamentos fue estimada usando los casos de IRA relacionada con medicamentos como numerador.
Las variables categóricas se expresaron en frecuencias y proporciones. Las variables numéricas en medias ± desviación estándar (DE) o medianas y rango intercuartílico (RI). La comparación de proporciones se efectuó con la prueba de Chi-cuadrado. La comparación de medias entre 2 grupos se llevó a cabo con la prueba t de Student para grupos independientes o bien con su alternativa no paramétrica (U de Mann-Whitney), de acuerdo con la distribución de cada variable. Se consideró un valor estadísticamente significativo una p < 0,05. El análisis estadístico se realizó mediante el programa estadístico IBM SPSS Statistics version 20 (IBM corp., Nueva York, EE. UU.).
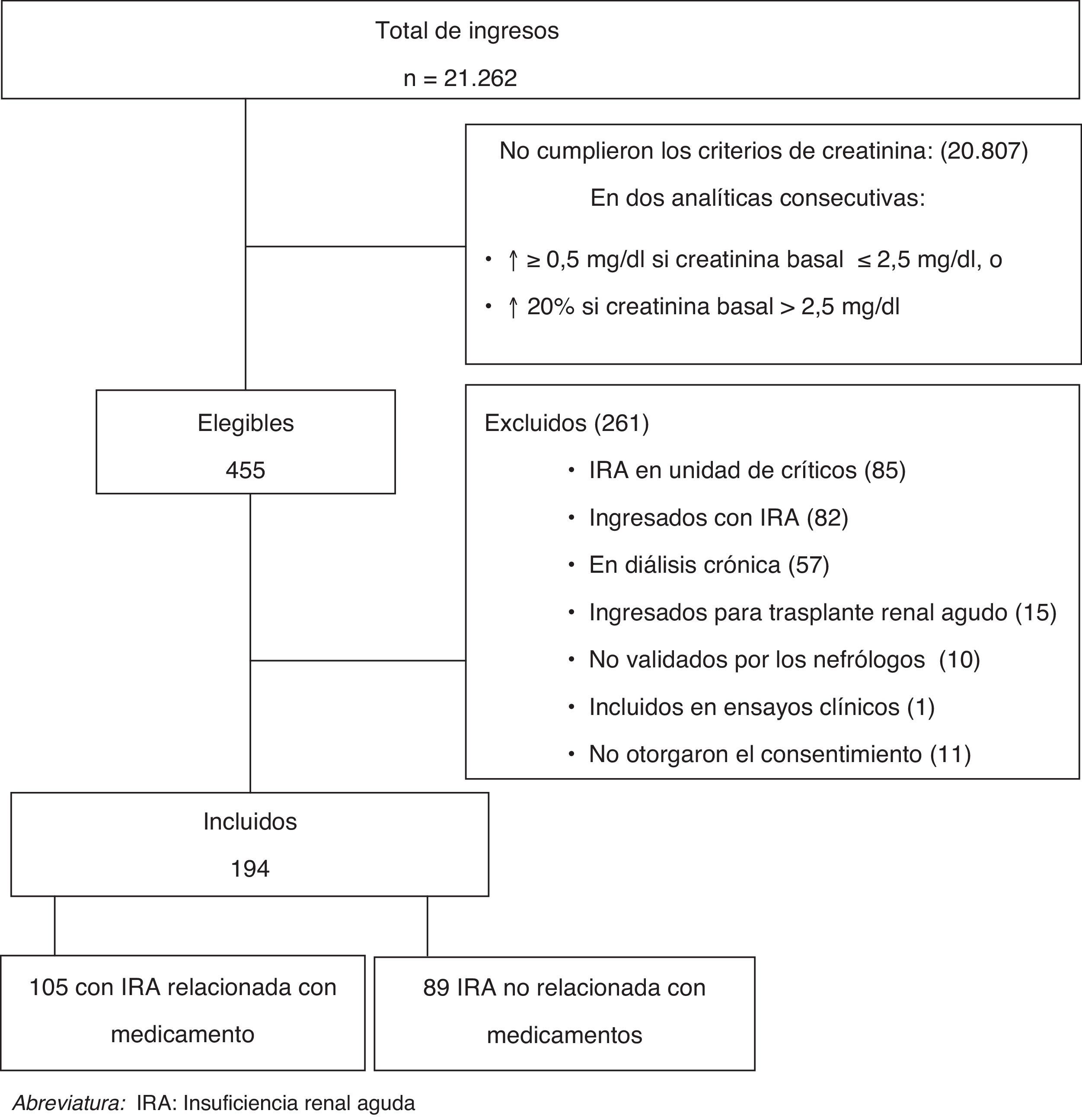
ResultadosDe un total de 21.262 ingresos, 194 casos de IRA durante la hospitalización fueron incluidos durante el periodo de estudio (2 pacientes ingresaron en 2 ocasiones y presentaron un episodio de IRA en cada ingreso). Un total de 20.807 ingresos fueron excluidos por no cumplir con los criterios de alteración de creatinina del estudio y 261 fueron excluidos por otras razones (fig. 1).
La incidencia de IRA durante la hospitalización fue de 9,6 por 1.000 ingresos (IC 95%: 8,4-11) y la relacionada con medicamentos fue 4,9 por 1.000 ingresos (IC 95%: 4-6). La tasa de incidencia de IRA durante la hospitalización fue de 1,4 por 1.000 camas-día (IC 95%: 1,2-1,6).
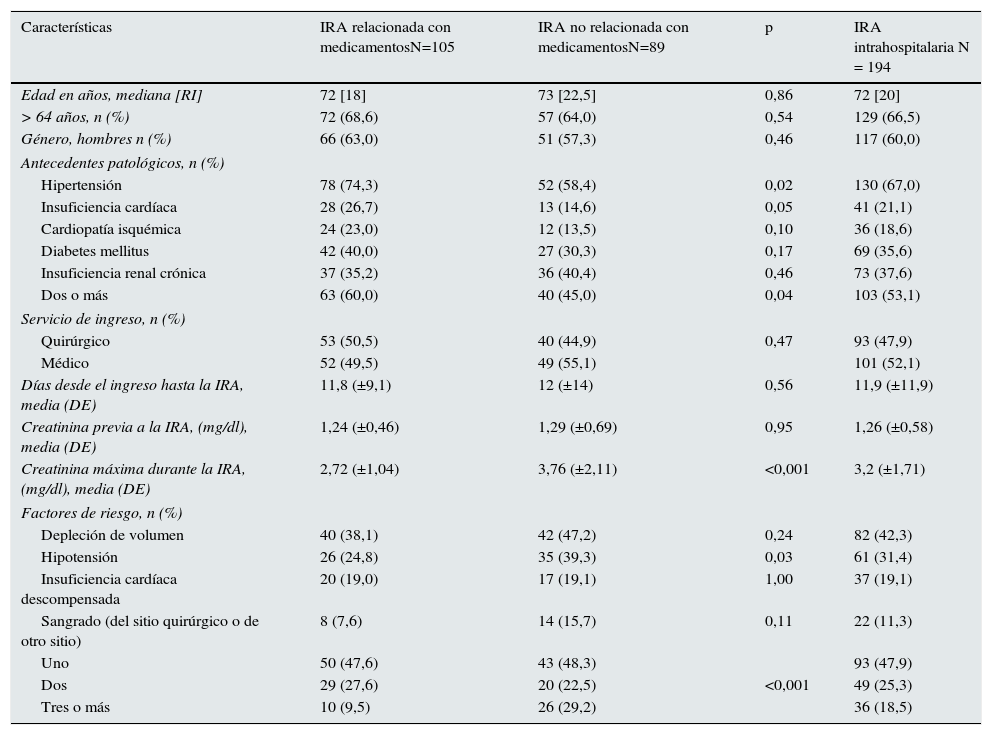
La mediana de edad de los pacientes fue de 72 años (RI 20), y un 60% fueron hombres. En la tabla 1 se describen las principales características demográficas y antecedentes patológicos de los pacientes.
Características basales
| Características | IRA relacionada con medicamentosN=105 | IRA no relacionada con medicamentosN=89 | p | IRA intrahospitalaria N = 194 |
|---|---|---|---|---|
| Edad en años, mediana [RI] | 72 [18] | 73 [22,5] | 0,86 | 72 [20] |
| > 64 años, n (%) | 72 (68,6) | 57 (64,0) | 0,54 | 129 (66,5) |
| Género, hombres n (%) | 66 (63,0) | 51 (57,3) | 0,46 | 117 (60,0) |
| Antecedentes patológicos, n (%) | ||||
| Hipertensión | 78 (74,3) | 52 (58,4) | 0,02 | 130 (67,0) |
| Insuficiencia cardíaca | 28 (26,7) | 13 (14,6) | 0,05 | 41 (21,1) |
| Cardiopatía isquémica | 24 (23,0) | 12 (13,5) | 0,10 | 36 (18,6) |
| Diabetes mellitus | 42 (40,0) | 27 (30,3) | 0,17 | 69 (35,6) |
| Insuficiencia renal crónica | 37 (35,2) | 36 (40,4) | 0,46 | 73 (37,6) |
| Dos o más | 63 (60,0) | 40 (45,0) | 0,04 | 103 (53,1) |
| Servicio de ingreso, n (%) | ||||
| Quirúrgico | 53 (50,5) | 40 (44,9) | 0,47 | 93 (47,9) |
| Médico | 52 (49,5) | 49 (55,1) | 101 (52,1) | |
| Días desde el ingreso hasta la IRA, media (DE) | 11,8 (±9,1) | 12 (±14) | 0,56 | 11,9 (±11,9) |
| Creatinina previa a la IRA, (mg/dl), media (DE) | 1,24 (±0,46) | 1,29 (±0,69) | 0,95 | 1,26 (±0,58) |
| Creatinina máxima durante la IRA, (mg/dl), media (DE) | 2,72 (±1,04) | 3,76 (±2,11) | <0,001 | 3,2 (±1,71) |
| Factores de riesgo, n (%) | ||||
| Depleción de volumen | 40 (38,1) | 42 (47,2) | 0,24 | 82 (42,3) |
| Hipotensión | 26 (24,8) | 35 (39,3) | 0,03 | 61 (31,4) |
| Insuficiencia cardíaca descompensada | 20 (19,0) | 17 (19,1) | 1,00 | 37 (19,1) |
| Sangrado (del sitio quirúrgico o de otro sitio) | 8 (7,6) | 14 (15,7) | 0,11 | 22 (11,3) |
| Uno | 50 (47,6) | 43 (48,3) | 93 (47,9) | |
| Dos | 29 (27,6) | 20 (22,5) | <0,001 | 49 (25,3) |
| Tres o más | 10 (9,5) | 26 (29,2) | 36 (18,5) | |
DE: desviación estándar; IRA: insuficiencia renal aguda; RI: rango intercuartílico.
El valor de p fue determinado usando la prueba Chi-cuadrado o la prueba T o la prueba U de Mann–Whitney.
El ingreso se produjo en servicios de cirugía en un 47,9% de los casos y en servicios médicos en un 52,1%. Los principales diagnósticos que motivaron el ingreso fueron: neoplasia (n = 58; 29,8%), enfermedad infecciosa (n = 18; 9,2%) y trasplante no renal (n = 16; 8,2%). La estancia media hospitalaria fue de 25,6 ± 20,4 días y la media desde el ingreso hasta cumplir los criterios de IRA del estudio fue de 11,9 ± 12 días.
Un 50% de los casos presentaron un aumento de la creatinina basal entre el 50 y el 99%. Un 30% presentaron riesgo de daño renal y un 48% daño renal según la clasificación RIFLE (tabla 2). La complicación más frecuente relacionada con IRA durante la hospitalización fue la hiperpotasemia (25,8% de los casos), seguida de la insuficiencia cardíaca descompensada (12,9%), arritmia (4,1%) y hemorragia digestiva (3,6%).
Gravedad de la insuficiencia renal aguda
| Gravedad | IRA relacionada con medicamentos N = 105 | IRA no relacionada con medicamentos N = 89 | p | IRA intrahospitalaria N = 194 |
|---|---|---|---|---|
| Incremento de creatinina n (%) | ||||
| ≥ 50% | 58 (55,2) | 38 (42,7) | 0,21 | 96 (49,5) |
| ≥ 100% | 28 (26,7) | 32 (36,0) | 60 (30,9) | |
| ≥ 200% | 19 (18,1) | 19 (21,3) | 38 (19,6) | |
| Clasificación de RIFLE n (%) | ||||
| Riesgo | 39 (37,1) | 19 (21,3) | 0,05 | 58 (29,9) |
| Lesión | 46 (43,8) | 47 (52,8) | 93 (47,9) | |
| Fallo | 20 (19,0) | 23 (25,8) | 43 (22,2) | |
IRA: insuficiencia renal aguda.
El valor de p fue determinado usando la prueba Chi-cuadrado.
En 95 casos (62,1%) la función renal se recuperó al alta de forma completa, en 39 casos (25,5%) de forma parcial y en 19 (12,4%) no se recuperó. En 8 casos (4,1%) los pacientes requirieron hemodiálisis y en 2 esta continuó al alta. La mortalidad durante la hospitalización en los pacientes con IRA fue del 22,4%. De los pacientes con desenlace mortal, en 11 (5,7%) la muerte se relacionó con la IRA y en el resto con otra causa.
En 89 (45,9%) casos la alteración de la función renal no fue de causa medicamentosa. En 74 (83,1%) de estos, la causa fue prerrenal, en 10 (11,3%) renal y en 5 (5,6%) fue posrenal (fig. 2).
En 105 (54,1%) casos la alteración de la función renal se relacionó con medicamentos (fig. 1). Las categorías de imputabilidad fueron posible en 22 (21%) casos, probable en 70 (66,6%) y definida en 13 (12,4%). Sin embargo, en un 85% de los casos relacionados con medicamentos, hubo uno o más factores de riesgo (tabla 1).
En los 105 casos con IRA relacionada con medicamentos hubo 305 fármacos implicados. Los subgrupos de medicamentos implicados con mayor frecuencia fueron los diuréticos (33,4%, furosemida con mayor frecuencia), agentes que actúan sobre el sistema renina-angiotensina (17,3%, enalapril el más frecuente), bloqueadores β-adrenérgicos (7,2%, bisoprolol el más frecuente), inmunosupresores (7,5%, tacrolimus el más frecuente), medios de contrastes iodados (5,9%) y AINE (5,5%) (tabla 3). En un 20,0% de los casos, la IRA se relacionó con un único medicamento sospechoso (diuréticos y contrastes para radioimagen fueron los más frecuentes, seguidos de IECA y AINE), en un 22% con 2 medicamentos, en un 24% con 3 medicamentos, en un 18% con 4 y en un 16% con 5 o más. La combinación de medicamentos sospechosos más frecuente fue un diurético y un agente de los que actúan sobre el sistema renina-angiotensina, solos o combinados con un tercero, o más medicamentos sospechosos (36 casos, 34,3%).
Grupos terapéuticos, subgrupos y medicamentos relacionados con la insuficiencia renal aguda
| Grupos terapéuticos N = 305 (%) | Subgrupos N = 305 (%) | Medicamentos N = 305 (%) | |
|---|---|---|---|
| Sistema cardiovascular 221 (72,4) | Diuréticos 102 (33,4) | Furosemida | 70 (22,9) |
| Hidroclorotiazida | 19 (6,2) | ||
| Espironolactona | 13 (4,3) | ||
| Agentes activos sobre el sistema renina angiotensina 53 (17,4) | Enalapril | 23 (7,5) | |
| Losartán | 17 (5,6) | ||
| Captopril | 13 (4,3) | ||
| Agentes betabloqueantes 22 (7,2) | Bisoprolol | 6 (1,9) | |
| Labetalol | 4 (1,3) | ||
| Atenolol | 4 (1,3) | ||
| Carvedilol | 3 (1,0) | ||
| Nadolol | 3 (1,0) | ||
| Propranolol | 2 (0,7) | ||
| Bloqueantes de los canales del calcio 21 (6,9) | Amlodipino | 14 (4,6) | |
| Nifedipino | 5 (1,7) | ||
| Diltiazem | 1 (0,3) | ||
| Nimodipino | 1 (0,3) | ||
| Terapia cardíaca 15 (4,9) | Nitroglicerina | 11 (3,6) | |
| Mononitrato de isosorbide | 2 (0,7) | ||
| Ivabradina | 1 (0,3) | ||
| Amiodarona | 1 (0,3) | ||
| Sistema cardiovascular 221 (72,4) | Antihipertensivos 8 (2,6) | Doxazosina | 7 (2,3) |
| Hidralazina | 1 (0,3) | ||
| Agentes antineoplásicos e inmunomoduladores 30 (9,8) | Inmunosupresores 23 (7,5) | Tacrolimus | 16 (5,1) |
| Micofenolato mofetilo | 3 (1,0) | ||
| Ciclosporina | 2 (0,7) | ||
| Everolimus | 2 (0,7) | ||
| Agentes antineoplásicos 7 (2,3) | Citarabina | 2 (0,7) | |
| Carmustina | 1 (0,3) | ||
| Rituximab | 1 (0,3) | ||
| Melfalan | 1 (0,3) | ||
| Bortezomib | 1 (0,3) | ||
| Etopósido | 1 (0,3) | ||
| Varios 18 (5,9) | Contrastes radiológicos18 (5,9) | Ioversol | 7 (2,3) |
| Iobitridol | 3 (1,0) | ||
| Iomeprol | 2 (0,7) | ||
| Iohexol | 1 (0,3) | ||
| Iopamidol | 3 (1,0) | ||
| Iopromida | 2 (0,7) | ||
| Sistema musculoesquelético 17 (5,5) | Antiinflamatorios no esteroideos 17 (5,5) | Dexketoprofeno | 16 (5,2) |
| Ibuprofeno | 1 (0,3) | ||
| Antiinfecciosos de uso sistémico 10 (3,3) | Antibacterianos 4 (1,3) | Vancomicina | 2 (0,7) |
| Trimetoprim-sulfametoxazol 2 (0,7) | |||
| Antimicóticos 3 (1,0)Antivirales 3 (1,0) | anfotericina b | 3 (1,0) | |
| Aciclovir | 1 (0,3) | ||
| Ganciclovir | 1 (0,3) | ||
| Valganciclovir | 1 (0,3) | ||
| Sangre y órganos hematopoyéticos 5 (1,6) | Inhibidores de la agregación de las plaquetas 5 (1,6) | Ácido acetilsalicílico | 5 (1,6) |
| Sistema genitourinario y hormonas sexuales 3 (1,0) | Antagonistas alfa-adrenérgicos 3 (1,0) | Tamsulosina | 3 (1,0) |
| Sistema nervioso 1 (0,3) | Antiepilépticos 1 (0,3) | Pregabalina | 1 (0,3) |
Los pacientes con IRA relacionada con medicamentos presentaron con mayor frecuencia 2 o más antecedentes patológicos, así como el antecedente de hipertensión arterial y de insuficiencia cardíaca en comparación con los de causa no medicamentosa (tabla 1). En cambio, presentaron con menor frecuencia 3 o más factores de riesgo de IRA e hipotensión, y la media de creatinina máxima fue menor (tabla 1). Además, la mortalidad durante la hospitalización fue menor en los pacientes con IRA relacionada con medicamentos que en los pacientes con IRA relacionada con otras causas (7,7% en comparación con 39,3%; p < 0,001). En ambos grupos la causa más frecuente de muerte fue una neoplasia. La IRA fue la causa de muerte en 4 pacientes con IRA relacionada con medicamentos y en 7 con IRA relacionada con otras causas.
DiscusiónEn nuestro estudio, 10 de cada 1.000 ingresos presentaron un episodio de IRA durante la hospitalización y en la mitad de estos el episodio se relacionó con medicamentos. Solo un 15% de los casos relacionados con medicamentos tenía el fármaco como único factor de riesgo; el resto de los pacientes presentaron además uno o más factores de riesgo. Los diuréticos y los IECA o antagonistas del receptor de angiotensina (ARA II), seguidos de los bloqueadores β-adrenérgicos y los de los canales del calcio, inmunosupresores, medios de contraste y AINE fueron los medicamentos más frecuentemente implicados. Los pacientes que durante el ingreso presentaron IRA relacionada con medicamentos tenían con mayor frecuencia 2 o más antecedentes patológicos; en cambio, presentaron menos factores de riesgo de IRA, una menor creatinina durante el episodio y tuvieron una menor mortalidad. Varios estudios han descrito la frecuencia de IRA intrahospitalaria5,8–15 y su etiología, incluyendo la causada por medicamentos5,8–13. Sin embargo, en este estudio se utiliza un algoritmo para establecer la causalidad de los medicamentos en la IRA y se describen en detalle las características de los pacientes con IRA relacionada con medicamentos.
La incidencia de IRA intrahospitalaria descrita en los estudios ha sido variable, de un 0,16% en el estudio de Liaño et al.15 a un 22,7% en el de Wang et al.16. La de nuestro estudio fue similar a la descrita por Kohli et al.8 (1,4%), Lauzurica et al.11 (1,6%) y Shusterman et al.10 (1,9%). Estas diferencias se deben a las distintas definiciones de IRA utilizadas y a que los criterios de inclusión de los pacientes también variaron. En el estudio de Barrantes et al.13, con los criterios de inclusión y exclusión más parecidos a los del nuestro, se describió una incidencia de IRA superior (12,6%) a la de nuestro estudio. Sin embargo, se utilizó una definición de IRA más amplia (aumento de creatinina de 0,3mg/dl o superior durante cualquier período de 48 h) y el cálculo de la incidencia no fue sobre el total de ingresos sino sobre los pacientes elegibles.
En el presente estudio los pacientes con IRA intrahospitalaria tenían una edad avanzada, predominaban los hombres sobre las mujeres, más del 50% presentaban una media de 2 o más antecedentes patológicos y casi un 40% tenían IRC. Estas características son similares a las descritas para la cohorte de pacientes con IRA intrahospitalaria en el estudio de Barrantes et al.13, aunque en este estudio el porcentaje de pacientes con IRC fue todavía superior (52,1%) y predominaron las mujeres (53,6%). En los estudios de Kohli et al.8 y de Liaño et al.15 publicados en años anteriores, la edad media de los pacientes fue menor y en el de Kohli et al.8 también lo fue la frecuencia de IRC. Sin embargo, la población que ingresa actualmente en los hospitales es de edad más avanzada, presenta mayor comorbilidad y está expuesta a más procedimientos diagnósticos y terapéuticos con un riesgo potencial superior de lesionar el riñón22.
Casi un 80% de los pacientes de nuestro estudio presentaron riesgo de daño renal o daño renal durante el episodio de IRA según la clasificación RIFLE. No se puede comparar la gravedad de la IRA con la de otros estudios, dado que no utilizaron la clasificación RIFLE; sin embargo, el porcentaje de pacientes que en nuestro estudio requirió diálisis (4,1%) fue menor al descrito en otros estudios5,8. Esto puede explicarse por el hecho de que en nuestro estudio no se incluyeron los episodios de IRA ocurridos en las áreas de críticos.
Por otro lado, la estancia media hospitalaria de los pacientes triplicó la estancia media del hospital (8,7 días) durante el período de estudio. En distintos estudios la estancia media de los pacientes con IRA ha sido superior a la de los controles sin esta complicación10,13. La IRA intrahospitalaria también se asocia a una mayor mortalidad10,13, incluso para los pacientes que la presentan fuera de las unidades de críticos13. La mortalidad descrita para los pacientes con IRA intrahospitalaria varía de un 10,8% en el estudio de Wang et al.16 a un 32% en el estudio de Hou et al.9. En nuestro estudio la mortalidad fue superior a la descrita en el de Barrantes et al.13 (14,8%) aunque la mayoría de las muertes se produjeron por una causa distinta a la IRA.
Los medicamentos son una causa conocida de IRA. Distintos autores han revisado los fármacos que la producen con mayor frecuencia, los mecanismos implicados o los factores predisponentes23–26. La frecuencia de IRA relacionada con medicamentos descrita en los estudios de Kohli et al.8 y Barrantes et al.13 (66 y 72,3%, respectivamente) es similar a la de nuestro estudio, en cambio en el estudio de Nash et al.5 y en el de Jha et al.12 se describe una frecuencia menor (16 y 29%, respectivamente). En todos estos estudios se incluyeron únicamente episodios de IRA intrahospitalarios y, solo en el de Barrantes et al.13, se excluyeron los episodios de IRA de pacientes ingresados en la UCI, de forma similar al nuestro.
Los diuréticos seguidos de los IECA o ARA II han sido los medicamentos relacionados con mayor frecuencia con los episodios de IRA. La combinación de diuréticos con antagonistas del sistema renina-angiotensina, sola o junto con otros fármacos, ha sido implicada en casi un 40% en los episodios de IRA por medicamentos en nuestro estudio. Cada uno de estos medicamentos puede afectar la función renal por distintos mecanismos y su combinación incrementa el riesgo de lesión renal aguda27,28. Por otro lado, los AINE también son reconocidos nefrotóxicos29. En un estudio reciente se ha descrito un aumento del riesgo de lesión renal aguda cuando se añaden al tratamiento con al menos 2 de los siguientes grupos de antihipertensivos: diuréticos, IECA o ARA II30. Los IECA5,8,13, diuréticos11 y los AINE5,8,13, también se han relacionado con casos de IRA intrahospitalaria en otros estudios. En cambio, los aminoglucósidos, primera causa de IRA intrahospitalaria relacionada con medicamentos en varios estudios5,8–11, no lo han sido en el presente estudio, probablemente por el menor uso que se hace de ellos en la actualidad31,32. Tampoco se describen casos relacionados con antibióticos β-lactámicos o quinolonas,23,33 a menudo relacionadas con nefritis intersticiales, pero en el presente estudio no se identificaron casos de nefritis intersticiales. En nuestro estudio, otros antihipertensivos como la amlodipina o el bisoprolol, inmunosupresores como el tacrolimus, y los medios de contraste, también se han relacionado con frecuencia con episodios de IRA. El tacrolimus, inmunosupresor a menudo utilizado para prevenir el rechazo de trasplantes de órganos sólidos y tratar algunas enfermedades sistémicas inmunológicas, es un conocido nefrotóxico34,35. Por otro lado, los medios de contraste continúan siendo una causa de alteración de la función renal en el medio hospitalario a pesar de las medidas preventivas recomendadas36–38.
Los pacientes que durante la hospitalización presentaron IRA relacionada con medicamentos tenían con mayor frecuencia antecedentes patológicos como la hipertensión o la insuficiencia cardíaca, y los fármacos cardiovasculares fueron los más frecuentemente implicados en los episodios de IRA durante la hospitalización. Por lo tanto, estos pacientes son especialmente vulnerables a la alteración de la función renal durante el ingreso. Para prevenir los episodios de IRA de estos pacientes, sería necesario prestar especial atención a las dosis de los medicamentos cardiovasculares, especialmente a las de los diuréticos y otros antihipertensivos, y evitar algunas combinaciones como por ejemplo con los AINE. Además, en la medida de lo posible se deberían evitar algunos factores de riesgo como la depleción de volumen, deshidratación e hipotensión durante la hospitalización. En nuestro estudio, la mayoría de los pacientes con un episodio de IRA relacionada con medicamentos presentaban concomitantemente uno o más factores de riesgo. En el estudio de Kohli et al.8 también se observó que la mayoría de los casos relacionados con medicamentos se acompañaban de otros factores de riesgo.
Este estudio tiene algunas limitaciones. Aunque es un estudio unicéntrico, pensamos que los resultados se pueden extrapolar a otros hospitales de características similares, dado que el nuestro es un hospital terciario y dispone de todas la especialidades médicas y quirúrgicas, y un nivel de complejidad similar al de los hospitales con estas características.
La información de los factores de riesgo de IRA se recogió según constaban en la historia clínica. Debido a esto, podría haberse omitido algún dato, aunque la información clínicamente relevante se registra.
Entre las fortalezas de nuestro estudio destacamos que es prospectivo y que la alteración de la función renal se detectó mediante un programa informático que permitió una estimación fiable de la incidencia de la IRA intrahospitalaria. Además, se utilizó un método estandarizado y reproducible para establecer la causalidad de los medicamentos en los episodios de IRA.
En conclusión, en nuestro estudio, la mitad de los episodios de IRA durante la hospitalización en servicios médicos y quirúrgicos se relacionaron con medicamentos. De estos, los más frecuentemente implicados fueron fármacos utilizados para tratar enfermedades cardiovasculares como diuréticos o los inhibidores del sistema renina-angiotensina u otros como los inmunosupresores, medios de contraste y AINE. Además, los pacientes con episodios de IRA relacionada con medicamentos presentaron más antecedentes patológicos cardiovasculares. Con el objetivo de evitar los episodios de IRA durante la hospitalización de estos pacientes, se debería ser especialmente cuidadoso en la dosificación de estos medicamentos y evitar ciertas combinaciones de fármacos y prestar especial atención a la presencia de factores de riesgo.
Conflicto de interesesLos autores declaran no tener conflictos de interés.
El proyecto fue financiado por el subsidio n.° 374/09/08 obtenido en la convocatoria pública para la concesión de subvenciones para proyectos de investigación en los servicios clínicos y de salud en el año 2008 (Departamento de Salud Catalán y la Agencia de Evaluación de Tecnología e Investigación Médicas de Catalunya en DOGC N.° 5464 de septiembre de 2009).