La infección por coronavirus SARS-CoV-2, o COVID-19, tuvo su origen en Wuhan, China, en diciembre del 20191. Esta infección se propagó alrededor del mundo rápidamente, afectando a numerosos países, siendo declarada como pandemia por la Organización Mundial de la Salud el 11 de marzo del 2020.
Se han detectado subgrupos de población de riesgo para el desarrollo de formas graves; es el caso de los pacientes con trasplante renal, que presentan una mayor incidencia de contagios e ingresos, así como requerimiento de cuidados intensivos2. Entre los motivos de la susceptibilidad de esta población se encuentra el tratamiento inmunosupresor.
Por otra parte, el manejo del tratamiento inmunosupresor en el contexto de la infección por SARS-CoV-2 no está claro3,4. Además, el perfil de seguridad e interacciones de determinados fármacos empleados en el tratamiento de la infección limita su uso. Dentro de este grupo de tratamientos, las inmunoglobulinas humanas inespecíficas intravenosas (IgIV) presentan quizás un buen perfil, convirtiéndolas en una interesante alternativa terapéutica5.
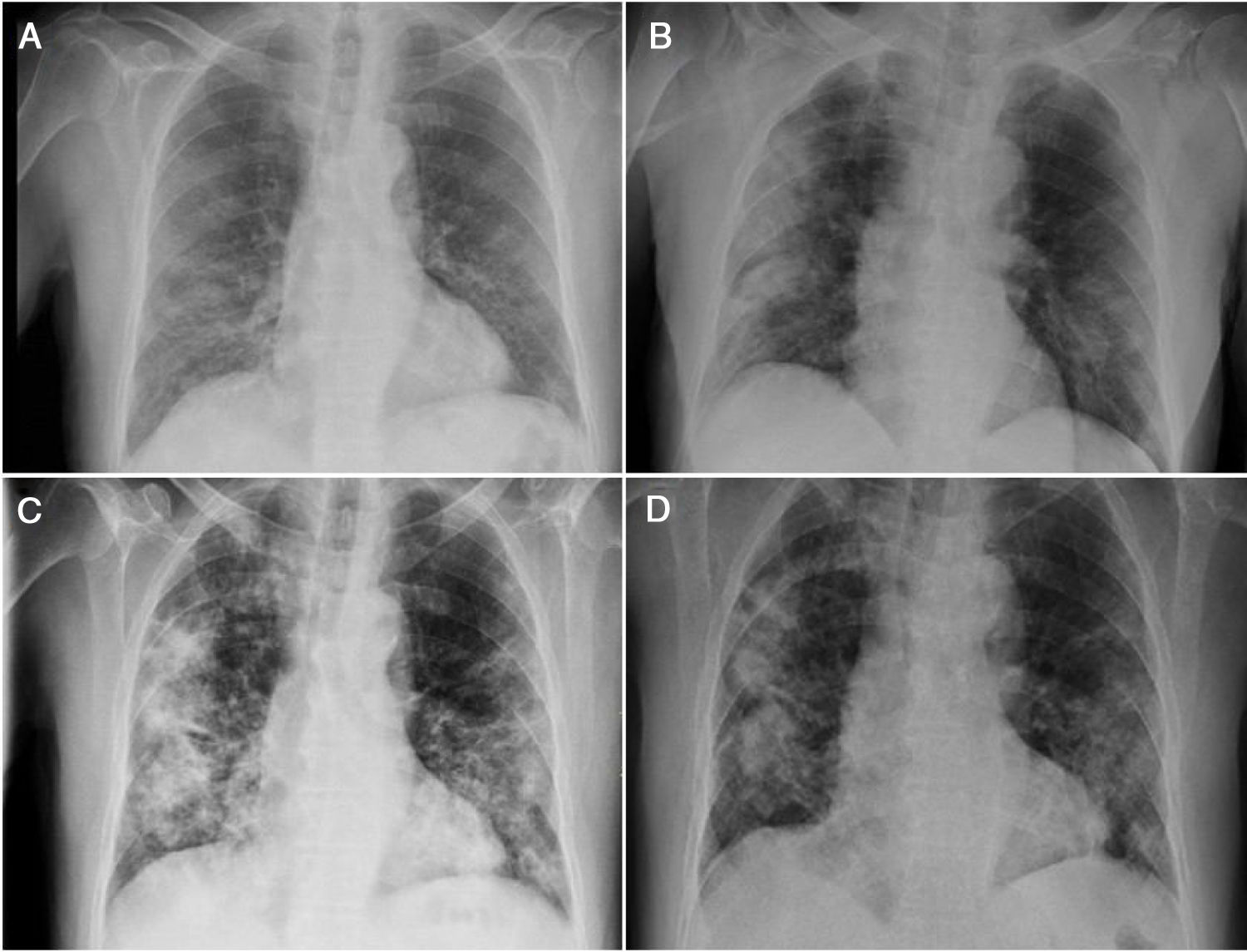
Se presenta el caso de un varón de 72 años, hipertenso, dislipidémico y trasplantado renal desde 2012. Mantenía tratamiento inmunosupresor con tacrolimús y everolimús, y presentaba una cifra de creatinina basal de 1,43mg/dl. El paciente acudió a urgencias refiriendo malestar general y cefalea de 3días de evolución. Presentaba cifras tensionales normales, temperatura axilar de 37°C y saturación de oxígeno (SatO2) del 92% respirando aire ambiental. En la radiografía de tórax presentaba infiltrados pulmonares bilaterales de perfil intersticial (fig. 1A) y a nivel analítico destacaba un fracaso renal agudo (valores de creatinina y urea: 2,52mg/dl y 77mg/dl, respectivamente) y una elevación de los niveles de tacrolimús (15,1 ng/ml) respecto a su último control. La determinación de PCR del exudado nasofaríngeo resultó positiva para SARS-CoV-2. Se decide ingreso, iniciándose tratamiento con hidroxicloroquina, azitromicina y lopinavir/ritonavir junto con ceftazidima y glucocorticoides (tabla 1), suspendiéndose el tratamiento inmunosupresor que tomaba el paciente.
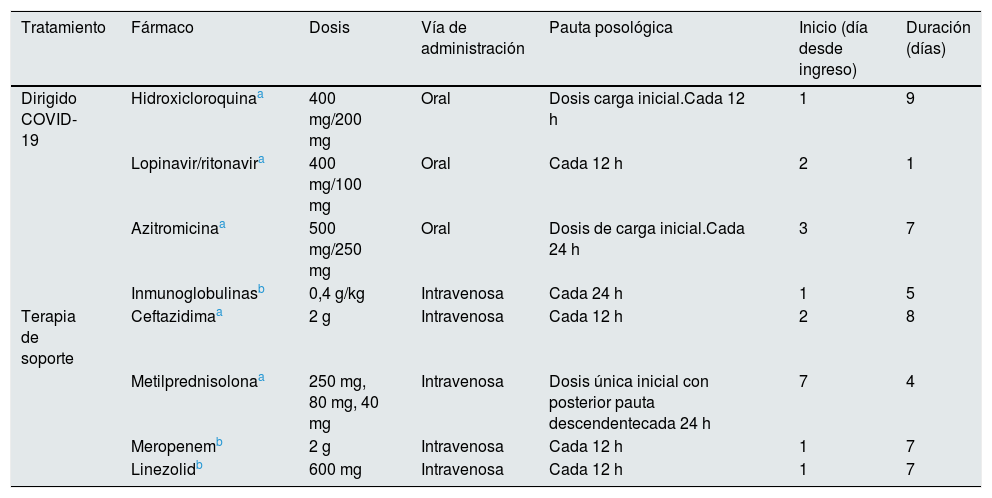
Tabla resumen de los tratamientos administrados durante el primer y el segundo ingreso
| Tratamiento | Fármaco | Dosis | Vía de administración | Pauta posológica | Inicio (día desde ingreso) | Duración (días) |
|---|---|---|---|---|---|---|
| Dirigido COVID-19 | Hidroxicloroquinaa | 400 mg/200 mg | Oral | Dosis carga inicial.Cada 12 h | 1 | 9 |
| Lopinavir/ritonavira | 400 mg/100 mg | Oral | Cada 12 h | 2 | 1 | |
| Azitromicinaa | 500 mg/250 mg | Oral | Dosis de carga inicial.Cada 24 h | 3 | 7 | |
| Inmunoglobulinasb | 0,4 g/kg | Intravenosa | Cada 24 h | 1 | 5 | |
| Terapia de soporte | Ceftazidimaa | 2 g | Intravenosa | Cada 12 h | 2 | 8 |
| Metilprednisolonaa | 250 mg, 80 mg, 40 mg | Intravenosa | Dosis única inicial con posterior pauta descendentecada 24 h | 7 | 4 | |
| Meropenemb | 2 g | Intravenosa | Cada 12 h | 1 | 7 | |
| Linezolidb | 600 mg | Intravenosa | Cada 12 h | 1 | 7 |
Tras 5días de ingreso, en los que la evolución clínica fue favorable, con disminución de los parámetros inflamatorios a nivel analítico y una normalización de la función renal, presentaba un aumento en los niveles de tacrolimús (29,31 ng/ml), normalizándose tras 4días. Se realizó una nueva radiografía en la que se descartó la presencia de progresión (fig. 1B), decidiéndose alta hospitalaria y reinicio del tratamiento inmunosupresor previo a dosis habituales.
Siete días más tarde acudió nuevamente a urgencias refiriendo fiebre los días previos con aumento progresivo de la sensación disneica acompañada de síndrome miccional. Se realizó una radiografía de tórax donde presentaba empeoramiento con respecto a la previa (fig. 1C). La determinación analítica reflejó leucocitosis (16,4 miles/μl) con linfopenia (0,6 miles/μl) y elevación de reactantes de fase aguda (PCR 7,6mg/dl, dímero D 886 μg/l y procalcitonina 3,88 ng/ml). Se inició tratamiento con IgIV, acompañado de linezolid y meropenem, y se cursó ingreso (tabla 1), suspendiéndose nuevamente el tratamiento inmunosupresor previo.
Completaron 5días de tratamiento con IgIV sin presentar reacciones adversas y con una marcada mejoría a nivel clínico, con desaparición de la disnea y mejoría radiológica (fig. 1D), lo cual permitió el alta hospitalaria precoz al sexto día.
El caso descrito refleja la complejidad del tratamiento de la infección por SARS-CoV-2 en un paciente trasplantado renal, encontrándose limitado por las interacciones medicamentosas. En el presente caso, se asumió la interacción entre tacrolimús y lopinavir/ritonavir como principal causante de la elevación en los niveles del primero, si bien el deterioro en la función renal pudo contribuir al mismo6. El manejo del tratamiento inmunosupresor en pacientes trasplantados con COVID-19 es controvertido. A pesar de disponer de algunas experiencias publicadas, se desconoce la repercusión que podría tener el mantenimiento de las dosis habituales de inmunosupresor en el contexto de esta infección3,4,7.
Por otro lado, la infección por SARS-CoV-2 todavía carece de un tratamiento efectivo. El bajo beneficio obtenido con lopinavir/ritonavir en estudios recientes pone en duda su utilidad, sobre todo en aquellos casos con mayor susceptibilidad a sus efectos tóxicos8.
Otro grupo de fármacos que han ido adquiriendo protagonismo en el control de las formas graves de infección son los biológicos. Sin embargo, su empleo se ve restringido en pacientes previamente inmunodeprimidos. En este sentido, el tratamiento con IgIV cobra importancia y supone una opción atractiva por su perfil de seguridad y su potencial eficacia, modulando la respuesta inflamatoria. Si bien la evidencia que respalda su empleo es limitada, casos recientemente publicados apuntan a un posible beneficio en formas graves de COVID-199. Por otra parte, existen experiencias en pacientes con trasplante renal en las que su empleo se asoció a una buena evolución clínica10. El caso que se presenta constituye el primero en nuestro país que apoya la utilización de IgIV en aquellos casos de pacientes con trasplante renal que presentan formas graves de COVID-19.
FinanciaciónNo se ha contado con ninguna fuente de financiación para la elaboración del presente trabajo.
Conflicto de interesesLos autores declaran la ausencia de conflictos de interés respecto al presente trabajo.