La asociación entre el desarrollo de vasculitis asociada a anticuerpos anticitoplasma de neutrófilo (ANCA) y el cáncer es conocida. En 1993 se describieron los primeros 4 casos de pacientes que presentaron carcinoma de pulmón o vejiga al poco tiempo del inicio clínico de glomerulonefritis con ANCA positivos1. Desde entonces, han aparecido pocos casos clínicos más y alguna evidencia de dicha asociación en registros de pacientes con ANCA positivos, tanto c-ANCA como p-ANCA2–5. Mayoritariamente, el método de detección fue la inmunofluorescencia indirecta o ELISA directos, que tenían una sensibilidad y una especificidad muy baja comparados con los métodos de captura actuales.
Presentamos el caso de un paciente varón de 48 años, fumador, que comienza con síndrome general y en el que se objetiva en la analítica (tabla 1) un deterioro de función renal (creatinina [Cr]: 1,8mg/dl; filtrado glomerular [FG]: 42ml/min) y sedimento con ++++ de proteínas, ++++ de hemoglobina y >100 hematíes/campo (60% dismórficos). Además, destacaba una proteinuria de 3.900mg/24h y una VSG 100mm. El estudio inmunológico mostró: inmunoglobulinas y complemento normal, anticuerpos antinucleares con patrón homogéneo a 1/640 sin especificidad demostrada y anticuerpos antimieloperoxidasa (MPO) >600 UI/ml; los anticuerpos antiproteinasa 3, el anticuerpo antimembrana basal glomerular y el factor reumatoide fueron negativos. La ecografía urológica y la radiografía de tórax, sin hallazgos patológicos. La biopsia renal mostró 22 glomérulos, 2de ellos esclerosados, 13con proliferación extracapilar epitelial, 3semilunas fibrosas y 4con lesiones incipientes de necrosis de ovillo glomerular. Además, había infiltrado intersticial disperso moderado compuesto por linfocitos, polimorfonucleares y células plasmáticas. Las arterias no tenían lesiones significativas y se mostraron depósitos mediante inmunofluorescencia positiva focal y segmentaria para C3 (++). Ante estos hallazgos se inicia tratamiento con 3bolos de 500mg de metilprednisolona en días consecutivos, seguido de prednisona vía oral a 1mg/kg, con descenso progresivo posterior y ciclofosfamida intravenosa a dosis de 1 g/m2/mes.
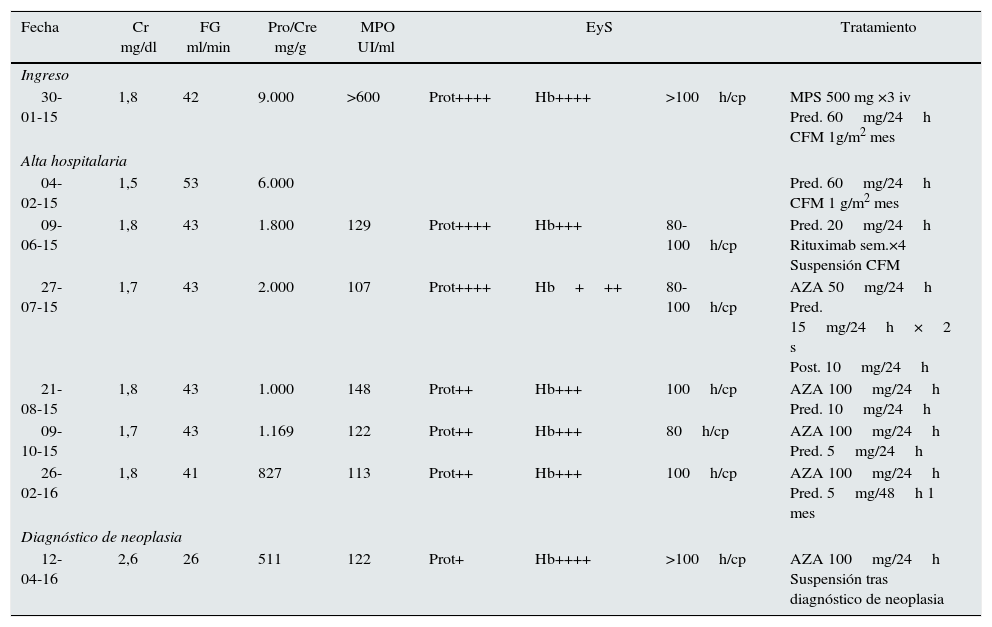
Evolución de los principales hallazgos analíticos del caso y tratamiento administrado
| Fecha | Cr mg/dl | FG ml/min | Pro/Cre mg/g | MPO UI/ml | EyS | Tratamiento | ||
|---|---|---|---|---|---|---|---|---|
| Ingreso | ||||||||
| 30-01-15 | 1,8 | 42 | 9.000 | >600 | Prot++++ | Hb++++ | >100h/cp | MPS 500 mg ×3 iv Pred. 60mg/24h CFM 1g/m2 mes |
| Alta hospitalaria | ||||||||
| 04-02-15 | 1,5 | 53 | 6.000 | Pred. 60mg/24h CFM 1 g/m2 mes | ||||
| 09-06-15 | 1,8 | 43 | 1.800 | 129 | Prot++++ | Hb+++ | 80-100h/cp | Pred. 20mg/24h Rituximab sem.×4 Suspensión CFM |
| 27-07-15 | 1,7 | 43 | 2.000 | 107 | Prot++++ | Hb+++ | 80-100h/cp | AZA 50mg/24h Pred. 15mg/24h×2 s Post. 10mg/24h |
| 21-08-15 | 1,8 | 43 | 1.000 | 148 | Prot++ | Hb+++ | 100h/cp | AZA 100mg/24h Pred. 10mg/24h |
| 09-10-15 | 1,7 | 43 | 1.169 | 122 | Prot++ | Hb+++ | 80h/cp | AZA 100mg/24h Pred. 5mg/24h |
| 26-02-16 | 1,8 | 41 | 827 | 113 | Prot++ | Hb+++ | 100h/cp | AZA 100mg/24h Pred. 5mg/48h 1 mes |
| Diagnóstico de neoplasia | ||||||||
| 12-04-16 | 2,6 | 26 | 511 | 122 | Prot+ | Hb++++ | >100h/cp | AZA 100mg/24h Suspensión tras diagnóstico de neoplasia |
AZA: azatioprina; CFM: ciclofosfamida; Cr: creatinina sérica; EyS; elemental y sedimento; FG: filtrado glomerular mediante fórmula CKD-EPI; Hb: hemoglobina; Pred: prednisona; Pro/Cre: índice proteínas/creatinina en orina.
Cinco meses después, ante ausencia de mejoría de función renal (Cr 1,8mg/dl y FG 43,5ml/min) y persistencia de sedimento activo (tabla 1) y de MPO positivos, se decide suspender la ciclofosfamida e iniciar tratamiento con rituximab.
Tras 4 dosis de rituximab, la analítica fue: Cr 1,2mg/dl, FG 63ml/min, Pro/Cre 2.727,3mg/g, sedimento (proteínas ++++, hemoglobina +++, 40-50 hematíes/campo) y MPO 130UI/ml. Por ello, se inicia tratamiento de mantenimiento con azatioprina.
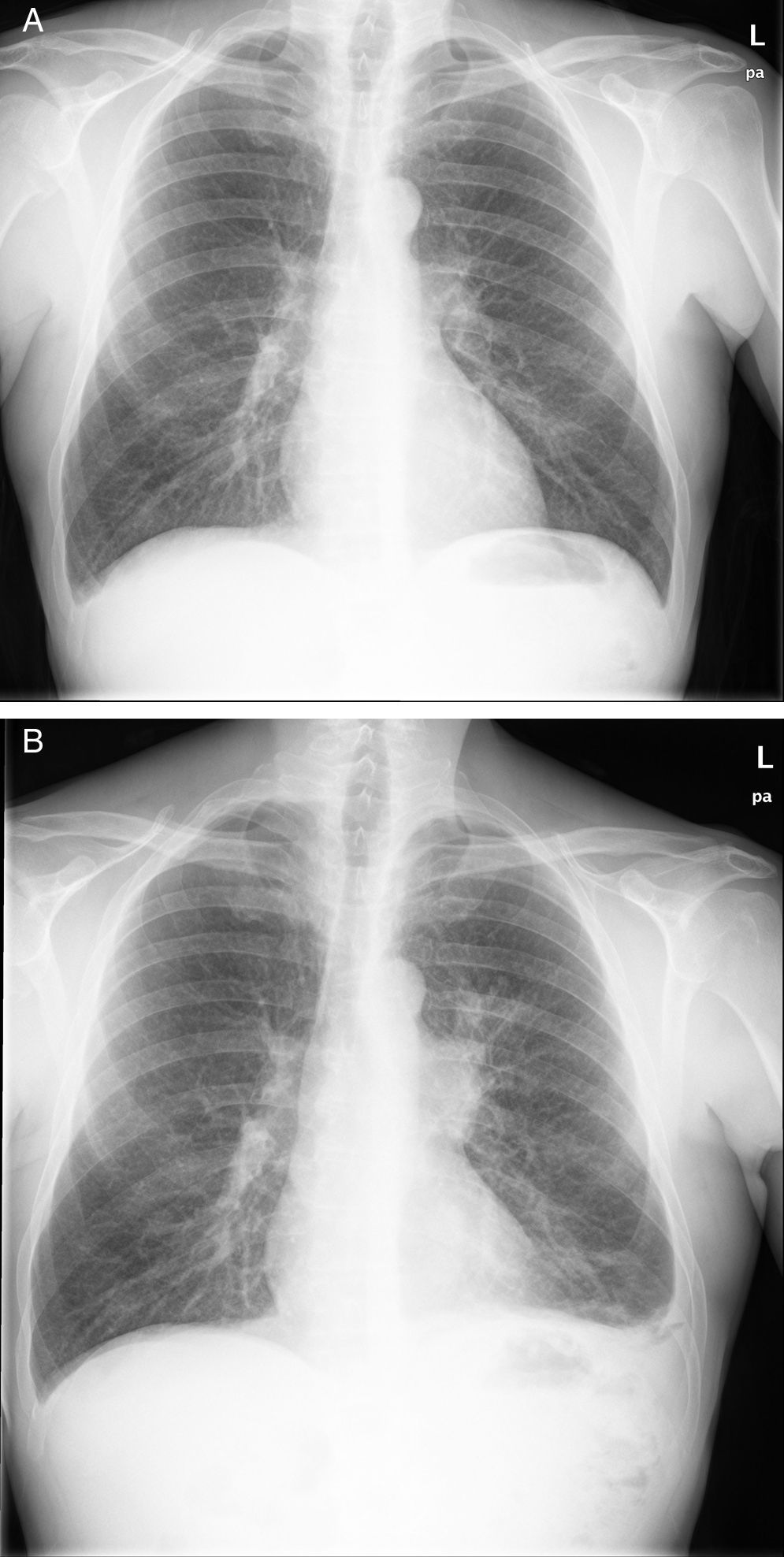
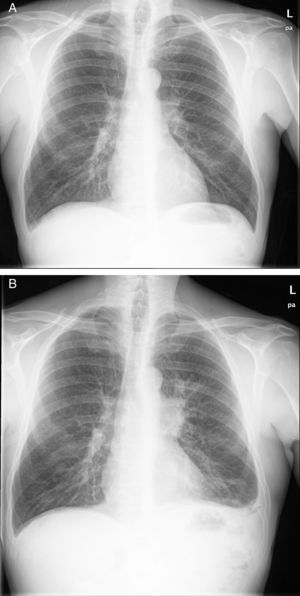
Nueve meses más tarde comenzó con tos y expectoración, sin mejoría tras antibioterapia. Se evidenció en radiografía de tórax una masa hiliar izquierda con diagnóstico anatomopatológico por biopsia transbronquial de carcinoma microcítico. La TAC mostró múltiples implantes tumorales pleurales, hepáticos y conglomerados adenopáticos paratraqueales y subcarinales (fig. 1). Ante este diagnóstico, se retira la inmunosupresión y se inicia tratamiento con carboplatino-etopósido, que no evita el empeoramiento clínico progresivo y el fallecimiento un mes después.
El caso presentado se suma a las evidencias previas y no muy abundantes de la presencia de ANCA como marcador paraneoplásico. El paciente, aunque con los antecedentes de tabaquismo, no mostró datos del carcinoma de pulmón al inicio de la glomerulonefritis. La presencia de títulos elevados de MPO, que se mantenían positivos a cifras considerables, junto con un sedimento urinario activo, obligó a un incremento de la inmunosupresión que incluía rituximab y, posteriormente, azatioprina. Tras ello, el paciente presentó un carcinoma de pulmón. Durante la evolución del paciente llamó la atención que los títulos de MPO fueron>600 U/ml al inicio de la glomerulonefritis y con el tratamiento inicial cayeron a cifras alrededor de 120 U/ml, pero siempre se mantuvieron a esos niveles, con independencia de la inmunosupresión añadida posteriormente. El método de detección de los anticuerpos es de anclaje, que incrementa la sensibilidad (50%) y mantiene una especificidad superior al 99%. A pesar de ello, el mantenimiento de los títulos de MPO en el caso clínico descrito puede reflejar un efecto paraneoplásico, puesto que los ANCA también se han descrito como autoanticuerpos paraneoplásicos tanto en tumores de órgano sólido como en neoplasias hematológicas6. Es posible que la disregulación del sistema inmunitario causante de la vasculitis esté en la base del posterior desarrollo de una neoplasia al favorecer el escape tumoral de los mecanismos de inmunovigilancia. Por otro lado, tampoco se puede descartar que el proceso tumoral estuviese ya en marcha en un paciente de mediana edad fumador y que la destrucción celular indujese epítopos que desencadenasen la respuesta humoral productora de MPO7. El tratamiento con rituximab probablemente precipitó la evolución. De hecho, el paciente tenía también anticuerpos antinucleares al inicio del fallo renal, lo cual también se ha relacionado con la exposición de neoepítopos en el contexto de destrucción celular en procesos inflamatorios8.
En conclusión, el presente caso refleja la importancia de tener en cuenta la asociación con el desarrollo de neoplasias en una glomerulonefritis con ANCA en la que el manejo de la inmunosupresión debe ser exquisito, especialmente en el caso de permanencia de títulos elevados de autoanticuerpos.