La respuesta inmunitaria a la vacuna de la hepatitis B (HB) está impedida en los pacientes en hemodiálisis (HD), y la persistencia de la inmunidad, la eficacia de la revacunación y la periodicidad de la realización de controles serológicos no están bien definidas. Presentamos la experiencia de un protocolo de vacunación de la HB con tres dosis intramusculares de 40 μg de vacuna recombinante (Engerix®-B) en un grupo de 136 pacientes atendidos en una unidad de HD a lo largo de 18 años. Se realizaron controles anuales de anticuerpos anti-HB en todos los pacientes, y semestrales en 31; y se administraba anualmente una dosis doble de vacuna a los pacientes que no respondían o cuando los niveles de anticuerpos descendían por debajo de 10 UI/ml. Setenta y cuatro pacientes (54,4%) presentaron seroconversión, mientras que 62 pacientes no respondieron. La edad de los pacientes era superior en el grupo de no respondedores, pero no se observaron diferencias en el sexo ni en la etiología de la enfermedad renal. Un 32% de los pacientes respondedores perdió la memoria inmunológica al primer año de la vacunación, y tan sólo un 18% de los pacientes permaneció inmunizado a los seis años. El título de anticuerpos inmediatamente después de completar la vacunación fue predictor del mantenimiento de la memoria inmunológica: un 75% de los pacientes con títulos de anticuerpos >1.000 UI/ml mantuvo la seroprotección a los tres años en comparación con un 47% con títulos entre 100-999 (p = 0,08), y un 34% con títulos entre 11-99 (p = 0,02). La administración de dosis de refuerzo fue efectiva en un 24% de los pacientes no respondedores, y un 69% mantenía la respuesta inmunológica al final del primer año. Las dosis de refuerzo repetidas en pacientes no respondedores a una primera dosis consiguieron nuevas seroconversiones en un 19,6% de los pacientes. La práctica de controles semestrales podría haber permitido administrar dosis de recuerdo antes del período anual en un 16% de los pacientes respondedores. En conclusión, nuestros resultados demuestran que un protocolo de vacunación de la HB con un seguimiento serológico regular y dosis de refuerzo sucesivas consigue una aceptable seroprotección en los pacientes en hemodiálisis.
INTRODUCCIÓN
En los años sesenta y setenta, la HB constituyó un grave problema en las unidades de HD. En las últimas décadas, la incidencia de la infección por el virus de la HB en este grupo de pacientes ha disminuido notablemente debido a los mejores métodos de estudio, a los controles más estrictos de los bancos de sangre, a los menores requerimientos transfusionales desde la disponibilidad de la eritropoyetina, a la optimización de la hemodiálisis de los pacientes infectados por el virus de la HB y al uso extensivo de la vacunación1,2.
La respuesta inmunológica a la vacuna de la HB se correlaciona con el grado de insuficiencia renal, con una mayor respuesta en pacientes con insuficiencia renal crónica prediálisis3, por lo que es más aconsejable una vacunación más precoz en esta fase de la enfermedad renal. Por el contrario, en los pacientes en HD, la respuesta a la vacuna de la HB es muy variable y menor que en la población general4,5, con una respuesta incluso por debajo del 50% con la administración de tres dosis de vacuna6,7 y algo superior con la administración de cuatro dosis8. Además, la persistencia de la respuesta inmunológica también es más baja, con una rápida disminución de los títulos de anticuerpos protectores en muchos de estos pacientes4,5,9. Los mecanismos responsables de esta disminución de la respuesta inmunológica son desconocidos. Recientemente, se ha demostrado que la baja respuesta serológica al virus de la HB en esta población está estrechamente relacionada con el impedimento en la producción de antígenos específicos dependientes de las células T, CD4+, como la IL-210.
Con objeto de mejorar la respuesta a la vacuna de la HB en la población de HD, se han propuesto diversas alternativas, como el aumento de la dosis administrada de vacuna11, su aplicación intradérmica12, la coadministración de cinc o de diversos inmunomoduladores4,5, o el uso más reciente de un nuevo adyuvante, el AS04, un derivado de los lipopolisacáridos de las bacterias13. Estas intervenciones han obtenido resultados variables14.
Muchos de los estudios publicados sobre la vacuna de la HB en los pacientes en hemodiálisis se han centrado sobre los resultados de la seroconversión de esta población8, pero la información sobre la evolución de la inmunidad en los pacientes respondedores o en los que son revacunados es más limitada.
Los objetivos de nuestro estudio han sido: a) valorar la respuesta inicial a la vacuna de la HB en pacientes en hemodiálisis, los factores que influyen en dicha respuesta y la relación existente entre la respuesta inicial y el progresivo descenso de los anticuerpos; b) analizar la eficacia y la utilidad de las revacunaciones; y c) evaluar si la realización de controles semestrales de niveles de anticuerpos aporta una información adicional sobre la obtenida en los controles anuales.
PACIENTES Y MÉTODOS
Estudio retrospectivo que analiza un protocolo de vacunación contra la HB realizado en una unidad de HD entre los años 1989 y 2002. Ciento treinta y seis pacientes en programa de HD con anti-Hbc (-) y anti-Hbs (-), sin evidencia de infección previa ni historia de vacunaciones, fueron vacunados contra la HB al inicio del tratamiento sustitutivo renal. Los pacientes recibieron tres dosis de 40 μg de vacuna recombinante (Engerix® -B, Glaxo Smith Kline Biologicals, Rixensart, Bélgica), inyectada por vía intramuscular en deltoides, en los meses 0, 1 y 6. Se realizaron controles anuales de anticuerpos y se procedía anualmente a la administración de una dosis doble de vacuna a los pacientes no respondedores (dosis de refuerzo) o en el caso de pacientes respondedores que perdían la tasa de anticuerpos (<10 UI/ml) (dosis de recuerdo). Los pacientes fueron seguidos hasta el año 2007 o hasta su fallecimiento, cambio de unidad de tratamiento o trasplante renal.
En todos los pacientes se analizó la respuesta a la vacuna, los factores que influían en la inmunización, y la eficacia de la revacunación en los pacientes que no respondieron a la vacunación inicial. También se evaluó el mantenimiento de los niveles de anticuerpos tras la primera revacunación positiva.
En un subgrupo de 63 pacientes con un seguimiento de tres años después del primer año de vacunación, se analizó la probabilidad de mantener la respuesta inmunológica en función del título de anticuerpos alcanzado durante el primer control anual. Así, los pacientes se clasificaron en tres grupos: grupo I, pacientes con anticuerpos >1.000 UI/ml; grupo II, pacientes con anticuerpos entre 100 y 999 UI/ml; y grupo III, pacientes con anticuerpos entre 11 y 99 UI/ml.
Finalmente, en un subgrupo de 31 pacientes se analizó si la realización de controles semestrales de niveles de anticuerpos aportaba alguna información adicional sobre los controles anuales de estos pacientes.
Los anticuerpos anti-Hbs se determinaron mediante enzimoinmunoanálisis de micropartículas (MEIA). El límite inferior de detección de los anticuerpos fue de 2 mUI/ml, y el coeficiente de variación intra e interensayo fue del 4,4 y 4,8%, respectivamente. Los pacientes con títulos iguales o superiores a 1.000 UI/ml fueron considerados como >1.000 UI/ml.
Los títulos de anticuerpos anti-Hbs >10 UI/ml se consideraron protectores, mientras que los títulos inferiores se definieron como pérdida de inmunidad.
El análisis estadístico se realizó utilizando el programa SPSS 11.0. Los resultados están expresados como media + DE. La comparación entre variables cuantitativas se realizó mediante la T de Student, y entre las variables categóricas mediante la chi-cuadrado.
La duración de la inmunidad según el título de anticuerpos anti-Hbs se analizó mediante las curvas de Kaplan-Meier.
Los valores p <0,05 se consideraron como significativos.
RESULTADOS
Pacientes respondedores
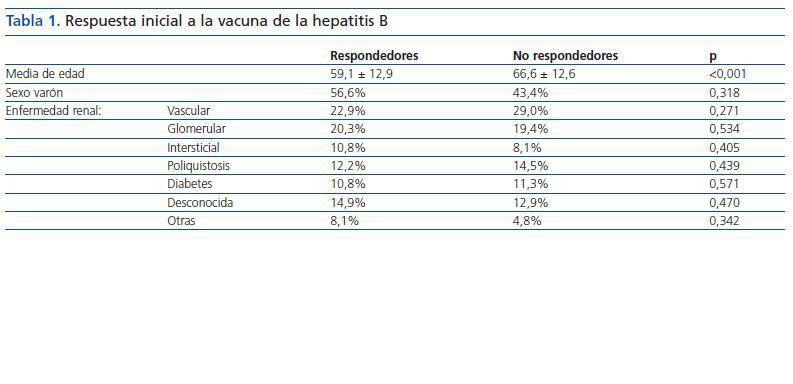
Setenta y cuatro pacientes (54,4%) desarrollaron inmunidad después de la vacunación contra la HB. De éstos, 39 pacientes (52,7%) presentaron un título de anticuerpos >100 UI/ml, nivel que se ha considerado como el umbral necesario para mantener una adecuada seroprotección en pacientes en HD. La respuesta a la vacuna de la HB estuvo relacionada con la edad, siendo la edad media de los pacientes no respondedores superior a la de los respondedores. Por el contrario, el sexo y la etiología de la enfermedad renal crónica no influyeron en la respuesta (tabla 1).
En los controles anuales sucesivos se detectó una disminución progresiva de los niveles de anticuerpos. En el primer control anual posvacunación, un 67,8% de los pacientes mantenía niveles protectores, y a los seis años tan sólo el 17,8% de los pacientes mantenía la memoria inmunológica.
Pacientes no respondedores
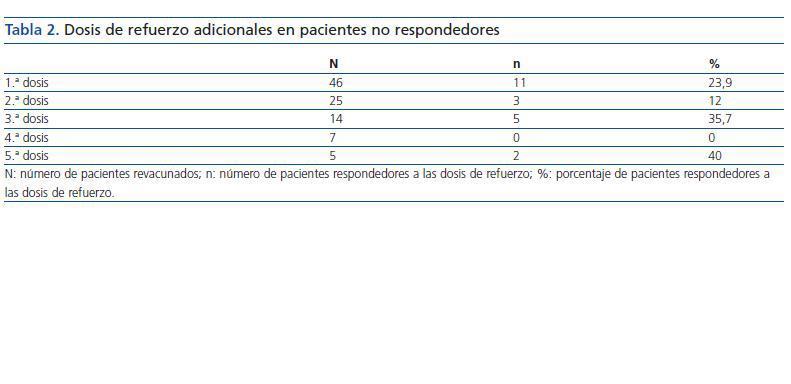
Los 62 pacientes que no respondieron a las tres dosis de vacunación inicial fueron sometidos a dosis de refuerzo adicionales, aunque sólo 46 pacientes pudieron ser evaluados al final del primer año, ya que el resto de pacientes fallecieron, fueron trasplantados o trasladados a otra unidad. La eficacia global de estas dosis fue del 21,6%: con la primera dosis, un 23,9% de los pacientes seroconvirtió; con la segunda dosis, un 12%; y con la tercera, un 37,7% (tabla 2). Un 42,8% de los pacientes que seroconvirtió presentó un nivel de anticuerpos anti-Hbs >100 UI/ml. El porcentaje de pacientes que mantuvo niveles de anticuerpos protectores tras la primera dosis de refuerzo fue del 69,2% en el primer control anual posterior.
Respuesta inmunológica y título de anticuerpos
En el subgrupo de 63 pacientes con un seguimiento de tres años, 7 pacientes fueron incluidos en el grupo I, 28 en el grupo II y 28 en el grupo III. La edad media de estos grupos fue de 55,5 (33-78), 62,8 (29-78) y 57,2 (26-75) años, respectivamente. El título de anticuerpos en el grupo II y III fue de 55 (12-98) y 290 (100-978) UI/ml, respectivamente.
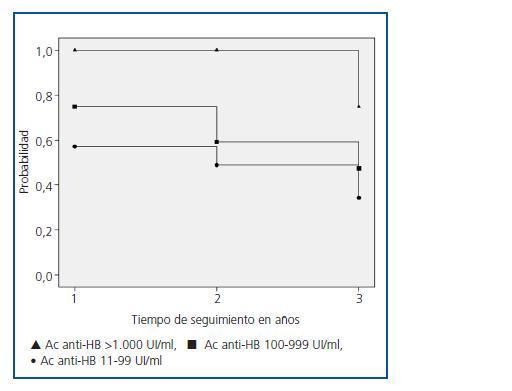
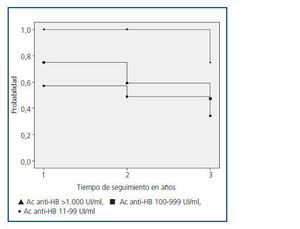
En la figura 1 se expresa la probabilidad de los pacientes de permanecer protegidos después de la vacunación. Al finalizar el seguimiento, el 75% de los pacientes del grupo I mantenía la seroprotección frente al 47% del grupo II (p = 0,08) y el 34% del grupo III (p = 0,02). Por el contrario, no se observaron diferencias significativas entre el grupo II y el grupo III.
Importancia de los controles semestrales de anticuerpos
De los 31 pacientes de los cuales se disponía de controles semestrales y anuales de anticuerpos, la determinación de los controles semestrales aportó una información adicional. En cuatro de los 25 pacientes respondedores a la vacuna, los niveles de anticuerpos ya se habían negativizado a los seis meses, por lo que estos pacientes podrían haberse beneficiado de una dosis de recuerdo más precoz. Finalmente, siete pacientes no respondedores al control anual presentaban niveles protectores de anticuerpos en los controles semestrales. Este grupo de pacientes se habría considerado como no respondedor a la vacuna si sólo se hubiera realizado un control anual.
DISCUSIÓN
En este trabajo, presentamos la experiencia de un protocolo de vacunación de la HB que finalizó en el año 2002 utilizando la pauta clásica de tres dosis dobles de vacuna. Apartir del año 2003, este protocolo se modificó en el año 2003 al finalizar el estudio, aumentando a cuatro dosis dobles de vacuna15,16, pauta que actualmente se está siguiendo en nuestra Unidad.
A pesar de la controversia existente en cuanto a efectividad de la vacuna de la HB en pacientes en HD, debido a la reducida eficacia de la vacuna y a la baja incidencia de infección por el virus de la HB, su uso se ha generalizado en esta población de pacientes17. En nuestra experiencia, el 54,4% de los pacientes vacunados desarrolla inmunidad, cifra similar a la mostrada en otros estudios8,18. Incluso en los protocolos que incluyen la administración de cuatro dosis dobles de vacuna en los meses 0, 1, 2 y 6, los resultados obtenidos de seroconversión tampoco son óptimos y oscilan entre un 58 y un 80%8,19. Esta insuficiente respuesta a la vacuna de la HB está relacionada con una deficitaria inmunocompetencia, característica de la enfermedad renal crónica avanzada4,5. También se han identificado otros factores moduladores que afectan de forma negativa esta respuesta, como la edad, la diabetes, a malnutrición, el déficit de eritropoyetina y la adecuación y la duración de la diálisis, entre otros19,20. La falta de respuesta de nuestros pacientes estuvo relacionada con la edad, de forma que el porcentaje de respondedores disminuyó con la mayor edad de los pacientes. Por el contrario, otros factores, como la presencia de diabetes, no influyeron en la respuesta de esta población.
En los pacientes que no responden a la vacunación inicial se ha recomendado la revacunación con tres dosis adicionales de vacuna, obteniéndose respuesta en un 40-50% de los pacientes8, aunque en algunos estudios ésta es muy inferior7. La utilización de la vía intradérmica ha demostrado utilidad como vía de revacunación en los pacientes no respondedores, aunque técnicamente plantea problemas en su administración12. Se ha especulado que los pacientes no respondedores a la vacunación inicial podrían haber desarrollado una inmunidad celular sin respuesta humoral, y que la revacunación sería capaz de inducir una respuesta humoral en esta población21.
La guía sobre enfermedades víricas en hemodiálisis de la S.E.N.2 recomienda la administración de una segunda pauta de vacunación en los pacientes que no hayan obtenido respuesta a la vacunación (AcHbs <10 UI/L). Si tras ello no se obtiene respuesta, se considerará definitivamente a los pacientes como no respondedores, y no existe evidencia de que los pacientes no respondedores con las dos pautas tengan una mayor tasa de respuesta posterior. Nuestros resultados demuestran que el establecimiento de un protocolo de administración de dosis de refuerzo en los pacientes sin respuesta inicial permite inmunizar a un gran número de pacientes. Así, con este protocolo, con la primera dosis se consiguió inmunizar a una cuarta parte de los pacientes no respondedores, y la administración de nuevas dosis de recuerdo consiguió nuevas inmunizaciones, incluso tras cinco dosis de refuerzo.
Una tercera parte de nuestros pacientes respondedores perdió la memoria inmunológica al primer año, resultado similar al mostrado en otros estudios8,19. El título de anticuerpos inmediatamente después de completar la vacunación es el mayor factor predictivo de mantenimiento de la inmunidad en estos pacientes19,22. Así, un 75% de los pacientes con anticuerpos >1.000 UI/ml mantenía la seroprotección a los cuatro años de la vacunación, mientras que este porcentaje fue inferior en los pacientes con títulos de anticuerpos inferiores. Un hecho llamativo en nuestro estudio fue no encontrar diferencias significativas en el mantenimiento de la memoria inmunológica entre los pacientes con títulos iniciales entre 11-99 y 100-999 UI/ml. Un título de anticuerpos de 100 UI/ml se considera como el umbral necesario para mantener una adecuada protección inmunológica en pacientes que están inmunocomprometidos13. En nuestro estudio, este título no ofreció una mayor seroprotección a largo plazo que los títulos inferiores, lo que sugiere que otros factores, independientes de la respuesta inicial a la vacunación, podrían influir en el mantenimiento o pérdida de la memoria inmunológica.
Las recomendaciones actuales en el seguimiento de los pacientes vacunados contra la HB sugieren realizar controles anuales de anticuerpos anti-HB16, aunque no hay unanimidad con relación a la frecuencia de estos controles. De hecho, existe una gran variabilidad en la periodicidad de estos controles en las diferentes unidades de diálisis23. Asimismo, debido al importante porcentaje de pacientes que pierden la memoria inmunológica y a que la pérdida de anticuerpos puede ser precoz, se ha sugerido que en estos pacientes podría ser útil la realización de controles más frecuentes, entre 6-12 meses después de la vacunación24. En nuestro estudio, el control anual de anticuerpos hace que el tiempo transcurrido entre la última dosis de vacuna y la determinación de la tasa de anticuerpos sea muy variable, y que enfermos clasificados como no respondedores, en realidad, puedan ser respondedores con baja tasa de anticuerpos y rápida desaparición de la misma. De hecho, nuestros resultados demuestran que la realización de controles semestrales podría facilitar el reconocimiento de un número importante de pacientes que podría beneficiarse de una dosis de recuerdo semestral en lugar de anual y, además, facilitaría una correcta identificación de la respuesta a la vacunación en estos pacientes no respondedores.
En resumen, en nuestra experiencia, la administración de tres dosis dobles de vacuna recombinante contra la HB consigue inmunizar a la mitad de los pacientes en HD. La edad es un factor determinante en la respuesta inicial a la vacunación. Una tercera parte de los pacientes pierde la memoria inmunológica en el primer año de seguimiento. El título de anticuerpos tras completar el protocolo de vacunación es predictor del mantenimiento de esta memoria. La administración de dosis de refuerzo consigue inmunizar a una cuarta parte de los pacientes no respondedores, y los controles semestrales pueden ser de utilidad para el mejor control y manejo de la vacunación en esta población.
Tabla 1.
Tabla 2.
Figura 1.