La enfermedad renal diabética (ERD) es la causa más común de enfermedad renal crónica (ERC) terminal, condicionando a estos pacientes a un peor pronóstico renal y mayor mortalidad cardiovascular y/o requerimiento de terapia renal sustitutiva. El uso de novedosas tecnologías de la información y la comunicación (TIC) enfocadas al ámbito de la salud puede facilitar una mejor calidad de vida y control de la enfermedad en estos pacientes. Nuestro objetivo es evaluar el efecto de monitorización de pacientes con ERD utilizando la aplicación NORA (NORA-app).
Materiales y métodosEstudio prospectivo de viabilidad/validación de la aplicación NORA-app en pacientes con ERD en estadio G3bA3 o superior, seguidos en consultas externas de un hospital de atención terciaria. NORA-app es una aplicación para teléfonos inteligentes diseñada para controlar los factores de riesgo, compartir información médica educativa, comunicarse vía chat con profesionales de la salud, aumentar el cumplimiento del tratamiento (Morisky-Green), así como evaluación de ansiedad y depresión utilizando la Escala Hospitalaria de Ansiedad y Depresión (HAD). Las variables clínico-analíticas se recogieron al inicio y a los tres meses, comparándose con los pacientes que desistieron del uso de NORA-app (grupo control).
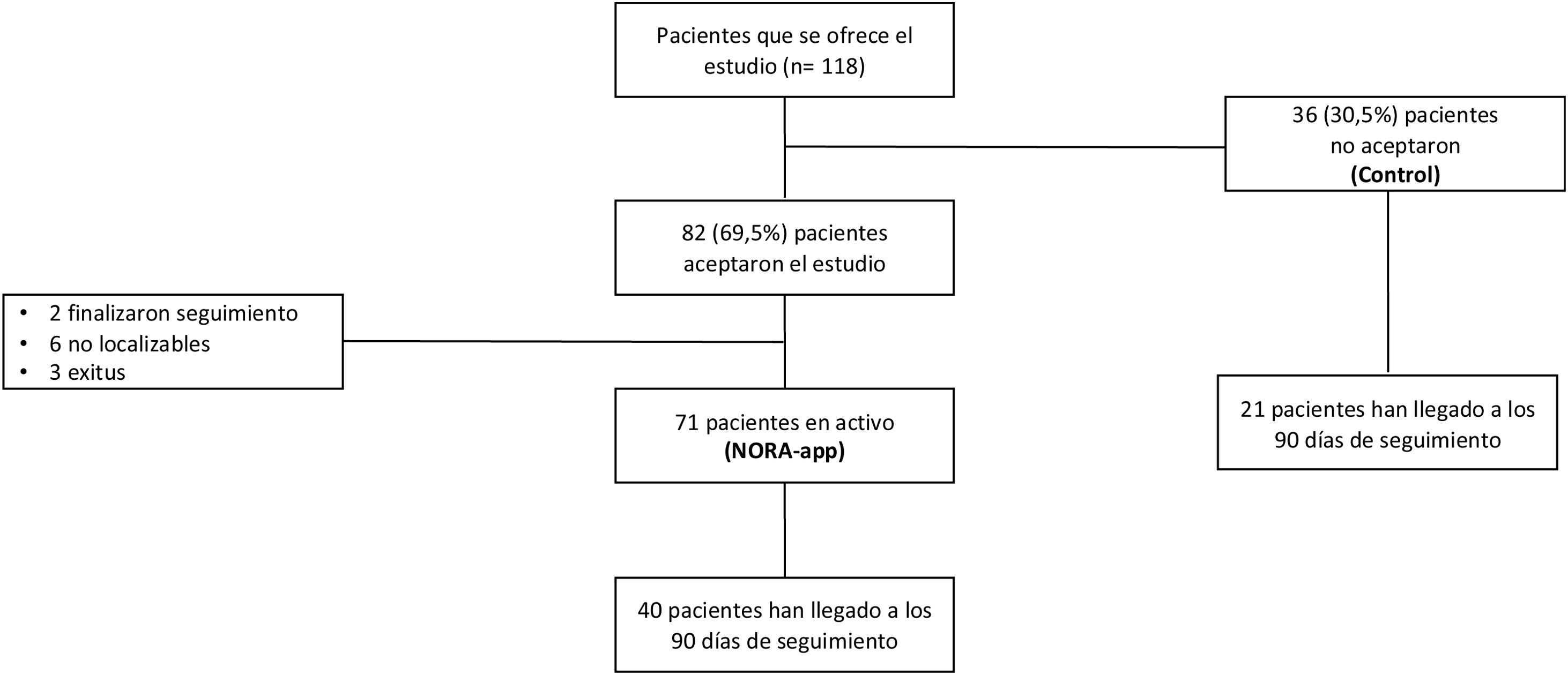
ResultadosDesde el 1 de enero de 2021 al 3 de marzo de 2022 se ofreció el uso de NORA-app a 118 pacientes, 82 aceptaron y 36 rechazaron (controles). Después de un periodo medio de seguimiento de 6,04 meses, 71 (86,6%) pacientes de NORA-app siguen siendo usuarios activos, dos han completado el seguimiento al año y nueve están inactivos (tres por fallecimiento y seis por no localizables). No hubo diferencias en las características basales, incluida la creatinina (2,1 [1,6-2,4] vs. 1,9 [1,5-2,5]) mg/dL y la alb/creat (962 [475-1.784] vs. 1.036 [560-2.183]) mg/g entre los pacientes NORA-app y grupo control, respectivamente. La tasa de cumplimiento terapéutico en el grupo NORA-app fue de 77%, mejorando a los 90 días a 91%. Los pacientes del grupo de NORA-app mostraron niveles significativamente más bajos de alb/creat que los controles (768 [411-1.971] mg/g vs. 2.039 [974-3.214]; p = 0,047) a los 90 días de seguimiento.
ConclusionesEn pacientes con ERD que mantuvieron el uso de NORA-app a largo plazo, llevó a presentar altos niveles de cumplimiento del tratamiento, logrando un mejor control de la enfermedad. Nuestro estudio sugiere que el uso generalizado de las TIC puede ayudar en el seguimiento personalizado de estos pacientes para retrasar la progresión de la enfermedad renal.
Diabetic kidney disease (DKD) is the most common cause of end-stage chronic kidney disease (CKD), conditioning these patients to a worse renal prognosis and higher cardiovascular mortality and/or requirement for renal replacement therapy. The use of novel information and communication technologies (ICTs) focused on the field of health, may facilitates a better quality of life and disease control in these patients. Our objective is to evaluate the effect of monitoring DKD patients using NORA-app.
Material and methodsProspective feasibility/validation study of NORA-app in patients with DKD stage G3bA3 or higher, followed in outpatient clinics of a tertiary care hospital. NORA-app is an application for smartphones designed to control risk factors, share educational medical information, communicate via chat with health professionals, increase treatment compliance (Morisky-Green), and collect patient reported outcomes such as anxiety and depression using HADs scale. Clinical-laboratory variables were collected at 3 months and compared to control patients who declined using NORA-app.
ResultsFrom 01/01/2021 to 03/03/2022 the use of NORA-app was offered to 118 patients, 82 accepted and 36 declined (controls). After a mean follow-up period of 6.04 months and at the time of data extraction 71 (86.6%) NORA-app patients remain active users, 2 have completed the follow-up at one year and 9 are inactive (3 due to death and 6 due to non-locatable). There were no differences in baseline characteristics including creatinine [2.1 (1.6–2.4) vs. 1.9 (1.5–2.5)] mg/dL and alb/creat [962 (475–1784) vs. 1036 (560–2183)] mg/g between Nora and control patients, respectively. The therapeutic compliance rate in the NORA-app group was 77%, improving at 90 days to 91%. Patients in the NORA-group showed significantly lower levels of alb/creat than controls (768 (411–1971) mg/g vs. 2039 (974–3214), p = 0.047) at 90-day follow-up.
ConclusionsIn patients with DKD the use of NORA-app was maintained in the long-term, leading to high levels of treatment compliance, and achieving a better disease control. Our study suggests that the generalized use of ICTs may help in the personalized monitoring of these patients to delay the progression of kidney disease.
La prevalencia de la enfermedad renal crónica (ERC) está aumentando de forma considerable en todo el mundo1, convirtiéndose en una de las patologías de mayor crecimiento como causa de muerte2,3. La ERC está asociada a un mayor riesgo de morbilidad cardiovascular, mortalidad prematura y disminución en la calidad de vida relacionada con la salud4. La principal causa de ERC es la enfermedad renal diabética (ERD), condicionando a estos pacientes a un peor pronóstico renal y mayor mortalidad cardiovascular5–7. Además, se ha observado un aumento sustancial en el número de personas con ERC en fase terminal (estadio 5) con requerimiento de terapia renal sustitutiva como la diálisis o el trasplante, por lo que actualmente el manejo de la ERC representa un gran desafío para los gobiernos y finanzas sanitarias8.
La prevención y el control de factores de riesgos cardiovasculares son esenciales en el manejo de la ERC. Durante los últimos años, se han realizado estudios de seguimiento sobre el control de factores de riesgo cardiovasculares según indican las guías KDIGO5, con el fin de modificar el estilo de vida y crear hábitos saludables, que disminuyan el riesgo de la progresión de la enfermedad renal. En este sentido, el estudio LOOK-AHEAD estudió el efecto de una pauta de modificación intensiva de los hábitos de vida dirigida a la reducción de peso en pacientes diabéticos con sobrepeso, en comparación con pacientes que siguieron el tratamiento estándar, los pacientes asignados al programa de seguimiento intensivo presentaron mayor reducción de peso, mejores registros de hemoglobina glicosilada y mejor control de diversos factores de riesgo cardiovascular, así como una reducción significativa de la alb/creat, además, destaca la importancia de los resultados conseguidos con la monitorización activa reduciendo la carga del riesgo vascular asociado a diabetes y considerando estas alternativas terapéuticas claves en el manejo del paciente diabético9. Adicionalmente, los clásicos estudios del grupo STENO han demostrado que un tratamiento intensivo de los factores de riesgo cardiovascular (HTA, tabaquismo, hemoglobina glicosilada...) enlentecen la progresión de la enfermedad renal crónica10. Actualmente se han desarrollado estrategias encaminadas a mejorar el cumplimiento terapéutico y modificación saludable del estilo de vida de los pacientes crónicos, ya que de poco sirve el diseño y desarrollo de nuevos fármacos encaminados a mejorar el control de la enfermedad si por otra parte existe un incumplimiento sistemático de las pautas y consejos médicos.
Existen estudios que han demostrado un incremento en el control de factores de riesgo cardiovascular específicos (obesidad, diabetes, hipertensión arterial), gracias a las tecnologías de la información y la comunicación (TIC), es decir la telemedicina11. En este sentido, la Unidad de Ictus del Hospital Universitario Vall d’Hebron ha desarrollado una aplicación para teléfonos inteligentes llamada NORA-app (antes conocida como Farmalarm), que permite el control del tratamiento médico mediante alarmas de medicación, registro del perfil biométrico (peso, talla) y control de factores de riesgo cardiovascular (registro de la presión arterial, niveles de glucosa capilar, saturación de oxígeno, peso y pasos diarios). Además, permite el envío de material de educación sanitaria, encuestas (adherencia al tratamiento, ansiedad/depresión, estado de salud), calendario de visitas, generación de informes, módulo de preguntas frecuentes, comunicación bidireccional mediante chat y videollamada e información de contacto de la unidad. NORA-app ha sido validada durante los últimos cinco años por la Unidad de Ictus del Hospital Universitario Vall d’Hebron, demostrando mejorar el control de los factores de riesgo cardiovascular en los pacientes que habían sufrido un ictus, aumentando el grado de conocimiento sobre la enfermedad12. Nuestro objetivo es adaptar y evaluar el efecto de la monitorización en pacientes con ERD utilizando NORA-app, enfocándose en el control de factores de riesgo de progresión de la enfermedad renal considerada como evento renal compuesto (MARE)13.
Material y métodosSe realiza un estudio prospectivo de viabilidad y validación de la aplicación NORA-app en pacientes mayores de 18 años con ERD en estadio G3bA3 o superior (FGe CKD-EPI<45 mL/min/m2 y alb/creat > 300 mg/g), seguidos en consultas externas de un hospital de tercer nivel y que dispongan de un dispositivo móvil (participante o familiar) que permita el uso de aplicaciones como WhatsApp. Se excluyeron aquellos pacientes con ERD estadio G3bA2 o menor, así como a pacientes en estadio G5 (FGe < 15 mL/min/m2) con previsión de requerimiento temprano (menos de un año) de terapia renal sustitutiva. Los pacientes con alteración cognitiva moderada-severa, patología psiquiátrica, barrera idiomática, déficits sensoriales severos (hipoacusia/falta de visión) y/o incapacidad para colaborar en el estudio (en caso de ser necesario, no tener soporte social/familiar) también fueron excluidos.
Entre las variables exploratorias del estudio incluyen las demográficas, comorbilidades, analíticas de laboratorio (determinación cada tres meses de creatinina sérica, filtrado glomerular estimado [CKD-EPI], alb/creat, hemoglobina glicosilada, hemoglobina, ferritina, índice de saturación de transferrina [IST], sodio, potasio, calcio, fósforo, hormona paratiroidea [PTH], calcidiol, colesterol total, colesterol HDL y LDL], y escalas como la de adherencia al tratamiento (Morisky-Green)14, signos y síntomas, depresión y ansiedad (HAD)15, estado de salud (PROMIS)16. Las escalas para evaluar el estado del paciente se envían en diferentes periodos: basal a los siete días, 90 días y al año de seguimiento.
La escala de Morisky-Green evalúa la adherencia al tratamiento farmacológico mediante cuatro ítems que preguntan sobre cómo el paciente cumple con las tomas de medicación pautada por el médico (anexo 1). Se considera alterada cuando una o más de las de las respuestas es positiva, indicando un mal cumplimiento por parte del paciente en la toma de la medicación14. La escala de signos y síntomas hace referencia a la presencia de nauseas/vómitos, edemas y dificultad respiratoria (anexo 2). La escala Hospitalaria de Ansiedad y Depresión (HAD) está compuesta por 14 ítems que se dividen en dos grupos HAD-ansiedad y HAD-depresión (Anexo 3). Los resultados obtenidos como números absolutos tienen un rango de 0 a 21, considerándose los mayores resultados como resultados desfavorables. Del 0 al 7 indica el límite de normalidad, de 7 a 10 «anormal» y mayor a 10 se determina como alterado en ansiedad y depresión15. El estado de salud es autoevaluado mediante la escala Patient-Reported Outcomes Measurement Information System 10 (PROMIS-10), que valora el estado de salud general a partir de 10 ítems (anexo 4): salud física, dolor, fatiga, estado emocional, relaciones sociales, percepción general del estado de salud. Los resultados obtenidos se agrupan en dos subgrupos «salud física» y «salud mental», y considerando números absolutos el rango es de cuatro como mínimo, resultado posible obtener 20 como máximo resultado. Por tanto, cuanto mayor sea el resultado, mejor percepción de su estado de salud tendrá la persona16. Este estudio fue aprobado por el Comité de Ética de Investigación con medicamentos y comisión de proyectos de investigación del Hospital Universitario Vall d’Hebron (PR(AG)608/2021).
ResultadosDesde el 1 de enero de 2021 al 3 de marzo de 2022 se ofreció el uso de NORA-app a 118 pacientes, de los cuales 82 aceptaron el estudio (NORA) y 36 no participaron (control) en el estudio, ya que se encontraban en ensayos clínicos (20 pacientes) o por no disponer de teléfono móvil inteligente (16 pacientes). Después de un periodo medio de seguimiento de 6,04 meses, 71 (86,6%) pacientes siguen siendo usuarios activos (27 a través de cuidador); dos pacientes han completado el seguimiento al año y nueve están inactivos, (tres por fallecimiento y seis por no localizables) (fig. 1).
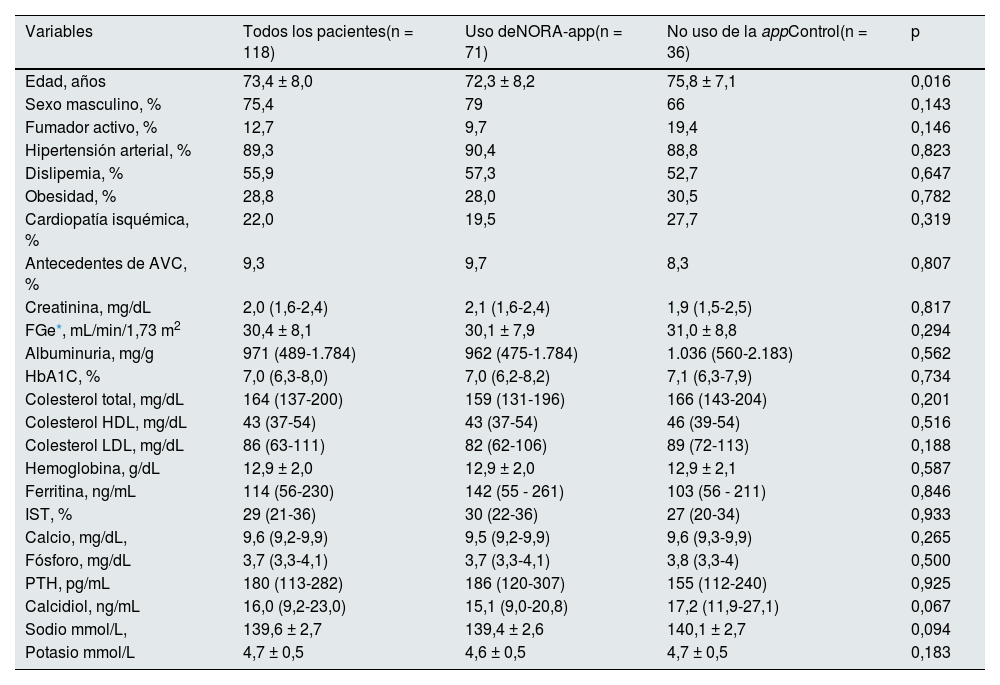
Las variables demográficas y de laboratorio basales se recogen en la tabla 1. La edad media de todos los pacientes fue de 73,4±8 años, en su mayoría de sexo masculino (75,4%), la creatinina sérica fue de 2,0 (1,6-2,4) mg/dL, con FGe 30,4±8,1 mL/min/1,73m2 (CKD-EPI), la alb/creat fue de 971 (489-1.784) mg/g y los niveles de hemoglobina glicosilada fueron de 7,0 (6,3-8,0) %. La edad media de los pacientes del grupo NORA-app fue de 72,3±8,2 años vs. 75,8±7,1 años del grupo control, siendo estadísticamente significativo (p = 0,016). No hubo diferencias significativas entre ambos grupos en cuanto a las comorbilidades ni en los valores analíticos basales, incluida la creatinina sérica (2,1 [1,6-2,4] vs. 1,9 [1,5-2,5]) mg/dL y la alb/creat (962 [475-1.784] vs. 1.036 [560-2.183]) mg/g.
Características clínicas y analíticas basales
| Variables | Todos los pacientes(n = 118) | Uso deNORA-app(n = 71) | No uso de la appControl(n = 36) | p |
|---|---|---|---|---|
| Edad, años | 73,4 ± 8,0 | 72,3 ± 8,2 | 75,8 ± 7,1 | 0,016 |
| Sexo masculino, % | 75,4 | 79 | 66 | 0,143 |
| Fumador activo, % | 12,7 | 9,7 | 19,4 | 0,146 |
| Hipertensión arterial, % | 89,3 | 90,4 | 88,8 | 0,823 |
| Dislipemia, % | 55,9 | 57,3 | 52,7 | 0,647 |
| Obesidad, % | 28,8 | 28,0 | 30,5 | 0,782 |
| Cardiopatía isquémica, % | 22,0 | 19,5 | 27,7 | 0,319 |
| Antecedentes de AVC, % | 9,3 | 9,7 | 8,3 | 0,807 |
| Creatinina, mg/dL | 2,0 (1,6-2,4) | 2,1 (1,6-2,4) | 1,9 (1,5-2,5) | 0,817 |
| FGe*, mL/min/1,73 m2 | 30,4 ± 8,1 | 30,1 ± 7,9 | 31,0 ± 8,8 | 0,294 |
| Albuminuria, mg/g | 971 (489-1.784) | 962 (475-1.784) | 1.036 (560-2.183) | 0,562 |
| HbA1C, % | 7,0 (6,3-8,0) | 7,0 (6,2-8,2) | 7,1 (6,3-7,9) | 0,734 |
| Colesterol total, mg/dL | 164 (137-200) | 159 (131-196) | 166 (143-204) | 0,201 |
| Colesterol HDL, mg/dL | 43 (37-54) | 43 (37-54) | 46 (39-54) | 0,516 |
| Colesterol LDL, mg/dL | 86 (63-111) | 82 (62-106) | 89 (72-113) | 0,188 |
| Hemoglobina, g/dL | 12,9 ± 2,0 | 12,9 ± 2,0 | 12,9 ± 2,1 | 0,587 |
| Ferritina, ng/mL | 114 (56-230) | 142 (55 - 261) | 103 (56 - 211) | 0,846 |
| IST, % | 29 (21-36) | 30 (22-36) | 27 (20-34) | 0,933 |
| Calcio, mg/dL, | 9,6 (9,2-9,9) | 9,5 (9,2-9,9) | 9,6 (9,3-9,9) | 0,265 |
| Fósforo, mg/dL | 3,7 (3,3-4,1) | 3,7 (3,3-4,1) | 3,8 (3,3-4) | 0,500 |
| PTH, pg/mL | 180 (113-282) | 186 (120-307) | 155 (112-240) | 0,925 |
| Calcidiol, ng/mL | 16,0 (9,2-23,0) | 15,1 (9,0-20,8) | 17,2 (11,9-27,1) | 0,067 |
| Sodio mmol/L, | 139,6 ± 2,7 | 139,4 ± 2,6 | 140,1 ± 2,7 | 0,094 |
| Potasio mmol/L | 4,7 ± 0,5 | 4,6 ± 0,5 | 4,7 ± 0,5 | 0,183 |
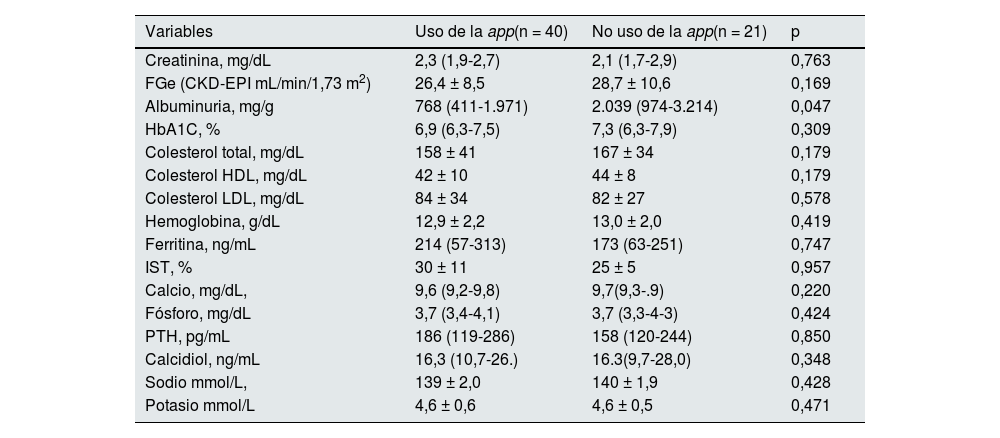
Del grupo de NORA-app, 40 pacientes han llegado a los 90 días de seguimiento, mientras que del grupo control fueron 21. Los pacientes del grupo de NORA-app mostraron niveles significativamente más bajos de alb/creat que los controles (768 [411-1.971] mg/g vs. 2.039 [974-3.214]; p = 0,047). La creatinina sérica fue de 2,3 (1,9-2,7) mg/dL en el grupo NORA-app vs. 2,1 (1,7-2,9) mg/dL en el grupo control, no siendo estadísticamente significativo (p = 0,763). El FGe fue de 26,4±8,5 mL/min/1,73 m2 (CKD-EPI), en el grupo NORA-app vs. 28,7±10,6 mL/min/1,73 m2 (CKD-EPI), en el grupo control, no siendo estadísticamente significativo (p = 0,169). Los niveles de colesterol total fueron de 158±41 mg/dL en el grupo NORA-app vs. 167±34 mg/dL en el grupo control no siendo estadísticamente significativo (p = 0,179) (tabla 2).
Variables analíticas a los 90 días de seguimiento
| Variables | Uso de la app(n = 40) | No uso de la app(n = 21) | p |
|---|---|---|---|
| Creatinina, mg/dL | 2,3 (1,9-2,7) | 2,1 (1,7-2,9) | 0,763 |
| FGe (CKD-EPI mL/min/1,73 m2) | 26,4 ± 8,5 | 28,7 ± 10,6 | 0,169 |
| Albuminuria, mg/g | 768 (411-1.971) | 2.039 (974-3.214) | 0,047 |
| HbA1C, % | 6,9 (6,3-7,5) | 7,3 (6,3-7,9) | 0,309 |
| Colesterol total, mg/dL | 158 ± 41 | 167 ± 34 | 0,179 |
| Colesterol HDL, mg/dL | 42 ± 10 | 44 ± 8 | 0,179 |
| Colesterol LDL, mg/dL | 84 ± 34 | 82 ± 27 | 0,578 |
| Hemoglobina, g/dL | 12,9 ± 2,2 | 13,0 ± 2,0 | 0,419 |
| Ferritina, ng/mL | 214 (57-313) | 173 (63-251) | 0,747 |
| IST, % | 30 ± 11 | 25 ± 5 | 0,957 |
| Calcio, mg/dL, | 9,6 (9,2-9,8) | 9,7(9,3-.9) | 0,220 |
| Fósforo, mg/dL | 3,7 (3,4-4,1) | 3,7 (3,3-4-3) | 0,424 |
| PTH, pg/mL | 186 (119-286) | 158 (120-244) | 0,850 |
| Calcidiol, ng/mL | 16,3 (10,7-26.) | 16.3(9,7-28,0) | 0,348 |
| Sodio mmol/L, | 139 ± 2,0 | 140 ± 1,9 | 0,428 |
| Potasio mmol/L | 4,6 ± 0,6 | 4,6 ± 0,5 | 0,471 |
FGe: filtrado glomerular estimado; CKD-EPI: Chronic Kidney Disease Epidemiology collaboration; HbA1C: hemoglobina glicosilada A1C; IST: índice de saturación de transferrina; PTH: hormona paratiroidea.
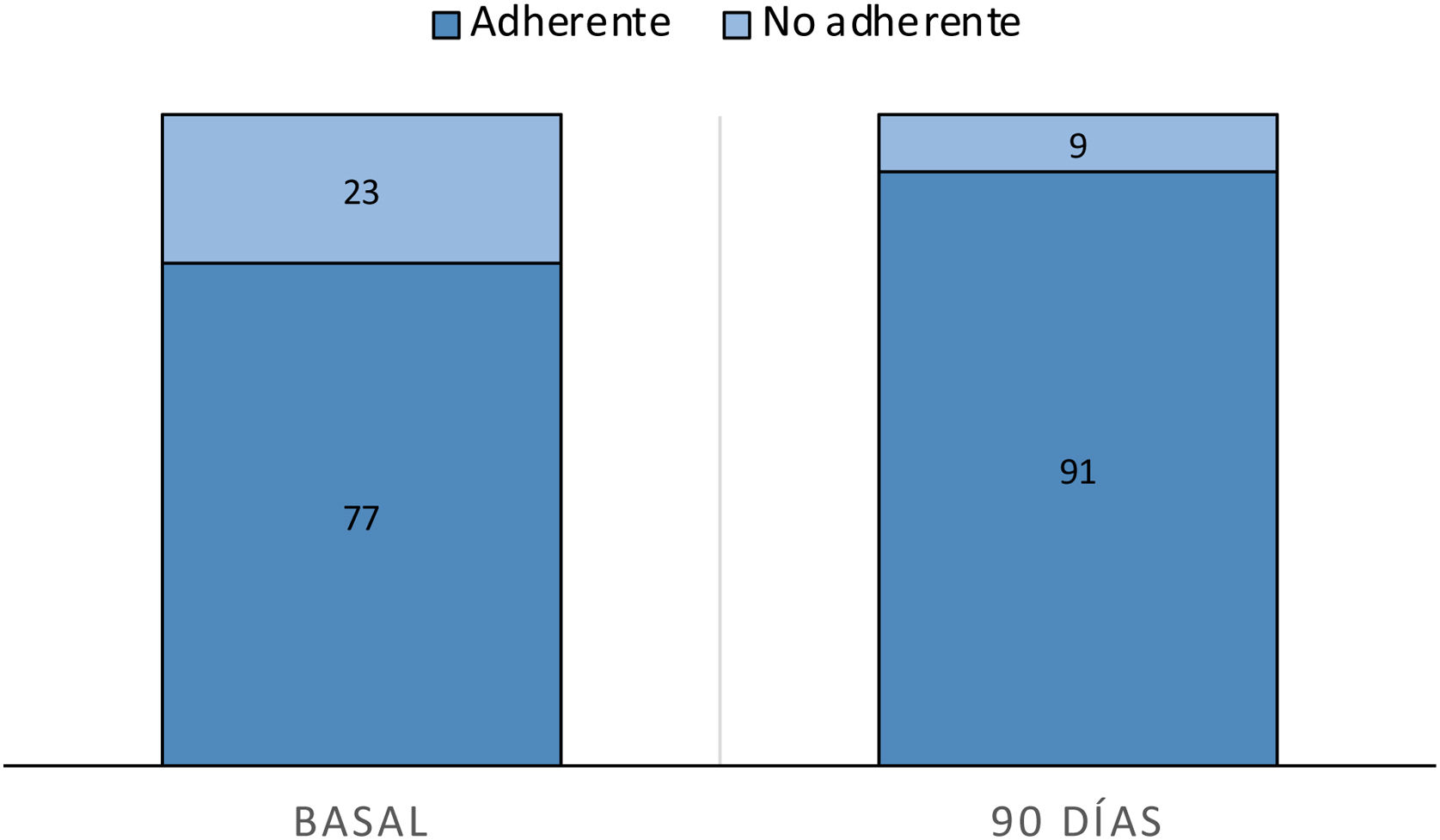
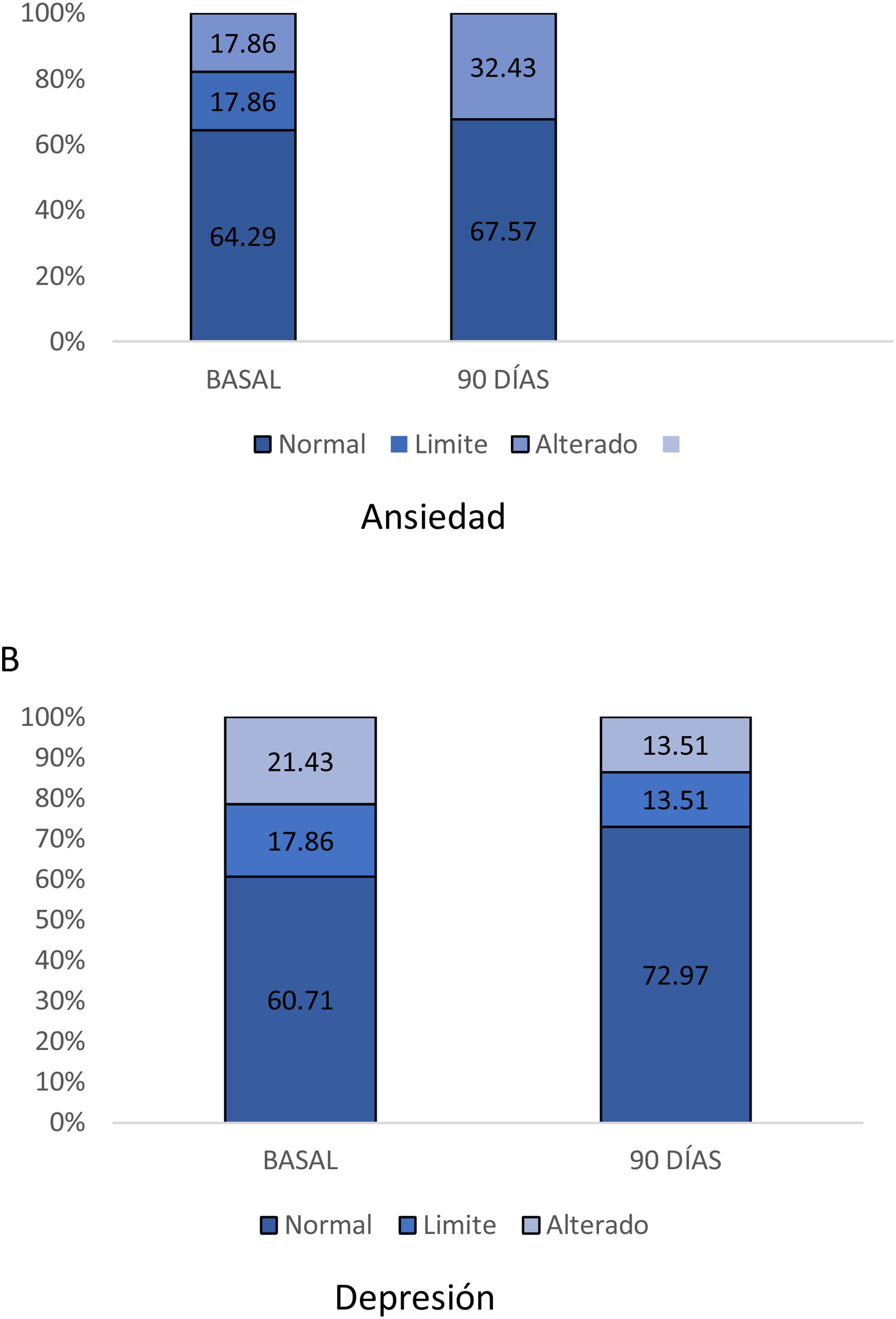
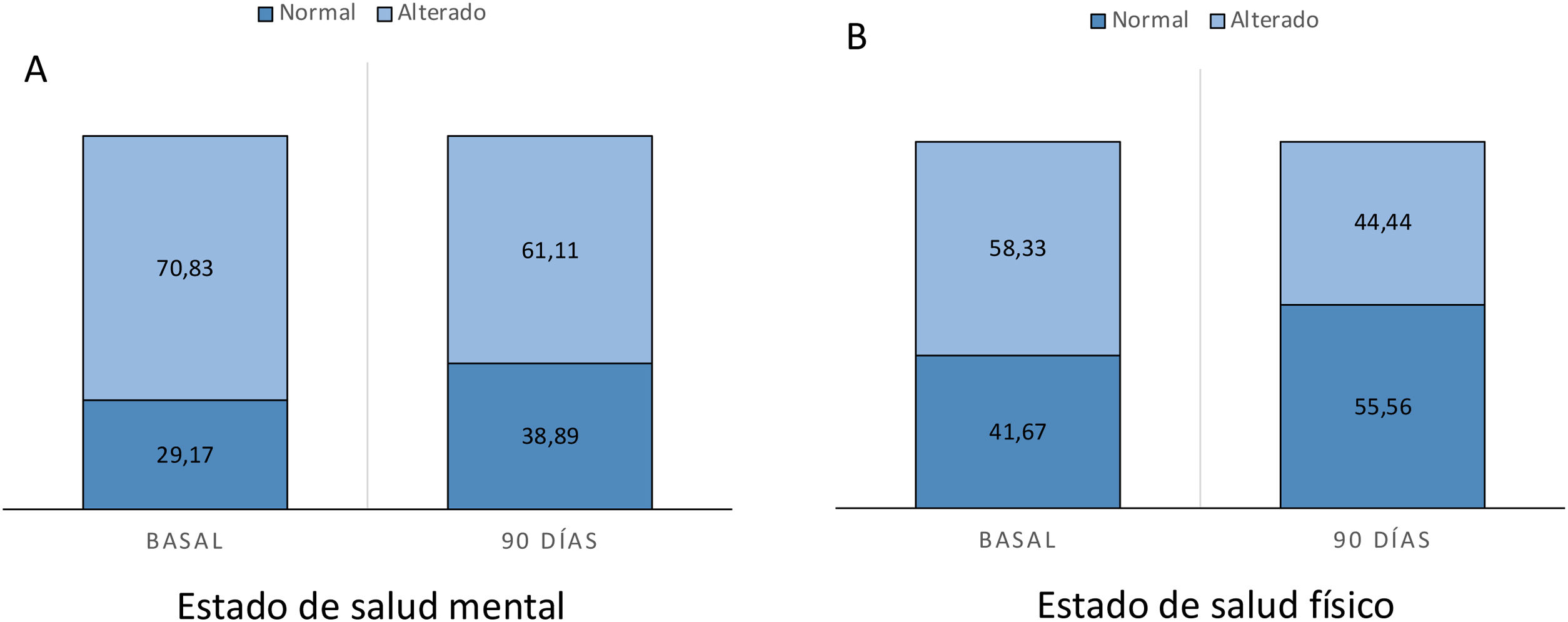
La tasa de cumplimiento óptimo del tratamiento medido mediante la escala de Morisky-Green fue de 77% al inicio del estudio y de 91% a los 90 días (fig. 2). La ansiedad medida mediante la escala HAD fue de 35,7% (límite 17,9%, alterado 17,9%) al inicio del estudio y de 32,43% a los 90 días, mientras que la depresión fue 39,29% (límite 17,86%, alterado 21,43%) al inicio del estudio y de 27,02% (límite 13,51%, alterado 13,51%) a los 90 días (fig. 3). Según la escala de estado de salud (PROMIS), la salud mental alterada al inicio del estudio fue de 70,83% y de 61,11% a los 90 días, mientras que la salud física alterada fue de 58,33% al inicio del estudio y de 44,44% a los 90 días (fig. 4).
DiscusiónNuestro estudio realizado por primera vez en pacientes con enfermedad renal avanzada y diabetes demuestra que el uso de una aplicación para teléfonos móviles que aporta información y manejo de factores de riesgo cardiovascular brinda un mejor control y concienciación de la enfermedad, ya que la tasa de adherencia al tratamiento mejor de 77 a 91% en los primeros 90 días de seguimiento. En el mismo sentido en otra patología como el ictus, Requena et al. demostraron que el uso de NORA-app mejoró la concienciación y la «compliance» del paciente (86 vs. 69,2%, p < 0,01), junto con un mejor control de los factores de riesgo cardiovascular a los 90 días de seguimiento12.
Para alcanzar el máximo potencial de las terapias de las que disponemos actualmente, es preciso garantizar un buen cumplimiento y concienciación por parte de nuestros pacientes de modo que se impliquen de forma activa en el control de su enfermedad, proceso conocido actualmente como alfabetización en salud17–19. Este cumplimiento terapéutico es especialmente importante en el caso de las enfermedades cardiovasculares en las que las tasas de recurrencia son altas20. Una plataforma digital que incentive el cumplimiento puede ofrecer un valor añadido a las pautas de tratamiento utilizadas habitualmente.
Hay que destacar que, a pesar de la edad avanzada de los pacientes con ERC, el uso de los dispositivos móviles se está generalizando entre personas en la sexta o séptima décadas de la vida. Actualmente no es infrecuente ver a nuestros pacientes con estos dispositivos y en los próximos años va a ser cada vez más habitual. Una revisión sistemática realizada en el 2019 demostró que la telemedicina fue aceptablemente utilizada por adultos mayores21, y si realizan un entrenamiento adecuado presentan mejorías significativas en su capacidad para realizar tareas en su unidad de telemedicina22. En nuestro estudio, los pacientes del grupo NORA-app tenían una media de edad de 72,3±8,2 años, de los cuales 44 tienen uso individual de la app, mientras que 27 es a través de cuidador, demostrando un fácil manejo con la app gracias a la interacción entre paciente y el profesional sanitario.
Es conocido clásicamente que la alb/creat es un biomarcador de progresión de enfermedad renal23, además es un factor de riesgo independiente de enfermedad cardiovascular, por lo que una mayor tasa de excreción de albumina urinaria se asocia con una mayor incidencia de morbilidad, mortalidad cardiovascular y progresión de la enfermedad renal24–26, por lo que su control es fundamental para retrasar la progresión de la enfermedad renal. Actualmente hay varias opciones farmacológicas encaminadas a controlar la alb/creat27–29, sin embargo, el uso de telemedicina podría ayudar al control mediante modificación saludable del estilo de vida de los pacientes con ERD. Katz et al. realizaron un programa de seguimiento virtual de pacientes con ERC con FGe < 30 ml/min/m2 y alb/creat > 30 mg/g y seguidos durante un año, informándose del adecuado seguimiento de los pacientes con seguridad y eficiencia30. En nuestro estudio, en pacientes afectos de diabetes y ERC, los pacientes que usaron la app-NORA presentaron significativamente niveles más bajos de alb/creat al seguimiento en relación con el grupo control, siendo estadísticamente significativo, favoreciendo de este modo a retrasar la progresión de la enfermedad, mientras que en las demás variables analíticas como el colesterol total, hemoglobina glicosilada presentaron una tendencia a ser menor que en el grupo control.
En cuanto a la evaluación de ansiedad y depresión, estudios han demostrado que la ERC tiene un alto riesgo de presentar enfermedades mentales, siendo más frecuente en pacientes en terapia renal sustitutiva31, además se ha demostrado que la mayor inflamación y el estrés oxidativo presentes en pacientes con ERC lleva a desarrollar cuadros de depresión32. Estudios han demostrado que las intervenciones digitales de salud mental pueden ser efectivas para mejorar la depresión, la ansiedad y el bienestar psicológico33, en nuestro estudio piloto los pacientes del grupo NORA-app presentaron una tendencia a mejorar la ansiedad y depresión durante los primeros 90 días de seguimiento. Narayanan et al. evaluaron una plataforma integrada de telemedicina para evaluar el estado de salud mediante escalas (PROMIS-10), en pacientes con patología oncológica demostrando la viabilidad y satisfacción por parte de los pacientes, presentando menor carga de signos y síntomas y mayor preocupación sobre el estilo de vida34, en este sentido nuestro trabajo demostró mejor estado de salud mental y físico en los primeros 90 días de seguimiento.
El uso de la telemedicina ha aumentado a lo largo de la última década para facilitar la comunicación entre el profesional de la salud y el paciente, brindando una atención médica a distancia que pretende dar respuesta a las necesidades reportadas por el paciente y promover una atención coordinada entre los diferentes servicios de la salud a través de la monitorización remota35,36. Las TIC parecen unas herramientas muy útiles en una sociedad cada vez más habituada al uso de las nuevas tecnologías y que permiten ofrecer servicios sanitarios a personas con limitación a nivel geográfico o dificultades a nivel logístico para desplazarse con facilidad al centro sanitario11,37,38. Además, en la época de pandemia por COVID-19 en la que nos hemos encontrado, se ha priorizado la implementación del seguimiento de forma telemática en pacientes con ERC para evitar acudir al hospital y visitas consiguientes con la finalidad de disminuir el riesgo de infección por COVID-19. Es de interés mencionar que la ERC terminal se ha identificado como uno de los primeros factores de riesgo de mortalidad secundaria a COVID-1938–42.
Nuestro estudio es uno de los pocos que ha evaluado la telemedicina en la progresión de la enfermedad renal diabética, demostrando a los primeros 90 días de seguimiento resultados esperanzadores para el control de la enfermedad, mejorando la alfabetización en salud. Por otro lado, entre las limitaciones más importantes de nuestro estudio se encuentra el número de pacientes incluidos, así como la falta de información respecto al nivel sociocultural y económico, ya que podrían influenciar en nuestros resultados. Además, al ser un estudio piloto no se dispone de datos como presión arterial, peso, etc. en el grupo control para realizar un análisis más detallado entre ambos grupos. Estudios randomizados en dicho grupo de personas afectas de diabetes mellitus y ERC podrían ser de gran utilidad en un futuro próximo.
ConclusionesEn pacientes con ERD que mantuvieron el uso de NORA-app en los primeros 90 días, llevó a presentar altos niveles de cumplimiento del tratamiento, logrando un mejor control de la enfermedad. El uso generalizado de las TIC puede ayudar en el seguimiento personalizado de estos pacientes, con la finalidad retrasar la progresión de la enfermedad renal, mejoría de calidad de vida y reducción del gasto sanitario.
FinanciaciónEl presente trabajo ha sido realizado gracias a una concesión de la beca: «Ayudas Fundación Senefro a la investigación en Nefrología», 2021 de la Sociedad Española de Nefrología.
Conflictos de interésM.J.S. informa honorarios por conferencias, consultoría desde AstraZeneca, Novo Nordisk, Esteve, Vifor, Bayer, Mundipharma, Ingelheim Lilly, Jansen, ICU Medical y Boehringer.
Los demás autores declaran no tener conflictos de interés
A los pacientes con enfermedad renal crónica y su implicación con las nuevas tecnologías disponibles.