El estudio PIBHE, promovido por la Asociación Española de Hígado y Riñón y el Grupo de Virus en Diálisis de la Sociedad Española de Nefrología, es el primer estudio que determina la situación de los pacientes en hemodiálisis con infección crónica por el VHB y la inmunización frente a la vacuna.
MétodoEstudio nacional multicéntrico, observacional, de corte transversal, entre enero de 2013 y de 2014. Se envió un cuaderno de recogida de datos a todos los servicios de nefrología y unidades extrahospitalarias de hemodiálisis de España, para que lo cumplimentaran a partir de la historia clínica del paciente, tras consentimiento informado. Los datos se incluyeron en una base central.
ResultadosParticiparon 215 centros (15.645 pacientes), con una prevalencia del VHB del 1,03%. El 7,2% de los pacientes VHB(+) estaba coinfectado por el VHC o VIH. La carga viral era inferior a 2.000 UI/ml en el 80%. Los niveles de GOT y GPT fueron de 19,1±10,1 y 15,9±9,6 UI/ml, respectivamente. La biopsia hepática se había realizado en el 7,1%. El 30% había recibido tratamiento antiviral, que se había suspendido en el 12,5%. El más empleado había sido entecavir (13,3%), seguido de lamivudina (10%), adefovir y tenofovir (6,7%) e interferón (3,3%). El 34,5% era candidato a trasplante renal y el 6,9% no había sido evaluado. Se encontraban en seguimiento por un digestólogo el 64,3%. No había sido vacunado el 27,2% de los pacientes VHB(⿿) sin inmunización. Se emplearon 14 pautas distintas de vacunación, con un 58,8% de inmunización. La media de anti-HBs se situaba en 165,7±297,8mUI/ml. El 72,7% de los pacientes había recibido un ciclo de vacunación; el 26,4%, 2 ciclos; el 1,0%, 3 ciclos y el 11,6%, una dosis de recuerdo. El 28,3% tuvo una respuesta pobre (anti-HBs 10-99mUI/ml); el 22,4%, una respuesta óptima (anti-HBs 100-999mUI/ml); y el 7,9%, una respuesta excelente (anti-HBs1.000mUI/ml). La edad se asoció significativamente con la respuesta a la vacunación, de manera que los pacientes que no respondieron tenían una edad media significativamente mayor que los pacientes que obtuvieron cualquier tipo de respuesta (p<0,05). La mayor probabilidad de conseguir una respuesta inmunitaria se alcanzaba con 4 dosis de 40mcg de vacuna adyuvada (OR: 7,3; IC 95%: 3,4-15,7), a igualdad de edad y número de revacunaciones y recuerdos. La edad, la vacuna adyuvada, la dosis y el esquema de vacunación influían en la respuesta inmunitaria y en el título de anti-HBs alcanzado (p<0,05).
ConclusiónLa prevalencia de la infección crónica por el VHB en hemodiálisis en España es baja, así como las tasas de inmunización frente a este virus. Los esquemas de vacunación empleados son muy diversos y se han correlacionado con la respuesta inmunitaria, por lo que sería necesario protocolizar la pauta más eficaz para aumentar la inmunización en estos pacientes.
The PIBHE study, promoted by the Spanish Liver and Kidney Association and the Dialysis Virus Group of the Spanish Society of Nephrology, is the first study to determine the status of haemodialysis patients with chronic HBV infection and the immunisation against the vaccine.
MethodThe study has a national multicentre, observational, cross-sectional design and was carried out between January 2013 and 2014. A data collection folder was sent to all the nephrology departments and outpatient haemodialysis units in Spain, to be completed based on patient medical files after informed consent. The data were recorded in a central database.
ResultsA total of 215 centres participated (15,645 patients), with an HBV prevalence of 1.03%. HCV or HIV was present in 7.2% of the HBV(+) patients. Viral load was below 2,000 IU/ml in 80%. GOT and GPT levels were 19.1±10.1 and 15.9±9.6 IU/ml, respectively. Liver biopsy was performed in 7.1%. Antiviral treatment was prescribed in 30% and suspended in 12.5%: entecavir (13.3%), lamivudine (10%), adefovir and tenofovir (6.7%), and interferon (3.3%). A total of 34.5% were candidates for renal transplantation and 6.9% had not been evaluated; 64.3% were followed up by a gastroenterologist; 27.2% of HBV(⿿) patients without immunisation had not been vaccinated. Fourteen different immunisation schedules had been used, with an immunisation rate of 58.8%. Mean anti-HBs stood at 165.7±297.8mIU/ml. A total of 72.7% of patients had received a vaccination course; 26.4%, 2 cycles; 1.0%, 3 cycles; and 11.6%, a booster dose. A total of 28.3% had a poor response (anti-HBs 10-99mIU/ml); 22.4%, an optimal response (anti-HBs 100-999mIU/ml); and 7.9%, an excellent response (anti-HBs 1,000mIU/ml). Age was significantly associated with response to vaccination; the mean age of nonresponders was significantly higher than patients who had a response of any kind (P<.05). The highest probability of an immune response was achieved with 4 doses of 40 mcg of adjuvanted vaccine (OR: 7.3; 95% CI 3.4 to 15.7), for the same age and number of cycles and boosters. Age, adjuvanted vaccine, dose and vaccination schedule influenced the immune response and the anti-HBs titres reached (P<.05).
ConclusionThe prevalence of chronic HBV infection in haemodialysis in Spain is low and so are the rates of immunisation against the virus. The vaccination schedules used are very diverse and have been observed to correlate with the immune response. It would therefore be necessary to establish a protocol for the most effective vaccination schedule to increase immunisation in these patients.
La infección por el virus de la hepatitis B (VHB) en pacientes con enfermedad renal crónica (ERC) es mayor que en la población general. En hemodiálisis, la prevalencia oscila entre el 0 y 10%1, con una alta variabilidad incluso entre las unidades de hemodiálisis de un mismo país. En España, la prevalencia de la infección por el VHB en hemodiálisis en 2003 se estimó en el 3,1%1. En los trasplantados renales, la prevalencia de la infección por el VHB varía en torno al 2%2, también con una amplia variabilidad geográfica y demográfica.
El contagio de la infección ha disminuido en esta población desde la instauración de medidas generales de prevención en los años setenta, incluida la posterior vacunación en 1986.
La historia natural de la hepatitis B en la población en diálisis es pobremente conocida debido a su lenta progresión, que puede ser promovida por varios factores: coinfección por el virus de la hepatitis C, ingesta de alcohol e inmunosupresión. La evolución de la hepatitis B crónica es más agresiva en los pacientes trasplantados renales que en los de diálisis, debido a la inmunosupresión y la baja actividad de linfocitos T citotóxicos, que aumentan la replicación viral3. Los pacientes en diálisis no suelen desarrollar síntomas de hepatitis B aguda y habitualmente tienen niveles de transaminasas normales o levemente elevados en la infección crónica4,5, por causas no aclaradas, aunque se ha postulado el efecto que pueden ejercer la uremia, el déficit de la vitamina B y el estado nutricional. La carga viral en los pacientes VHB(+) en diálisis suele mantenerse baja y estable a lo largo del tiempo6.
El objetivo primordial en el tratamiento de la infección crónica por el VHB es conseguir el aclaramiento del HBsAg con seroconversión a anti-HBs. Sin embargo, esta meta se alcanza solo en una minoría de pacientes inmunocompetentes y resulta menos frecuente en pacientes inmunocomprometidos. Un objetivo más realista es lograr suprimir eficiente y persistentemente la replicación del VHB para reducir la actividad necroinflamatoria hepática y detener o retrasar la progresión de la fibrosis para prevenir el desarrollo de complicaciones como la cirrosis, la descompensación hepática y el hepatocarcinoma.
Las indicaciones para el tratamiento de la infección por el VHB están basadas en la carga viral, el nivel de transaminasas y la gravedad de la insuficiencia hepática. Todos los fármacos precisan ajuste de dosis en los pacientes con ERC y deben ser utilizados con precaución, con monitorización de los niveles séricos de creatinina y, en algunos casos, de fósforo. El uso de interferón está contraindicado en el trasplante renal por el riesgo de rechazo.
Se recomienda la vacunación universal de los pacientes con ERC o en diálisis y del personal sanitario. La pauta más recomendada es la dosis doble (40mcg) de la vacuna convencional (Engerix®, HBVaxpro®) a los 0, 1, 2 y 6 meses7. Las tasas de inmunización en los pacientes vacunados frente al VHB en hemodiálisis son del 40-70% en comparación con el 97% de la población general8, con una posterior pérdida progresiva de la inmunización a medida que pasa el tiempo. Se han estudiado diferentes adyuvantes para mejorar la tasa de inmunización en poblaciones especiales (factor estimulante de colonias de granulocitos y macrófagos, interleucina-2, interferón, timopentina)9,10, hasta el desarrollo de una vacuna con 3-O-desacil-40-monofosforil lípido A. En un ensayo clínico realizado por Tong et al.11, se comparó la inmunización con la vacuna convencional a doble dosis frente a la dosis simple de la vacuna adyuvada (Fendrix®) a los 0, 1, 2 y 6 meses, lográndose unas tasas de inmunización del 84 vs. 91%. Se han implicado varios factores en la respuesta a la vacunación frente al VHB: anemia, malnutrición12⿿14, peso, sexo masculino15,16, función renal, hiperparatiroidismo secundario, disminución en la producción de inmunoglobulinas, disminución de la interleucina-2 por los linfocitos T, disfunción en los macrófagos y niveles altos de indoleamina-2,3-dioxigenasa17.
Resulta fundamental establecer estrategias de prevención y manejo de la infección por el VHB en la población con ERC, debido a su alta exposición a productos sanguíneos, a las frecuentes punciones venosas, procedimientos invasivos, equipamiento médico y personal sanitario.
Al no disponer de datos en la literatura médica sobre el nivel de estudio y seguimiento de la hepatitis B crónica de los pacientes en hemodiálisis y el nivel de inmunización y vacunación empleada en los pacientes sin hepatitis B, surgió la necesidad de realizar un estudio transversal para la recogida de todos los aspectos relacionados, con el fin de detectar mejoras en su manejo y la intervención multidisciplinar con nefrólogos y hepatólogos. Este trabajo, promovido por la Asociación Española de Hígado y Riñón (AEHR) y el Grupo de Virus en Diálisis de la Sociedad Española de Nefrología (SEN), es el primer estudio que tiene como objetivos: 1) determinar la prevalencia de la infección crónica por el VHB en los pacientes con ERC en tratamiento sustitutivo renal con hemodiálisis en España, los aspectos relacionados con su enfermedad hepática y su situación con respecto al trasplante renal; 2) conocer el estado de inmunización frente al VHB en esta población y los factores de respuesta asociados.
MétodoSe confeccionó un cuaderno de recogida de datos con las variables del estudio, para rellenar a partir de la historia clínica de cada paciente de hemodiálisis. Este se envió junto con una carta de presentación del registro, tanto por correo ordinario como por email, a todos los servicios de nefrología y unidades extrahospitalarias de hemodiálisis de España, a los que se telefoneó para confirmar que habían recibido la documentación. Este sistema se repitió a los 6 meses con los centros no respondedores. El cuaderno de recogida de datos debía ser cumplimentado por un investigador representante de cada centro y devuelto a la dirección postal del centro coordinador o email del grupo coordinador del estudio, para incluir los datos recogidos en una base central.
Los pacientes tenían que firmar un consentimiento informado para la prestación de sus datos, si el centro sanitario no disponía de una autorización previa para el uso de estos en investigaciones científicas.
El estudio fue aprobado por el Comité de ÿtica e Investigación Clínica del centro coordinador, el Hospital La Mancha-Centro, Alcázar de San Juan (Ciudad Real), España.
La recogida de datos se realizó de enero de 2013 a enero de 2014, con su posterior centralización y análisis.
Variables-
Centro
-
Número de pacientes en el centro, número de pacientes VHB(+)
-
Investigador/a
-
Fecha
-
Pacientes VHB(+)
-
Iniciales del paciente
-
Edad
-
Coinfección VHC/VIH (sí/no)
-
Carga viral
-
GOT/GPT
-
GGT
-
-
Biopsia hepática (sí/no, descripción)
-
Tratamiento previo del VHB (interferón, lamivudina, entecavir, tenofovir, adefovir, varios)
-
Duración del tratamiento
-
Dosis
-
Suspensión (sí/no, causa)
-
Candidato a trasplante renal (sí/no/no evaluado, rechazo del paciente)
-
Seguimiento en Digestivo (sí/no)
-
-
Pacientes VHB(⿿)
-
Serología: anticuerpos anti-HBs, anticuerpos anti-HBc
-
Vacunación frente al VHB (sí/no)
-
Tipo de vacuna (Engerix®, Fendrix®)
-
Pauta (0-1-6, 0-1-2-6, otra)
-
Dosis
-
Revacunación (sí/no), tipo de vacuna, pauta, dosis
-
-
-
¿Le ha ayudado este cuestionario a valorar el manejo de la infección del VHB en su unidad? (sí/no)
Las variables cuantitativas se describieron mediante medidas de tendencia central (media o mediana), acompañadas de sus medidas de dispersión (desviación estándar o rango intercuartílico), según su distribución normal. Las variables cualitativas se describieron mediante frecuencias relativas y absolutas.
Para las comparaciones entre variables cualitativas se utilizó el test de chi-cuadrado, y t de Student o U de Mann-Whitney para comparar las medias de las variables cuantitativas. Para evaluar la asociación entre la inmunización y los distintos esquemas terapéuticos se utilizó un modelo de regresión logística multivariante. Se consideraron diferencias significativas cuando la p fue<0,05.
Los datos fueron analizados mediante el programa SPSS versión 18.0.
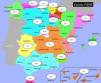
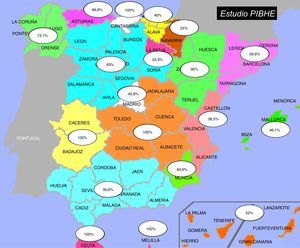
ResultadosDatos de los centros participantesDe los 366 centros de hemodiálisis de España, participaron en el estudio 215 (59%), el 53,7% eran hospitalarios. Todos mandaron sus datos de prevalencia y 42 enviaron el cuaderno de recogida de datos completo. En la figura 1 se representa el porcentaje de participación por comunidades autónomas.
De los 15.645 pacientes registrados, 162 eran VHB(+), lo que constituye una prevalencia de hepatitis B en hemodiálisis en España del 1,03%, a partir de la muestra encuestada. El 64,2% de los centros tenía al menos un paciente VHB(+).
Se recibieron los cuadernos de recogida de datos de 2.187 pacientes.
Situación de los pacientes VHB(+)Los pacientes VHB(+) tenían una media de 50±14,6 años, con un rango de edad de 26 a 66 años.
El 7,2% estaba coinfectado por el virus de la hepatitis C o por el virus de la inmunodeficiencia humana. El 19,2% tenía anti-HBe(+) y en un 3,8% no se había determinado. La carga viral era inferior a 2.000UI/ml en el 80%. Los niveles de GOT y GPT fueron de 19,1±10,1 y 15,9±9,6UI/ml, respectivamente. La biopsia hepática se había realizado en el 7,1%.
El 30% de los pacientes había recibido tratamiento antiviral, que se había suspendido en el 12,5%. Entre los tratamientos antivirales utilizados, el más empleado había sido el entecavir (13,3%), seguido de la lamivudina (10%), adefovir y tenofovir a partes iguales (6,7%), interferón (3,3%) y otros (3%).
El 34,5% era candidato a trasplante renal y el 6,9% no había sido evaluado. Se encontraban en seguimiento por un digestólogo el 64,3%.
Situación de los pacientes VHB(⿿)Los pacientes VHB(⿿) tenían una media de 66,8±14,9 años, con un rango de edad de 19 a 100 años.
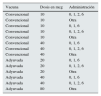
El 27,2% de los pacientes sin inmunización no había sido vacunado. Se encontró anti-HBc(+) en el 17,9%, sin estar vacunado el 66,1% de ellos. Se emplearon 14 pautas distintas de vacunación, que pueden observarse en la tabla 1. El 58,8% de los pacientes vacunados había alcanzado títulos de inmunización. La media de anti-HBs se situaba en 165,7±297,8mUI/ml (0-1.000).
Pautas de vacunación
| Vacuna | Dosis en mcg | Administración |
|---|---|---|
| Convencional | 10 | 0, 1, 2, 6 |
| Convencional | 10 | Otra |
| Convencional | 10 | 0, 1, 6 |
| Convencional | 10 | 0, 1, 2, 6 |
| Convencional | 10 | Otra |
| Convencional | 40 | 0, 1, 6 |
| Convencional | 40 | 0, 1, 2, 6 |
| Convencional | 40 | Otra |
| Adyuvada | 20 | 0, 1, 6 |
| Adyuvada | 20 | 0, 1, 2, 6 |
| Adyuvada | 20 | Otra |
| Adyuvada | 40 | 0, 1, 6 |
| Adyuvada | 40 | 0, 1, 2, 6 |
| Adyuvada | 80 | Otra |
En un 23% de los pacientes no se conocía la vacuna empleada. Engerix® era la más utilizada, con un 52,3%, seguida de Fendrix® con un 26,9% y HBVaxPro® con un 20,9%.
El 72,7% de los pacientes había recibido un ciclo de vacunación; el 26,4%, 2 ciclos; el 1,0%, 3 ciclos y el 11,6%, una dosis de recuerdo. La inmunización según el número de ciclos de vacunación fue del 80% con un ciclo, el 19,5% con 2 ciclos y el 0,5% con 3 ciclos.
La vacuna más utilizada en la revacunación de los pacientes fue Engerix® (39,3%), seguida de Fendrix® (32,5%) y HBVaxPro® (24,0%). En el 3,3% se desconocía la vacuna empleada en la revacunación.
Respuesta a la vacunaciónEl 41,4% de los pacientes no respondió a la vacunación. El 28,3% tuvo una respuesta pobre (anti-HBs 10-99 mUI/ml); el 22,4%, una respuesta óptima (anti-HBs 100-999mUI/ml); y el 7,9%, una respuesta excelente (anti-HBs1.000mUI/ml).
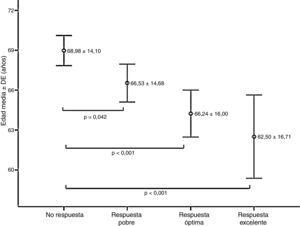
La edad se asoció significativamente con la respuesta a la vacunación, de manera que los pacientes que no respondieron tenían una edad media significativamente mayor que los pacientes que obtuvieron cualquier tipo de respuesta (p<0,05) (fig. 2).
La mayor probabilidad de conseguir una respuesta inmunitaria se alcanzaba con 4 dosis de 40mcg de vacuna adyuvada (OR: 7,3; IC 95%: 3,4-15,7), a igualdad de edad y número de revacunaciones y recuerdos. La edad, la vacuna adyuvada, la dosis y el esquema de vacunación influían en la respuesta inmunitaria y en el título de anti-HBs alcanzado (p<0,05).
Autovaloración del cuestionarioEl 78% de los investigadores respresentantes de cada centro estimó que el cuestionario le había ayudado a valorar el manejo de los pacientes en su unidad, con respecto a la infección e inmunización frente al VHB, el 17,1% creyó que no y el 4,9% no contestó.
DiscusiónEste estudio sitúa la prevalencia de la hepatitis B crónica en hemodiálisis en España en el 1,03%, frente a la del 3,1% estimada por Burdick et al. en el estudio DOPPS de 20031. Esta reducción de la prevalencia del VHB en hemodiálisis en España puede ser debida a varias causas: la muerte de pacientes infectados por transfusiones contaminadas antes de los años noventa y las medidas de prevención implantadas en las unidades de hemodiálisis respecto al aislamiento y la vacunación. El DOPPS incluía 308 centros a nivel internacional, con solo 20 centros de hemodiálisis en España, frente a los 215 partipantes en el estudio PIBHE, con lo que también se puede haber originado un sesgo de muestra, teniendo en cuenta, además, que los pacientes VHB(+) están aún más centralizados que los VHC(+). Esto lo demuestra el dato de que el 64,5% de los centros tenía al menos un paciente VHB(+), frente al 75,9% de los centros con pacientes VHC(+), reflejado en el estudio SHECTS18.
La edad de los pacientes VHB(+) es menor que la de los VHB(⿿), con una media de 50±14,6 frente a 66,8±14,9 años, respectivamente, lo que puede estar en relación con una menor expectativa de vida a causa de la infección. No hay estudios sobre morbimortalidad relacionada con el VHB en los pacientes con ERC o en diálisis, pero sí en trasplantados renales, en los que la mortalidad a los 10 y 20 años es del 85 y 71%, respecto al 98 y 95% de los trasplantados VHB(⿿), a pesar del tratamiento antiviral19. Un metaanálisis de Fabrizi et al.20 reveló que los pacientes trasplantados renales con infección por el VHB tienen un riesgo de mortalidad postrasplante 2,49 veces mayor que los no infectados.
La biopsia hepática es poco utilizada (7,1%). Entre las causas del poco uso podría estar el riesgo de sangrado incrementado en los pacientes renales y la aparición de la elastografía, aunque esta técnica aún no ha sido validada en esta población.
La nefrotoxicidad asociada a tenofovir y adefovir puede haber llevado a un mayor uso de entecavir y lamivudina, como refleja el tratamiento antiviral empleado. Este puede haber sido prescrito solo en un 30% de pacientes, entre otras causas, por la situación de portador inactivo del VHB, debido a su baja replicación y nivel normal de transaminasas.
Aunque este estudio muestra que la mayoría de pacientes VHB(+) son evaluados para trasplante renal, es bajo el número de pacientes candidatos (34,5%), por causas no aclaradas.
El riesgo de reactivación del VHB y de hepatocarcinoma hacen aconsejable el seguimiento de todos los pacientes por un digestólogo. Sin embargo, este trabajo pone en evidencia que es seguido solo un 64,3%.
Con respecto a los VHB(⿿), destaca que exista un 23% de pacientes que no hayan sido vacunados, a pesar de que las guías clínicas recomiendan la vacunación en todos los pacientes en hemodiálisis.
El 17,3% de los sujetos tiene anti-HBc(+), pero un porcentaje considerable carece de inmunización y no ha sido vacunado (33,8%); estos pacientes, además, tienen una mayor posibilidad de inmunizarse por la memoria inmunológica y, a su vez, un mayor riesgo de reactivación en situación de inmunosupresión, por lo que su vacunación se hace aún más recomendable.
La cifra global de pacientes inmunizados en hemodiálisis es similar a la de estudios previos, con un 61,9 frente al 68,7% encontrado en el estudio de Siddiqui et al.21 con 40mcg de vacuna convencional, aunque la variabilidad en las pautas de vacunación (hasta 14) y el bajo empleo de un segundo ciclo (21,5%) ponen de manifiesto la existencia de mejoras plausibles en la respuesta inmunológica con pautas más eficaces. Esta estrategia ya ha sido llevada a cabo en otros estudios, con el rescate de un alto número de pacientes con un segundo ciclo de vacuna convencional y un tercer ciclo con vacuna adyuvada22. El segundo ciclo de vacunación en el estudio PIBHE consigue rescatar a un 19,5% de pacientes no respondedores. Pese a que las guías de práctica clínica no son muy claras con respecto a las pautas de vacunación y revacunación, sí están de acuerdo en la necesidad de doblar la dosis de vacuna convencional23, por lo que destaca que haya esquemas de vacunación con 10mcg, que son dosis pediátricas, y con 20mcg, así como dosis de vacuna adyuvada de 40 y 80mcg, no probadas antes en ensayos clínicos ni estudios controlados.
La alta valoración que los nefrólogos realizan sobre la utilidad del cuestionario (78%) lleva al planteamiento de estrategias de este tipo con el fin de realizar una autoevaluación del manejo de los pacientes y tomar actitudes intervencionistas.
Este trabajo es el primero a nivel mundial que valora el grado de estudio y seguimiento de los pacientes VHB(+) y la vacunación e inmunización de los pacientes VHB(⿿) en hemodiálisis. Pone de manifiesto el descenso que ha experimentado la prevalencia del VHB en hemodiálisis en España en 10 años y la alta variabilidad en las pautas de vacunación de los pacientes junto a su baja inmunización, con posibilidades de aumento de diseñarse mejores estrategias. Sería necesario establecer un manejo multidisciplinar entre nefrólogos y hepatológos y actualizar las guías de práctica clínica respecto a la vacunación frente al VHB en hemodiálisis.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.