Presentamos un inusual caso de hipercalcemia severa de inicio neonatal.
Paciente de 4 días de vida traída a urgencias por estreñimiento de 48h. Buena tolerancia oral y apetito. Hipotónica con buena respuesta a estímulos, sin otra sintomatología. No presenta antecedentes familiares ni personales de interés.
Analítica sanguínea con hemograma, fórmula leucocitaria y niveles de plaquetas normales; gasometría capilar y bioquímica sanguínea con discreta acidosis metabólica: pH7,33, bicarbonato19,2 y calcio iónico4,84mmol/l confirmado con calcio sérico 28,1mg/dl. Ante los hallazgos de hipercalcemia severa, ingresa en la unidad de cuidados intensivos pediátricos para completar estudio.
Al ingreso se objetivan cifras de parathormona (PTH) >5.000pg/m (límite alto de la normalidad para su edad, 78pg/ml), cifras compatibles con hiperparatiroidismo primario neonatal severo. Actividad tiroidea normal. A destacar déficit de vitaminaD (VitD): 16ng/ml, en probable relación con déficit materno.
En el estudio radiológico destaca osteopenia incipiente, y el cardiológico muestra un intervalo Qt corregido corto, con resto de valores y corazón estructuralmente normal.
La ecografía abdominal mostró indicios de nefrocalcinosis renal derecha, sin otros hallazgos, y la ecografía tiroidea no mostraba hiperplasia ni adenomas glandulares.
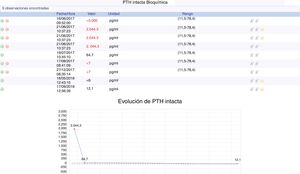
Realizamos gammagrafía tiroidea, que sorprendentemente objetivaba distribución fisiológica del trazador. Ante la presencia de hipercalcemia grave por sospecha de hiperparatiroidismo primario neonatal severo (HPPNS), se inicia tratamiento urgente con hidratación abundante (suero salino fisiológico a 100/m2/h), terapia de depuración extrarrenal, furosemida (1mg/kg/día), corticoide sistémico (metilprednisolona 2mg/kg/día), calcitonina (5UI/kg/día) y pamidronato (1mg/kg/día). Precisa ventilación mecánica las primeras 48h. Dicho tratamiento resulta efectivo, con normalización de los valores de calcio (2,43mmol/l de Ca iónico) en las primeras 48h y leve disminución de PTH (tras 5días de tratamiento, 2.044pg/ml) (fig. 1).
Tras dichos resultados se inicia descenso de tratamiento, comprobándose nuevo aumento de las cifras de calcio iónico (máximo 2,1mmol/l y 11mg/dl), obligando a reiniciarlo.
A los 12 días de vida se traslada a servicio ORL infantil, donde es intervenida mediante paratiroidectomía total, con confirmación diagnóstica intraoperatoria de visu. Se extirparon seis glándulas paratiroideas, ortotópicas todas ellas, reimplantándose una en antebrazo, no funcionante aparentemente. Por el contrario, en el último control analítico se objetivaron cifras de PTH en ascenso (12,1pg/ml) que podrían mostrar reinicio de actividad, no suficiente por el momento para el mantenimiento adecuado del metabolismo fosfocálcico.
Las glándulas paratiroideas reimplantadas pueden tardar en reiniciar su actividad entre 6 y 12meses, según la bibliografía descrita. Sin embargo, podríamos plantearnos el aumento de este rango en espera de comprobar el ascenso y la recuperación progresiva en pacientes varios meses más allá de la intervención, como en nuestro caso, tras 16meses de la reimplantación.
El estudio genético posterior reveló una doble mutación en heterocigosis del gen CaSR, diagnosticándose de hiperparatiroidismo neonatal severo sintomático.
Tras la intervención, la paciente presenta hipocalcemia progresiva, sin pérdidas renales, junto a hipofosforemia e hipomagnesemia. Compatible con «síndrome del hueso hambriento», se inicia tratamiento con 1,25-hidroxi-vitaminaD3 (calcitriol, 0,50μg/día) y suplementos de calcio (carbonato cálcico, 1.000mg/día vía oral, y gluconato cálcico, 216mg/día vía oral, con aportes totales de calcio de 345mg/kg/día) junto con fósforo y magnesio.
Actualmente la paciente tiene 15 meses de vida, se encuentra asintomática y evoluciona favorablemente. Como principal secuela presenta un hipoparatiroidismo permanente con hipocalcemia y osteopenia difusa, en tratamiento de mantenimiento con suplementos de calcio, colecalciferol y calcitriol.
La presentación del hiperparatiroidismo neonatal severo es diversa; desde casos asintomáticos hasta sintomatología respiratoria, neurológica, fallo de medro, etc. Es necesario un diagnóstico diferencial exhaustivo1 (fig. 2).
No existe prueba diagnóstica gold standard, y las pruebas de imagen han resultado ineficaces, con alto índice de falsos negativos.
El tratamiento se basa fundamentalmente en:
- •
La corrección urgente y vital de los altos niveles de hipercalcemia iniciales con hiperhidratación, calcimiméticos (cinacalcet), bifosfonatos (pamidronato), diuréticos (furosemida) y corticoterapia (metilprednisolona).
- •
Tratamiento etiológico quirúrgico.
- •
Tratamiento de las secuelas posteriores: hipocalcemia y síndrome del hueso hambriento; tratadas con 25OH-vitaminaD3 (calcitriol/alfacalcidol) y calcio (gluconato y carbonato cálcicos).
La existencia de un marcador biológico que determinase la respuesta favorable o no al tratamiento médico ahorraría períodos de farmacoterapia innecesarios. Sin embargo, no existe actualmente tal parámetro1,2. Por lo tanto el tratamiento quirúrgico es de elección cuando no se consigue un control adecuado con farmacoterapia, como en nuestro caso.
En cuanto al estudio genético, mutaciones en el gen CASR de las células paratiroides se relacionan con alteración de la homeostasis del calcio. Este receptor censa los niveles de calcio en sangre. Su mutación provoca una insensibilidad de dichas células a las variaciones de calcemia, generando aumento de PTH e hiperplasia glandular. Esta mutación se observa en hiperplasia, adenomas y HPPNS.
En nuestra paciente se llevó a cabo amplificación de ADN mediante PCR del gen CASR, detectando dos cambios en heterocigosis. La mutación c.73C>T ya había sido descrita previamente; sin embargo, la segunda mutación encontrada, la c.1981T>C, es de novo y probablemente patogénica.
Más de la mitad de casos de hiperparatiroidismo en niños reportados en la bibliografía muestran antecedentes familiares; en nuestro paciente, el estudio de progenitores reveló ausencia mutaciones en padre y mutación c.73C>T en la madre. Muchos autores defienden que el cribado familiar podría ser eficaz y eficiente en el control de la enfermedad3.
En conclusión, el HPPNS debe ser considerado en el diagnóstico diferencial de los recién nacidos con hipercalcemia. El tratamiento médico inicial será vital para el paciente, determinando la necesidad o no de tratamiento quirúrgico posterior. Es fundamental establecer el diagnóstico genético, además de un seguimiento médico de por vida.
A todos los compañeros del Hospital Materno-Infantil de Badajoz por su trabajo en equipo, su tesón, su paciencia y su buen hacer en medicina basada en la evidencia, siempre a favor de nuestros pacientes.