INTRODUCCIÓN
En el último número de Nefrologia (2012;32[3]:367-73), del Pozo et al.1 reflexionan sobre las discrepancias encontradas en el uso de metformina en pacientes con diabetes mellitus tipo 2 (DM2): la ausencia de criterios uniformes acerca de su indicación en los diferentes estadios de insuficiencia renal y su empleo en estos pacientes.
Creemos que el artículo merece un comentario muy detenido a modo de editorial sobre este importante problema del manejo diario en la clínica práctica.
CONTROL METABÓLICO GLUCÉMICO EN ENFERMEDAD RENAL CRÓNICA
En el paciente con DM2 que padece enfermedad renal crónica (ERC), el mejor control metabólico posible es el método más adecuado para prevenir y/o enlentecer la evolución progresiva de ésta, actuando además sobre otros factores de progresión como la hipertensión arterial, la albuminuria, el tabaquismo y el sobrepeso. El objetivo de control glucémico suele plantearse como una cifra de hemoglobina glicosilada (HbA1c) < 7%2. Para lograr este óptimo control, se presentan dos dificultades importantes: la inconveniencia de administrar determinados fármacos hipoglucemiantes por estar contraindicados en la ERC y la predisposición en estos pacientes a la hipoglucemia.
A) Antidiabéticos orales
Clasificación de los antidiabéticos orales
Los antidiabéticos orales (ADO) se clasifican en:
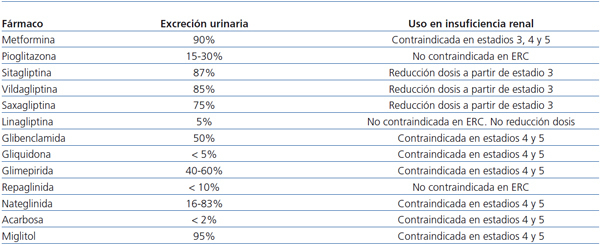
- Fármacos secretagogos de insulina (tabla 1): sulfonilureas, meglitinidas, inhibidores de dipeptidil-peptidasa 4 (iDPP4).
- Fármacos que estimulan la acción periférica de la insulina: metformina, pioglitazona.
- Fármacos que inhiben la α-glucosidasa a nivel intestinal (retrasan la absorción de glucosa): acarbosa, miglitol.
Características generales de los principales grupos de antidiabéticos orales
Sulfonilureas: Son fármacos capaces de estimular a las células β para que aumenten su secreción endógena de insulina. Las sulfonilureas están contraindicadas en caso de insuficiencia renal. Sus principales efectos secundarios son las hipoglucemias, que pueden ser graves, y el aumento de peso.
Meglitinidas (repaglinida y nateglinida): Ambas tienen una vida media breve, por lo que se administran antes de las principales comidas. La potencia de la repaglinida es mayor y su eliminación es principalmente biliar, por lo que está aceptado su uso en cualquier estadio de ERC, incluso en pacientes en diálisis. La nateglinida, pese a tener metabolismo hepático, se degrada en metabolitos activos que se depuran a nivel renal, por lo que no está recomendada en ERC. Ambas pueden inducir hipoglucemia, aunque, dada su menor vida media, ésta es menos frecuente que con las sulfonilureas.
Metformina: La metformina es una biguanida cuyo mecanismo de acción principal es la reducción de la producción hepática de glucosa actuando sobre la neoglucogénesis, aunque también aumenta la captación muscular de glucosa. Su eliminación es renal, por lo que está contraindicada en ficha técnica en pacientes con aclaramiento de creatinina < 60 ml/min por riesgo de acidosis láctica. No obstante, se puede utilizar hasta con un filtrado glomerular (FG) de 30 ml/min/1,73 m2 (ver explicación mas adelante).
Glitazonas: La rosiglitazona fue retirada del mercado por un posible aumento del riesgo cardiovascular. Su principal mecanismo de acción es aumentar la sensibilidad a la insulina mediante el incremento de la captación y utilización de la glucosa en músculo y tejido graso. También disminuye, aunque en menor medida, la neoglucogénesis y la síntesis de ácidos grasos a nivel hepático. Se metaboliza en el hígado y se excreta por heces, por lo que puede utilizarse en cualquier estadio de ERC. Su asociación con aumento de peso, debido a la retención hídrica, ha hecho que se haya contraindicado en caso de insuficiencia cardíaca o hepática, y por otra parte hay que tener presente la posibilidad de aumento de fracturas distales en mujeres. En Francia y Alemania la pioglitazona ha sido retirada del mercado por un posible aumento del riesgo de cáncer de vejiga.
Inhibidores de α-glucosidasa (acarbosa y miglitol): Inhiben de forma competitiva y reversible la α-glucosidasa de las microvellosidades intestinales, retrasando la absorción de los hidratos de carbono complejos y disminuyendo el pico glucémico posprandial. En monoterapia no producen incremento de peso ni hipoglucemia. Están contraindicados en ERC grave.
Inhibidores de la dipeptidil-peptidasa 4: Potencian la acción de las incretinas al inhibir la enzima dipeptidil-peptidasa IV, que degrada al péptido similar al glucagón tipo 1 (GLP-1), el cual se produce en el intestino en respuesta a la ingesta. El GLP-1 estimula la secreción de insulina e inhibe la de glucagón. Así, estos fármacos producen una secreción fisiológica de la insulina mediada por la ingesta y una inhibición del exceso de glucagón. Los iDPP4 comercializados en España en el momento actual son sitagliptina, vildagliptina, saxagliptina y linagliptina. Este grupo farmacológico presenta la gran ventaja frente a los secretagogos clásicos de no producir hipoglucemias, dado que su mecanismo estimulador de la secreción de insulina es dependiente de la glucosa, característica que los hace especialmente atractivos en presencia de ERC por la predisposición de estos pacientes a desarrollar hipoglucemias.
Sitagliptina, vildagliptina y saxagliptina precisan ajuste de dosis, dado que su eliminación es fundamentalmente renal. Los estudios recientes con linagliptina muestran que su eliminación es hepatobiliar y su vida media apenas se prolonga, en la ERC avanzada, un máximo de 14 a 18 horas, por lo que no precisa ajuste de dosis, habiendo sido incluso utilizada en pacientes diabéticos en hemodiálisis.
Antidiabéticos orales en pacientes con enfermedad renal crónica no en diálisis
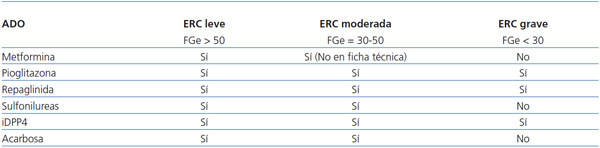
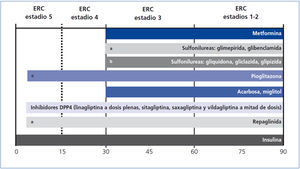
En la tabla 2 se recogen las indicaciones de los diferentes grupos terapéuticos de antidiabéticos orales en enfermedad renal crónica, y en la figura 1, la utilización de los distintos grupos terapéuticos de antidiabéticos orales e insulinoterapia en los diferentes estadios de la enfermedad renal crónica.
Para el manejo adecuado de la hiperglucemia, desde el consenso de la Asociación Americana de Diabetes (ADA) y de la Asociación Europea para el Estudio de la Diabetes (EASD) de 20083, se recomienda en todo paciente con DM2 desde el momento del diagnóstico el tratamiento con metformina, excepto en caso de contraindicación formal o de intolerancia. El tratamiento inicial con metformina se sigue recomendando en el nuevo consenso de ambas sociedades3,4 y ha sido respaldado por las principales sociedades españolas involucradas en el tratamiento de la DM25. No obstante, la metformina se encuentra contraindicada en ficha técnica en casos de aclaramiento de creatinina < 60 ml/min. Las Guías NICE6, así como trabajos recientes7, consideran que su uso es seguro en caso de aclaramientos de creatinina > 30 ml/min, aconsejando reducción de la dosis con filtrado glomerular (FG) < 45 ml/min. La Food and Drug Administration (FDA) se basa únicamente en las concentraciones de creatinina (contraindicada a partir de creatinina sérica ≥ 1,5 mg/dl en varón y ≥ 1,4 mg/dl en mujer). Se ha publicado recientemente un estudio en el que se utilizaba metformina en pacientes con aclaramiento de creatinina de alrededor de 20 ml/min, a dosis de 200-500 mg diarios8. Como sugieren Lipska et al.9, parecería razonable suspender metformina en pacientes con FG estimado (FGe) inferior a 30 ml/min/1,73 m2, y con FG menor de 45 ml/min/1,73 m2 en aquellos pacientes con factores de riesgo para desarrollar acidosis láctica (hipoperfusión periférica –pie diabético, insuficiencia cardíaca–, hepatopatía avanzada, antecedente de acidosis láctica previa).
Los cambios en el tratamiento deben ser precoces para prevenir o retrasar las complicaciones, instaurando de forma temprana el tratamiento combinado. En ficha técnica las sulfonilureas se contraindican en pacientes con insuficiencia renal grave (ERC en estadios 4 y 5). En estadio 3 podrían utilizarse gliquidona, glipizida o gliclazida, aunque el riesgo de hipoglucemia es elevado.
La repaglinida se elimina principalmente por vía biliar y sólo un 8% es de eliminación renal, por lo que puede utilizarse en cualquier estadio de ERC10. Está contraindicada su utilización junto con el gemfibrozilo, por la posibilidad de aumento del número de hipoglucemias si no se ajusta la dosis de repaglinida. Por el contrario, la nateglinida se metaboliza por el hígado, con la formación de numerosos metabolitos activos, que se eliminan por vía renal. Su metabolización a través del CYP2C9 puede provocar interacciones con diversos fármacos de uso común (amiodarona, warfarina). Se han descrito hipoglucemias graves asociadas a su empleo en enfermedad renal11. Todo ello no hace aconsejable su uso cuando se administre en pacientes con ERC.
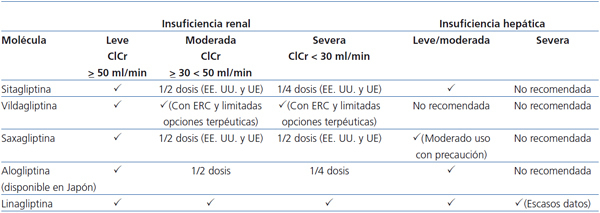
La utilización de los iDPP4 en pacientes con DM2 y función renal alterada se limita a pocos estudios con un número de pacientes reducido en lo que se refiere a sitagliptina12,13, saxagliptina14 y vildagliptina15. Sitagliptina, vildagliptina y saxagliptina precisan ajuste de dosis a partir de aclaramiento de creatinina < 50 ml/min/m2 dado que la eliminación de éstas es fundamentalmente renal. Esta presentación de sitagliptina (50 mg) no se encuentra comercializada en España en el momento actual. La presentación de mitad de dosis de saxagliptina (2,5 mg) se encuentra comercializada, pero no financiada en estos momentos en España. Un estudio muy reciente15 en 124 pacientes con DM2 y ERC grave (FGe medio: 21,9 ± 5,7 ml/min) ha mostrado que vildagliptina descendió eficazmente la HbA1c y los efectos adversos fueron similares a los del grupo placebo. En el caso de la vildagliptina, la dosis recomendada en ERC y diálisis es de 50 mg diarios (1 comprimido), en lugar de cada 12 horas. La linagliptina merece mención especial al ser el único iDPP4 de eliminación casi exclusivamente biliar, lo que permite su uso en cualquier grado de ERC, incluida diálisis, sin precisar ajuste de dosis16 (tabla 3).
El grupo de inhibidores de α-glucosidasas tienen escasa potencia hipoglucemiante. La acarbosa prácticamente no se absorbe. El miglitol se absorbe bien, no se metaboliza y se elimina por vía renal con una semivida de 2-3 horas. Sus concentraciones plasmáticas aumentan en pacientes con insuficiencia renal, por lo que el miglitol está contraindicado en caso de ERC.
La pioglitazona se puede utilizar en cualquier estadio de ERC, aunque en caso de ERC grave hay que tener precaución por la posibilidad de efectos adversos (aumento de peso, edema, agravamiento de insuficiencia cardíaca). No se precisa ajuste de dosis en enfermos con ERC leve o moderada. En pacientes con ERC, las concentraciones plasmáticas de pioglitazona y sus metabolitos son menores que las observadas en individuos con la función renal normal. Sin embargo, el aclaramiento de la sustancia original es similar. Por tanto, la concentración de pioglitazona libre permanece inalterada, por lo que su uso no está contraindicado en pacientes con ERC. La pioglitazona puede producir retención de líquidos en casos de ERC leve o moderada, por lo que se recomienda vigilar más estrechamente a los pacientes que puedan presentar insuficiencia cardíaca, así como asegurar el tratamiento diurético cuando sea utilizada. La pioglitazona está indicada en tratamiento combinado con sulfonilureas, metformina, iDPP4 o insulina. En monoterapia sólo está indicada si el tratamiento con metformina se halla contraindicado (en caso de ERC moderada o grave) o en casos de intolerancia a la metformina.
En caso de ERC con aclaramiento de creatinina < 30-60 ml/min, se puede usar la combinación de iDPP4 o repaglinida (que mejoran la secreción de insulina, en caso de que persista reserva insulínica) con pioglitazona (que mejora la sensibilidad a la insulina), siempre que el paciente no muestre tendencia a la retención de líquidos. Los iDPP4 presentan la gran ventaja frente a la repaglinida de no producir hipoglucemias.
Antidiabéticos orales en pacientes con enfermedad renal crónica en diálisis
A medida que desciende el FG, existe una menor degradación de la insulina. En dicha situación el paciente percibe que requiere menos dosis de ADO (llegando en ocasiones a suspenderlos transitoriamente por alargamiento de la vida de la insulina endógena) o se reducen las dosis habituales de insulina. Por este motivo, el paciente se resiste con frecuencia a la insulinización si recibía ADO. En el caso de recibir insulina, puede percibir una mejoría del tratamiento de la hiperglucemia.
Las sulfonilureas deben evitarse en los pacientes en hemodiálisis. Se unen fuertemente a la albúmina y por ello los niveles elevados del fármaco no se pueden eliminar con hemodiálisis. La administración simultánea de betabloqueantes, aspirina o dicumarínicos aumenta la proporción de fármaco libre en sangre y puede producir hipoglucemia grave. Esta situación es menos acusada con algunas sulfonilureas (glipizida o glimepirida). No obstante, se recomienda no administrarlas en hemodiálisis.
Las glitazonas se asocian a alto riesgo de edema e insuficiencia cardíaca, siendo mayor a medida que el FG es menor. Por ello, se desaconseja su uso en pacientes en diálisis, aunque puedan usarse en pacientes con ERC avanzada. La repaglinida, al tener un metabolismo hepático, puede utilizarse en estos pacientes, aunque con mucha precaución por el alto riesgo de hipoglucemia. Se debe iniciar tratamiento con la mínima dosis (0,5 mg) y monitorizar cuidadosamente la dosis. Recientemente, se han publicado buenos resultados del tratamiento de la hiperglucemia con vildagliptina en pacientes con DM2 en hemodiálisis, sin efectos secundarios y sin hipoglucemias17. La linagliptina puede usarse en diálisis al ser de eliminación casi exclusivamente biliar. Sin embargo, la insulinoterapia sigue siendo el tratamiento de elección en el paciente en diálisis, tanto hemodiálisis como diálisis peritoneal. Sin duda, el aprendizaje en el manejo de los nuevos iDPP4 en los pacientes con ERC avanzada o en diálisis nos aportará nuevas perspectivas en el manejo de la hiperglucemia en estos pacientes.
B) Insulinoterapia
Ajustes de dosis de insulina en el paciente con insuficiencia renal crónica sin diálisis
La insuficiencia renal crónica se asocia a un descenso del catabolismo renal de la insulina. Por ello, los niveles de glucemia de los pacientes diabéticos con insuficiencia renal en tratamiento insulínico se deben monitorizar de forma estrecha y realizar ajustes en la dosificación de manera individual. No obstante, se han establecido determinadas recomendaciones generales para la dosificación de la insulina en estos pacientes18,19:
- No se precisa ajuste de dosis si el FG es superior a 50 ml/min/1,73 m2.
- La dosis de insulina se debe reducir un 25% cuando el FG se encuentra entre 10 y 50 ml/min/1,73 m2.
- La dosis se debe reducir un 50% cuando el FG es inferior a 10 ml/min/1,73 m2.
Pautas de insulina subcutánea en pacientes en diálisis
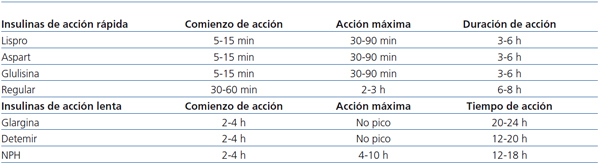
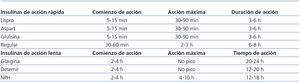
En hemodiálisis, se pueden utilizar, al igual que en el paciente diabético sin insuficiencia renal, diversos regímenes de insulinoterapia, como insulina premezclada 2-3 veces al día o pautas basal-bolus (insulina de acción lenta junto con insulina de acción rápida antes de las principales ingestas)20,21. Aunque no existe una pauta única recomendada para estos pacientes19, son especialmente recomendables los análogos de insulina frente a las insulinas humanas, puesto que los análogos han demostrado menor frecuencia de hipoglucemias. Por ello, se prefieren los análogos basales (glargina, 1 vez al día o detemir, 1-2 veces al día) frente a la insulina NPH (Neutral Protamine Hagedorn), y los análogos de acción rápida (lispro, aspart y glulisina) frente a la insulina regular (tabla 4).
Insulina intraperitoneal en pacientes en diálisis peritoneal
En los pacientes diabéticos se recomienda utilizar soluciones de líquido peritoneal con bajo contenido de glucosa o líquidos sin glucosa, como los basados en aminoácidos o polímeros de la glucosa. La administración de insulina se puede efectuar por la vía subcutánea clásica o por vía intraperitoneal, introduciendo la insulina en las bolsas de diálisis peritoneal justamente antes de la infusión en peritoneo. Si sólo se utiliza la vía subcutánea, la administración de ésta debe repartirse en 2 dosis de insulina premezclada, 1 o 2 dosis de análogos de insulina de acción lenta e incluso algunos pacientes se manejan aceptablemente con 3 dosis de insulina regular en relación con las comidas. La vía intraperitoneal presenta ventajas e inconvenientes respecto a la vía subcutánea, pero permite un excelente control de la glucemia y por ello puede ser la mejor opción para dicho tratamiento en pacientes muy disciplinados, autosuficientes y con gran motivación. Esta ruta de administración es más fisiológica que la subcutánea, pues la insulina se absorbe directamente a la vena porta como ocurre en personas no diabéticas con la insulina endógena, reduciendo los efectos secundarios derivados de la absorción de la insulina directamente a circulación sistémica. Se debe utilizar siempre insulina rápida y realizar la administración en las bolsas en el momento previo a la infusión, haciendo coincidir el horario de los intercambios de bolsa con las comidas principales. Se precisan agujas relativamente largas (3,8 cm) para asegurar que se inyecta la dosis total en la bolsa de la solución de diálisis. Esta bolsa se debe invertir en varias ocasiones tras la inyección para asegurar una adecuada mezcla.
En el caso de técnicas de diálisis peritoneal automatizada (diálisis peritoneal cíclica continua o diálisis peritoneal intermitente nocturna), en las cuales la mayor parte de la diálisis se lleva a cabo por la noche, la dosis intraperitoneal se debe añadir como insulina regular en cualquiera de los recipientes de diálisis asociados a la cicladora, y su administración proporciona cobertura basal durante la noche22-24.
C) Análogos de GLP-1
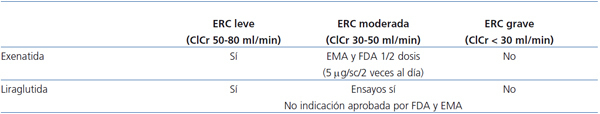
Los agonistas de GLP-1 se ligan al receptor de esta hormona, producida a nivel intestinal ante la llegada del bolo alimentario, incrementando en el páncreas endocrino la secreción de insulina e inhibiendo la de glucagón. Además, enlentecen el vaciado gástrico y disminuyen el apetito, por lo que su uso se asocia con frecuencia a pérdida de peso. Los efectos adversos más frecuentes de estos fármacos son náuseas y vómitos. Los dos agonistas de GLP-1 comercializados en la actualidad para el tratamiento de la DM2 son exenatida y liraglutida (tabla 5).
Dado que su eliminación es renal, exenatida precisa ajuste de dosis con aclaramientos de entre 30 y 50 ml/min, y no se recomienda su uso en ERC en estadios 4 y 5 (aclaramiento de creatinina < 30 ml/min).
La seguridad de liraglutida no está establecida en ERC, aunque los estudios farmacocinéticos sugieren que los niveles de fármacos no se encuentran alterados en esta población25. No se precisa ajuste de dosis con liraglutida en ERC leve (aclaramiento mayor de 60 ml/min). Por debajo de esta cifra, la muy limitada experiencia en estadio 3 y la falta de experiencia en estadios 4 y 5 desaconsejan su utilización. Actualmente no se puede recomendar el uso de estos fármacos en pacientes con ERC moderada o grave, incluidos los pacientes con ERC en estadio 5.
En conclusión, el manejo actual de los agentes hipoglucemiantes en el paciente diabético requiere cambios conceptuales, que implican a todos los profesionales encargados del cuidado integral de dichos pacientes. Cuando el paciente presenta ERC, se debe tener en cuenta no sólo la ficha técnica de los fármacos antidiabéticos, sino también la vía de metabolización de éstos y su perfil de seguridad. Dada la escasez de estudios realizados en pacientes con ERC en relación con el tratamiento de la hiperglucemia, la continua aparición de nuevas opciones terapéuticas y la alta prevalencia de diabetes mellitus en este tipo de pacientes, es de gran interés la actualización en el tratamiento de la hiperglucemia del paciente con ERC.
Conflictos de interés
Los autores declaran que no tienen conflictos de interés potenciales relacionados con los contenidos de este artículo.
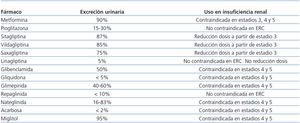
Tabla 1. Antidiabéticos orales y uso en enfermedad renal crónica según ficha técnica
Tabla 2. Indicaciones de los diferentes grupos terapéuticos de antidiabéticos orales en enfermedad renal crónica
Tabla 3. Uso aprobado de los inhibidores de la DPP4 en insuficiencia renal y hepática (2012)
Tabla 4. Características farmacocinéticas de las diferentes insulinas
Tabla 5. Análogos de péptido similar al glucagón tipo1 en pacientes con enfermedad renal crónica
Figura 1. Utilización de los distintos grupos terapéuticos de antidiabéticos orales e insulinoterapia en los diferentes estadios de la enfermedad renal crónica