El abordaje multidisciplinar y el uso de ecografía doppler (ED) en la creación y vigilancia del acceso vascular (AV) puede mejorar la prevalencia y permeabilidad de las fístulas arteriovenosas (FAV) para hemodiálisis. El objetivo de este estudio es analizar el impacto de una nueva consulta multidisciplinar (CMD) de AV con ED de rutina.
Material y métodosEvaluamos los resultados de la consulta de AV en 2014 (pre-CMD) y 2015 (CMD), antes y después de la implantación de un equipo multidisciplinar (cirujano vascular/nefrólogo) con ED de rutina en mapeo prequirúrgico y FAV prevalente.
ResultadosSe evaluaron 345 pacientes en 2014 (pre-CMD) y 364 pacientes en 2015 (CMD). En ambos periodos se realizó un número similar de cirugías, 172 vs. 198, p=0,289, con tendencia a aumentar las cirugías preventivas de reparación de FAV en el periodo CMD, 17 vs. 29 (p=0,098). En FAV de nueva creación (155 vs. 169), disminuyó la tasa de fallo primario en el periodo CMD, 26,4 vs. 15,3%, p=0,015 y aumentó de forma no significativa la realización de FAV radiocefálicas distales, 25,8 vs. 33,2% (n=40 vs. 56), p=0,159. También aumentó la concordancia entre la indicación quirúrgica en la consulta y la cirugía realizada (81,3 vs. 93,5%, p=0,001). En el periodo CMD se solicitaron menos exploraciones radiológicas desde la consulta, 78 vs. 35 (p<0,001), con una reducción del gasto sanitario (81.716€ vs. 59.445€).
ConclusionesEl manejo multidisciplinar y la utilización del ED de rutina permiten mejorar los resultados de AV, con disminución de la tasa de fallo primario de FAV, más opciones de FAV distal nativa, mejor manejo de la FAV prevalente disfuncionante y menor coste en exploraciones radiológicas.
A multidisciplinary approach and Doppler ultrasound (DU) assessment for the creation and maintenance of arteriovenous fistulas (AVF) for haemodialysis can improve prevalence and patency. The aim of this study was to analyse the impact of a new multidisciplinary vascular access (VA) clinic with routine DU.
Material and methodsWe analysed the VA clinic results from 2014 and 2015, before and after the implementation of a multidisciplinary team protocol (vascular surgeon/nephrologist) with routine DU in preoperative mapping and prevalent AVF.
ResultsWe analysed 345 and 364 patients from 2014 and 2015 respectively. The number of surgical interventions was similar in both periods (p=.289), with a trend towards an increase in preventive surgical repair of AVF in 2015 (17 vs. 29, p=.098). 155 vs. 169 new AVF were performed in 2014 and 2015, with a significantly lower primary failure rate in 2015 (26.4 vs. 15.3%, p=.015), and a non-significant increase in radiocephalic AVF, 25.8 vs. 33.2% (n=40 vs. 56), p=.159. The concordance between the indication at the clinic and the surgery performed also increased (81.3 vs. 93.5%, p=.001). Throughout 2015 fewer complementary imaging test were requested from the clinic (78 vs. 35, p <.001), with a corresponding reduction in costs (€87,716 vs. €59,445).
ConclusionsMultidisciplinary approach with routine DU can improve VA results, with a decrease in primary failure rate, higher likelihood of radiocephalic AVF, better management of dis-functioning AVF and lower radiological test costs.
La fístula arteriovenosa autóloga (FAV) es el acceso vascular (AV) de elección en los pacientes en hemodiálisis (HD). Al compararla con los catéteres venosos centrales (CVC) y las fístulas protésicas (PTFE), la FAV se asocia con menor tasa de infección, complicaciones y gasto sanitario, y presenta mayor permeabilidad a largo plazo1–3. Sin embargo, en las últimas décadas, debido al aumento de la edad y comorbilidad de los pacientes en HD, conseguir una FAV funcionante y duradera, que permita obtener una diálisis adecuada, es cada vez más complejo4–8. Se estima que la tasa de fallo primario precoz de la FAV, según la definición del consorcio norteamericano de acceso vascular (NAVAC)5 se sitúa entre el 23-37% y la permeabilidad primaria no asistida a un año se encuentra entre el 40 y el 64%4,6,7. Entre un 21 y un 50% de las FAV realizadas no llegan nunca a madurar lo suficiente para ser utilizadas en HD4,6,7.
Los programas multidisciplinares de creación y seguimiento del AV recomendados en las guías clínicas1–3 pueden mejorar la tasa de fallo primario y la permeabilidad a medio y largo plazo de la FAV8–11. La utilización de la ecografía doppler (ED), tanto en la evaluación preoperatoria como en la posterior vigilancia de la FAV, también ha demostrado importantes beneficios en la supervivencia primaria, asistida y secundaria de la misma12–14.
En este contexto, buscando mejorar los resultados de AV de nuestro centro, pusimos en marcha la consulta multidisciplinar (CMD) de AV del Hospital Gregorio Marañón a principios del año 2015. Se incorporó la evaluación conjunta de los pacientes por parte de los servicios de Cirugía Vascular Periférica (CVP) y Nefrología, y la utilización de la ED de rutina.
El objetivo del presente estudio, de carácter observacional y retrospectivo, es analizar los resultados del AV en el primer año de puesta en marcha de esta CMD y compararlos con el año previo a su inicio.
Material y métodosLa consulta de AV del Hospital General Universitario Gregorio Marañón cubre en la actualidad un área sanitaria de aproximadamente 800.000 habitantes, recibiendo pacientes del Hospital Infanta Leonor de Madrid, el Hospital Universitario del Sureste y dos centros de diálisis externos (FMC- Dialcentro y FMC-Los Enebros). Hasta finales del año 2014 estaba constituida como una consulta monográfica del servicio de CVP. El cirujano/a basaba la indicación de nuevo AV o reparación de FAV en la historia clínica del paciente y la exploración física de miembros superiores.
Desde comienzos del año 2015, se puso en marcha la CMD de AV, que reúne las siguientes características:
- -
Valoración conjunta del paciente por CVP y Nefrología.
- -
Incorporación de un equipo de ED portátil (Logic e-GE) con exploración ecográfica de rutina a todo paciente valorado en la consulta.
- -
Creación de un grupo de 5 cirujanos vasculares subespecializados en realizar intervenciones de reparación y creación de FAV.
- -
Coordinación intensiva con cada uno de los centros de derivación de pacientes, asegurando el flujo de información bidireccional y el consenso en las actuaciones decididas en consulta.
En el mapeo prequirúrgico realizado con ED se ha considerado que para indicar una FAV radiocefálica (RC), la arteria radial debe tener un calibre recomendado mínimo de 1,7mm y una velocidad pico sistólica (VPS) superior a 35cm/sg y la vena cefálica un calibre de al menos 1,8mm medido con compresor2,3,15,16. En cada una de las indicaciones de FAV, se ha especificado la localización más adecuada para la anastomosis, indicando la distancia entre la arteria y la vena y las características anatómicas individuales en cada caso (colaterales, trayecto, profundidad, etc.).
En la valoración de FAV prevalentes, los criterios para intervenir una estenosis se han basado en el cumplimiento de dos criterios principales (reducción del calibre del vaso mayor al 50% y VPS en la región estenótica/VPS región preestenótica >2) y uno adicional (caída del flujo de acceso [QA] por debajo de 500ml/min, caída de QA> 25% respecto al previo en FAV con QA <1000ml/min o diámetro residual <2mm), recogidos en las guías españolas multidisciplinares de AV (GEMAV)3.
Tras el primer año de puesta en marcha de esta CMD evaluamos de forma retrospectiva las características de los pacientes valorados, las intervenciones quirúrgicas realizadas y los resultados obtenidos en términos de tipo de FAV realizada y fallo primario de FAV. El fallo primario se ha definido como una FAV incapaz de proporcionar una diálisis adecuada a los tres meses de su creación5.
El análisis estadístico se ha llevado a cabo mediante el sistema informático SPSS V.21.0. Las variables cualitativas están expresadas en porcentaje y las variables cuantitativas en media y desviación estándar o mediana y rango intercuartil según las características de la variable. La comparación entre grupos se ha realizado mediante el test de la chi-cuadrado o el test de Fisher para variables cualitativas y mediante la t de Student para variables cuantitativas.
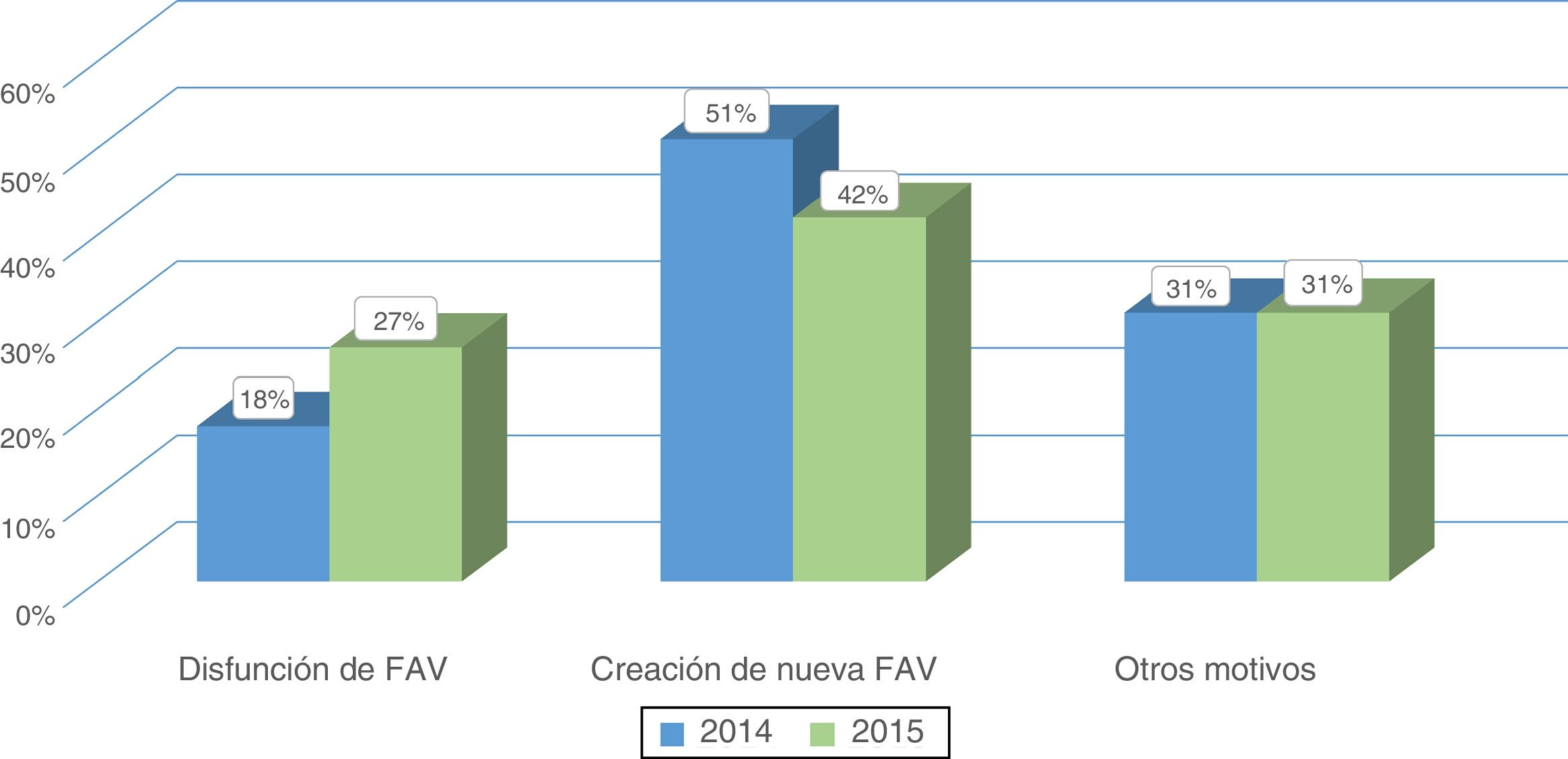
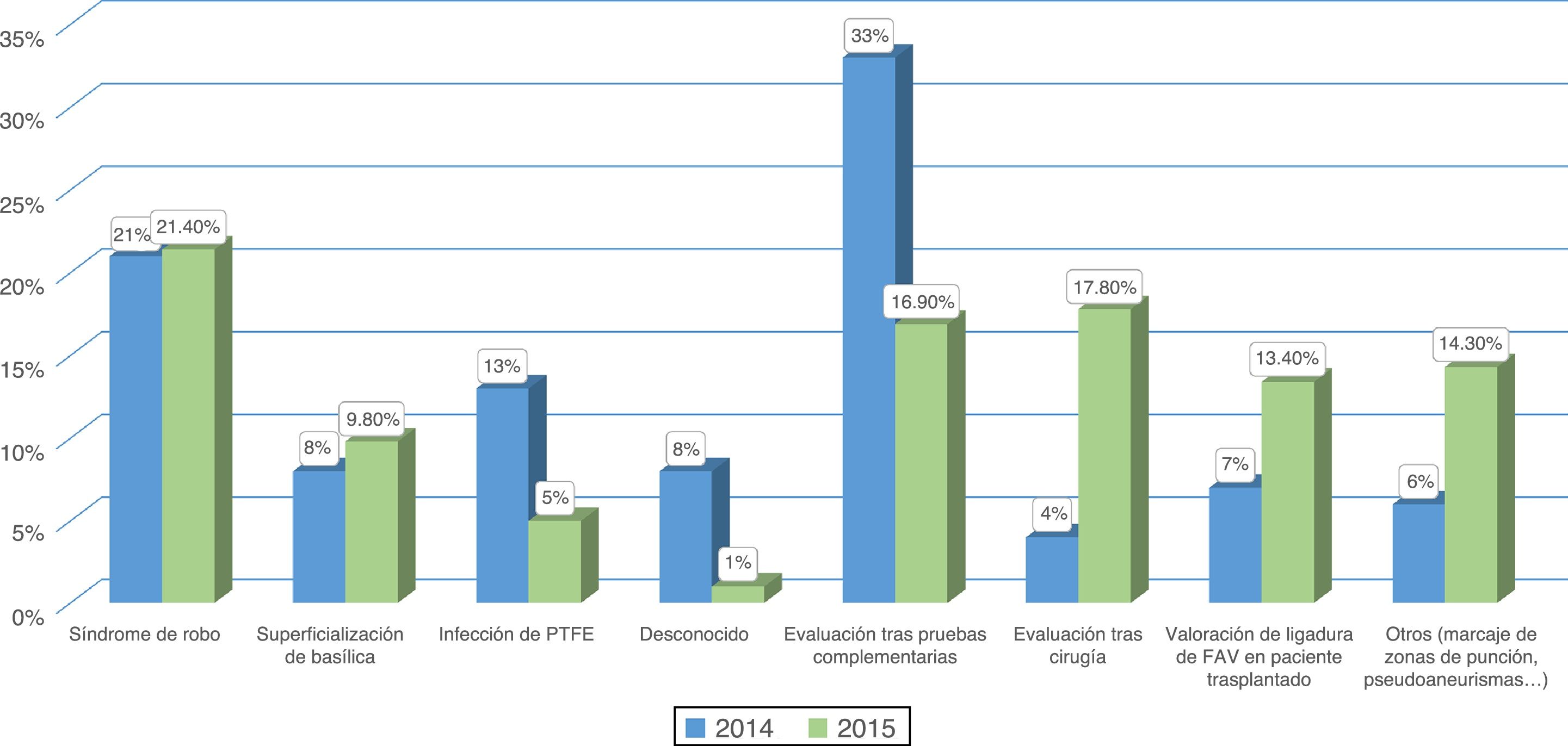
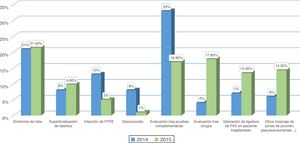
ResultadoPacientes evaluados y motivos de consultaA lo largo de los años 2014 (pre-CMD) y 2015 (CMD) fueron evaluados en la consulta de AV 345 y 364 pacientes respectivamente. Se encontraron diferencias significativas al comparar los motivos de consulta entre ambos periodos (figs. 1 y 2). En el periodo de CMD, un mayor porcentaje de pacientes consultaron por FAV disfuncionante y para valorar el QA tras un procedimiento quirúrgico o intervencionista, a la vez que disminuyó el porcentaje de pacientes que acudieron para ser evaluados tras la realización de pruebas complementarias, por infección de una fístula protésica o por un motivo desconocido.
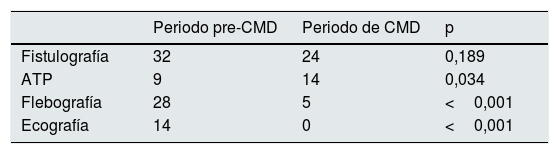
Solicitud de pruebas complementarias (PC) desde la consultaEn el periodo pre-CMD, se solicitaron 78 exploraciones complementarias desde la consulta (22,6% sobre el total de consultas) frente a 35 en el periodo de CMD (9,6% del total), p<0,001. No hubo diferencias significativas en el número de fistulografías realizadas, pero sí en el porcentaje de angioplastias, mayor en el periodo de CMD, p=0,034 (tabla 1). El coste en exploraciones complementarias citadas desde la consulta se redujo de 81.716 € (pre-CMD) a 59.445 € (CMD).
Exploraciones complementarias solicitadas desde la consulta de acceso vascular al servicio de Radiología en ambos periodos
| Periodo pre-CMD | Periodo de CMD | p | |
|---|---|---|---|
| Fistulografía | 32 | 24 | 0,189 |
| ATP | 9 | 14 | 0,034 |
| Flebografía | 28 | 5 | <0,001 |
| Ecografía | 14 | 0 | <0,001 |
ATP: angioplastia transluminal percutánea; CMD: consulta multidisciplinar.
No hubo diferencias significativas en el número total de cirugías realizadas entre ambos periodos, 172 frente a 198 (p=0,289), pero al analizar las cirugías de reparación de FAV, encontramos una tendencia a realizar mayor número de cirugías preventivas de reparación de FAV en elevado riesgo de trombosis en el periodo de CMD, 17 pre-CMD frente a 29 CMD (p=0,098).
También se encontraron diferencias en el tiempo de lista de espera quirúrgica (LEQ) para la intervención, más prolongado en el periodo de CMD, 27 (16-41) días en el periodo pre-CMD, frente a con 48 (27-83) días en el periodo CMD (p<0,001).
Se realizaron 155 FAV nuevas en el periodo pre-CMD (25,8% RC, 58,7% FAV autólogas en codo y 15,5% protésicas) y 169 FAV nuevas en el periodo CMD (33,2% RC, 56,2% FAV autólogas en codo y 10,6% protésicas). Por tanto, en el periodo de CMD, aumentó el porcentaje y el número total de FAV RC realizadas (n=40 vs. 56) con descenso del porcentaje y número de FAV protésicas (n=24 vs. 18), aunque este aumento no alcanzó la significación estadística (p=0,159).
Al analizar la tasa de fallo primario de las FAV de nueva creación, esta tasa se redujo del 26,4% en el periodo pre-CMD a un 15,3% en el periodo de CMD (p=0,015). En el periodo de CMD aumentó además la concordancia entre la cirugía indicada desde la consulta de AV y la cirugía finalmente realizada, siendo de un 81,3% en el periodo pre-CMD frente a 93,5% en el periodo de CMD, p=0,001.
Manejo conservadorEl porcentaje de FAV disfuncionantes en las que se decidió un manejo conservador sin necesidad de solicitar PC ni incluir en LEQ fue similar en ambos periodos, 28,6% (n=18) pre-CMD vs. 23% (n=23) CMD, p=0,425. Sin embargo, en el periodo de CMD, en los 23 pacientes se identificó la causa de la disfunción de la FAV (9 estenosis no significativas, 6 pseudoaneurismas trombosados o parcialmente trombosados y 8 pacientes con peculiaridades anatómicas de profundidad o colateralidad que dificultaban las punciones). En todos ellos se adjuntó un esquema para facilitar las punciones al equipo de enfermería del centro correspondiente y las FAV con estenosis no significativas han sido seguidas de forma trimestral con evaluación periódica del QA. En el periodo pre-CMD, esto no fue posible al no disponer del dispositivo de ED portátil en la consulta.
DiscusiónLa instauración de una consulta multidisciplinar de AV con ecografía doppler ha mejorado los resultados de AV de nuestro centro, tanto en las FAV de nueva creación, con un descenso significativo de la tasa de fallo primario y un incremento no significativo de la realización de FAV distales, como en el manejo de las FAV prevalentes disfuncionantes, con un aumento significativo del número de FAV reparadas endovascularmente y una tendencia a aumentar las FAV reparadas quirúrgicamente por encontrarse en elevado riesgo de trombosis. Todo ello asociado a una reducción de las exploraciones complementarias solicitadas desde la consulta, con el consiguiente ahorro económico.
Las consultas multidisciplinares de AV son de reciente creación y aún disponemos de pocos datos en la literatura. En una encuesta realizada recientemente a 47 expertos de 37 países europeos, en solo el 16% de los casos un equipo multidisciplinar estaba a cargo del seguimiento y evaluación del acceso vascular prevalente, aunque el 62% de los encuestados tenían alguna forma de centralización del cuidado y la planificación del AV17.
Hay evidencias de que un equipo multidisciplinar de AV o la figura de un coordinador de AV, puede mejorar el porcentaje de FAV autólogas, disminuyendo las FAV protésicas y la prevalencia de CVC18–21. Además, el abordaje multidisciplinar del AV, puede mejorar la satisfacción del paciente, los costes y los resultados a medio plazo de permeabilidad del acceso22,23. Sin embargo, no todos los estudios encuentran beneficios con la aparición de equipos multidisciplinares. Recientemente se ha publicado una importante serie de pacientes incidentes donde la creación de un equipo multidisciplinar en la creación y vigilancia de la nueva FAV aumentó el intervencionismo durante el primer año de diálisis sin conseguir una disminución en el tiempo libre de CVC24.
Por otro lado, la ED ha cobrado un importante protagonismo a lo largo de los últimos años hasta situarse como la primera exploración diagnóstica a realizar en caso de disfunción de la FAV y quedando la fistulografía relegada para aquellos casos en los que el resultado de la ED no sea concluyente3.
La presencia de ED en la consulta explica el incremento de pacientes derivados por FAV disfuncionante, ya que no solo ha permitido seleccionar de forma más eficaz aquellos pacientes que precisaban una angioplastia transluminal percutánea o una reparación quirúrgica para evitar la trombosis, sino que también ha permitido dilucidar la causa de la disfunción en aquellas FAV sin estenosis significativas, solucionando fácilmente el problema al modificar las zonas de punción o al aportar información sobre la profundidad de la vena o la presencia y características de venas colaterales.
La ED ha permitido el seguimiento periódico del QA en aquellas fístulas con estenosis sin criterios de intervención y de las FAV reparadas quirúrgica o endovascularmente, ya que sabemos que la medida periódica del QA puede mejorar la supervivencia secundaria de las FAV y reducir el riesgo de trombosis13,14.
La ED además, ha logrado minimizar la solicitud de exploraciones complementarias desde la consulta, limitándolas a aquellos pacientes en los que el ED no fue concluyente, como ante una sospecha de estenosis central, o a los pacientes en los que se detectó una estenosis con criterios de intervención. En manos experimentadas, la ED presenta una excelente correlación con la fistulografía y permite aportar información de gran utilidad sobre la localización y características de la estenosis, facilitando la actuación por parte del equipo de radiología intervencionista25.
Respecto a las FAV de nueva creación, hoy en día se recomienda el mapeo sistemático mediante ED en todos los pacientes3,12, aunque aún no hay consenso sobre los calibres mínimos de arteria y vena para poder indicar una FAV distal con garantías, ya que, hay numerosos factores que influyen en el riesgo de fallo primario2,3,15,26. Por ello, el principal riesgo de aumentar el porcentaje de FAV RC con calibres límites es aumentar a la vez el riesgo de fallo primario, especialmente teniendo en cuenta la avanzada edad, el lecho vascular subóptimo y la importante comorbilidad de nuestros pacientes incidentes y prevalentes en HD5. Sin embargo, en nuestros resultados, gracias en gran parte a la información aportada por la ED y al equipo de CVP subespecializado en creación de FAV, hemos conseguido reducir la tasa de fallo primario y al mismo tiempo realizar más FAV distales, con un porcentaje de fallo primario inferior a la mayoría de las series publicadas4,6,7. La ED ha sido fundamental, no solo para describir los calibres de arteria y vena, la calcificación y VPS de la arteria, sino también para definir el lugar exacto de la anastomosis más favorable, con la distancia entre la arteria y la vena, la presencia de colaterales o las zonas donde la vena es menos compresible, informando al cirujano sobre los eventuales problemas que puede encontrar durante la intervención. Todo ello ha permitido reducir drásticamente los casos de discordancia entre la FAV indicada y la FAV realizada.
El descenso de consultas por infección de fístula protésica disminuyó en el periodo de CMD en probable relación con el menor número de prótesis realizadas y la subespecialización del equipo quirúrgico. La especialización y experiencia del equipo quirúrgico ha demostrado ser uno de los factores clave para reducir la tasa de fallo primario y disminuir el número de complicaciones quirúrgicas15.
Gracias a la coordinación intensiva entre centros se pudieron tomar decisiones consensuadas con los nefrólogos responsables de cada paciente y se minimizó el número de pacientes que acudieron a la consulta por un motivo desconocido. Además, aunque es difícilmente mesurable, la comunicación constante entre CVP y nefrología ha permitido integrar información clínica y quirúrgica, de tal forma que las decisiones tomadas en la CMD (paciente candidato o no a FAV, FAV más adecuada en cada paciente, prioridad de cada caso en la LEQ, etc.), se han realizado de forma consensuada.
Entre las limitaciones de este estudio cabe señalar que se trata de una experiencia de un solo centro y la recogida de datos ha sido retrospectiva.
Basándonos en nuestra experiencia, podemos concluir que el abordaje multidisciplinar en la consulta de AV con ED de rutina supone importantes beneficios para el paciente con menor riesgo de fallo primario de FAV de nueva creación, más opciones de realización de FAV distal nativa y mayor eficacia en el manejo de la FAV prevalente disfuncionante. Además, permite a la vez minimizar y optimizar las exploraciones complementarias, con disminución del coste sanitario en fistulografías y flebografías. Aunque los datos son esperanzadores y coinciden con la mayoría de series publicadas aún disponemos de poca información y son necesarios más estudios para conocer el impacto real que pueden tener los equipos multidisciplinares sobre los resultados de creación y permeabilidad de FAV, calidad de vida de nuestros pacientes y coste sanitario.
FinanciaciónIsciii Retic Redinren Rd016/009 Fondos Feder.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.