Se ha descrito que el nivel circulante del receptor soluble de la uroquinasa (suPAR) podría ser útil para diferenciar la glomeruloesclerosis focal y segmentaria idiopática de las formas secundarias, pero los resultados publicados son discordantes. En el presente estudio, se analiza la variabilidad intraindividual, las variables clínicas y anatomopatológicas asociadas con los niveles de suPAR y si los niveles circulantes de suPAR permiten diferenciar las formas de glomeruloesclerosis focal y segmentaria (GFS) idiopáticas de las GFS secundarias, independientemente de la presencia de síndrome nefrótico y de la fase de actividad. Métodos: Se estudiaron 35 pacientes afectos de GFS idiopática y 48 con GFS secundaria (83 en total). Se realizaron mediciones de suPAR circulante en el momento del diagnóstico y/o tras la remisión y se analizaron las correlaciones entre niveles de suPAR y variables demográficas, clínicas y bioquímicas. La capacidad de suPAR para diferenciar entre ambas formas de GFS se analizó mediante curvas ROC y análisis de regresión logística. Resultados: En ambas formas de GFS, los niveles de suPAR fueron independientes de la proteinuria y del subtipo histopatológico de GFS y se asociaron significativamente a la edad y a la función renal. Tras ajustar por ambas variables, los niveles de suPAR fueron significativamente superiores en los enfermos con GFS idiopática, tanto en fase de síndrome nefrótico como en situación de remisión parcial o total. El nivel de suPAR con mayor sensibilidad (80 %) y mayor especificidad (73 %) para discriminar entre formas idiopáticas y secundarias fue de 3443,6 pg/ml (área bajo la curva [ABC] 0,78 ± 0,083, p < 0,001). En el análisis de regresión logística, tras ajustar por edad, función renal y presencia de síndrome nefrótico, los niveles de suPAR se asociaron de forma independiente con el diagnóstico de GFS idiopática, pero el modelo tuvo un mal ajuste para categorías de riesgo bajas, en las que tendió a clasificar las formas primarias como secundarias (χ 2 = 11,2 p = 0,027). Conclusiones: Los niveles de suPAR carecen de sensibilidad para diferenciar entre GFS idiopática y secundaria. Sin embargo, valores de suPAR superiores a 4000 ng/ml son altamente específicos de GFS primaria, por lo que, ante un patrón morfológico de GFS asociado a proteinuria no nefrótica, indicarían una baja probabilidad de GFS secundaria.
Background: It has been reported that the circulating level of the soluble urokinase receptor (suPAR) could be useful for distinguishing idiopathic from secondary focal segmental glomerulosclerosis, but the results published are conflicting. In this study, we analyse the intraindividual variability and clinical and anatomopathological variables associated with the suPAR levels and if circulating suPAR levels allow the different forms of focal segmental glomerulosclerosis (FSGS) to be distinguished, i.e., idiopathic forms from secondary FSGS, regardless of the presence of nephrotic syndrome and the activity phase. Method: We studied 35 patients affected by idiopathic FSGS and 48 with secondary FSGS (83 in total). We carried out measurements of circulating suPAR at the time of diagnosis and/or after remission and we analysed correlations between suPAR levels and demographic, clinical and biochemical variables. The ability of suPAR to distinguish between both forms of FSGS was analysed by ROC curves and logistic regression analysis. Results: In both forms of FSGS, suPAR levels were independent of proteinuria and the histopathological subtype of FSGS and they were significantly associated with age and renal function. After adjusting for both variables, suPAR levels were significantly higher in patients with idiopathic FSGS, both in the nephrotic syndrome phase and in partial or complete remission. The most sensitive suPAR level (80%) and the most specific (73%) for discriminating between idiopathic and secondary forms was 3443.6pg/ml (area below curve [ABC] 0.78±0.083, P<.001). In the logistic regression analysis, after adjusting for age, renal function and presence of nephrotic syndrome, suPAR levels were independently associated with the diagnosis of idiopathic FSGS, but the model was poorly adjusted for low risk categories in which it tended to classify primary forms as secondary forms (χ 2 = 11.2 p=.027). Conclusions: SuPAR levels lack sensitivity for differentiating between idiopathic and secondary FSGS. However, suPAR values greater than 4000ng/ml are highly specific to primary FSGS, and as such, with a morphological FSGS pattern associated with non-nephrotic proteinuria, they would indicate a low probability of secondary FSGS.
INTRODUCCIÓN
La glomeruloesclerosis focal y segmentaria (GFS) es una enfermedad glomerular con múltiples posibles etiologías y patogenias1. Se clasifica en idiopática o secundaria en función de si se identifica o no una etiología responsable de esta2. Distinguir entre formas idiopáticas y secundarias tiene interés terapéutico y pronóstico, dado que en las guías de tratamiento solo los enfermos con formas idiopáticas que cursan con síndrome nefrótico son considerados candidatos a tratamiento inmunosupresor3. La diferenciación entre ambas se basa en el perfil clínico y el examen ultraestructural renal mediante microscopía electrónica4,5. Esta clasificación está basada exclusivamente en criterios clínicos y morfológicos y tiene connotaciones arbitrarias, ya que no incluye ningún aspecto relacionado con la patogenia.
La GFS idiopática puede cursar en forma de brotes, por lo que, si en el momento del diagnóstico hay proteinuria pero no síndrome nefrótico clínico, es difícil determinar si se trata de una forma idiopática en remisión parcial o bien de una forma secundaria para la que no se ha identificado una etiología concreta. Esta diferenciación tiene importancia pronóstica, ya que en el primer caso el paciente puede sufrir nuevos brotes de actividad sensibles a inmunomodulación con posibilidad de recidiva tras el trasplante, mientras que en el segundo esta no es la evolución esperable6,7. En las formas idiopáticas, existe la hipótesis de que la lesión podocitaria es producida por un factor o factores circulantes8-10. En un estudio reciente11, se ha identificado el receptor soluble de la uroquinasa (suPAR) como un posible factor soluble responsable de la lesión podocitaria, se ha descrito un modelo patogénico relacionado con suPAR y se ha propuesto que un nivel sérico superior a 3000 pg/ml11 podría ser un biomarcador sensible y específico para diferenciar la GFS idiopática de otras enfermedades causantes de síndrome nefrótico. Por ello, el nivel de suPAR podría ser útil para diferenciar entre formas de GFS idiopáticas y secundarias. En dicho estudio, sin embargo, se apreció una elevada dispersión en los niveles de suPAR y se incluyeron enfermos con niveles de proteinuria no nefrótica o en los que no se pudo disponer de los niveles de albumina sérica o de los datos de la biopsia renal. Por estas razones, existe la posibilidad de que el grupo de enfermos con GFS incluyera tanto formas idiopáticas con síndrome nefrótico como formas secundarias con proteinuria no nefrótica o enfermos con formas idiopáticas en remisión parcial.
Los resultados de este estudio son difícilmente extrapolables a estudios realizados con criterios de clasificación distintos y, hasta la fecha, aunque algunos datos confirman que los niveles de suPAR son más elevados en los enfermos con GFS idiopática con relación a otras nefropatías12, otros no confirman estos resultados13 y tampoco hay constancia de que, en enfermos con GFS secundaria, los niveles de suPAR sean independientes de la causa responsable de esta. Por otra parte, los datos sobre la relación entre niveles de suPAR y actividad de la enfermedad en la GFS son escasos y controvertidos y se dispone de poca información sobre los niveles de suPAR en enfermos con GFS que se hallan en remisión total o parcial14. Además, los datos descritos en los distintos estudios publicados hasta la fecha se basan en una única determinación de los niveles de suPAR, por lo que no se dispone de información acerca de la variabilidad de los valores cuando se miden en un mismo individuo en períodos de tiempo distintos, sin que cambien las características clínicas de la enfermedad.
Los objetivos del presente estudio, son: 1) Analizar las variables clínicas, bioquímicas y anatomopatológicas asociadas a los niveles circulantes de suPAR en enfermos con GFS idiopática y secundaria. 2) Analizar si, en los enfermos con GFS secundaria, los niveles de suPAR difieren en función de la etiología de esta. 3) Analizar la variabilidad de los niveles de suPAR cuando se determinan en un mismo individuo, sin que haya cambios en el perfil clínico de la enfermedad. 4) Analizar si los niveles circulantes de suPAR permiten diferenciar las formas de GFS idiopáticas de las GFS secundarias, independientemente de la presencia de síndrome nefrótico y de la fase de actividad.
MATERIALES Y MÉTODOS
Se trata de un estudio observacional de corte transversal donde se comparan grupos de pacientes con diagnóstico de GFS primaria y secundaria.
Muestra
Se estudiaron 35 pacientes diagnosticados de GFS idiopática y 48 pacientes con GFS secundaria. El diagnóstico se realizó por biopsia renal y criterios clínicos. Los enfermos fueron clasificados como formas idiopáticas solo si cumplían todos los criterios que se detallan a continuación: 1) Diagnóstico histológico de glomeruloesclerosis focal y segmentaria con evidencia de borramiento difuso de podocitos en microscopía electrónica. 2) Presencia de síndrome nefrótico clínico en el momento en el que se realizó el diagnóstico. 3) Exclusión de etiologías secundarias, incluyendo: reducción de masa renal, obesidad mórbida, nefropatía asociada a virus de la inmunodeficiencia humana, consumo de heroína o cocaína, consumo de analgésicos, reflujo vésico-ureteral y apnea obstructiva del sueño. 4) Ausencia de antecedentes familiares de enfermedad renal crónica o tratamiento sustitutivo renal. 5) En enfermos menores de 30 años (n = 4), ausencia de mutaciones demostrables en NPHS2.
El diagnóstico de GFS secundaria se realizó ante la evidencia de proteinuria sin síndrome nefrótico clínico, lesiones de GFS en la biopsia renal, borramiento no difuso de los podocitos en la microscopía electrónica y evidencia de una etiología responsable.
En el momento de obtener las muestras de sangre para la medición de los niveles de suPAR, se registraron las variables demográficas, clínicas y bioquímicas de los enfermos. La creatinina sérica se midió mediante un método compensado IDMS trazable (Hitachi Modular P-800 Roche Diagnostics, Germany). El filtrado glomerular estimado (eGFR) se calculó mediante la fórmula CKD-EPI15. Las determinaciones de los niveles de suPAR se realizaron en muestras de suero utilizando un ELISA comercial (Human uPAR Quantikine® ELISA kit; R&D Systems, Minneapolis, MN, USA; variabilidad intraensayo: 4,1 %-7,5 %; variabilidad interensayo: 5,1-5,9 %)11. Para analizar la reproductibilidad de las medidas, en 11 de los 20 enfermos que fueron estudiados en el momento del diagnóstico, se realizaron tres o más determinaciones de suPAR durante la fase nefrótica previa al inicio del tratamiento.
Análisis anatomopatológico de las biopsias renales
Las biopsias fueron teñidas con hematoxilina-eosina, PAS (ácido peryódico de Schiff)-metenamina y tricrómico de Masson para análisis morfológico y se realizaron estudios de inmunofluorescencia con anticuerpos frente a IgA, IgG, IgM, C3, fibrinógeno y cadenas ligeras y procesadas para estudio con microscopía electrónica. Las lesiones de GFS fueron clasificadas según los criterios de D’Agati et al.16.
Análisis estadístico
Las variables cuantitativas se expresan como la media ± 1 desviación estándar y las cualitativas como proporción. Las comparaciones de medias entre grupos se realizaron mediante el análisis de la varianza para más de dos grupos o la t de Student para datos independientes y, entre proporciones, mediante la prueba de χ2 o el test exacto de Fisher. La correlación entre variables cuantitativas se analizó mediante el coeficiente de correlación de Pearson. La variabilidad intraindividual tras mediciones repetidas de los valores de suPAR se calculó mediante el coeficiente de variación de Pearson. Para identificar las variables independientemente asociadas con los valores séricos de suPAR, se realizó un análisis univariado y, posteriormente, un análisis de regresión múltiple paso a paso considerando como variable dependiente el nivel de suPAR circulante. La sensibilidad y la especificidad de los niveles de suPAR para identificar a los pacientes con GFS idiopática se analizó mediante curvas ROC. Posteriormente, se realizó un análisis de regresión logística paso a paso para identificar los predictores independientes del diagnóstico de GFS idiopática y se analizó la capacidad discriminativa de este por categorías de riesgo, mediante la prueba de Hosmer-Lemeshow17. Se consideró significativo todo valor de p < 0,05. Los cálculos estadísticos se realizaron utilizando el programa SPSS versión 20.0.
Definiciones
Se consideró proteinuria de rango nefrótico todo valor > 3,5 g/día. El síndrome nefrótico se definió como proteinuria > 3,5 g/día asociada con hipoalbuminemia < 3,5 g/dl. Remisión completa: proteinuria < 0,3 g/día en dos controles consecutivos. Remisión parcial: proteinuria < 3,5 g/día y > 0,3 g/día.
El estudio cumplió la normativa contemplada en la Declaración de Helsinki y fue aprobado por el comité ético del hospital.
RESULTADOS
Fueron incluidos en el estudio 83 pacientes con GFS, 42,2 % (n = 35) tenían GFS primaria y 57,8 % (n = 48) secundaria. En ambos grupos se observó un número mayor de varones, siendo significativo en el caso de los pacientes con GFS secundaria. En 20 de los enfermos con GFS idiopática, las determinaciones del nivel de suPAR se realizaron durante la fase de síndrome nefrótico antes de recibir ningún tratamiento y en 15 en situación de remisión total (n = 2) o parcial (n = 13) tras haber finalizado el tratamiento inmunosupresor (estos 15 enfermos presentaban síndrome nefrótico en el momento del diagnóstico y recibieron tratamiento con esteroides n = 15, anticalcineurínicos n = 11 y micofenolato mofetilo n = 5). El grupo de 48 enfermos con GFS secundaria incluyó 6 enfermos con obesidad mórbida, 12 enfermos con nefropatía crónica por reflujo, 11 enfermos con GFS asociada a reducción de parénquima renal, 4 enfermos con historia de consumo prolongado de antiinflamatorios no esteroideos y otros analgésicos y 15 enfermos con lesiones de glomeruloesclerosis asociadas a arteriolo-nefroangioesclerosis.
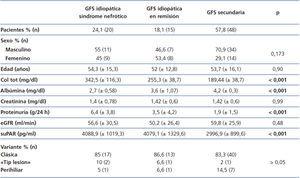
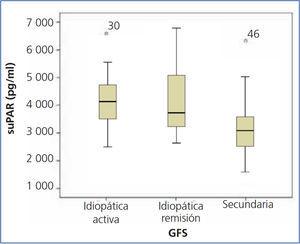
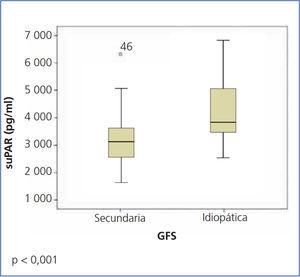
En la tabla 1, se resumen las características clínicas y demográficas de los enfermos estudiados. No hubo diferencias en cuanto a la edad, creatinina o filtrado glomerular entre grupos. Los enfermos con GFS estudiados durante la fase de síndrome nefrótico presentaron valores de colesterol total y LDL significativamente más altos, valores inferiores de albúmina y mayor proteinuria en comparación con los otros dos grupos de enfermos. Los niveles de suPAR circulante fueron significativamente más altos en los pacientes con GFS idiopática, tanto en fase nefrótica como en remisión total o parcial, que en los enfermos con GFS secundaria (tabla 1 y figura 1). No se apreciaron diferencias significativas entre GFS idiopática en fase de síndrome nefrótico y en remisión (tabla 1 y figura 2). En el grupo de 15 enfermos en los que el nivel de suPAR se midió tras la remisión del síndrome nefrótico, no se apreciaron diferencias entre enfermos en remisión total (n = 6) o parcial (n = 9) (3745,3 ± 661,3 vs. 3642,1 ± 1056,9 pg/ml, p = 0,48).
La variante histológica de GFS observada con más frecuencia en los tres grupos fue la clásica y no se asoció significativamente con los valores séricos de suPAR (tabla 1).
Analizando los valores se suPAR en muestras tomadas a un mismo paciente en momentos diferentes, se observó una variación intraindividual igual o menor a 11 %.
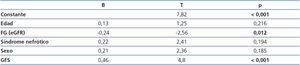
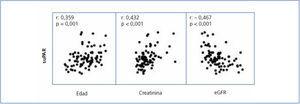
Al analizar las variables asociadas a niveles de suPAR en el conjunto de la muestra estudiada, se observó que, además de estar relacionados con la forma de GFS, los niveles de suPAR se asociaron significativamente con la edad (r = 0,36, p = 0,02) y la función renal (creatinina y eGFR) (r = 0,432, y r = –0,467, p ≤ 0,001; respectivamente) (figura 3). En el análisis de regresión múltiple se apreció que, tras ajustar por edad y filtrado glomerular, el diagnóstico de GFS idiopática fue un predictor independiente de los niveles de suPAR. En conjunto, el modelo explicó el 39 % en la variabilidad de estos (tabla 2). No se apreció asociación entre niveles de suPAR y ninguna de las características clínicas o bioquímicas de la enfermedad en el momento del diagnóstico (datos no mostrados). Al analizar las variables relacionadas con los niveles de suPAR en enfermos con GFS secundaria, la edad y el filtrado glomerular se identificaron como únicos predictores independientes, explicando un 32 % en la variabilidad de estos. No se apreció asociación significativa entre niveles de suPAR y la etiología de la GFS secundaria.
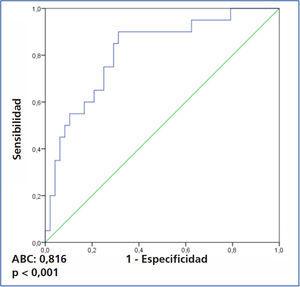
En el análisis mediante curvas ROC, incluyendo a todos los enfermos, se apreció que el valor de suPAR con mayor sensibilidad (85 %) y mayor especificidad (71 %) para discriminar entre formas primarias y secundarias fue de 3336,9 pg/ml (área bajo la curva [ABC] 0,81 ± 0,056, p <0,001) (figura 4).
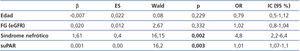
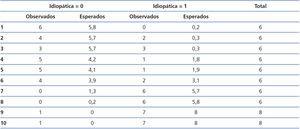
En el modelo logístico (tabla 3), las variables independientemente asociadas al diagnóstico de GFS idiopática fueron la presencia de síndrome nefrótico clínico y el nivel de suPAR circulante. En conjunto, el modelo logístico ajustado por edad y función renal tuvo mayor capacidad predictiva que sin ajustar por dichas variables (ABC: 0,81 ± 0,068 vs. 0,74 ± 0,134 [p = 0,034]). El modelo, sin embargo, no tuvo un buen ajuste para todas las categorías de riesgo (χ2: 11,2 p = 0,027). En las categorías de riesgo altas, las diferencias entre casos observados y esperados no fueron estadísticamente significativas, mientras que en las categorías de riesgo bajas el modelo tuvo una tendencia significativa a clasificar las formas idiopáticas como secundarias (tabla 4). La capacidad de suPAR para diferenciar entre formas idiopáticas y secundarias de GFS fue similar tanto cuando en el análisis se incluyeron los 15 enfermos afectos de GFS secundaria a arteriolo-nefroangioesclerosis como cuando este subgrupo fue excluido del análisis.
DISCUSIÓN
Los resultados de nuestro estudio aportan los siguientes datos de interés acerca de la utilidad clínica de la determinación de suPAR en enfermos con GFS: en primer lugar, demuestran que los niveles de suPAR, cuando se miden por enzimo-inmunoanálisis en un mismo individuo en repetidas ocasiones, sin que cambien las características clínicas de la enfermedad, tienen variaciones intraindividuales no superiores al 11 %, lo que indica que las medidas son fiables y reproducibles, y que cambios superiores a estos valores no pueden ser atribuibles a la técnica de medida. En segundo lugar, estos datos contribuyen a poner en evidencia la existencia de notables diferencias en los niveles de suPAR en distintos grupos de enfermos con GFS. Los valores de suPAR observados en el grupo de enfermos con GFS idiopática son similares a los descritos por Wei et al.14. Sin embargo, tanto los valores medios observados en nuestros enfermos como los descritos por Wei14 son superiores a los descritos por Huang et al.12. Estas diferencias en los niveles absolutos entre estudios podrían ser debidas a aspectos relacionados con la falta de estandarización de las técnicas de medida, distintos criterios de clasificación entre formas idiopáticas y secundarias, o a posibles influencias étnicas en la distribución de los niveles de suPAR que ya han sido objetivadas en estudios previos13 y requerirían ser analizadas en estudios más amplios en los que se incluyeran enfermos de distintas etnias. En tercer lugar, nuestros datos indican que, en enfermos con GFS tanto idiopática como secundaria, los niveles de suPAR son independientes de la proteinuria y de la forma anatomo-patológica de GFS, pero están significativamente asociados con la edad y la función renal. Por ello, ambas variables deben ser tenidas en consideración al analizar el posible valor de los niveles de suPAR para discriminar entre formas de GFS idiopáticas y secundarias. La relación entre niveles de suPAR, edad y filtrado glomerular coincide con la descrita hasta la fecha en todos los estudios previos que se han publicado12-14. Tras ajustar por ambas variables en el análisis multivariado, nuestros datos coinciden con los publicados en estudios previos12,14 e indican que el nivel de suPAR es significativamente superior en los enfermos con GFS idiopática que en las formas consideradas secundarias. El cuarto aspecto de interés de nuestro estudio hace referencia a la relación entre niveles de suPAR y actividad de la enfermedad en enfermos con GFS idiopática. Los datos publicados hasta el momento indican que, en la GFS de riñón nativo, los cambios relativos en los niveles de suPAR son predictores independientes de la probabilidad de obtener una remisión completa tras el tratamiento, después de ajustar por edad, sexo, etnia, filtrado glomerular y niveles de suPAR basal. Por otra parte, se ha descrito que, en los enfermos que entran en remisión tras el tratamiento, el aumento en los niveles de suPAR tras la remisión se asocia a mayor riesgo de reaparición de la proteinuria14.
Nuestros resultados, al carecer de seguimiento evolutivo, no aportan nuevos datos a los previamente publicados sobre la relación entre niveles y actividad, pero indican que, independientemente de la fase en la que se midan, los niveles circulantes de suPAR son significativamente superiores en la GFS idiopática que en las formas secundarias. Como prueba de ello, en el análisis de regresión logística, el nivel de suPAR circulante se asocia al diagnóstico de GFS idiopática independientemente de la presencia de síndrome nefrótico. Aunque en el análisis univariado no se apreciaron diferencias significativas en edad o función renal entre formas idiopáticas y secundarias, considerando que ambas variables tuvieron una asociación significativa con los niveles de suPAR, se introdujeron en el análisis de regresión logística como posibles variables de confusión. En conjunto, el modelo logístico ajustado por edad y función renal tuvo mayor capacidad predictiva que sin ajustar por dichas variables, pero solo tuvo un buen ajuste para las categorías de riesgo altas. En las categorías de riesgo bajas, representadas por ausencia de síndrome nefrótico, valores de suPAR bajos y filtrado glomerular alto, el modelo tuvo una tendencia significativa a clasificar las formas idiopáticas como secundarias. Estos datos se explican por la gran superposición de valores entre grupos debida fundamentalmente al elevado número de enfermos con GFS idiopáticas que presentan niveles de suPAR bajos y, en conjunto, coinciden con los descritos por Huang et al. recientemente12.
Aunque la sensibilidad de suPAR para diferenciar entre formas idiopáticas y secundarias es baja, nuestros datos indican que valores superiores a 3800 ng/ml son infrecuentes en GFS secundarias y altamente específicos de GFS idiopática, por lo que, ante un patrón morfológico de GFS asociado a proteinuria no nefrótica, valores superiores a esta cifra podrían indicar una baja probabilidad de GFS secundaria.
Este estudio tiene como limitación principal el tamaño de la muestra estudiada. Sin embargo, dada la gran superposición de valores que se aprecia a bajas concentraciones de suPAR entre GFS idiopática y secundaria, parece incuestionable que, aun incrementando el número de enfermos estudiado, un valor bajo de suPAR no permitiría excluir el diagnóstico de GFS idiopática. Otra limitación a tener en cuenta es el posible error de clasificación entre GFS idiopática y secundaria. Los criterios de selección utilizados en el presente estudio minimizan pero no excluyen la posibilidad de que enfermos con GFS idiopática hayan sido clasificados como formas secundarias, ya que en todos los casos se investigó sistemáticamente la presencia de las etiologías responsables actualmente conocidas, y en todos los enfermos que fueron estudiados en fase de remisión total o parcial hay constancia de la presencia de síndrome nefrótico previo y de la respuesta favorable al tratamiento. Sin embargo, dentro del grupo de enfermos inicialmente catalogados como formas secundarias, no es posible descartar que alguno presentara una GFS idiopática en situación de remisión parcial. Siendo conscientes de esta limitación, consideramos que es poco probable que este hecho conlleve un error sistemático que tenga una influencia relevante en los resultados.
En resumen, nuestros datos indican que la medición de los niveles circulantes de suPAR en enfermos con GFS proporciona resultados fiables y reproducibles. Tanto en la GFS idiopática como en las secundarias, los niveles de suPAR son independientes de la proteinuria y del subtipo histopatológico de GFS y se asocian significativamente a la edad y a la función renal. Tras ajustar por ambas variables, los enfermos con GFS idiopática presentan niveles de suPAR significativamente superiores a los de los enfermos con GFS secundarias, tanto en fase de síndrome nefrótico como en situación de remisión parcial o total. La gran superposición de valores entre formas primarias y secundarias motiva que los valores de suPAR no proporcionen una información útil en la práctica clínica para diferenciar entre ambas entidades. Sin embargo, ante un patrón morfológico de GFS asociado a proteinuria nefrótica, valores de suPAR superiores a 3800 ng/ml podrían indicar una baja probabilidad de GFS secundaria.
Conflictos de interés
Los autores declaran que no tienen conflictos de interés potenciales relacionados con los contenidos de este artículo.
Tabla 1. Variables clínico-demográficas según grupos de pacientes
Tabla 2. Predictores independientes de la variabilidad en los niveles de suPAR circulante en el análisis de regresión múltiple ajustado por edad, síndrome nefrótico y sexo
Tabla 3. Modelo de regresión logística para predecir diagnóstico de glomeruloesclerosis focal y segmentaria idiopática
Tabla 4. Análisis de la capacidad discriminativa del modelo logístico según categorías de riesgo mediante prueba de Hosmer-Lemeshow
Figura 2. Valores de receptor soluble de la uroquinasa en glomeruloesclerosis focal y segmentaria idiopática activa, en remisión y secundaria
Figura 3. Correlación receptor soluble de la uroquinasa con edad, creatinia sérica y filtrado glomerular estimado
Figura 4. Curva ROC para diferenciar entre glomeruloesclerosis focal y segmentaria idiopática y secundaria
Figura 1. Valores de receptor soluble de la uroquinasa en glomeruloesclerosis focal y segmentaria idiopática y secundaria