Los inhibidores de la bomba de protones (IBP) utilizados, entre otros, en el tratamiento de la dispepsia, úlcera péptica, reflujo gastroesofágico, así como para la prevención de gastropatía derivada del uso de los AINE, son por lo general bien tolerados y con escasos efectos secundarios, lo que les hace encontrarse entre los medicamentos más prescritos. Presentamos el caso de una paciente, quien tras la ingesta de IBP desarrolla una nefritis intersticial aguda (NIA).
Mujer de 31 años sin antecedentes médicos de interés que inicia tratamiento con omeprazol por dolor a nivel epigástrico. Dos días después, la analítica objetiva deterioro de la función renal (Cr 2,28mg/dl y FG 27ml/min). Tras una semana de tratamiento, se produce un empeoramiento (Cr 2,75mg/dl y FG 22ml/min), acordándose la suspensión del omeprazol. En pruebas complementarias destacó en elemental y sedimento la presencia de proteinuria+ y leucocituria++ (10-15/campo). Ante el empeoramiento progresivo de la función renal, hasta una Cr de 3mg/dl, se decidió la realización de biopsia renal, en la cual se objetivó: 21 glomérulos sin esclerosis, intersticio con edema e infiltrado masivo por linfocitos y numerosos eosinófilos, y ausencia de granulomas o fenómenos de vasculitis. El C4d reveló tinción extensa en capilares peritubulares. Ante estos hallazgos se inició tratamiento con prednisona vía oral a dosis de 1mg/kg durante 10 días, iniciándose posteriormente pauta descendente de corticoides hasta su completa suspensión 6 meses después. Ante sospecha de nefropatía intersticial secundaria a omeprazol se realizó test de activación de basófilos (TAB) mostrando este a 10μg/ml un porcentaje de activación del 10,2% y un índice de estimulación de 4,1, confirmándose así la sospecha diagnóstica.
La NIA inducida por fármacos es causa frecuente de insuficiencia renal aguda (IRA), caracterizada por la presencia de infiltrados inflamatorios y edema en el intersticio, tubulitis, y en algunos casos, fibrosis intersticial eventual, habiéndose constatado que tras la retirada del fármaco inductor entre un 30-70% de los pacientes no recuperan en su totalidad su función renal basal, quedando con algún grado de insuficiencia renal, pudiendo evolucionar a enfermedad renal crónica (ERC) y muerte1,2. La NIA se halla presente entre el 1-3% de las biopsias practicadas para la evaluación de hematuria o proteinuria, y aproximadamente en un 15% de las practicadas a pacientes con IRA, si bien su incidencia real puede ser superior, especialmente entre pacientes mayores de 65 años, en muchos casos polimedicados con mezclas de antibióticos y de AINE3–5. La incidencia a causa de los IBP es relativamente escasa, aunque su uso masivo y en ocasiones sin justificación, motiva que se haya incrementado en los últimos años. El hecho de que la NIA ocurra solamente en un pequeño porcentaje de pacientes expuestos a un determinado medicamento, la ausencia de una relación dosis/dependiente, la asociación a manifestaciones extrarrenales de hipersensibilidad y la recurrencia ante nuevas tomas de medicamento sugieren una base inmunológica como causa etiológica de la NIA4, lo que ha originado el uso de corticoides para su tratamiento.
Los basófilos son las células típicas para el estudio in vitro de reacciones alérgicas. Constituyen una pequeña fracción de leucocitos totales (<0,3%) y al igual que los mastocitos expresan en su superficie receptores IgE de alta afinidad a los que se une la IgE específica que en contacto con el alérgeno provoca la activación del basófilo y la posterior liberación de diversas citocinas y mediadores de reacciones inflamatorias que son los responsables de la sintomatología de las reacciones alérgicas.
El TAB, con el soporte de la citometría de flujo para la determinación cuantitativa de la degranulación de basófilos, constituye un método complementario para el diagnóstico de alergias a medicamentos especialmente para fármacos nuevos o no detectables mediante técnicas serológicas, tales como la determinación de la IgE específica, permitiendo eludir en muchos casos, la realización de la prueba de exposición al alérgeno y a diferencia de otros procedimientos, permite la evaluación simultánea de varios fármacos6,7.
En nuestro caso destacó la pronta aparición de las manifestaciones de daño renal y el rápido agravamiento de la IRA. Las claves del diagnóstico se basaron en un alto nivel de sospecha clínica ante una IRA de origen desconocido, con leucocituria asociada y la exposición a un conocido fármaco inductor de reacciones alérgicas de hipersensibilidad. La rápida descontinuación de la exposición al fármaco y la favorable respuesta a los corticoides constituyeron la clave de la recuperación de la función renal de la paciente. Los resultados del TAB resultaron concluyentes. Con un porcentaje de activación superior al 5% y un índice de estimulación superior a 2, quedó confirmada la sospecha fundada sobre el agente inductor (fig. 1).
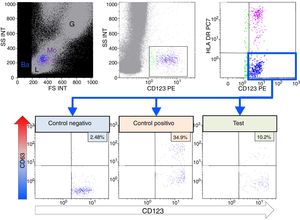
Test de activación de basófilos. Mediante citometría de flujo se pueden diferenciar las diferentes subpoblaciones leucocitarias: linfocitos (L), monocitos (Mo), granulocitos (G), mediante tamaño o forward scatter (FS) y complejidad o side scatter (SS). Los basófilos (Ba) en azul, se identifican mediante la expresión del receptor de la IL-3 (CD123) y ausencia de expresión de HLA-DR. Para evaluar la degranulación de los basófilos, se mide el % de expresión de CD63, en ausencia de estímulo (Control Negativo), tras activación con fMLP y al incubar con omeprazol. El índice de estimulación se calcula con el cociente entre el %CD63 del test y el %CD63 del control negativo.
Concluimos que ante una IRA inexplicable y una exposición a IBP, incluso sin presencia de eosinofiluria y piuria, los médicos no deben excluir el riesgo de NIA, así como desalentar el uso indiscriminado de estos medicamentos. Los TAB, constituyen herramientas útiles para la identificación de fármacos inductores de NIA.