En los últimos años el tratamiento con anticuerpos monoclonales ha aumentado de forma exponencial, adquiriendo especial importancia en aquellos pacientes con enfermedades de etiología autoinmune que son refractarios a la terapia estándar. El empleo de estos fármacos biológicos ha depositado una gran esperanza en este grupo de pacientes, ya que han demostrado resultados prometedores. El gran inconveniente de los mismos actualmente es el desconocimiento de sus posibles efectos secundarios, debido principalmente al inicio muy reciente de su uso y, por tanto, a la limitada experiencia tanto a corto como a largo plazo.
Un ejemplo de empleo de estos tratamientos en el campo de la Dermatología es en la psoriasis1, donde los más utilizados son adalimumab (Humira®) y ustekinumab (Stelara®)2–4. Este último es un anticuerpo IgG1 kappa, que actúa a través de su unión específica a la subunidad p40 de las interleucinas 12 y 23, evitando así la interacción de dichas interleucinas con su receptor; con ello se consigue bloquear la vía de activación de las células natural killer y los linfocitos T, además de impedir la diferenciación de las células T CD4+ a células Th1 (linfocitos helper)5,6.
Tras revisar la literatura no hemos encontrado asociaciones de este tratamiento con síndrome nefrótico, por lo que consideramos de interés esta revisión.
Presentamos el caso de un varón de 51 años, dislipidémico en tratamiento con estatinas y antecedente de litiasis renal izquierda en la juventud, en seguimiento por Dermatología por psoriasis en placas que afectaban predominantemente a los miembros superiores, el tronco y el cuero cabelludo. Con respecto a este diagnóstico había recibido tratamiento con Neotigason® (acitretina), aplicación tópica de corticoides, análogos de la vitamina D y radiación ultravioleta A, presentando buena respuesta al tratamiento pero con reaparición de las lesiones tras la retirada del mismo. En este contexto, se inició terapia con adalimumab, experimentando una respuesta parcial. Ante la persistencia de lesiones en el cuero cabelludo y el tronco, se decidió cambiar por ustekinumab. La administración de este fármaco se realizó según la pauta habitual de 45mg de inducción, seguidos de otros 45mg a las 4 semanas, para posteriormente administrar las siguientes dosis cada 12 semanas7. En torno a los 2 años de haber iniciado el tratamiento, cuando había recibido una dosis total de 585mg, a los pocos días de la administración de la última dosis, se objetiva la presencia de proteinuria en el sistemático de orina, confirmada en muestra de orina de 24h. Esos valores de proteinuria fueron inicialmente de 3,7g/día y se acompañaban de hipoproteinemia sanguínea leve (albúmina 3,2g/dl) y de elevación del colesterol y los triglicéridos, manteniendo la función renal conservada, por lo que se derivó a consultas de Nefrología para estudio de posible glomerulopatía.
Una vez en nuestras consultas, el paciente refiere orina espumosa de unas semanas de evolución, sin objetivar hematuria ni otra sintomatología. Ante la sospecha de que una glomerulonefritis fuera la causante del cuadro, se inicia valoración de la misma en la que se incluyeron estudio de inmunoglobulinas, complemento, con espectro electroforético en sangre y orina, ANA, ANCA y serologías víricas. Los resultados confirmaron la presencia de síndrome nefrótico, siendo el resto de las pruebas complementarias normales o negativas. Finalmente, ante los hallazgos obtenidos, se realiza biopsia renal percutánea ecoguiada.
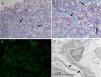
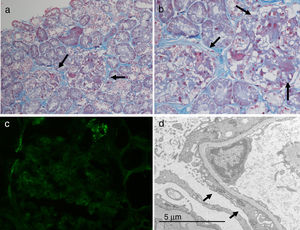
En el estudio anatomopatológico se visualizan un total de 19 glomérulos, ninguno de ellos con esclerosis global. La gran mayoría presentan frecuentes sinequias del ovillo con la cápsula de Bowman. En 3 glomérulos se identifican discretas consolidaciones segmentarias del ovillo. En el estudio de inmunofluorescencia directa se identifican depósitos granulares focales segmentarios de IgM y C3. Por todo ello, se concluye con el diagnóstico de glomeruloesclerosis focal y segmentaria, del tipo variante clásica (fig. 1).
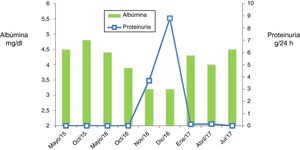
Dada la relación temporal entre la administración del tratamiento y la aparición de la proteinuria, se decide suspender ustekinumab ante la sospecha de cuadro secundario al tratamiento. Simultáneamente se inició de forma paralela tratamiento con prednisona a las dosis estándar de tratamiento según las guías KDIGO empleadas para el manejo de los cuadros de glomeruloesclerosis primaria (mg/kg de peso)8. En este caso no fue posible asociar bloqueantes del sistema renina-angiotensina por hipotensiones sintomáticas del paciente. En las siguientes revisiones presenta una evolución favorable, con negativización de la proteinuria y recuperación de la hipoalbuminemia desde el primer mes de inicio del tratamiento y cese del ustekinumab. Esta rápida respuesta, junto con la ausencia de hipertensión y microhematuria, apuntan al diagnóstico de cuadro secundario al tratamiento frente a un origen primario de la glomerulonefritis. A pesar de ello, se decide completar 12 semanas de prednisona oral, con retirada progresiva hasta su suspensión. Actualmente el paciente continúa sin datos de enfermedad renal activa (ausencia de proteinuria y función renal normal) (fig. 2).
Estamos ante un caso clínico con afectación glomerular en forma de glomeruloesclerosis focal y segmentaria demostrada anatomopatológicamente. De acuerdo con la forma de presentación y la rápida respuesta tras el cese de ustekinumab, el cuadro podría haber estado desencadenado por este mismo tratamiento. Este acontecimiento no está referido en la ficha técnica del fármaco7 ni ha sido descrito en la bibliografía hasta el momento, pudiendo tratarse de un efecto secundario no conocido ya que, como se dijo anteriormente, aún desconocemos el espectro de efectos adversos que son capaces de producir estos fármacos debido al reciente inicio de utilización de los mismos. En este caso, se considera una reacción adversa a medicamentos del tipo B (idiosincrática) grave, puesto que afecta directamente a la función de un órgano vital como es el riñón.
Presentamos un caso clínico de una probable relación entre el tratamiento con ustekinumab y la aparición de un síndrome nefrótico secundario a glomerulonefritis focal y segmentaria, dada la coincidencia temporal entre ambos. La relación causa-efecto no se puede asegurar, puesto que para ello sería necesario administrar el tratamiento con ustekinumab una segunda vez y que se reproduzca la proteinuria. Este proceder no es ético y, por lo tanto, la causa-efecto en este caso es imposible de demostrar. No obstante, ante este hecho, recomendamos monitorizar la función renal y la proteinuria en los pacientes que reciban este fármaco.