Sr. Director:
El síndrome hemofagocítico es una rara entidad clínica, caracterizada por una proliferación generalizada, no maligna, de histiocitos con importante actividad hemofagocítica1-3. La etiología de este cuadro se puede dividir en dos: primario o genéticamente determinado o secundario: vírico, bacterias, hongos, parásitos, neoplasias, colagenosis, inmunodeficiencias o fármacos1-7. El cuadro clínico se caracteriza por fiebre, hepatoesplenomegalia, linfoadenomegalia, síntomas neurológicos, edema y erupción cutánea1,2,8,9. Los hallazgos de laboratorio más importantes son pancitopenia, hipertrigliceridemia, hipofibrinogenemia, hiponatremia, hipoproteinemia, elevación de enzimas hepáticas, elevación de LDH y ferritina, pleocitosis en LCR y actividad defectuosa de células NK10. Desde el punto de visto histopatológico, la existencia de hemofagocitosis en la médula ósea, en el bazo y en los ganglios linfáticos, la falta de hallazgos malignos y un 2% de células con actividad hematofagocítica son suficientes para el diagnóstico1-3. El síndrome hemofagocítico tiene mal pronóstico a pesar de tratamiento, con una supervivencia media de 2 semanas desde que se inicia el cuadro clínico. La supervivencia puede llegar al 60% a 5 años si hay una respuesta adecuada al tratamiento11,12. Como alternativas terapéuticas se encuentran el empleo de agentes que interrumpen la función de los histiocitos y macrófagos activados como etopósido, esteroides, dosis altas de Ig i.v., ciclosporina A, globulina antitimocito, anticuerpos anti-TNF y, en casos seleccionados, trasplante de médula ósea13,14.
Hombre de 53 años, sometido a trasplante renal que acude a urgencias por presentar cuadro febril con temperatura de 38,5 ºC de 24 horas de evolución con escalofríos, dolor abdominal leve difuso, astenia, anorexia y disminución subjetiva del volumen de diuresis. La exploración física fue normal y en las diferentes pruebas practicadas de urgencia no se encontró patología relevante: radiografías normales, analítica de sangre y orina normal, hemocultivo y urocultivo negativo, antígeno precoz CMV negativo (en este momento no se disponía de PCR de CMV en nuestro hospital). El cuadro progresó con un aumento del dolor abdominal, en la tomografía axial computarizada (TAC) se observó dilatación de asas de delgado de posible etiología isquémica o infecciosa. Ante los hallazgos y el empeoramiento clínico se realizó laparotomía exploratoria sin observarse anomalías. En el líquido peritoneal creció un estafilococo coagulasa negativo tratado con meropenem a dosis de 500 mg cada 12 horas. Tras la intervención presentó una mejoría clínica a pesar de la aparición de íleo paralítico posquirúrgico con resolución espontánea del mismo. A los pocos días aparecieron nuevos picos febriles junto con cuadro diarreico, inicialmente sin productos patológicos pero, posteriormente con melenas, asociado a deterioro neurológico, hepatoesplenomegalia, así como alteración función hepática, anemia y trombocitopenia. Se solicitaron nuevas pruebas en las que destacaron: antígeno precoz CMV positivo con PCR de CMV mayor a 100.000 copias/ml. Esoagogastroduodenoscopia: esofagitis infecciosa. Analítica: GOT/GPT 135/156 U/l; LDH 558 U/l; sodio 130 meq/l, fibrinógeno 133 mg/dl, hemoglobina 9,2 g/dl, y hematocrito del 26,8% y plaquetas de 48.000 µl con leucocitos normales (5.500 µl con fórmula normal), aumento muy importante de triglicéridos (738 mg/dl), deterioro progresivo de función renal (creatinina entorno a 4-5 mg/dl). Haptoglobina normal, test de Coombs negativo. Extensión sangre periférica: algún esquistocito con ausencia de reticulocitos. Punción de médula ósea: compatible con síndrome hemofagocítico (figura 1).
Ante dichos hallazgos, se diagnosticó al paciente de síndrome hemofagocítico reactivo a infección por CMV; se consultó con la unidad de enfermedades infecciosas y se inició terapia con la siguiente pauta: terapia anti-CMV con ganciclovir 50 mg/12 h y gammaglobulina inespecífica i.v. 30 g/48 h y para el síndrome hemofagocítico con bolos de metilprednisolona, manteniendo la ciclosporina que llevaba el paciente a dosis bajas (niveles en torno a 50 ng/ml). A pesar del tratamiento se produjo un deterioro del estado general y del estado neurológico y el paciente fue ingresado finalmente en la UCI por desaturación, donde falleció poco después por fallo multiorgánico, a los 12 días del ingreso. En la autopsia se observaron: infección por CMV diseminada, con afectación fundamental de tracto digestivo y pulmón (figura 2) y síndrome hemofagocítico reactivo (figura 1).
El síndrome hemofagocítico tiene una prevalencia estimada del 0,4% en pacientes con trasplante renal11, lo cual lo hace ser una complicación rara en este grupo de pacientes. Además, en éstos la etiología más frecuente es la secundaria a una infección14. Otro punto a considerar es el mal pronóstico de estos pacientes, siendo fundamental el diagnóstico precoz para inicio de una terapia precoz. En cuanto a las estrategias de tratamiento, no hay un consenso, y se han propuesto multiples tratamientos como el uso de esteroides y ciclosporina14, el empleo de inmunoglobulina específica, el tratamiento del agente etiológico, etc.
Por otro lado, la infección por CMV en el paciente trasplantado renal es una complicación bien conocida, aunque actualmente su incidencia y repercusión cada vez es menor por la profilaxis empleada15. No obstante, a pesar de ello, es un diagnóstico que debemos tener en cuenta ante cualquier deterioro del estado general del paciente trasplantado, porque las complicaciones de este cuadro infeccioso son todas graves y el diagnóstico precoz con inicio de terapia apropiada mejora mucho el pronóstico.
El síndrome hemofagocítico es una complicación rara tras el trasplante renal. No obstante, es una entidad clínica que debemos tener presente en el diagnóstico diferencial de estos pacientes sobre todo si se asocia con fiebre, organomegalias y pancitopenia. Para el diagnóstico de presunción los datos de los análisis de sangre (pancitopenia, alteración de la función hepática, aumento de LDH, disminución de fibrinógeno, aumento de triglicéridos, hiponatremia, etc.), nos pueden orientar, pero es el análisis de la médula ósea la prueba que nos va a acercar más al diagnóstico. En cuanto a la etiología más probable en estos pacientes inmunodeprimidos, será la infección viral la que en el mayor número de casos esté implicada como agente desencadenante del proceso. El problema de esta entidad clínica es que todavía no existe un tratamiento específico, teniendo una supervivencia muy baja del paciente trasplantado, y si sobrevive es raro que el injerto renal sea funcionante.
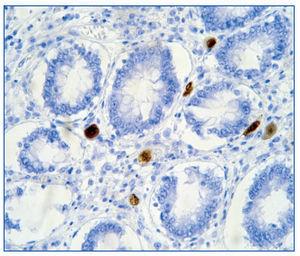
Figura 2. Tinción con inmunoperoxidasa. Células conteniendo CMV en tejido intestinal.
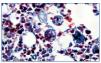
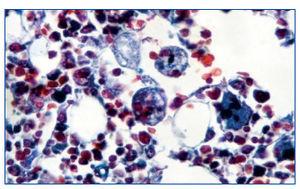
Figura 1. Tricrómico. Histiocitos con hematíes en su interior indicando su actividad hematófaga en la médula ósea.