Describimos la evolución de un niño que presentó 2 raras complicaciones extrarrenales, osteonecrosis de ambas cabezas femorales y colelitiasis, derivadas de una recaída de síndrome hemolítico-urémico atípico (SHUa) producida tras la suspensión del tratamiento con eculizumab en un niño afecto de SHUa sin mutación en el sistema complemento.
Presentamos el caso de un niño de 8 años que inició en el periodo neonatal un SHUa con afectación grave y multisistémica. Con la administración de eculizumab consiguió la recuperación hematológica y renal completa1. Desde el periodo neonatal hasta los 3 años y 6 meses continuó el tratamiento con eculizumab, manteniéndose la enfermedad en remisión completa.
Se realizó un estudio exhaustivo de todos los genes conocidos que pudieran causar un SHUa y no se encontraron mutaciones, por lo que se interrumpió el tratamiento. Los genes estudiados fueron: ADAMSTS13, ARMS2, C1S, C2, C3, C3ARI, C4BPA, C4BPAP1, C4BPAP2, C4BPB, C5, C5ARI, C6, C7, C8A, C8B, C8G, C9, CD46, CD46, CD55, CD59, CFB, CFD, CFH, CFHR1, CFHR2, CFHR3, CFHR4, CFHR5, CFI, CFP, CLU, CPB2, CR1, CR1L, CR2, CRP, DGKE, F12, F2, F3, FCN1, HTRA1, KDR, MASP1, MASP2, MBL2, NR5A2, PHG, PIGA, PLG, PROC, PROCR, PROS1, PTX3, RP1, RP1L1, SELP, SERPING1, TFP1, THBD, THBS1, VSIG4, VTN y VWF. Tampoco se encontraron variantes (haplotipos) de riesgo en el gen MCP ni en gen CFH.
Tres meses después, tras un cuadro catarral leve, ingresó por fallo renal agudo. Se inició nuevamente tratamiento con eculizumab, con normalización de todos los parámetros en pocos días (tabla 1).
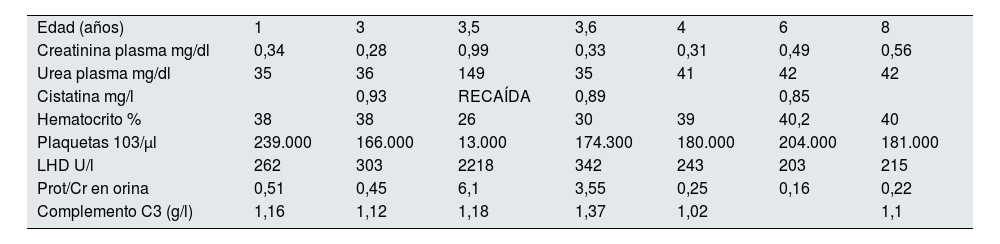
Datos analíticos evolutivos
| Edad (años) | 1 | 3 | 3,5 | 3,6 | 4 | 6 | 8 |
| Creatinina plasma mg/dl | 0,34 | 0,28 | 0,99 | 0,33 | 0,31 | 0,49 | 0,56 |
| Urea plasma mg/dl | 35 | 36 | 149 | 35 | 41 | 42 | 42 |
| Cistatina mg/l | 0,93 | RECAÍDA | 0,89 | 0,85 | |||
| Hematocrito % | 38 | 38 | 26 | 30 | 39 | 40,2 | 40 |
| Plaquetas 103/μl | 239.000 | 166.000 | 13.000 | 174.300 | 180.000 | 204.000 | 181.000 |
| LHD U/l | 262 | 303 | 2218 | 342 | 243 | 203 | 215 |
| Prot/Cr en orina | 0,51 | 0,45 | 6,1 | 3,55 | 0,25 | 0,16 | 0,22 |
| Complemento C3 (g/l) | 1,16 | 1,12 | 1,18 | 1,37 | 1,02 | 1,1 |
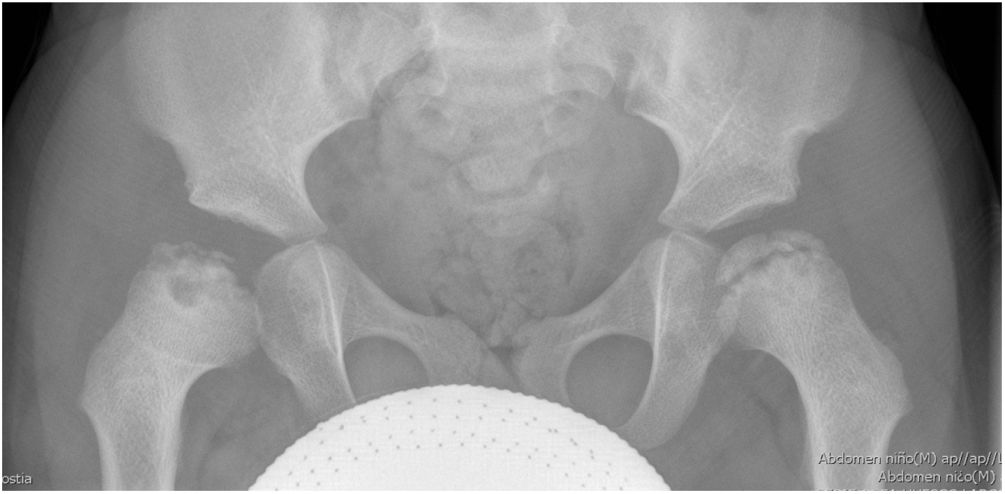
Un año después de la última recaída se detectó, de forma casual, una necrosis bilateral sincrónica y asimétrica de ambas cabezas femorales (fig. 1). Por el momento evolutivo en el que se encontraron las lesiones, la osteonecrosis se produjo durante la recaída producida tras la retirada del medicamento. La ausencia de antecedentes de enfermedad degenerativa articular coxofemoral y de otras causas secundarias de osteonecrosis permitieron excluir otras posibilidades etiológicas.
En el mismo estudio, y también de forma asintomática, se detectó una litiasis biliar.
Cinco años después el niño continúa recibiendo tratamiento con eculizumab, con buena tolerancia (tabla 1), sin presentar evidencias de actividad de microangiopatía trombótica (MAT).
DiscusiónEn el SHUa el complejo de ataque a la membrana produce un daño a nivel del endotelio y esto desencadena la MAT.
Aunque las lesiones en el SHUa afectan predominantemente a los vasos renales, el carácter difuso y sistémico de la MAT conduce a la afectación de la microvasculatura de otros órganos (cerebro, corazón, intestino, páncreas, pulmones2…).
Nuestro paciente presentó, además de la triada de anemia hemolítica, trombocitopenia e insuficiencia renal aguda, una necrosis avascular de ambas cabezas femorales, presumiblemente a causa de la MAT sistémica producida durante la recaída. El daño en el endotelio de la microvasculatura en la circulación terminal de la cabeza femoral causaría una hipoperfusión tisular con interrupción del suministro vascular, infarto óseo y finalmente una necrosis de ambas cabezas femorales3. Su asociación con SHUa no está descrita.
Dentro de las complicaciones gastrointestinales se han publicado en la literatura algunos casos de cálculos biliares varios meses después del episodio agudo de SHU típico4; sin embargo, esta complicación es excepcional en un SHUa.
Uno de los temas más debatidos actualmente es la duración del tratamiento con eculizumab5,6, puesto que la decisión de retirada de tratamiento no está exenta de riesgos, sobre todo en pacientes con una presentación clínica del SHUa al comienzo muy severa y de riesgo vital. Esta controversia se acentúa en la edad pediátrica, ya que los eventos comunes que conducen a la activación del complemento (infecciones, vacunas…) son frecuentes en este grupo de edad.
En un 30-40% de los pacientes con SHUa no se identifican mutaciones de los genes del complemento. Existen evidencias de que la gravedad del SHUa y la respuesta al eculizumab es similar en pacientes con o sin riesgo genético identificado6, si bien mantener el tratamiento es más difícil en pacientes en los que no se han encontrado mutaciones en el sistema del complemento.
FinanciaciónEste trabajo no ha recibido ningún tipo de financiación.