La inmunosupresión basada en los inhibidores de la calcineurina (INC) ha hecho posible la reducción del rechazo agudo en el trasplante renal y el aumento de la supervivencia del injerto a corto pero no a largo plazo, siendo la muerte del receptor con injerto funcionante y la disfunción crónica del injerto sus principales causas. Los fármacos inhibidores de la m-Tor son inmunosupresores con capacidad antiproliferativa y antimigratoria, lo que les confiere un potencial papel protector en la disfunción del injerto renal, una mejora del perfil cardiovascular y una reducción en el desarrollo de neoplasias; todo ello podría, teóricamente, preservar la función renal y la vida del paciente a largo plazo en un grupo seleccionado de pacientes. Por otro lado, el uso de monoterapia en un paciente facilita su adherencia a cualquier tratamiento crónico. El objetivo del estudio es evaluar el uso de inhibidores de la m-Tor en monoterapia a largo plazo en un grupo seleccionado de receptores de trasplante renal de bajo riesgo inmunológico mediante un estudio observacional y prospectivo, desarrollado en el período 2001-2011. Los pacientes en tratamiento con inhibidores de la m-Tor junto con micofenolato mofetilo o prednisona fueron evaluados inmunológicamente de cara a ser incluidos en el protocolo de monoterapia con inhibidores de la m-Tor. Se incluyeron los pacientes considerados de bajo riesgo inmunológico: sin antecedentes de episodios previos de rechazo agudo, ausencia de anticuerpos antidonante específico y una producción de ATP inferior a 520 ng/dl. La valoración inmunológica se repitió a los 3 y 12 meses del inicio de la monoterapia. La población del estudio fueron 47 receptores de trasplante renal procedente de donante cadáver en tratamiento con inhibidores de la m-Tor en monoterapia, 34 con sirolimus y 13 con everolimus, con una edad media de 55,6 ± 12,5 (23-75 años), 25 varones y 22 mujeres. En el momento de incluirse en el estudio, 18 de ellos (38,2%) recibían prednisona y 29 (61,7%) micofenolato mofetilo, procediéndose a la suspensión de ambos fármacos. Un total de 5 pacientes habían recibido inducción sin INC, mientras que 42 pacientes fueron convertidos desde regímenes con INC por efectos secundarios de éstos o neoplasias. El seguimiento medio de los pacientes en monoterapia fue de 46,9 meses (IC 95%: 38,8-55,0). Durante su evolución, 7 de los 47 receptores incluidos en protocolo (11,5%) precisaron cambio la inmunosupresión por diferentes efectos adversos del tratamiento, sin pérdida del injerto durante el siguiente año. A lo largo del seguimiento, 4 pacientes (8,5%) perdieron el injerto debido en un caso a una muerte súbita con injerto funcionante y en tres casos a rechazo crónico. Se objetivó un episodio de rechazo agudo (2,1%) que respondió favorablemente al tratamiento con esteroides y reconversión a FK 506 y micofenolato mofetilo. Este paciente no desarrolló durante el seguimiento anticuerpos antidonante específico y mantuvo un nivel de activación linfocitaria bajo, con una producción de ATP de 170 ng/dl. Durante el estudio, ningún receptor desarrolló anticuerpos antidonante específico y todos mantuvieron los niveles de activación linfocitaria por debajo de 520 ng/dl. La supervivencia del injerto y el paciente fue del 100% al año y del 88,7 y 95,7%, respectivamente, a los cinco años. El porcentaje de pacientes que se mantuvieron en monoterapia fue de 97,9% al año y del 70,5% a los cinco años. La función renal mejoró en los 36 pacientes que se mantuvieron en monoterapia, pasando la creatinina media en plasma de 2,16 ± 1,05 mg/dl a 1,49 ± 0,56 mg/dl (p = 0,001) al final del seguimiento, y el filtrado glomerular estimado de 39,23 ± 25,23 a 52,23 ± 23,20 ml/mn (p = 0,001), con un incremento no significativo de la proteinuria de 306,6 ± 400 a 418,1 ± 514,1 mg/24 h (p = 0,17). El uso de factores eritropoyéticos e inhibidores de la enzima convertidora de angiotensina/antagonistas de los receptores de la angiotensina II se incrementó significativamente con el tratamiento m-Tor, pero no así el peso corporal, el uso de hipolipemiantes e hipotensores o el porcentaje de receptores con diabetes mellitus. Durante el seguimiento no se detectó ningún caso de falta de adherencia al tratamiento. Podemos concluir que la monoterapia con inhibidores de la m-Tor es una inmunosupresión eficaz a largo plazo en un grupo seleccionado de receptores de trasplante renal.
Calcineurin inhibitors have reduced acute rejection rates and improved short-term graft survival, but without any improvement in long-term outcomes, since calcineurin inhibitors cause nephrotoxicity and death with a functioning graft. mTOR inhibitors have antiproliferative and anti-angiogenic effects with no nephrotoxicity. These properties could improve patient and graft long-term survival rates in select transplant recipients. In addition, monotherapy always diminishes the rate of non-compliance in chronic patients. We examined the evolution of 47 low immunological risk kidney transplant recipients with mTOR inhibitor monotherapy. The mean age was 45±10 years (range: 18-69 years), with 25 males y 22 females. We performed an immunological evaluation before and at 3 and 12 months after starting monotherapy by detection of donor-specific antibodies by microsphere cytometry and the determination of lymphocyte activity with production of ATP by CD4+ T-lymphocytes activated by PHA mitogen. We considered patients to be of low immunological risk when the patient had an ATP production less than 520ng/dl and no history of acute rejection episode or donor-specific antibodies. Initially, 5 patients received immunosuppression induction without calcineurin inhibitors (mycophenolate, prednisone, mTOR inhibitors and anti-CD25), and 42 were converted to mTOR inhibitors due to secondary effects of calcineurin inhibitors or malignancies. A total of 34 recipients had received sirolimus and 13 everolimus. Eighteen out 47 patients (38.2%) received prednisone and 29 (61.7%) mycophenolate with mTor before starting monotherapy. The mean follow-up period after starting monotherapy was 46.9 months (95% CI: 38.8-55.0 months). At the end of the follow-up, 7 out of 47 recipients (11.5%) had to change immunosuppression without losing their grafts after 1 year, due to heavy proteinuria in 2 cases, pulmonary infection in 1, acute rejection in 1, hepatotoxicity in 1, vasculitis in 1 and a temporary inclusion on dialysis after acute pyelonephritis in 1. Four out of 47 patients (8.5%) lost their grafts, as a result of chronic rejection in 3 cases, and as a result of death with a functioning graft in 1. The rate of acute rejection was 2.1%, one episode, which was solved with steroid pulses and switching from mTOR inhibitors to tacrolimus and mycophenolate. No patients developed donor-specific antibodies, and all of them maintained an ATP production less than 520ng/dl. The rates of graft and recipient survival were both 100% at 1 year, and 88.7% and 95.7% at 5 years. The percentages of patients on monotherapy were 97.9% and 70.5 % at 1 and 5 years, respectively. At the end of the follow-up, 36 out of 47 recipients remained on mTOR inhibitor monotherapy. Serum creatinine and glomerular filtration rates improved significantly, from 2.16±1.05mg/dl to 1.49±0.56mg/dl (P=.001) and from 39.23±25.23ml/min to 52.23±23.20ml/min (P=.001), respectively. Proteinuria increased but not significantly, from 306.6±400mg/24h to 418.1±514.1mg/24h (P=.17). The patients treated with mTOR inhibitors received significantly more erythropoietin and angiotensin-converting enzyme inhibitors/angiotensin receptor blockers than before starting mTOR, but there was no change in the treatment with statins or hypotensive agents. Body weight and the percentage of diabetic recipients were similar during the study. No cases of non-compliance were observed during the follow-up. The present study supports the safety and efficacy of monotherapy with mTOR inhibitors in select kidney transplant recipients.
La inmunosupresión basada en los inhibidores de la calcineurina (INC) ha hecho posible la reducción de la incidencia del rechazo agudo en el trasplante renal y el aumento de la supervivencia del injerto a corto plazo1.
Sin embargo, la supervivencia del trasplante a largo plazo no se ha incrementado de la misma manera2, siendo la muerte del receptor con injerto funcionante3 y la disfunción crónica del injerto4 las principales causas de pérdida de injerto. Esto es una consecuencia lógica, pues los INC aumentan los factores clásicos de riesgo cardiovascular3, entre los que se incluye la insuficiencia renal por disfunción del injerto4. Además, los INC no tienen efecto protector frente al desarrollo de neoplasias en el receptor5,6.
Los fármacos inhibidores de la m-Tor son inmunosupresores sin efectos nefrotóxicos, con capacidad antiproliferativa y antimigratoria por bloqueo de la señalización intracelular que regula la proliferación de células T activadas7. Esto les confiere un papel protector potencial en la disfunción del injerto renal, una mejoría del perfil cardiovascular y una reducción en el desarrollo de neoplasias, al disminuir de manera importante la angiogénesis7. Estas propiedades condicionan su uso precoz en el trasplante8 por incrementar las complicaciones quirúrgicas, al interferir en la cicatrización9 y al presentar tasas más altas de rechazo agudo que con la inmunosupresión basada en los INC10, pero su uso a medio plazo debería considerarse.
Además, a diferencia de los INC, los m-Tor expanden selectivamente la subpoblación linfocitaria T reguladora (CD4+, CD25, highFOX3+), que induce una función reguladora en linfocitos T, CD4+naive y actúa de forma sinérgica junto al bloqueo de la coestimulación para inducir tolerancia en el trasplante renal11,12.
Nos encontramos con unos fármacos que teóricamente pueden preservar la función renal y la vida del paciente a largo plazo en un grupo seleccionado de afectados.
Todo ello justificaría la conversión a m-Tor en pacientes que no presenten contraindicación para ello y puedan tolerarlos, ya que la tasa de retirada de dichos fármacos por efectos secundarios alcanza el 25%13.
Por otro lado, el uso de monoterapia en un paciente favorece su adherencia al tratamiento14, lo que facilitaría la inmunosupresión crónica en el paciente trasplantado.
El objetivo del estudio es evaluar el uso de m-Tor en monoterapia a largo plazo en un grupo seleccionado de receptores de trasplante renal de bajo riesgo inmunológico.
MATERIAL Y MÉTODOS
Estudio observacional y prospectivo desarrollado en el período 2001-2011 en un centro de trasplante renal.
Los pacientes en tratamiento con m-Tor junto con micofenolato mofetilo o prednisona fueron evaluados inmunológicamente de cara a ser incluidos en el protocolo de monoterapia con m-Tor (figura 1).
La evaluación inmunológica consistió en:
- Determinación de los anticuerpos antidonante específicos mediante citometría de microesferas (Luminex®).
- Valoración de la actividad linfocitaria: producción de ATP en cultivo de linfocitos T y CD4+ activados por el mitógeno PHA (ImmuKnow CyleX®).
Se incluyó al paciente en protocolo de monoterapia cuando cumplía las siguientes características: sin antecedentes de episodios previos de rechazo agudo en el último año, ausencia de anticuerpos antidonante específicos y una producción de ATP inferior a 520 ng/dl, por lo que se le consideraba de bajo riesgo inmunológico.
Se determinó en todos los pacientes la presencia de anticuerpos antidonante específicos junto con la producción de ATP a los 3 y 12 meses del inicio de protocolo de monoterapia.
La población a estudio consistió en 47 receptores de trasplante renal procedente de donante cadáver, con una edad media de 55,6 ± 12,5 (23-75 años), siendo 25 varones y 22 mujeres, que fueron considerados de bajo riesgo inmunológico; 34 fueron tratados con sirolimus y 13 con everolimus. En el momento de incluirse en el estudio, 18 de los 47 (38,2%) recibían prednisona y 29 (61,7%) micofenolato mofetilo junto con m-Tor, procediéndose a la suspensión de ambos fármacos (figura 1).
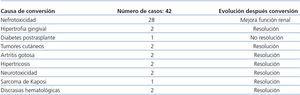
Entre los 47 pacientes de la serie, 5 (10,6%) habían recibido inicialmente una inmunosupresión de inducción sin INC que consistió en anti-CD25 + m-Tor + micofenolato mofetilo + prednisona, siendo la causa de este tratamiento en tres de ellos un donante subóptimo, en un caso el antecedente de enfermedad linfoproliferativa y en el último una historia previa de neurotoxicidad por INC. El resto, 42 pacientes (89,4%), procedían de regímenes que incluían INC, siendo convertidos a m-Tor con un tiempo medio postrasplante de 20,8 meses (intervalo de confianza [IC] 95%: 14,4-27,1) por diferentes causas mostradas en tabla 1. La conversión de INC a m-Tor se efectuó mediante la reducción de la dosis de INC a la mitad en la primera semana con introducción de m-Tor y suspensión de INC en la segunda semana con niveles de sirolimus entre 10-16 ng/dl y de everolimus entre 6-9 ng/dl.
La concentración plasmática de sirolimus y everolimus se determinó por inmunoensayo (ACMIA autoanalizador Dimension XPand®) y cromatografía de alta resolución con detector de masas, respectivamente. El límite de sensibilidad de dichas técnicas fue de 1,7 y 0,5 ng/ml, respectivamente.
La función renal de los receptores que se mantuvieron en monoterapia se valoró mediante creatinina en plasma y filtrado glomerular estimado (MDRD-4) en el momento en que se retiró el INC o en caso de inducción sin INC cuando se estabilizó la función renal en el postrasplante y al final del seguimiento.
Se evaluó el efecto de la terapia m-Tor sobre diferentes parámetros clínicos y analíticos, como el peso corporal, la incidencia de diabetes mellitus (DM) y el uso de medicación para el control de la anemia, la dislipemia, la proteinuria y la tensión arterial, y se compararon al inicio del tratamiento con m-Tor y al final de éste.
La adherencia al tratamiento se valoró mediante entrevista personal y medición de los niveles del fármaco en cada una de las visitas de seguimiento.
Las variables continuas se han expresado como medias e IC 95%, o como medianas y rango intercuartil, dependiendo de la distribución de los datos. Para la descripción de variables categóricas se han utilizado el número y el porcentaje de pacientes por categoría de respuesta.
Se han empleado técnicas estadísticas para asegurar el cumplimiento de los supuestos estadísticos, previas a la realización de las pruebas paramétricas correspondientes para comparar medias y proporciones. En caso de que no se cumplieran los supuestos establecidos, se han utilizado las pruebas no paramétricas correspondientes.
El análisis comparativo de las variables entre grupos se ha realizado mediante la prueba ANOVA en variables continuas o su equivalente no paramétrico, dependiendo de las características inherentes a la variable en estudio, y la prueba de McNemar al analizar variables de tipo categórico de muestras relacionadas.
La supervivencia del injerto, el receptor y el porcentaje de pacientes que se mantuvieron en monoterapia m-Tor se valoró mediante curvas de supervivencia Kaplan-Meier.
Para el análisis estadístico se ha utilizado el paquete estadístico SPSS versión 19.0. En todas las pruebas estadísticas realizadas con las variables de resultado se ha utilizado un nivel de significación estadística (α) de 0,05.
RESULTADOS
Durante el seguimiento, 7 de los 47 receptores incluidos en protocolo (11,5%) precisaron cambio de inmunosupresión por diferentes causas, mostradas en la tabla 2, sin pérdida del injerto al menos durante el siguiente año después de la reconversión. Durante la evolución, otros 4 pacientes perdieron el injerto debido en un caso a una muerte súbita con injerto funcionante y en tres casos a rechazo crónico, en dos de ellos por su patología de base no podían ser cambiados de inmunosupresión (casos 1 y 2 de la tabla 3), mientras que en el tercero la conversión a m-Tor se realizó con una importante insuficiencia renal (caso 3 de la tabla 3),
El nivel sérico medio de sirolimus al final del seguimiento fue de 12,5 ng/ml (IC 95%: 11,1-13,9 ng/ml), mientras que el de everolimus fue de 6,7 ng/ml (IC 95%: 4,3-9,1 ng/ml).
El seguimiento medio de los pacientes en monoterapia fue de 46,9 meses (IC 95%: 38,8-55,0).
Se objetivó un episodio de rechazo agudo (2,1%) que fue diagnosticado histológicamente y respondió de manera favorable al tratamiento con esteroides y reconversión a FK y mofetilo (tabla 2). Este paciente no desarrolló durante el seguimiento anticuerpos antidonante específico y mantuvo un nivel de activación linfocitaria bajo, con una producción de ATP de 170 ng/dl.
Durante el seguimiento ningún receptor desarrolló anticuerpos antidonante específico y mantuvieron niveles de activación linfocitaria por debajo de 520 ng/dl.
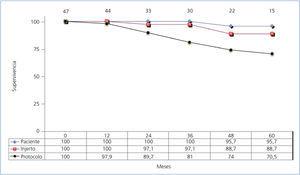
La supervivencia del injerto y el paciente fue del 100% al año y del 88,7 y 95,7% a los cinco años, respectivamente. El porcentaje de pacientes que se mantuvieron en monoterapia fue del 97,9% al año y del 70,5% a los cinco años (figura 2).
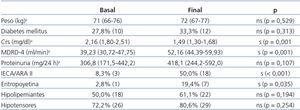
La función renal mejoró significativamente durante el seguimiento en los 36 pacientes que se mantuvieron en monoterapia, con un incremento no significativo de la proteinuria (tabla 4). No observamos diferencias significativas en la evolución de estos parámetros entre el grupo de receptores que recibía sirolimus o everolimus.
El uso de factores eritropoyéticos e inhibidores de la enzima convertidora de angiotensina (IECA)/antagonistas de los receptores de la angiotensina II (ARA II) se incrementó significativamente durante el seguimiento, pero no así el peso corporal, el uso de hipolipemiantes e hipotensores o el porcentaje de receptores con DM (tabla 4).
Durante el seguimiento no se detectó ningún caso de falta de adherencia al tratamiento.
DISCUSIÓN
Los pacientes de nuestra serie en monoterapia con m-Tor tuvieron una adherencia al tratamiento del 100%, sin que evidenciáramos efectos secundarios que impidieran la toma del fármaco en ningún caso13. Esto era esperable, ya que los pacientes incluidos en el protocolo de monoterapia llevaban un tiempo en tratamiento con m-Tor con buena tolerancia, aunque junto con otros fármacos inmunosupresores. Por ello, aquellos pacientes que no lo habían tolerando bien no habían seguido con el fármaco y nunca podrían haber sido incluidos en el estudio (figura 1).
La patología determinante del paso de INC a m-Tor en los pacientes de conversión se resolvió en todos los casos, excepto en un paciente que había desarrollado DM de novo postrasplante (tabla 1). A pesar de las esperanzas depositadas en los m-Tor, estos fármacos pueden aumentar el riesgo de DM postrasplante. En efecto, un estudio americano publicado por Johnston con miles de pacientes demostró que el riesgo de DM de novo postrasplante se incrementaba significativamente en aquellos pacientes tratados con m-Tor15, por lo que no es sorprendente que nuestro paciente con DM postrasplante mantuviera esta patología a pesar de la conversión de FK-506 a m-Tor. Cabe destacar que el porcentaje de pacientes diabéticos en nuestra serie no se incrementó significativamente durante el seguimiento (tabla 4).
La proteinuria fue el principal efecto adverso responsable de la retirada de pacientes del protocolo de monoterapia con m-Tor13. Aunque inicialmente se pensó que la proteinuria era consecuencia de la retirada de INC, parece existir un efecto del m-Tor independiente para su desarrollo, que en parte podría deberse a hiperfiltración glomerular16. Así, dos receptores precisaron reconversión a INC por proteinuria con respuesta parcial a la conversión (casos 1 y 2, tabla 2).
En esta línea, cabe destacar el incremento significativo en nuestra serie de IECA y ARA II tras el uso de m-Tor en un intento de reducir la proteinuria favorecida por estos fármacos. En dos casos es poco probable que el m-Tor fuera el causante de la patología que conllevó su retirada, ya que la hepatotoxicidad es un efecto secundario muy excepcional en los m-Tor17 y este paciente presentaba otros factores asociados que podrían haber sido los responsables de la patología (caso 4, tabla 2). En cuanto al otro receptor (caso 3, tabla 2), tenía una infección pulmonar con buena respuesta a antibióticos y no una neumonitis asociada a m-Tor18, por lo que el porcentaje de enfermos que hubieran necesitado la retirada de m-Tor en nuestra serie hubiera sido inferior. No obstante, la tasa de retirada de pacientes del protocolo es semejante a la única serie similar publicada19.
Sólo un paciente en nuestra serie desarrolló un episodio de rechazo agudo durante el seguimiento (caso 5, tabla 2), que respondió favorablemente al tratamiento con esteroides y reconversión a FK-506 y micofenolato mofetilo. Se trata de un caso de disociación clínico-inmunológica, ya que este paciente no desarrolló durante el seguimiento anticuerpos antidonante y mantuvo unos niveles de activación linfocitaria bajos, datos que no indicaban que el paciente presentaría un episodio de rechazo agudo. El hecho de que ningún receptor de la serie desarrollara anticuerpos antidonante específico y se mantuvieran unos niveles de activación linfocitaria bajos durante el tiempo con monoterapia, junto con la baja tasa de rechazo agudo observada, indica una suficiente potencia inmunosupresora de los m-Tor en monoterapia7.
Es destacable que los pacientes en nuestra serie no sólo no experimentaron el deterioro de la función renal esperable como resultado del paso del tiempo postrasplante2, sino que mejoraron su función renal, indicador claro del efecto no nefrotóxico y suficientemente inmunosupresor de estos fármacos7.
Un total de cuatro pacientes perdieron el injerto durante su seguimiento en monoterapia, estando en dos de los casos (casos 1 y 2, tabla 3) contraindicado por su patología el cambio de inmunosupresión8, ya que era prioritario en ambos impedir la progresión de la enfermedad que había recomendado su inclusión en el protocolo20,21. En cuanto al último caso (caso 3, tabla 3), la conversión a m-Tor se produjo en una situación de insuficiencia renal crónica avanzada que en la actualidad había contraindicado su conversión22.
El uso de medicación concomitante, sobre todo factores eritropoyéticos e IECA/ARA II, se ha incrementado significativamente, lo que indica la presencia de conocidos efectos secundarios del tratamiento con m-Tor, como son un aumento de la anemia, la proteinuria y las dislipemias, pero los mencionados tratamientos han sido bien tolerados y han facilitado el control de los efectos adversos producidos por los m-Tor13.
A pesar de que la monoterapia con m-Tor en teoría es atractiva, resulta sorprendente la escasez de publicaciones sobre el tema. Destaca la experiencia comunicada por Pinto et al. en un ensayo multicéntrico retrospectivo con 138 pacientes, con un seguimiento medio de 29 meses, donde refieren una tasa de rechazo del 1,4% y de retirada del régimen inmunosupresor del 14%, con mantenimiento de la función renal e incremento de la proteinuria, datos superponibles a los nuestros. Por el contrario, hay que destacar la ausencia de datos inmunológicos que orientaran sobre la indicación o no de incluir al paciente en monoterapia con m-Tor19.
Este estudio es observacional, por lo que sus conclusiones se ven limitadas por la ausencia de grupo control, pero reporta una experiencia original que puede ser útil en la práctica clínica diaria.
Podemos concluir que la monoterapia con m-Tor es una inmunosupresión eficaz a largo plazo en un grupo seleccionado de receptores de trasplante renal.
Conflictos de interés
Los autores declaran que no tienen conflictos de interés potenciales relacionados con los contenidos de este artículo.
Tabla 1. Causas de conversión de inhibidores de la calcineurina a inhibidores de la m-Tor
Figura 1. Protocolo de inclusión en monoterapia m-TOR
Tabla 2. Causas de cambio de inmunosupresión en receptores de monoterapia m-Tor. Tiempo de seguimiento, inmunosupresión final y evolución
Tabla 3. Causas de pérdida de injerto en receptores de monoterapia m-Tor. Indicación para su inclusión y tiempo de evolución
Tabla 4. Variación en el peso, porcentaje de diabetes, Crs, MDRD-4, proteinuria y en el uso de fármacos concomitantes entre la conversión a m-Tor y el final del seguimiento
Figura 2. Supervivencia actuarial paciente, injerto y mantenimiento en protocolo de receptores en monoterapia m-Tor