Introducción: La insuficiencia cardíaca congestiva (ICC) es una complicación frecuente en la enfermedad renal crónica (ERC). Además de los factores de riesgo clásicos, otros relacionados más específicamente con la ERC, como la anemia, la sobrehidratación o los accesos vasculares, también podrían jugar un papel importante. Objetivos: Determinar la incidencia y las características clínicas asociadas al desarrollo de ICC en pacientes con ERC avanzada y analizar la influencia de la creación de accesos vasculares prediálisis sobre esta complicación. Pacientes y métodos: Estudio de cohorte prospectivo y de observación en el que se incluyeron 562 pacientes (edad media 65 ± 15 años, 260 mujeres) con un filtrado glomerular medio de 15,1 ± 5,0 ml/min, no en diálisis. La variable de resultado principal fue el desarrollo de al menos un episodio de ICC definida por criterios clínicos y radiológicos convencionales. Además de los datos demográficos y clínicos de interés, se incluyó también como covariable la fístula arteriovenosa (FAV). Resultados: Con una mediana de seguimiento de 461 días, la incidencia de ICC fue de 19 episodios por cada 1000 pacientes/año, presentando esta complicación un 17% del total de los pacientes. Mediante regresión logística multivariable, los mejores determinantes del desarrollo de ICC fueron, además de los factores de riesgo clásicos (mujer, añosa, obesa, diabética, con antecedentes de cardiopatía), la realización con éxito de una FAV (odds ratio: 9,541; intervalo de confianza 95%: 4,841; 18,806; p < 0,0001). Mientras que 4 de los 51 pacientes (8%) con FAV distales desarrollaron ICC, 43 de los 109 pacientes (40%) con FAV proximales desarrollaron esta complicación. No se observaron diferencias en la mortalidad de los pacientes con o sin ICC, aunque el inicio no programado (urgente) de diálisis fue mucho más frecuente entre los que desarrollaron ICC que en el resto (63 vs. 3%, p < 0,0001). Conclusiones: La incidencia de ICC es muy elevada en pacientes con ERC avanzada prediálisis. Además de los factores de riesgo clásicos, la realización de un acceso vascular incrementa significativamente la probabilidad de desarrollo de esta complicación cardiovascular.
Introduction: Congestive heart failure (CHF) is a common complication in patients with chronic kidney disease (CKD). In addition to classical risk factors (e.g. age and pre-existing cardiac diseases), other potential reversible abnormalities linked to CKD such as anaemia, volume overload, or vascular access placement may also influence the incidence and severity of acute exacerbations of CHF. Objective: This study aims to determine the incidence and main determinants of CHF in a cohort of patients with stage 4-5 pre-dialysis CKD. Patients and Method: The study group consisted of 562 patients (mean age: 65±15 years, 260 females, 31% diabetics). Native arteriovenous fistulas (AVF) were created in 160 patients who chose haemodialysis as the initial technique for renal replacement therapy. The main outcome variables were: acute decompensated CHF (defined by standard criteria), dialysis initiation (planned and unplanned), and death before dialysis initiation. In addition to demographics, comorbidities, and clinical and biochemical data, AVF creation was also included as a potential determinant of CHF in multiple logistic regression models. Results: Ninety-five patients (17%) developed at least one episode of acute decompensated CHF, and the incidence rate was 19 episodes per 1000 patient-years. In addition to classical risk factors (age, female sex, obesity, diabetes, and previous history of CHF or coronary artery disease), creation of a successful AVF significantly increased the risk of CHF (OR=9.54, 95% CI: 4.84-18.81, P<.0001). In 47 out of 95 patients who developed CHF, a functioning AVF had previously been created, 92% of which were upper arm native AVF, with a median of 51 days between the surgical procedure and CHF episode. The mortality of patients with CHF was similar to that of the rest of the study patients, although unplanned dialysis initiation was significantly more frequent in those who developed CHF. Conclusions: Acute decompensated CHF episodes are common in pre-dialysis CKD patients. In addition to classical risk factors, pre-emptive AVF placement was strongly associated with the development of CHF.
INTRODUCCIÓN
Las enfermedades cardiovasculares son muy prevalentes en los pacientes con enfermedad renal crónica (ERC), y la insuficiencia cardíaca congestiva (ICC) es una de sus manifestaciones más frecuentes1-5.
Factores como la edad, el sexo, la hipertensión arterial, la sobrecarga de volumen, la cardiopatía isquémica, la anemia y la hipoalbuminemia han demostrado ser determinantes del desarrollo de ICC en la ERC1-3, que se acompaña a su vez de cambios morfológicos y funcionales cardíacos, sobre todo del ventrículo izquierdo, como son la hipertrofia y/o dilatación ventricular, y la disfunción sistólica o diastólica6.
Íntimamente ligada a las peculiaridades de la ERC avanzada, la creación de una fístula arteriovenosa (FAV) también puede convertirse en un factor de riesgo de desarrollo de ICC7-10.
Numerosos estudios han demostrado que iniciar un tratamiento crónico de hemodiálisis con una FAV tiene ventajas sustanciales en la supervivencia de estos pacientes comparada con la utilización de catéteres venosos como primeros accesos vasculares11-13. Así, la creación de FAV en pacientes programados para hemodiálisis es en la actualidad uno de los objetivos más recomendables en los cuidados prediálisis14,15.
La observación de una alta incidencia de episodios de ICC en nuestros pacientes seguidos en la consulta de ERC avanzada motivó la realización de este estudio, cuyos objetivos fueron determinar la incidencia y las características clínicas asociadas al desarrollo de ICC, y analizar el papel que puede jugar la creación de accesos vasculares prediálisis, así como las consecuencias de este suceso cardiovascular en la mortalidad e inicio urgente de diálisis.
MATERIAL Y MÉTODOS
Pacientes
El número total de pacientes incluidos en este estudio fue de 562 (edad media 65 ± 15 años, 260 mujeres, 302 hombres) incidentes o prevalentes en la consulta externa de Enfermedad Renal Crónica Avanzada (ERCA) del Hospital Infanta Cristina de Badajoz, durante el período comprendido entre el 1 de enero de 2004 y el 1 de julio de 2010.
Los criterios de inclusión fueron: edad mayor de 18 años, padecer una insuficiencia renal crónica estadio 4-5 no en diálisis y no secundaria a fracaso de un trasplante renal.
La etiología más frecuente de la ERC fue la etiquetada como no filiada (223 pacientes), seguida de la nefropatía diabética (109 pacientes) y glomerulopatías primarias (91 pacientes).
La comorbilidad fue muy prevalente. El número total de pacientes diabéticos fue de 177; 97 pacientes tenían antecedentes de cardiopatía isquémica, 74 pacientes de isquemia cerebral y 52 pacientes de isquemia periférica. En 84 pacientes se recogió el antecedente de al menos un episodio de insuficiencia cardíaca congestiva; 56 pacientes presentaban fibrilación auricular crónica, y 48 pacientes estaban diagnosticados de enfermedad pulmonar obstructiva crónica.
Los fármacos prescritos con más frecuencia fueron: antihipertensivos (inhibidores de la enzima de conversión, bloqueadores receptores angiotensina, betabloqueantes), diuréticos, estatinas, antiagregantes, captores del fósforo y eritropoyetinas.
Datos clínicos y análisis de laboratorio
Además de los datos demográficos, se incluyeron las mediciones de la presión arterial sistólica y diastólica (dispositivo automático Omron M3) y el índice de masa corporal. El grado de comorbilidad fue cuantificado por el método de Davies et al.16.
Durante el período de estudio los pacientes fueron seguidos y tratados con criterios homogéneos. Entre las medidas de preparación para la diálisis en aquellos pacientes con deterioro severo del filtrado glomerular (FG < 12 ml/min/1,73 m2) y que fueron orientados para realizar hemodiálisis, se programó la creación de un acceso vascular permanente (fístula arteriovenosa nativa).
Todos los accesos vasculares fueron autólogos (ninguna prótesis) y se realizaron en los miembros superiores, siendo elegido el territorio venoso —proximal o distal— por el cirujano vascular tras la exploración clínica.
Las causas de no lograr un acceso vascular funcionante durante el período de estudio fueron: seguimiento demasiado breve en consulta de ERCA, elección de diálisis peritoneal, rechazo por parte del paciente a la realización del acceso, intentos fallidos o no realización por escasa posibilidad de éxito según criterio del cirujano vascular.
En el momento de la inclusión del estudio se extrajo sangre a cada uno de los pacientes para estudio hematológico (hemograma) y bioquímico, que incluía, entre otros, los siguientes parámetros de interés para el estudio: urea, creatinina, albúmina (método bromocresol púrpura), sodio, potasio, cloro, calcio, fósforo, proteinuria en muestras de 24 horas (expresada como miligramos por gramo de creatininuria). Las determinaciones bioquímicas se realizaron con un autoanalizador (Advia® Chemistry, Siemens Healthcare Diagnostics). También se determinó bicarbonato en sangre venosa (analizador de gases ABL 800 FLEX, Radiometer Ibérica).
El FG fue estimado mediante la fórmula MDRD-417.
Diseño del estudio y métodos estadísticos
Estudio de cohorte prospectivo y de observación, en el que la variable de resultado principal fue el desarrollo de al menos un episodio de ICC descompensada definida por criterios clínicos y radiológicos convencionales18 realizados en centro hospitalario durante el período de seguimiento. Otros sucesos analizados fueron la muerte por cualquier causa durante el período de seguimiento prediálisis y el inicio de diálisis, tanto programada como urgente.
La mediana de seguimiento fue de 461 días (rango intercuartílico, 215-897 días).
Para establecer los determinantes del desarrollo de insuficiencia cardíaca se utilizó un modelo de regresión logística multivariable, en el que se introdujeron las siguientes covariables: edad, sexo, índice de masa corporal, presión arterial sistólica y diastólica, hemoglobina, FG, niveles basales séricos de úrico, calcio total, fósforo, fosfatasa alcalina, bicarbonato, potasio, albúmina, hormona paratiroidea, antecedentes de insuficiencia cardíaca, fibrilación auricular, cardiopatía isquémica, prescripción de diuréticos, inhibidores de la enzima conversora de angiotensina/antagonistas de los receptores de angiotensina, betabloqueantes y fístula arteriovenosa funcionante.
La elección de las covariables en el modelo se realizó de forma automática mediante el proceso de eliminación progresiva condicional (hacia atrás).
Para establecer si existía una asociación independiente entre el tipo de acceso vascular y el desarrollo de ICC se utilizaron modelos multivariables de riesgo proporcional de Cox, y se determinaron las relaciones de tasas instantáneas (hazard ratios) con sus intervalos de confianza (IC) del 95%.
Para la comparación de dos variables continuas independientes se utilizó el test t de Student para muestras no pareadas, o el test no paramétrico de Mann-Whitney según las características de distribución de las variables. Para la comparación de variables discretas se utilizó el test χ2.
Los datos de este estudio se presentan como media y desviación estándar (±DE), o como mediana y rangos intercuartiles o valor mínimo-máximo. Una p < 0,05 fue considerada como estadísticamente significativa. El análisis estadístico y los gráficos se realizaron con el programa SPSS versión 15.0 (SPSS, Chicago, EE. UU.).
RESULTADOS
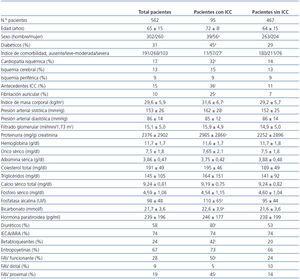
Las características clínicas y analíticas del grupo de estudio se detallan en la tabla 1.
El número total de pacientes que desarrollaron al menos un episodio de ICC fue de 95 (17%). La incidencia fue de 19 episodios por cada 1000 pacientes/año.
En la tabla 1 se muestran las diferencias entre los pacientes que desarrollaron o no ICC. El perfil clínico del paciente que desarrolló ICC en prediálisis se puede resumir como mujer, añosa, obesa, diabética, con antecedentes de cardiopatía isquémica o episodios previos de ICC o fibrilación auricular, con una presión sistólica más elevada, sin diferencias analíticas destacables salvo una fosfatasa alcalina más elevada; tratada más frecuentemente con diuréticos y betabloqueantes, y en quien se había realizado con éxito un acceso vascular, preferentemente proximal (humerocefálica o humerobasílica).
Mediante regresión logística multivariable, los mejores determinantes del desarrollo de un episodio de ICC se detallan en la tabla 2, donde destaca la gran influencia del acceso vascular permanente en el desarrollo del suceso (odds ratio: 9,541; IC 95%: 4,841; 18,806; p < 0,0001).
Durante el período de seguimiento se realizaron con éxito 160 accesos vasculares (51 FAV radiocefálicas y 109 humerocefálicas). Mientras que 4 de los 51 pacientes (8%) con FAV distales desarrollaron ICC, 43 de los 109 pacientes (40%) con FAV proximales desarrollaron esta complicación.
La mediana de tiempo entre la realización de la FAV y el desarrollo del episodio de ICC fue de 51 días (rango intercuartílico 26-138).
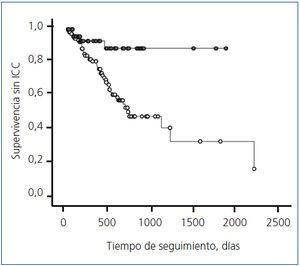
Como se observa en la figura 1, el riesgo de desarrollar ICC durante el período posterior a la realización de la FAV fue significativamente mayor en los pacientes a los que se les realizó una FAV proximal que a los que se les realizó una FAV distal (log-rank =12,13; p < 0,0001).
Como se observa en la figura 1, el riesgo de desarrollar ICC durante el período posterior a la realización de la FAV fue significativamente mayor en los pacientes a los que se les realizó una FAV proximal que a los que se les realizó una FAV distal (log-rank:12,13; p < 0,0001).
El número total de pacientes fallecidos durante el período de seguimiento fue de 97 (17%), con una tasa de mortalidad anual oscilante entre el 8-12%.
No se observaron diferencias en la mortalidad en los pacientes con o sin desarrollo de episodios de ICC (16,5 vs. 17%, respectivamente).
El número total de pacientes que necesitaron iniciar diálisis fue de 304 (54%). Los que desarrollaron ICC necesitaron con más frecuencia iniciar diálisis frente a los que no desarrollaron esta complicación (67 vs. 51%, p = 0,005). Además, el inicio no programado (urgente) de diálisis fue mucho más frecuente entre los que desarrollaron ICC que en el resto (63 vs. 3%, p < 0,0001).
DISCUSIÓN
Los resultados de este estudio muestran que la incidencia de ICC es muy alta en los pacientes con ERC avanzada prediálisis. El conjunto de características que definieron a los pacientes con mayor riesgo de desarrollo de esta complicación (mujer, añosa, diabética, obesa, con antecedentes de cardiopatía, etc.) es típico, y sin duda bien reconocible por aquellos nefrólogos con actividad asistencial. Pero quizá el hallazgo más destacable de este estudio fue la fuerte asociación entre la creación de una FAV y el desarrollo de ICC.
La proximidad temporal entre la realización de la FAV y el desarrollo de ICC, así como la mayor frecuencia de esta complicación en pacientes con FAV proximales, son argumentos para vincular causalmente ambos procesos. Aunque la asociación entre FAV e ICC en pacientes en diálisis se ha considerado casi como un suceso anecdótico7-10, la creación de una FAV provoca una serie de cambios hemodinámicos que pueden favorecer el desarrollo de ICC y que de forma resumida consisten en: aumento del retorno venoso cardíaco, incremento de la frecuencia y contractilidad cardíaca, con aumento de las presiones de llenado, lo que conduce todo ello a un mayor gasto cardíaco que se acompaña de incremento del volumen plasmático y disminución de las resistencias periféricas10,19-21.
En algunos pacientes, sobre todo en aquellos con patología cardíaca previa, este estado circulatorio hiperdinámico no puede ser compensado, desencadenándose la ICC. Además, si persiste de forma crónica, puede provocar cambios estructurales cardíacos —hipertrofia o dilatación ventricular izquierda—, como sugiere la observación de una reversión de esta alteración cuando se ligan las FAV22; y al mismo tiempo puede predisponer a la isquemia miocárdica por desequilibrio entre la cantidad de oxígeno subendocárdico ofertado y el aumento de la demanda de éste debido al mayor gasto cardíaco23.
El incremento del gasto cardíaco es proporcional al flujo arteriovenoso24,25, y este hecho puede ayudar a explicar la mayor probabilidad de desarrollo de ICC en los pacientes en los que se realizó una FAV proximal.
Los resultados de este estudio plantean dos cuestiones: ¿por qué desarrollan ICC con más frecuencia los pacientes prediálisis en los que se crea una FAV que en los ya sometidos a diálisis?, y ¿cómo se podría prevenir esta complicación?
La primera cuestión podría ser explicada por la escasa capacidad de compensación que tienen un buen número de estos pacientes ante un incremento forzado del gasto cardíaco, y porque a diferencia de los pacientes ya sometidos a hemodiálisis, en aquellos seguidos en la consulta de ERCA no es posible ejercer un control tan exhaustivo (tres veces por semana) ni un tratamiento tan efectivo (ultrafiltración) de una ICC en curso.
La medida más simple para prevenir esta complicación cardiovascular podría ser la de no realizar FAV prediálisis, aunque esta opción no nos parece recomendable, ya que la relación beneficio/riesgo de una FAV prediálisis es probablemente muy superior a la del uso de los catéteres temporales. Como se muestra en este estudio, la ICC no se asoció con una mayor mortalidad prediálisis, y el efecto adverso más destacable fue el inicio urgente (no programado) de la hemodiálisis.
Los resultados de este estudio también pueden ayudar a sugerir a los cirujanos vasculares que intenten agotar todas las posibilidades para conseguir FAV distales en pacientes en prediálisis, sobre todo en aquéllos con factores de riesgo para el desarrollo de ICC, aunque son precisamente las características clínicas y la disponibilidad de vasos de estos últimos los que más dificultades plantean para lograr FAV radiales.
Como última posibilidad, sería recomendable un seguimiento más estrecho de la respuesta y la tolerancia cardiovascular a la creación de la FAV, que permitiera un diagnóstico precoz de la ICC, y control, en caso necesario, de la sobrehidratación, sobre todo en los pacientes con más alto riesgo.
Este estudio tiene limitaciones. No se realizaron mediciones hemodinámicas (flujo de FAV, gasto cardíaco, etc.) ni estudios ecocardiográficos seriados, por lo que la vinculación patogénica entre la ICC y la realización de la FAV está basada en la observación clínica y epidemiológica. Tampoco se recogió información sobre la incidencia y peculiaridades de la ICC en pacientes ya sometidos a hemodiálisis, por lo que la afirmación de una menor asociación de episodios de ICC relacionados con los accesos vasculares en estos pacientes se sustenta en la experiencia ajena reportada en la literatura.
En conclusión, la incidencia de ICC es muy elevada en pacientes con ERC avanzada prediálisis. Además de los factores de riesgo clásicos, la realización de un acceso vascular incrementa significativamente la probabilidad de desarrollo de esta alteración cardiovascular. Este hecho se debe tener en cuenta en pacientes con alto riesgo a los que se les programa la realización del acceso vascular.
Conflictos de interés
Los autores declaran que no tienen conflictos de interés potenciales relacionados con los contenidos de este artículo.
Tabla 1. Características clínicas y analíticas del grupo total y de los subgrupos según el desarrollo o no de insuficiencia cardíaca congestiva
Tabla 2. Determinantes del desarrollo de insuficiencia cardíaca descompensada en el grupo de estudio, mediante regresión logística múltiple
Figura 1. Riesgo de desarrollar insuficiencia cardíaca congestiva durante el período posterior a la realización de la fístula arteriovenosa