Se reconocen 2 variedades de hiperpotasemia temprana de la infancia (del inglés Early childhood hyperkalemia) según la presencia o no de pérdida salina urinaria. Se trata de una entidad atribuida a un desorden madurativo en los receptores de aldosterona caracterizada por hiperpotasemia, acidosis metabólica hiperclorémica por diminución de la eliminación de amonio y bicarbonaturia, y creatinina normal con retraso de crecimiento. Presentamos 3 pacientes de la forma con ausencia de pérdida salina, a la que denominaremos hiperpotasemia transitoria del lactante sin pérdida salina, y discutimos su fisiopatología con relación a los nuevos conocimientos en el manejo tubular del sodio y el potasio por la aldosterona. En 3 pacientes de entre 30 y 120 días de edad con bronquiolitis y retraso de crecimiento se encontró hiperpotasemia en laboratorio de rutina. Presentaban creatinina normal, excreción fraccionada de potasio disminuida o inapropiadamente normal junto a niveles de aldosterona y renina plasmática inadecuadamente normales para el estado de hiperpotasemia, pero sin pérdida salina. También cursaban con acidosis metabólica hiperclorémica con bicarbonaturia (excreción fraccionada de bicarbonato 0,58-2,2%), anión restante urinario positivo durante acidosis metabólica y capacidad normal para acidificar la orina. En base a estos hallazgos se diagnosticó hiperpotasemia transitoria del lactante sin pérdida salina y se trataron con bicarbonato de sodio e hidroclorotiazida con buena respuesta. El cuadro fue transitorio permitiendo la suspensión del tratamiento. Dado que la hiperpotasemia transitoria del lactante sin pérdida salina es un desorden tubular transitorio con síntomas leves debe tenerse presente en el diagnóstico diferencial de hiperpotasemia en niños pequeños.
Two types of early-childhood hyperkalemia had been recognized, according to the presence or absence of urinary salt wasting. This condition was attributed to a maturation disorder of aldosterone receptors and is characterized by sustained hyperkalemia, hyperchloremic metabolic acidosis due to reduced ammonium urinary excretion and bicarbonate loss, and normal creatinine with growth delay. We present three patients of the type without salt wasting, which we will call transient early-childhood hyperkalemia without salt wasting, and discuss its physiopathology according to new insights into sodium and potassium handling by the aldosterone in distal nephron. In three children from 30 to 120-day-old admitted with bronchiolitis and growth delay hyperkalemia was found in routine laboratory. Further studies revealed a normal creatinine with inappropriately normal or low fractional excretion of potassium, accompanied by inadequately normal serum aldosterone and plasma renin activity for their higher plasma potassium levels, but without urine salt wasting. They also presented hyperchloremic metabolic acidosis with fractional excretion of bicarbonate 0.58–2.2%, positive urinary anion gap during metabolic acidosis and normal ability to acidify the urine. Based on these findings a diagnosis of transient early-childhood hyperkalemia without salt wasting was made and they were treated sodium bicarbonate and hydrochlorothiazide with favorable response. The condition was transient in all cases leading to treatment discontinuation. Given that transient early-childhood hyperkalemia without salt wasting is a tubular disorder of transient nature with mild symptoms; it must be keep in mind in the differential diagnosis of hyperkalemia in young children.
En el año 1981, McSherry menciona en un Nephrology Forum sobre acidosis tubular renal a un grupo de 13 lactantes con una entidad a la que denominó Early childhood hyperkalemia1. La misma se caracterizaba por la presencia de hiperpotasemia y acidosis metabólica (AM) hiperclorémica debida a disminución en la eliminación de amonio y bicarbonaturia. En orina presentaban además excreción fraccionada (EF) de potasio (K+) disminuida o inapropiadamente normal para los valores elevados de K+ sérico y EF de sodio (Na+) normal, con valores de actividad de renina y aldosterona plasmática elevados o inadecuadamente normales. Este síndrome fue atribuido a un probable desorden madurativo, en el número o función de los receptores mineralocorticoides del túbulo distal, que originaría una resistencia a la acción de la aldosterona en la nefrona distal1–3. Sin embargo, esta teoría no explicaba la ausencia de pérdida salina que ocurría en estos pacientes4. En 1986 Appiani et al. publican por primera vez los casos de 5 pacientes con Early childhood hyperkalemia, pero con un fenotipo diferente, ya que a diferencia de los casos anteriores, presentaban pérdida salina por orina2. Debido a que posteriormente, según nuestro conocimiento, no se han reportado nuevos casos, presentamos 3 pacientes adicionales con el síndrome descripto por McSherry1, al que denominaremos a lo largo del manuscrito como «hiperpotasemia transitoria del lactante sin pérdida salina» (HTL sin pérdida salina) para diferenciarlo de la variante descripta por Appiani et al.2, y aportar un nuevo enfoque fisiopatológico en función de los avances en el conocimiento de los canales y transportadores que regulan el transporte de Na+ y de K+ mediados por la aldosterona en el túbulo distal.
MétodosLos gases en sangre se determinaron en muestras capilares arterializadas. El pH y la pCO2 en sangre y en orina fueron determinados por un equipo ABL 520® en tanto que el Na+ y el K+ lo fueron con un analizador ion específico Radiometer®. Las orinas fueron recolectadas por sonda vesical y se mantuvieron en forma anaeróbica en jeringa sellada hasta que se determinó pH, pCO2 y bicarbonato (HCO3−) urinario (pHu, pCO2u y HCO3-u respectivamente). El HCO3-u fue calculado a través de la ecuación de Henderson-Hasselbalch, usando la constante de solubilidad de la pCO2 de la sangre (α=0,00301) y un pK sanguíneo de 6,15. El amonio urinario fue inferido por el anión restante (AR) urinario, frente a la AM espontánea o durante el test de furosemida6. Las EF de Na+, K+ y HCO3− fueron calculadas con la fórmula (u/p de la sustancia) / (u/p creatinina)×100; donde u y p representan las concentraciones en orina y plasma respectivamente. La creatinina se determinó con el método de Jaffé en tanto que la aldosterona y la renina plasmática fueron medidas por radioinmunoanálisis en muestras recolectadas a las 9 de la mañana. Hipercloremia se definió como una concentración de cloro (Cl−)>75% de la concentración de Na+7. El AR plasmático se calculó con la fórmula Na+–(Cl−+HCO3−) considerándose un valor normal de 12±2, y el urinario con la fórmula (Na++K+)–Cl- considerando que todo valor negativo permite inferir una excreción normal de amonio en tanto que cualquier valor positivo refleja una disminución de su excreción. La prueba de sobrecarga alcalina, para determinar la diferencia de la pCO2 en sangre y orina (pCO2u-s), fue adaptada para su utilización en niños y se consideró normal una diferencia≥20mmHg8. La calciuria se determinó en orina aislada, promediando 3 determinaciones, dividiendo la concentración de calcio con la de la creatinina considerando un valor normal<0,89. El gradiente transtubular de potasio fue calculado con la fórmula (U/P de K+) / (U/P osmolar)x100, la osmolaridad se midió con osmómetro de presión de vapor (Wescor®) y esperando en lactantes con hiperpotasemia un valor>53. Los valores normales de electrólitos así como los de la creatinina fueron los habituales para los grupos etarios estudiados9-12. La tensión arterial fue registrada con dispositivo oscilométrico, se realizaron 3 lecturas sucesivas considerando el valor promedio de las 3 mediciones13.
PacientesTres pacientes (2 de sexo masculino) de 30, 45 y 120 días respectivamente que se internaron por síndrome bronquiolítico presentaron parámetros de laboratorio compatibles con HTL sin pérdida salina. Dos de ellos carecían de antecedentes perinatológicos, en tanto que el de 120 días había nacido a las 30 semanas de gestación con un peso de 1,735kg (peso adecuado para la edad gestacional) y había presentado enfermedad de membrana hialina requiriendo 7 días de asistencia respiratoria mecánica. Durante la internación en todos los casos se constató hiperpotasemia sostenida, acompañada de natremia normal y AM hiperclorémica. Ninguno recibía medicación o aporte exógeno que pudiera condicionar elevación del K+ sérico; además, dicho trastorno persistía a pesar del tratamiento con agonistas β2 indicado por el cuadro respiratorio. Todos cursaron con tensión arterial normal, el paciente de 30 días tenía 70/50mmHg, el de 45 días 75/55mmHg y el restante 70/50mmHg. Los valores de AR, ácido láctico, amonio y creatinina en sangre fueron normales en todos los pacientes. La actividad de renina plasmática y la aldosterona sérica fueron inadecuadamente normales en los 3 casos. Además, todos presentaron EFK+ baja o inapropiadamente normal para el grado de hiperpotasemia con EFNa+ normal (tabla 1). El gradiente transtubular de potasio se determinó solo en el paciente de 120 días y su valor fue de 2,66. La excreción de calcio fue normal, con valores de 0,66, 0,5 y 0,72 en los pacientes de 30, 45 y 120 días respectivamente y se descartó infección urinaria por urocultivo negativo. Las ecografías renales fueron normales, sin hallazgos compatibles con uropatía como dilatación de la vía urinaria y/o patología vesical. Se descartó hiperplasia suprarrenal congénita en base al hallazgo de genitales externos normales junto a dosajes séricos de 17-OH progesterona, 18-OH corticosterona, ACTH, cortisol y sulfato dehidroepiandrosterona sérica también normales. El AR urinario fue positivo, negativizándose tras de la administración de furosemida; en tanto que la EFHCO3− fue elevada luego de normalizar sus valores en sangre con alcalinos (tabla 2). Además, se descartó compromiso en la eliminación de hidrogeno (H+) por el túbulo distal como causa de la AM, ya que la pCO2 u-s fue normal (>20mmHg) (tabla 3).
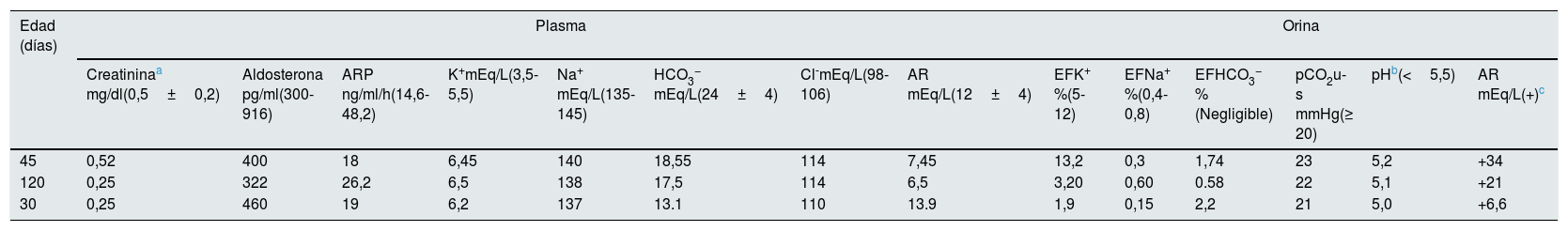
Perfil metabólico en 3 pacientes con hiperpotasemia transitoria del lactante sin pérdida salina
| Edad (días) | Plasma | Orina | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Creatininaa mg/dl(0,5±0,2) | Aldosterona pg/ml(300-916) | ARP ng/ml/h(14,6-48,2) | K+mEq/L(3,5- 5,5) | Na+ mEq/L(135-145) | HCO3− mEq/L(24±4) | Cl-mEq/L(98-106) | AR mEq/L(12±4) | EFK+ %(5-12) | EFNa+ %(0,4-0,8) | EFHCO3− %(Negligible) | pCO2u-s mmHg(≥ 20) | pHb(<5,5) | AR mEq/L(+)c | |
| 45 | 0,52 | 400 | 18 | 6,45 | 140 | 18,55 | 114 | 7,45 | 13,2 | 0,3 | 1,74 | 23 | 5,2 | +34 |
| 120 | 0,25 | 322 | 26,2 | 6,5 | 138 | 17,5 | 114 | 6,5 | 3,20 | 0,60 | 0.58 | 22 | 5,1 | +21 |
| 30 | 0,25 | 460 | 19 | 6,2 | 137 | 13.1 | 110 | 13.9 | 1,9 | 0,15 | 2,2 | 21 | 5,0 | +6,6 |
AR: anión restante; ARP: actividad de renina plasmática; EF: excreción fraccionada; pCO2 u-s diferencia de la pCO2 en sangre y orina.
Entre paréntesis se muestran los valores normales para la edad
Determinación de la bicarbonaturia y de la excreción fraccionada de bicarbonato en 3 pacientes con hiperpotasemia transitoria del lactante sin pérdida salina
| Edad (días) | HCO3-s mEq/L | pHu | pCO2u mmHg | HCO3-u mEq/L | EFHCO3− % |
|---|---|---|---|---|---|
| 30 | 21 | 7,15 | 40 | 15 | 2,2 |
| 45 | 23.6 | 7,0 | 46,7 | 12,5 | 1,74 |
| 120 | 22 | 7,1 | 30 | 11 | 0,58 |
Valores luego de la administración de sobrecarga alcalina.
s Determinación en suero.
u Determinación en orina.
Prueba de sobrecarga alcalina para determinar la diferencia de pCO2 entre orina y sangre (pCO2 u-s) en 3 pacientes con hiperpotasemia transitoria del lactante sin pérdida salina
| Edad (días) | pHu | pCO2u mmHg | HCO3-u mEq/L | pCO2 u-s mmHg |
|---|---|---|---|---|
| 30 | 7,48 | 55 | 39 | 21 |
| 45 | 7,50 | 60 | 45 | 23 |
| 120 | 7,49 | 67 | 40 | 22 |
Valores luego de la administración de sobrecarga alcalina.
s Determinación en suero.
u Determinación en orina.
El tratamiento de la hiperpotasemia se realizó con resinas de intercambio catiónico a 1g/kg/cada 8-12h y furosemida a 1mg/kg/cada 6h. Esta última fue luego reemplazada por hidroclorotiazida, para evitar la hipercalciuria de los diuréticos de asa. Sin embargo, recién se logró normalizar la concentración sérica de K+, al igual que la AM, tras la adición de bicarbonato de sodio por vía oral a 2mEq/kg/día. Durante el seguimiento, el tratamiento fue suspendido en algunas oportunidades con reaparición de los trastornos metabólicos, hasta que se constató la resolución definitiva a los 6, 7 y 11 meses en los pacientes de 30, 120 y 45 días respectivamente. Durante la evolución se observó en todos los casos recuperación de peso y talla; el paciente de 30 días pesaba al momento del diagnóstico 3,6kg (percentilo 3-10) y su talla era de 52cm (percentilo 10) alcanzando a los 6 meses de vida un peso de 7,9kg y una talla de 67cm, ambas en el percentilo 25-50. En el caso del de 45 días, que al inicio tenía un peso de 3,6kg y una talla de 50cm, ambas por debajo del percentilo 3, a los 11 meses de vida alcanzó un peso de 9,4kg (percentilo 50) y una talla de 74cm (percentilo 25-50). De manera similar, el paciente de 120 días que presentaba un peso de 3,25kg (percentilo 3) y una talla de 52cm (percentilo 3-10) al diagnóstico alcanzó un peso de 5,5kg y una talla de 60cm, ambas mediciones en percentilo de 25-50 a los 7 meses de vida.
DiscusiónEn este estudio se describen en detalle 3 pacientes con HTL sin pérdida salina con un patrón metabólico semejante a los comentados por McSherry1. Los mismos presentaron AM inducida por la misma hiperpotasemia ya que ésta inhibe la amoniogénesis produciendo disminución de la eliminación urinaria de amonio14. Además, la elevación de la concentración de K+ también es responsable de la bicarbonaturia observada, que si bien se manifestó por una excreción menor a la observada en la ATR proximal, es superior a la que ocurre en lactantes y niños sanos en quienes la eliminación de HCO3− es negligible15. Por lo tanto, la AM persistente producida por los 2 mecanismos mencionados pudo causar el retardo de crecimiento observado en estos niños. La eliminación de H+ por el túbulo colector cortical (TCC) fue adecuada en base a que la pCO2 u-s fue normal, que es el marcador más sensible en la eliminación de H+ por las células intercaladas α, con lo que se puede descartar ATRD. Merece mencionarse que si bien en aquellas debidas a defecto de gradiente por aumento de la permeabilidad de la membrana luminal del TCC, como puede ocurrir en la toxicidad por anfotericina, la pCO2 u-s es normal (≥20mmHg) pero el pH urinario se mantiene superior a 5,5 frente a la AM16, contrario a lo observado en los pacientes presentados en los que descendió de 5,5, lo que indica que es poco probable que dicho mecanismo sea responsable de la acidosis. Nuestros pacientes pueden diferenciarse del seudohipoaldosteronismo tipo 13 y del secundario a infección urinaria y/o malformaciones del tracto urinario17, por la ausencia de pérdida salina por el riñón y de hiponatremia, así como por la ausencia de hallazgos ecográficos compatibles con uropatía y el urocultivo negativo. También pueden diferenciarse del cuadro descripto por Spitzer-Weinstein, caracterizado por un patrón similar al síndrome de Gordon pero sin hipertensión arterial, por la menor edad de presentación, la necesidad de asociar bicarbonato de sodio a las tiazidas para normalizar el medio interno y la transitoriedad del cuadro18.
Dos pacientes presentaban una disminución marcada de la EFK+ (1,9% y 3,2%); consistentemente, en el paciente en el que se calculó el gradiente transtubular de potasio se observó un valor bajo concordante con la EFK+ disminuida. Además, merece mencionarse que en el paciente de 45 días la EFK+ también fue considerada inadecuada para su hiperpotasemia pese a tener un valor normal de 13,2% ya que en situaciones de hiperpotasemia aguda y crónica la EFK+ debe aumentar dramáticamente19.
Como hemos mencionado previamente, la fisiopatología de los pacientes presentados por McSherry fue atribuida a un probable desorden madurativo de los receptores mineralocorticoides del túbulo distal1,2. Sin embargo, esta teoría no explica la ausencia de pérdida salina que sería esperable junto a la retención de K+ al no poder unirse adecuadamente la aldosterona a su receptor tubular, como sucede en el seudohipoaldosteronismo tipo 1 o secundario a infección urinaria y/o uropatías3,17.
En estudios realizados en mamíferos recién nacidos se ha observado la presencia de un número adecuado de receptores para aldosterona así como de los sitios de unión del complejo hormona-receptor a nivel nuclear, por lo que actualmente se considera que el fenómeno de hiposensibilidad temprana a aldosterona representa un fenómeno posreceptor19. Esto podría explicar la disociación de la respuesta normal a la aldosterona observada en los pacientes presentados, quienes retenían K+ anormalmente pero conservaban una adecuada reabsorción de Na+. De hecho, el complejo mineralocorticoide-receptor una vez en el núcleo, en una primera fase temprana, produce la activación y represión de genes capaces de modular la actividad de los principales transportadores de Na+ y K+ ya existentes en los segmentos tubulares distales, especialmente la bomba Na+/K+ ATPasa, el cotransportador Na+/Cl− sensible a tiazidas (NCC) y el Canal Epitelial de Sodio (ENaC)20. Entre esos genes inducidos precozmente por la aldosterona también se encuentran distintas quinasas, entre ellas las WNK4 (quinasas deficientes en lisina), la Sgk-1 (quinasa regulada por suero y glucocorticoides 1) y las de la familia de proteínas tirosin-quinasas Src (SFK)20–24. Posteriormente, en su fase tardía, modula directamente los niveles de expresión de los diferentes transportadores de Na+ y K+20. De esta forma, la aldosterona favorece la reabsorción de Na+ estimulando la bombas Na+/K+ ATPasa, el NCC y el ENaC; y también en forma indirecta por intermedio de la Sgk-1 que estimula la actividad de ENaC y de la bomba Na+/K+ ATPasa20,22. Con relación al manejo de K+, la acción de la aldosterona se produce modulando a través de distintas quinasas las acciones de los canales ROMK (canal renal medular externo de potasio) que regulan el eflujo del catión en el túbulo colector20,21. La WNK4 inhibe la expresión de los canales ROMK disminuyendo la excreción de K+, acción revertida por la Sgk121,23,25. Además, la inhibición de la WNK4 por la SgK1 es atenuada por las SFK para prevenir la secreción de K+ en ausencia de hiperpotasemia23. Esta atenuación se observa también en la hipovolemia, en la que hay un aumento de aldosterona y de la actividad de la SgK1 con lo que ocurre ganancia de Na+ y aumento de la excreción de K+. Pero, si concomitantemente el ingreso de K+ es bajo, como fue mencionado previamente, la SFKs atenúa la SgK1, por lo cual la WNK4 restaura la inhibición de los ROMK, disminuyendo la eliminación de K+. En esta situación puede verse cómo los efectos de la aldosterona pueden disociarse23. Otra situación donde se observa esta disociación es en los pacientes con síndrome de Gordon (seudohipoaldosteronismo tipo 2) en el que los mecanismos inhibitorios distintos de las WNK4 mutadas sobre los NCC y los canales ROMK podrían explicar dicho desacoplamiento. Las mutaciones sin sentido de dichas quinasas producen pérdida de la inhibición sobre la expresión de los NCC generando retención de Na+ e hipertensión arterial y, por otro lado, aumento de la inhibición sobre los canales ROMK, expresándose con hiperpotasemia26. De manera similar, la falta de coordinación entre el complejo mecanismo de regulación y contrarregulación de las quinasas, especialmente de la WNK4 como regulador multifuncional que puede disociar los efectos de la aldosterona sobre la excreción de Na+ y K+, podría ser la responsable de lo observado en los pacientes presentados, que reabsorbían normalmente Na+ pero que presentaban excreción de K+ disminuida. Esto podría representar la acentuación de un proceso fisiológico necesario en los recién nacidos y en los lactantes en los primeros meses, quienes necesitan un balance positivo de K+ y de Na+ para afrontar el rápido crecimiento somático al que son sometidos. El mismo se debe fundamentalmente a ganancia de dichos electrólitos por el TCC, hecho que también genera que tengan niveles séricos de K+ más elevados que los lactantes mayores y los niños25,27,28. Aún más, como se ha demostrado en modelos animales durante las primeras 3 semanas de vida posnatal, hay ausencia de expresión de la proteína del canal ROMK de las células principales del TCC, alcanzando recién a las 6 semanas de vida una excreción de K+ comparable a la del adulto29. En la misma línea, el canal Maxi K+, que es el otro canal implicado en la secreción de K+ en TCC, particularmente frente al aumento del flujo tubular distal, recién se expresa a la quinta semana de vida postnatal29,30, por lo que podría ser otro factor que contribuye a la hiperpotasemia. Estas observaciones también explicarían el hecho de que se trate de un desorden tubular transitorio, como ocurrió en nuestros pacientes.
En conclusión, se podría inferir que el HTL sin pérdida salina podría expresar la exageración de un fenómeno madurativo, caracterizado por una expresión más tardía de los canales que regulan el manejo del K+ en el TCC bajo influencia de la aldosterona, cuya maduración es normalmente lenta a fin de asegurar una alta ganancia de K+ necesaria para el rápido crecimiento somático. Dado que se trata de una entidad transitoria y con pocas manifestaciones clínicas debe tenerse presente entre las causas de hiperpotasemia y retraso de crecimiento en los primeros meses de vida.
Conflicto de interesesNada que declarar.
La presente investigación no ha recibido ayudas específicas provenientes de agencias del sector público, sector comercial o entidades sin ánimo de lucro.
El presente estudio fue aprobado por el Comité de Ética de nuestra Institución.