Sr. Director:
La sarcoidosis puede inducir nefritis intersticial granulomatosa (15-40 %), alteraciones en el equilibrio calcio-fósforo (hipercalciuria 50 %, hipercalcemia 10 %), tubulopatía distal con diabetes insípida nefrogénica, uropatía obstructiva y glomerulonefritis (GN) membranosa; en menor proporción, membranoproliferativa, mesangial o focal y segmentaria (GNFyS). Exponemos un ejemplo alusivo.
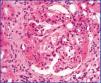
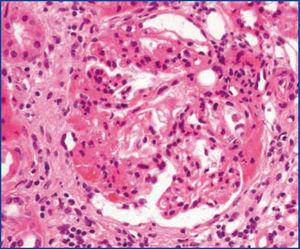
Se trata de un varón marroquí de 35 años, sin enfermedades previas. Consulta por proteinuria. Exploración física sin hallazgos. Analítica con creatinina en plasma 1,1 mg/dl, aclaramiento creatinina 97 ml/min/1,73 m2, proteinuria 3,67 g/d, glomerular no selectiva. Albúmina 3,9 mg/dl, colesterol 239 mg/dl, sistemático de orina con proteinuria 300 mg/dl y microhematuria. Velocidad de sedimentación globular 8 mmHg 1.ª hora, serología vírica, marcadores tumorales, perfil tiroideo, inmunología, proteinograma, inmunoelectroforesis de proteínas en plasma y orina, perfil hepatopancreático y radiografía de tórax normales. Ecografía renal con riñones de 110 y 114 mm y cortical conservada. Biopsia renal (figura 1) que demuestra 7 glomérulos: 3 esclerosados, 4 con lesiones hialinas segmentarias, proliferación celular y sinequias, ampliación mesangial, fibrosis y atrofia tubular grado I/III, intersticio con infiltrados linfoplasmocitarios. Arterias y arteriolas sin lesiones. A la inmunofluorescencia directa: depósitos de IgM y C’3 en el mesangio. No se realizó microscopia electrónica (ME). Con diagnóstico de GNFyS, se inicia tratamiento con inhibidores de la enzima de conversión de angiotensina (IECA). A los 3 meses la proteinuria disminuye a 1 g/d. Se inicia doble bloqueo (IECA y antagonistas de los receptores de angiotensina II). A los 6 meses mantiene filtrado glomerular (FG) estable y una proteinuria de 0,5-0,7 g/día. A los 12 meses, debuta con dolor abdominal, diarrea, vómitos y aumento de amilasa. Se realiza tomografía computarizada (TC) tóraco-abdominal que objetiva adenopatías laterocervicales, axilares hiliares, mediastínicas y del hilio hepático y nódulos centrolobulillares. Serie ósea y perfil tiroideo normales, serología para virus de Epstein-Barr, citomegalovirus, rubeola, brucella, lúes y toxoplasma y marcadores tumorales negativos, enzima convertidora de angiotensina 46,3 U/l (rango 20-70), 25 OH vitamina D3 15,3 ng/ml, 1-25 di(OH) vitamina D3 45,4 ng/ml (rango 18-78), hormona paratiroidea intacta: 30 pg/ml (rango 15-60), calciuria 40 mg/d, fosfaturia 732 mg/d, calcemia 10 mg/dl, fosfatemia 3,0 mg/dl. Broncoscopia con lavado broncoalveolar y punción-aspiración de ganglio mediastínico que evidencia celularidad de predominio macrofágico. Biopsia transbronquial sugerente de proceso inflamatorio granulomatoso, no necrotizante, acúmulos de histiocitos y células gigantes multinucleadas. Tinción de Zhiel Nielsen y cultivo de Lowenstein negativo. Lavado broncoalveolar con celularidad de predominio linfocitario y aumento de la razón CD4/CD8. Con diagnóstico de sarcoidosis, se inicia tratamiento con prednisona, que se mantiene 12 meses. Evoluciona positivamente. TC a los 6 meses con desaparición de adenopatías mediastínicas y de afectación parenquimatosa. Tras 24 meses, el FG permanece estable, mantiene proteinuria de 0,5 g/d y no han ocurrido incidencias de consideración.
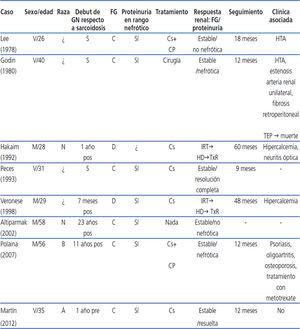
La asociación entre sarcoidosis y GNFyS data de 19781. Solo hay 7 casos descritos en PubMed1-7 (tabla 1). Afectan a un 50 % de varones, con edad media de 37,8 años. En todos, la proteinuria se encontraba en rango nefrótico. Solo en 2 se acompañó de insuficiencia renal y en ambos progresó a terminal, precisando hemodiálisis y posteriormente trasplante renal. En todos los casos la respuesta a la clínica pulmonar fue buena; no así la evolución de la proteinuria, que se mantuvo en rango nefrótico en 4, disminuyó cuantitativamente en 2 y se resolvió en otros 2. El diagnóstico de GN con posterioridad al de sarcoidosis ocurrió en el 50 % de casos. En todas las biopsias existía esclerosis glomerular, lesiones segmentarias y focales y hialinosis. Atrofia tubular solo en 5, infiltración inflamatoria intersticial en 4, sinequias e incremento de la matriz mesangial en 3, fibrosis periglomerular en 2 e Inmunofluorescencia directa negativa en 2, con depósitos de IgG en 1, C’3 en 4, IgM en 4 y C’1q en 1 caso situados en mesangio y subendotelio. Solo se realizó ME en 2 casos; en ambos se puso de manifiesto fusión podocitaria y ausencia de inmunocomplejos. En solo uno2 de los casos descritos se encontraron granulomas renales intersticiales, lo cual supone una afectación del 12,5 %, menor de lo referido en la literatura (15-40 %). Resulta destacable la buena evolución del FG y de la proteinuria con tratamiento conservador, evolución que no mejoró al añadir corticoterapia por su patología pulmonar.
Esta asociación puede resultar paradójica. En la sarcoidosis existe un disbalance inmunitario con suprarregulación de la vía TH1, y en la GNFyS una suprarregulación de la vía TH28,9. Sin embargo, en fases tardías predomina la TH17, que induce la secreción de interleucina 1710 que favorece el desarrollo de fibrosis. La citocina 1 similar a la cardiotrofina, que se halla implicada en el desarrollo de GNFyS, está aumentada en la vía TH1711-13, lo que podría ser el vínculo entre ambas11.
Exponemos, pues, el caso de un paciente con debut de GNFyS que al año fue diagnosticado de sarcoidosis, con buena evolución pulmonar y renal a tratamiento con corticoides y bloqueo del sistema renina-angiotensina-aldosterona.
Conflictos de interés
Los autores declaran que no tienen conflictos de interés potenciales relacionados con los contenidos de este artículo.
Figura 1. Glomerulosclerosis focal y segmentaria
Tabla 1. Resumen de casos publicados de glomerulonefritis focal y segmentaria asociada a sarcoidosis