Los pacientes con infección por el virus de la inmunodeficiencia humana (VIH) y enfermedad renal que terminan en tratamiento sustitutivo renal constituyen un grupo especial con interés creciente para la nefrología. Con el objetivo de conocer datos epidemiológicos de los pacientes VHI+ en España, recogimos información individualizada durante los años 2004 a 2011 (periodo de uso de tratamiento antiviral de alta eficacia) en las comunidades autónomas (CCAA) de Andalucía, Aragón, Asturias, Cataluña, Comunidad Valenciana, Castilla-La Mancha, Castilla y León, Galicia, Madrid, La Rioja y País Vasco, que comprendían un 85% de la población española. Se analizó a un total de 271 pacientes incidentes y 209 prevalentes. Se compararon con el resto de pacientes en tratamiento sustitutivo durante el mismo periodo de tiempo. La incidencia anual fue de 0,8 pacientes por millón de habitantes, con un aumento significativo a lo largo del periodo de seguimiento. La proporción de pacientes prevalentes VIH+ fue de 5,1/1.000 pacientes en tratamiento sustitutivo, intervalo de confianza (IC) del 95%: 4,4-5,8. Las causas glomerulares constituyeron la mayoría (42%), aunque hubo un 14% de nefropatía diabética. En el total de España, esos porcentajes son 13 y 25%, respectivamente. Comparando frente al total de pacientes en tratamiento, el riesgo de muerte fue significativamente mayor en el grupo VIH+: hazard ratio (HR) ajustado por edad, sexo y presencia de diabetes: 2,26 (IC 95%: 1,74-2,91). La coinfección por hepatitis C aumentó el riesgo de muerte dentro del grupo VIH+: HR 1,77 (IC 95%: 1,10-2,85). La probabilidad de recibir trasplante renal en los VIH+ solo alcanzó el 17% a los 7 años, comparando con el total de pacientes en diálisis HR: 0,15 (IC 95%: 0,10-0,24).
A pesar del uso de las nuevas combinaciones de antivirales, la incidencia de pacientes VIH+ en diálisis se ha incrementado, su mortalidad supera todavía al resto de pacientes, y tienen una tasa de trasplante muy baja. Se hace necesario profundizar en el conocimiento de esta enfermedad para mejorar los resultados.
Patients on renal replacement therapy (RRT) infected with the human immunodeficiency virus (HIV) are a special group with growing interest. In order to study the epidemiological data of HIV+ patients on RRT in Spain, we collected individual information from 2004-2011 (period of use of highly active antiretroviral therapy [HAART] in the Autonomous Communities of Andalusia, Aragon, Asturias, Catalonia, Valencia, Castilla la Mancha, Castilla León, Galicia, Madrid, La Rioja and the Basque Country, comprising 85% of the Spanish population. A total of 271 incident and 209 prevalent patients were analysed. They were compared with the remaining patients on RRT during the same period. The annual incidence was 0.8 patients per one million inhabitants, with a significant increase during the follow-up period. The proportion of prevalent HIV+ patients was 5.1 per 1,000 patients on RRT (95% confidence interval [CI] 4.4-5.8. Although glomerular diseases constituted the majority of cases (42%), diabetic nephropathy was the cause in 14% of patients. The nation-wide totals for these percentages were 13 and 25%, respectively. Compared to the total of patients in treatment, the risk of death was significantly higher in the HIV+ group: hazard ratio (HR) adjusted for age, sex and diabetes was 2.26 (95% CI 1.74 - 2.91). Hepatitis C coinfection increased the risk of death in the HIV+ group (HR 1.77; 95% CI 1.10 - 2.85). The probability of kidney transplantation in HIV+ was only 17% after 7 years, comparing with total RTT patients (HR 0.15; 95% CI: 0.10-0.24).
Despite the use of HAART, the incidence of HIV+ patients on dialysis has increased; their mortality still exceeds non-HIV patients, and they have a very low rate of transplantation. It is necessary to further our knowledge of this disease in order to improve results.
El perfil de los pacientes afectados por el virus de la inmunodeficiencia humana (VIH) ha cambiado de forma significativa desde mediados de los años 90, tras la introducción del tratamiento antirretroviral de alta eficacia (TARGA). Mientras que la mayoría de estos pacientes que iniciaban diálisis en época pre-TARGA lo hacían por nefropatía asociada al VIH (NAVIH), en los últimos años las etiologías son diversas, destacando, junto a la previa, la nefropatía diabética, la nefroangioesclerosis y la nefrotoxicidad1. No obstante, la incidencia de enfermedad renal crónica en tratamiento sustitutivo (ERC-5D) en estos pacientes no ha disminuido.
Los pacientes con infección por VIH constituyen un grupo con algunas características diferentes del resto2. El nivel de inmunocompetencia condiciona la selección de pacientes para incluir en lista de espera, y para lograr una aceptable supervivencia es necesario un protocolo especial de manejo postrasplante3. Sin embargo, a pesar del uso de protocolos específicos, se ha observado una mayor tasa de retraso en la función del injerto en los pacientes VIH+4. La coexistencia de insuficiencia renal con la infección VIH incrementa el riesgo de enfermedades cardiovasculares5.
En nuestro país la incidencia y la prevalencia de esta infección en los sujetos en ERC-5D se asumen como bajas, pero no hay estudios poblacionales y globales que las cuantifiquen6.
Disponemos de publicaciones españolas que describen sus características específicas, lo que refleja el interés existente por profundizar en este problema7. Recientemente 3 sociedades científicas (Sociedad Española de Nefrología, Grupo de Estudio del SIDA-SEIMC y Sociedad Española de Química Clínica y Enfermedad Molecular) han elaborado un exhaustivo documento de consenso sobre la detección y manejo de las alteraciones renales en pacientes con infección por el VIH, con recomendaciones específicas para pacientes con distintos estadios de enfermedad renal, así como para pacientes en diálisis y trasplante. Este documento está disponible en las webs de las 3 sociedades científicas participantes8.
Actualmente en casi todas las comunidades autónomas (CCAA) de España existe un registro de pacientes en ERC-5D, donde, además de la información básica, se registran también datos sobre infecciones virales como hepatitis B, C y VIH.
Con estas premisas nos propusimos realizar un estudio epidemiológico en nuestro país, basado en los registros existentes, que describiera las causas de enfermedad renal primaria, la incidencia y prevalencia de la infección por VIH en la población de enfermos en diálisis y trasplante, la supervivencia y los factores que pueden influyen en ella.
Pacientes y métodosSe solicitó información a los registros de enfermos renales de las siguientes CCAA: Andalucía, Aragón, Asturias, Cataluña, Comunidad Valenciana, Castilla-La Mancha, Castilla y León, Galicia, Madrid, La Rioja y País Vasco. Este conjunto abarca un 85% de la población española. Enviaron información sobre pacientes en tratamiento renal sustitutivo, con serología VIH positiva, incidentes desde el 1 de enero de 2004 hasta el 31 de diciembre de 2011, y prevalentes a 31 de diciembre de 2011. Las variables recogidas fueron: fecha de nacimiento, sexo, fecha y modalidad del primer tratamiento sustitutivo y de los tratamientos sucesivos, etiología de enfermedad renal primaria codificada según el sistema de codificación de la European Renal Association-European Dialysis and Transplantation Association (ERA-EDTA) de 1995, estado de serología de hepatitis B y C al inicio del tratamiento, fecha de fallecimiento si lo hubiere y CCAA que registra el caso. Los datos de las diferentes CCAA fueron agrupados en un fichero común.
Como grupo de comparación se utilizó una base de datos del total de pacientes en tratamiento sustitutivo incidentes entre los años 2004 y 2011 de las mismas CCAA (a excepción de Madrid y La Rioja porque sus registros no abarcaban la información completa durante el mismo periodo de tiempo). Aunque en esta base de datos no se disponía de información sobre serología de VIH, dada su baja incidencia y prevalencia, el error en la estimación de los riesgos considerando el grupo total como no expuesto, resulta despreciable. Dicha base de datos estaba compuesta por 30.693 pacientes. Los resultados del análisis de supervivencia realizado se presentaron en la sesión de registros del congreso de la Sociedad Española de Nefrología (SEN) 20139.
Para el cálculo de incidencia se tomó la población de cada CCAA a mitad del intervalo de 8 años, el 1 de enero de 2008, a partir de las estimaciones de población del censo de 2001. Para el cálculo de la prevalencia se usó la población a 31 de diciembre de 2011. Los datos se obtuvieron del Instituto Nacional de Estadística (www.ine.es).
Análisis estadísticoSe utilizaron estadísticos descriptivos como media, mediana, desviación estándar y porcentajes de frecuencias. Para la comparación de frecuencias se empleó el test ordinario de X2, o el test exacto de Fisher cuando el primero no era apropiado. Se compararon las medias entre 2 grupos utilizando la prueba basada en la distribución de t de Student. Para realizar comparaciones ajustadas de la proporción de nefropatía diabética en el grupo HIV+ frente al global, se empleó el método de Mantel-Haenszel, estratificando por edad.
Para el análisis de supervivencia se utilizó solo la base de datos de pacientes incidentes, se usó el método de Kaplan Meier para el análisis no ajustado y la regresión de Cox para el análisis ajustado de supervivencia, empleando como variables de ajuste la edad (como variable continua y lineal) y el sexo. Se utilizó también como variable de ajuste la diabetes como causa de enfermedad renal primaria, dado que en diferentes presentaciones del Registro de Diálisis y Trasplante se ha observado que esta variable tiene gran importancia pronóstica9.
En el cálculo de la probabilidad de trasplante a lo largo del tiempo, se comparó el grupo de incidentes VIH+ frente al total de pacientes en diálisis. Se tomó en cuenta el riesgo competitivo entre fallecimiento y trasplante, ya que un paciente fallecido no tiene opción de trasplante y no puede considerarse como pérdida de seguimiento. Se utilizó el método de Fine y Gray aplicado por Scrucca10, para el programa R project. En este modelo se utilizaron como covariables de ajuste la edad, como variable continua sin trasformar, y el sexo. Para comprobar variables asociadas con cambios de incidencia se usó la regresión de Poisson. Los cálculos estadísticos se realizaron utilizando el software R project, versión 2.13 bajo licencia GNU11.
ResultadosIncidencia, prevalencia y enfermedad renal primariaSe seleccionó a un total de 271 pacientes incidentes y 209 prevalentes. Los datos demográficos de ambos grupos, así como la primera modalidad de tratamiento sustitutivo, se indican en la tabla 1.
Datos demográficos de los pacientes VHI+, incidentes y prevalentes frente al total de población control en tratamiento sustitutivo
| VIH+ | Controles | ||
|---|---|---|---|
| Incidentes | Prevalentes | Incidentes | |
| N | 271 | 209 | 30.693 |
| Edad media (DE) | 46,8 (10,8) | 45,7 (10,7) | 63,9 (12,5) |
| Edad (mín-máx) | 15,5-85,9 | 15,1-85,9 | 15,0-96,7 |
| Mujeres/hombres | 63/208 | 48/161 | 11.069/19.624 |
| 1.er modo de tratamiento | Último modo de tratamiento | 1.er modo de tratamiento | |
| Hemodiálisis | 228 | 147 | 26.250 |
| D. peritoneal | 42 | 32 | 3.775 |
| Trasplante | 1 | 30 | 668 |
Los resultados de incidencia anual en promedio de los 8 años, y de la prevalencia a 31 de diciembre de 2011, agrupados por las CCAA participantes, se presentan en la tabla 2, las tasas se expresan como número de pacientes por millón de habitantes. La prevalencia de sujetos VIH+ fue de 5,1, con un intervalo de confianza del 95% (IC 95%): 4,4-5,8 por cada 1.000 pacientes en tratamiento sustitutivo.
Número de pacientes por comunidad autónoma, con los cálculos de incidencia y prevalencia por millón de habitantes
| Comunidad autónoma | Incidentes | Prevalentes | Incidencia anual PMP | Prevalencia PMP |
|---|---|---|---|---|
| Cataluña | 66 | 44 | 1,14 | 6,012 |
| Andalucía | 58 | 42 | 0,901 | 5,069 |
| Madrid | 42 | 41 | 0,848 | 6,418 |
| C. Valenciana | 41 | 26 | 1,048 | 5,188 |
| País Vasco | 16 | 16 | 0,935 | 7,517 |
| Castilla y León | 15 | 9 | 0,749 | 3,630 |
| Aragón | 14 | 9 | 1,349 | 6,845 |
| Galicia | 11 | 12 | 0,503 | 4,397 |
| Castilla-La Mancha | 4 | 3 | 0,253 | 1,463 |
| Asturias | 3 | 6 | 0,354 | 5,700 |
| La Rioja | 1 | 1 | 0,401 | 3,203 |
| Global | 271 | 209 | 0,882 | 5,349 |
Teniendo en cuenta los datos generales de prevalentes e incidentes de los registros de las CCAA participantes, se calculó que la proporción de pacientes incidentes VIH+ sobre el total fue de 0,74%. En el caso de los prevalentes esta proporción fue de 0,51%.
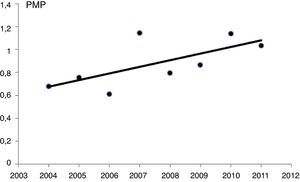
Mediante regresión de Poisson, sin utilizar variables de ajuste, se comprobó un incremento estadísticamente significativo de la incidencia desde el año 2004 hasta el 2011, (p=0,014). Con este método, se estimó un aumento anual de un 6,8% (IC 95%: 1,3-12,5%) (fig. 1).
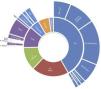
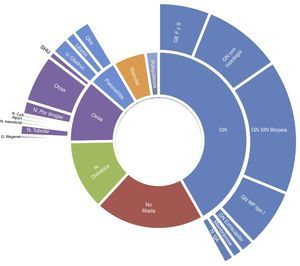
La frecuencia de causas de enfermedad renal primaria en los pacientes incidentes, agrupadas según la clasificación utilizada por el registro de EDTA, fueron las siguientes: glomerulares 42%, no filiadas 20%, nefropatía diabética 13%, otras 12%, pielonefritis crónica 5%, vascular/n. hipertensiva 5%, poliquistosis 2% y nefropatía isquémica 1%. La causas más específicas están expresadas en la figura 2. En el total de pacientes en tratamiento sustitutivo en las mismas CCAA, la nefropatía diabética fue la causa en un 22% de los incidentes y las causas glomerulares afectaron al 12%. En la comparación de porcentaje de incidentes con nefropatía diabética entre los grupos VHI+ y el resto, ajustando por categorías de edad, la razón de tasas mediante Mantel-Haenszel dio un valor de 0,50 (IC 95%: 0,35-0,71).
No hubo cambios significativos en la incidencia de cada grupo diagnóstico de enfermedad renal primaria en los diferentes años de seguimiento, tampoco hubo diferencias en etiologías comparando diferentes periodos, antes y después de 2 puntos de corte: 1 de enero de 2008 y 1 de enero de 2006.
Trasplante renalDe los 271 pacientes incidentes, a lo largo del tiempo de observación, 21 recibieron al menos un trasplante renal, uno de ellos por segunda vez. La probabilidad acumulada de recibir un primer injerto renal a lo largo del tiempo, teniendo en cuenta los riesgos competitivos de muerte y trasplante, fue de 5, 10 y 17% a los 2, 5 y 7 años respectivamente, frente al 19, 26 y 32%, en el total de pacientes en tratamiento sustitutivo. Son comparaciones brutas sin ajustar por variables de confusión.
Se estimó mediante el modelo de regresión de riesgos competitivos de Fine y Gray la razón de riesgos de recibir un trasplante renal de los pacientes VIH+ frente al resto, ajustando por edad y sexo. Dicha estimación dio un valor de 0,15 (IC 95%: 0,10-0,24). Expresado de otro modo: la probabilidad de recibir un trasplante renal a lo largo del tiempo se estimó en 6,6 veces menor para un paciente VIH+ respecto al resto, IC 95%: 4,2 a 10 veces (tabla 3).
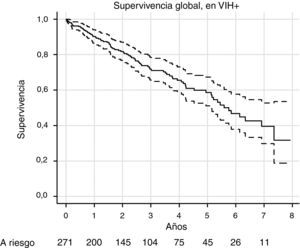
SupervivenciaPara el análisis de supervivencia, se utilizó la cohorte de pacientes incidentes VIH+. En el total de 271 pacientes, hubo 84 fallecimientos. La estimación de la mediana de supervivencia por el método de Kaplan Meier fue de 5,75 años (IC 95%: 5,13-7,35). El gráfico de supervivencia se expone en la figura 3.
Se investigaron variables que pudieran estar asociadas con la supervivencia en el modelo de Cox, que incluía, edad, sexo, nefropatía diabética y periodo de inicio de tratamiento: antes y después de 1 de enero de 2008 (para comprobar si había mejoría de supervivencia a lo largo del tiempo). No se encontró significación estadística alguna.
Se comparó la supervivencia de los pacientes VIH+ frente al total de pacientes incidentes de las mismas CCAA durante los mismos años 2004 a 2011. El análisis de la regresión de Cox, ajustando por edad, sexo y nefropatía diabética, estimó un riesgo de muerte para los pacientes VIH de poco más de 2 veces sobre el resto de pacientes, HR: 2,26 (IC 95% 1,74-2,91) (tabla 4).
Modelo de regresión de Cox para supervivencia global, con las variables indicadas
| HR | IC 95% | p | |
|---|---|---|---|
| Sexo: mujer | 0,85 | 0,81-0,88 | <0,001 |
| Edad, años | 1,06 | 1,57-1,60 | <0,001 |
| N. diabética | 1,46 | 1,39-1,51 | <0,001 |
| VIH+ | 2,26 | 1,74-2,91 | <0,001 |
Se estima el efecto de tener serología VHI+ sobre el resto de pacientes, ajustando por edad, sexo y nefropatía diabética
La coinfección de hepatitis B (HBsAg+) en los pacientes VIH+ fue del 7,8%, mientras que la proporción de pacientes con anticuerpos antihepatitis C fue de 53,1%. Ante una proporción tan baja de hepatitis B no se realizó ningún análisis exploratorio para ese grupo. El grupo de seropositivos para hepatitis C (VHC) era significativamente más joven, edad media: 45,5 vs. 48,4 años (p=0,034). No hubo diferencias significativas en cuanto al sexo, año de incidencia ni incidencia de nefropatía diabética.
Usando la regresión de Cox, se analizó la supervivencia en el grupo de pacientes incidentes VIH+ según serología positiva para VHC, ajustando por edad, sexo y nefropatía diabética. El riesgo de muerte de los pacientes con coinfección VHC frente a monoinfección VIH+ fue casi 2 veces superior, HR: 1,77 (IC 95%: 1,10-2,85) (tabla 5).
Modelo de regresión de Cox para supervivencia global en la cohorte de pacientes VIH+, donde se estima el efecto de la serología positiva para hepatitis C junto con la edad, nefropatía diabética y el sexo
| HR | IC 95% | p | |
|---|---|---|---|
| Sexo: mujer | 1,25 | 0,75-2,10 | 0,390 |
| Edad, años | 1,03 | 1,00-1,05 | 0,017 |
| N. diabética | 1,78 | 0,97-3,25 | 0,062 |
| Hepatitis C+ | 1,77 | 1,10-2,85 | 0,019 |
En España la incidencia de infección por VIH en los pacientes en ERC-5D a lo largo de los años 2004-2011 representa una proporción de casi el 1%, similar a otras series europeas. En la prevalencia, esa proporción es más baja. La menor tasa de prevalencia respecto de la incidencia puede deberse a una menor supervivencia de este grupo de pacientes frente al resto. Encontramos un incremento progresivo en la incidencia, que no puede deberse a un aumento en la incidencia de infección por VIH en la población general, dado que esta ha disminuido desde el año 1998. Podría estar en relación con el aumento en la edad de los nuevos casos de infección VIH y con el aumento de la supervivencia a partir de la utilización de TARGA. Esto conlleva un aumento de la exposición a factores de riesgo de enfermedad renal como toxicidad por antivirales, coinfección por VHC, hipertensión, dislipidemia y diabetes12. Hay muchas evidencias de que los pacientes infectados por VIH, independientemente del sexo y la edad, tienen un mayor riesgo de desarrollar enfermedad cardiovascular arteriosclerótica13. Esta enfermedad se asocia y constituye un factor de riesgo de enfermedad renal crónica.
Los resultados del porcentaje de prevalentes VIH+ en 2011, sobre el resto de pacientes en tratamiento sustitutivo, son muy similares a los publicados por el grupo español GESIDA en una encuesta realizada en 20066, los intervalos de confianza se superponen. Aunque han transcurrido 5 años entre la estimación de ambos índices y hemos detectado un incremento anual de la incidencia, es posible que el incremento progresivo de la prevalencia en el total de pacientes en ERC-5D y su mayor supervivencia compensen el aumento de pacientes incidentes VIH+.
Si tenemos en cuenta una prevalencia de infección por VIH en la población adulta del 1,5/1.000, como se ha publicado en Andalucía durante el año 200814, podemos estimar con nuestros datos y los datos de los registros de diálisis y trasplante la razón de prevalencias de tratamiento renal sustitutivo de los infectados por VIH entre la población general, en este caso este cociente es de 3,5. Este cociente, bajo ciertas condiciones15, se puede interpretar como el riesgo relativo de desarrollar ERC-5D para los infectados por VIH frente a la población general.
Estos resultados también indican que la infección por VIH en ERC-5D implica un riesgo aumentado de muerte. Es importante contextualizar que los datos epidemiológicos de Cataluña durante la época de uso extensivo de TARGA reportan una mortalidad de los infectados por VIH 5 veces superior a la de la población general16. En las últimas 2 décadas el pronóstico de estos pacientes ha mejorado de forma sustancial, pero esta mejoría se ha consolidado cuando se adquirió la experiencia suficiente para el manejo de la farmacocinética del TARGA en diálisis17. Se ha publicado que esta mejoría ha llegado hasta igualar la supervivencia a la del resto de los pacientes, en un estudio realizado en Francia, deduciendo que la infección por VIH no incrementa el riesgo de muerte en los pacientes en diálisis y trasplante18. Sin embargo, el análisis de una cohorte de pacientes VIH+ que comenzaban diálisis en España, durante los años 1999 a 2006, observó que la supervivencia era menor que en el resto de los pacientes incidentes en diálisis19. Nuestros resultados son acordes con la segunda observación, debido, probablemente, al mismo origen demográfico de los pacientes y a factores de riesgo similares.
Sobre este riesgo ya aumentado, la coinfección con VHC se asocia con más mortalidad todavía, hasta casi el doble del riesgo de muerte por cualquier causa. Se ha descrito que la coinfección con VHC se relaciona con la infección por VIH mediante el uso de drogas ilegales por vía intravenosa y una duración más larga de la infección VIH6, factores que podrían influir en una menor supervivencia.
En este sentido, la prevalencia de VHC en nuestra cohorte es el doble de la reportada en Europa2 y similar a la de otros estudios en España. Esta diferencia se puede explicar por una mayor proporción de infección por VIH mediante el uso de drogas intravenosas en nuestro país. En un metaanálisis que incluyó a un total de 145.608 pacientes en diálisis, la serología positiva para VHC se asoció con una mayor mortalidad en ERC-5D20; también en los pacientes VHI+ sin enfermedad renal la coinfección implica un mayor riesgo de muerte21.
Las etiologías de enfermedad renal primaria difieren del resto de pacientes si comparamos con el registro de diálisis y trasplante del año 2010. Hay un notable predominio de causas glomerulares: un tercio en VIH+ frente a un 12% en el registro general. En este grupo destacan la glomeruloesclerosis focal y segmentaria, que probablemente correspondan a la nefropatía asociada a VIH (NAVIH), dado que no existe este código específico en la lista de EDTA; en tal caso representa un porcentaje mucho menor que el reportado en las series americanas como cabe esperar en una población con baja proporción de raza negra.
Siguen predominando otras causas glomerulares, en probable relación con la asociación de coinfección con VHC y glomerulopatías22.
Aunque la nefropatía diabética en este grupo es menos importante, 13 frente a 22% en el registro general, representa una causa significativa de comienzo de diálisis. Se ha demostrado una disminución progresiva en la incidencia de NAVIH en los años 1995 a 2004 durante la implementación de TARGA23 y, por otra parte, en una revisión de necropsias de pacientes VIH+ bajo TARGA, el diagnóstico de nefroangioesclerosis fue uno de los más comunes24. Parece que en los últimos 10 años en nuestro país, cuando el uso de TARGA se ha generalizado, ha cambiado el espectro de enfermedad renal primaria en los pacientes VIH+, con una tendencia hacia diagnósticos más parecidos a la población sin VIH en ERC-5D. La ausencia de cambios en los diagnósticos con el tiempo en nuestros datos puede deberse a que en el periodo de estudio el uso de TARGA ya está implantado y no ha habido cambios drásticos en el tratamiento de la infección por VIH. Por ello, a pesar de que el TARGA ha logrado controlar la evolución de la enfermedad sin lograr disminuir la incidencia de ERC-5D, se hacen necesarias estrategias complementarias para la prevención de otras causas diferentes de la glomerulonefritis y NAVIH, como la nefropatía diabética, las causas vasculares y nefrotóxicas.
Como ya suponíamos, hemos observado una baja tasa de trasplante renal en los pacientes VIH+: incluso ajustando por el riesgo competitivo que existe entre la muerte y el trasplante renal, la probabilidad de recibir un injerto renal es mucho más baja en este grupo que en el resto de los pacientes en diálisis. Es llamativo que, aunque la infección por VIH no supone una contraindicación para el trasplante renal, sea casi 7 veces menos probable recibir un trasplante renal si se padece una infección por VIH.
Dado el escaso número de trasplantes realizados, solo 21, no se realizó ningún análisis de supervivencia en este grupo particular por la escasa potencia estadística para detectar diferencias.
Nuestro estudio adolece de falta de información detallada que incluya variables como tipo e historia de tratamiento antiviral, tiempo de infección por VIH, forma de contagio, causas de muerte, entre otras muchas, y esto no permite realizar un análisis más detallado. Sin embargo, al estar basado en registros de pacientes, podemos conseguir una alta calidad de la información asegurada por procedimientos establecidos de validación de los datos en cada uno de los registros participantes. Además, disponemos de la totalidad de los casos existentes en esas comunidades que, por sus características demográficas y porcentaje de población abarcada, se pueden asimilar a la población española.
Creemos que este trabajo puede servir para profundizar en el conocimiento de las características de los pacientes VIH+ en ERC-5D de nuestro país y así continuar mejorando en la atención a este grave problema de salud.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.