INTRODUCCIÓN
La posibilidad de un embarazo a término, es uno de los beneficios obtenidos en mujeres después del trasplante de un órgano sólido. La disfunción gonadal, que produce la insuficiencia renal o de otro órgano, es revertida en pocos meses tras el normal funcionamiento del injerto1-3. La información existente sobre embarazo y trasplante de órganos sólidos ha sido obtenida de registros voluntarios, casos clínicos y estudios hospitalarios retrospectivos, siendo los primeros los que han permitido un mejor conocimiento sobre este tema1-3. La experiencia acumulada en el trasplante renal1-6, contrasta con el limitado número de casos publicados o reportados a los registros en el trasplante simultáneo de riñón y páncreas (TSRP)1-3, 6, 7. Existen riesgos comunes en ambos tipos de trasplante tanto para el feto (aborto, parto prematuro o malformaciones), la madre (hipertensión arterial, preeclampsia y aumento de infecciones) y el injerto renal (rechazo agudo y deterioro de función renal)1-3, siendo menos claro, en el TSRP, el efecto del embarazo sobre la función del injerto pancreático y los problemas ante la existencia de dos órganos a nivel pélvico. En el presente artículo, reportamos un embarazo a término en una receptora de TSRP, que ha mantenido una adecuada función de ambos injertos post-parto, actualizando los aspectos de interés sobre este tema.
CASO CLÍNICO
Primigesta de 35 años afecta de diabetes mellitus tipo 1 e insuficiencia renal, portadora de TSRP desde 2003. El injerto pancreático fue implantado intra-peritoneal en fosa iliaca derecha con derivación entérica y el injerto renal en fosa ilíaca izquierda extra-peritoneal. Recibió inmunosupresión con Tymoglobulina, tacrolimus, micofenolato mofetil (MMF) y esteroides, suspendiéndose estos a los 6 meses. A los 26 meses del trasplante la paciente plantea la posibilidad de quedar embarazada, estando en ese momento en tratamiento con tacrolimus, MMF y estatinas, con tensiones arteriales normales sin medicación, sin proteinuria patológica y con función normal de ambos injertos. Tras informar de los riesgos del embarazo, se suspende el tratamiento con estatinas y MMF añadiéndose azatioprina. Tras quedar embarazada, la gestación es controlada en la consulta de embarazo de alto riesgo de Obstetricia y en Nefrología, cursando sin complicaciones salvo un episodio de bacteriuria asintomática. La paciente ingresa en la semana 38, iniciándose el parto de forma fisiológica. A las dos horas se produce bradicardia fetal mantenida que no se recupera, por lo que el equipo medico de guardia indica cesárea urgente por sospecha de perdida del bienestar fetal, extrayéndose un recién nacido varón de 2.980 g, que es valorado por el equipo de Neonatología de guardia, no reportando anomalías de interés. El postoperatorio transcurre de manera favorable para la madre y el niño. Se realiza inhibición de la lactancia por tratamiento inmunosupresor materno y dada la excelente evolución se decide su alta a los 4 días. En la tabla I se muestran diversos parámetros de interés pre-embarazo, en los tres trimestres del mismo y a los 5 meses post-parto.
DISCUSIÓN
De los cientos de casos de embarazo y trasplante de órganos publicados o reportados a los diferentes registros, más del 75% son trasplantes renales, seguido del trasplante hepático o cardiaco siendo en el TSRP menos del 5%1-3. Ello explica que las guías clínicas publicadas, tanto americanas como europeas8-10, hacen referencia principalmente al trasplante renal. Aunque el embarazo ha de considerarse de alto riesgo, este se considera bajo si se cumplen los criterios de la tabla II1, 9, 10.
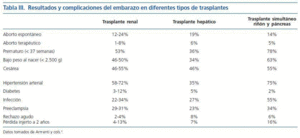
Un mayor riesgo de aborto, parto prematuro (< 37 semanas) y bajo peso al nacer (< 2.500 g) se ha descrito en los diferentes tipos de trasplante, con una mayor frecuencia de prematuridad y bajo peso en el TSRP y trasplante renal que en el trasplante hepático1, 2. Por otro lado, las receptoras de TSRP presentan con mayor frecuencia hipertensión arterial, preeclampsia e infecciones con una incidencia similar de rechazo agudo2 (tabla III). En nuestro caso la paciente evolucionó sin ninguna complicación salvo la bacteriuria asintomática ya comentada. El embarazo fue a término y con peso normal al nacer lo cual ha de achacarse a la función renal normal y ausencia de hipertensión y proteinuria patológica antes y durante el embarazo. En este sentido, un estudio reciente muestra que la función renal alterada (creatinina plasmática > 1,69 mg/dl) y el uso de hipotensores pre-embarazo son factores de riesgo independiente de prematuridad, siendo esta debida a cesárea electiva, indicada por hipertensión, preeclampsia o deterioro de la función renal, en la mayoría de los casos3.
El equilibrio entre riesgo de rechazo agudo y efecto teratogénico de los fármacos sobre el feto es otro aspecto importante a considerar. Se ha sugerido que el embarazo produce un estado de inmunosupresión pero la evidencia actual indica que el útero es un «lugar inmunoprivilegiado», mientras la madre mantiene un sistema inmunológico competente1, 9, 10. Por lo tanto una inmunosupresión inadecuada puede conducir a un rechazo agudo del injerto1. Aunque en la actualidad existe un amplio número de fármacos inmunosupresores, el régimen adecuado en cuanto a asociaciones y dosis está por definir1, 2, 11. La FDA clasifica los fármacos en cinco categorías según el riesgo teratogénico (en estudios en animales y/o en humanos) que puede resumirse de la siguiente forma: A = posibilidad remota; B = no riesgo evidente en humanos; C = no puede descartarse riesgo en humanos (valorar riesgo/beneficio); D = riesgo evidente en humanos (su beneficio puede hacerlo aceptable); y X = totalmente contraindicado1. La mayoría de los inmunosupresores (ciclosporina, tacrolimus, sirolimus y MMF) han sido clasificados clásicamente en el grupo C, mientras que la azatioprina corresponde al grupo D1, 2. Sin embargo, recientemente (octubre de 2007), la FDA ha modificado la clasificación del MMF de categoría C a D12. En nuestro caso la paciente estaba libre de esteroides y se decidió mantener tacrolimus en rango terapéutico, cambiando el MMF por azatioprina. Esta modificación se hizo, en aquel momento, siguiendo las guías europeas que contraindican el MMF y recomiendan la azatioprina10, quizá debido a una experiencia más amplia con azatioprina. Por otra parte, un estudio reciente observa una mayor incidencia de anomalías estructurales en el niño en trasplantadas en tratamiento con MMF frente a otras terapias12. Este hecho, junto al cambio de categoría por la FDA hace mantener ciertas reservas, con respecto al uso de MMF, en pacientes trasplantadas que desean quedarse embaarazadas, como se ha sugerido por otros autores1,9.
En conclusión, aunque la experiencia en embarazo y trasplante simultáneo de riñón y páncreas es limitada, creemos que si se cumplen los requisitos conocidos en el trasplante renal y se mantiene una inmunosupresión similar a los meses previos evitando, si es posible, aquellos fármacos con los que existe una menor experiencia, los riesgos para la receptora, los órganos y el niño aunque existentes pueden ser asumibles.
Tabla 1.
Tabla 2.
Tabla 3.