Los pacientes con enfermedad renal crónica en programa de hemodiálisis se encuentran expuestos a grandes cantidades de agua, ya que esta constituye cerca del 96% del líquido de diálisis. Es conocido que el uso de agua de mejor calidad disminuye el estado de inflamación crónica en los pacientes en diálisis. La desinfección como parte del tratamiento del agua tiene un papel importante para cumplir los estándares de calidad establecidos. En la actualidad, la desinfección por calor es muy recomendable, sin embargo, la dosis no está claramente establecida en la bibliografía. El objetivo de esta revisión es conocer los datos disponibles sobre la dosis de desinfección por calor que se debe utilizar en hemodiálisis, así como presentar nuestra experiencia con este método a una dosis establecida de 12.000 A0.
Patients with chronic kidney disease in the hemodialysis program are exposed to large amounts of water, as this constitutes about 96% of the dialysis fluid. It is known that the use of better quality water decreases the state of chronic inflammation in dialysis patients. Disinfection as part of water treatment plays an important role in meeting the established quality standards; currently, heat disinfection is highly recommended, however its dose is not clearly established in the literature. The objective of this review is to know what is available in the literature on the dose of heat disinfection that should be used in hemodialysis and to present our experience with this method at a set dose of 12.000 A0.
Los pacientes con enfermedad renal crónica en programa de hemodiálisis (HD) se encuentran expuestos a grandes cantidades de agua (entre 90 y 190 litros por sesión)1 ya que constituye el principal componente del líquido de diálisis. La membrana semipermeable del dializador es la única barrera que separa el líquido de diálisis de la sangre del paciente, por lo que la presencia de contaminantes químicos y biológicos en el agua y su contacto con la sangre tiene un impacto negativo, claramente documentado en la bibliografía, sobre la salud del paciente. Con base en la evidencia disponible, las principales guías de práctica clínica2,3 establecen los estándares de calidad que debemos exigir al agua que utilizamos en las sesiones de hemodiálisis y prevenir, así, las complicaciones asociadas al líquido de diálisis.
El tratamiento del agua para el uso en la sesión de HD consta de 3fases. Una primera, cuyo principal objetivo es eliminar la mayoría de las partículas en suspensión, así como sustancias orgánicas y reducir el número de cationes (decalcificador, filtro de carbón, filtro de arena) y que se conoce como fase de pretratamiento. La segunda fase tiene como objetivo eliminar restos de compuestos químicos y contaminantes bacterianos (osmosis inversa); esta es la fase de tratamiento. Y la tercera fase, conocida como postratamiento, tiene como objetivo asegurar la distribución de agua a los monitores, teniendo en cuenta que los diseños del circuito con curvaturas externas o fondos de saco favorecen al estancamiento de agua y, por ende, la contaminación.
La guía de gestión de la calidad del líquido de diálisis de la Sociedad Española de Nefrología (SEN)4 establece 2estándares de calidad del agua para contaminantes biológicos y define como agua purificada la presencia de ≤100unidades formadoras de colonias (UFC) por cada mililitro y de ≤0,25 unidades de endotoxinas (UE) por mililitro y como agua ultrapura la presencia de ≤10UFC/ml y de ≤0,03 UE/ml.
Cuando la carga de contaminación microbiana es elevada, puede condicionar la aparición de complicaciones graves que requieren una actuación urgente en el paciente. Si la carga de contaminación es baja, las consecuencias son más larvadas, pero no menos peligrosas. Hoy en día disponemos de evidencia suficiente para afirmar que la exposición crónica a una baja carga de contaminación biológica provoca un estado de inflamación crónica de baja intensidad, que se relaciona con el desarrollo de ateromatosis, estrés oxidativo, malnutrición, anemia, resistencia a la eritropoyetina y mortalidad por cualquier causa1,5,6. Por este motivo, las nuevas guías de gestión de calidad del agua del líquido de diálisis del 2016 introducen en sus recomendaciones el uso habitual de líquido ultrapuro en todo tipo de HD para prevenir y retrasar la aparición de estas complicaciones4.
Para asegurar la inactivación/eliminación de la microflora en el agua, existen modernas plantas de tratamiento que producen eficazmente agua que cumple los requisitos de calidad exigidos; pero, además, es necesario disponer de sistemas de desinfección adecuados que garanticen el mantenimiento de los estándares de calidad del agua a lo largo de todo el circuito de distribución. La eficacia de los sistemas de desinfección estará determinada por 2aspectos fundamentales:
Frecuencia de la desinfección. La frecuencia de las desinfecciones del circuito de distribución debe seguir una estrategia preventiva de contaminación, e incorporar, además, una evaluación periódica de resultados y una modificación de la estrategia en función de los resultados obtenidos (sistema de validación/revalidación).
Distribución. La desinfección debe llegar a todos los elementos del sistema: membrana de osmosis inversa, anillo de distribución, entrada a los monitores y al propio monitor de diálisis. Para garantizarla es fundamental un diseño adecuado del circuito de distribución que evite zonas muertas y fondos de saco en el anillo.
Los sistemas germicidas disponibles para llevar a cabo la desinfección tienen una serie de desventajas. Es conocido que la infusión de cloro al inicio del pretratamiento puede alterar las características de determinadas membranas de osmosis; los filtros submicrónicos impiden el paso de bacterias de tamaño superior a 0,1 μ; las lámparas de radiación ultravioleta necesitan un buen diseño para ser efectivas, su efecto depende de la potencia de la lámpara, de la pureza del agua, del tiempo y flujo de exposición, y su principal peligro es la liberación masiva de endotoxinas en aguas muy contaminadas; el ozono precisa para su eliminación de una lámpara ultravioleta multifrecuencia de gran potencia para su trasformación en peróxido molecular; por último, la desinfección periódica de la planta mediante sustancias desinfectantes y desincrustantes requiere de aclaramiento de las sustancias utilizadas y comprobación posterior de su nivel residual (establecido para cada sustancia). En cuanto a la desinfección por calor, actualmente se está utilizando sin conocer si la dosis aplicada es la necesaria para garantizar la correcta desinfección.
Concepto de desinfecciónEtimológicamente desinfección es un concepto químico que hace referencia a la eliminación o inactivación de agentes patógenos que se encuentran en un objeto inerte. El término desinfección es complejo, ya que no existe una clara definición, y más bien hace referencia al cumplimiento de una serie de estándares de calidad, los cuales van a estar determinados por un contexto y circustancias particulares8 (por ejemplo, el concepto de desinfección de una cuña del hospital es totalmente diferente al concepto que aplicamos a la desinfección del material quirúrgico o del circuito de HD).
Recientemente se ha introducido el concepto de dosis de calor, entendida como la energía necesaria para conseguir eliminar/inactivar determinados microorganismos en un determinado contexto. Es decir, una determinada dosis de calor va a conseguir una determinada desinfección9. El objetivo de esta revisión es conocer los datos disponibles en la bibliografía sobre la dosis de desinfección por calor que se debe utilizar en HD, así como presentar nuestra experiencia con este método utilizando una dosis establecida.
Dosis de calorEs un concepto teórico que expresa la relación existente entre la temperatura aplicada y el tiempo de exposición para conseguir una inactivación definida de microorganismos. Esta relación expresa la energía que aplicamos, que es mayor cuanta más temperatura o más tiempo expongamos el material que queremos desinfectar.
Los parámetros que rigen la dosis de desinfección térmica están definidos y controlados por el valor A0 mediante la norma EN ISO 15883-110, en el que una unidad de A0 significa un segundo a 80°C, que origina cierta desinfección, conocido como el valor de z. Este valor es una medida en °C de la relación de temperatura y proceso de destrucción, mediante el cual se puede saber el aumento de temperatura necesario para reducir el valor D de un microorganismo (el valor D es el tiempo requerido a una temperatura establecida para eliminar/inactivar el 90% de la población de microorganismos). El valor z también es empleado en el concepto A0. Un valor A0 se puede lograr con las diversas combinaciones entre temperaturatiempo (tabla 1)7.
Tiempos de exposición a diferentes temperaturas para lograr valores A0 de 600, 3.000 o 12.000
| Valores A0 | 70°C | 75°C | 80°C | 85°C | 90°C |
|---|---|---|---|---|---|
| 600 | 100 min | 31,5 min | 10 min | 3,16 min | 1min |
| 3.000 | 500 min | 158 min | 50 min | 15,8 min | 5 min |
| 12.000 | 2.000 min | 632 min | 200 min | 63,2 min | 20 min |
Fuente: adaptado de Nystrand et al.7.
La desinfección es el resultado de la dosis de calor aplicada; es decir, aplicamos una determinada dosis de calor y conseguimos eliminar/inactivar un número determinado de microorganismos. Por ejemplo, al aplicar una dosis de 3.000 A0 conseguimos desactivar el 99,999% de un determinado microorganismo. Para evitar los decimales, comúnmente se expresa en forma de logaritmos (log); de esta manera podríamos decir, de forma simplificada, que el logaritmo representa el número de 9 en el porcentaje de microorganismos desactivados. Volviendo al ejemplo, al aplicar 3.000 A0 conseguimos una desinfección de 5 log (99,999%). A mayor valor de log, mayor porcentaje de microorganismos estamos eliminando/inactivando y, de esta manera, podemos cuantificar la desinfección que estamos consiguiendo.
La ISO 158883-1 establece un A0 de 60 como la dosis de calor necesaria para la desinfección de dispositivos médicos que entren en contacto con la piel intacta10, mientras que la ISO 23500 estipula un A0 de 600 como requisito mínimo para la desinfección térmica de instrumentos quirúrgicos11. En HD, la dosis no está establecida aún, pero los requisitos deben ser mucho más exigentes, ya que se trata de grandes instalaciones y existe además la posibilidad de formación de biofilm.
Si quisiéramos aplicar una dosis de 12.000 A0, podríamos conseguirla con diferentes combinaciones de temperatura del agua y tiempo de exposición (tabla 1)7. En la tabla se muestra como temperatura y tiempo son equivalentes, y como mediante las distintas combinaciones se consiguen las dosis de 600, 3.000 o 12.000 A0, respectivamente, y como todas producen la misma desinfección.
El concepto de Ao permite calcular todas las combinaciones posibles de tiempo y temperatura para lograr un determinado grado de desinfección de una forma más eficiente y económica, adaptada a las necesidades de cada Unidad de HD. La programación automática de la desinfección térmica basada en este concepto nos ofrece la posibilidad de aumentar la frecuencia de los procedimientos, favoreciendo así en mayor medida la erradicación de la actividad microbiológica en el líquido de diálisis.
Desinfección del circuito de hemodiálisisComo venimos expresando, una determinada dosis de calor (A0) aplicada en un determinado contexto va a condicionar un determinado porcentaje de desinfección. La dosis necesaria está condicionada, a su vez, por el tipo de microorganismo que se desea eliminar/inactivar, así como por el contexto en el que se aplica. No todos los microorganismos son iguales de erradicar/inactivar (tabla 2)7,12.
Ejemplo de 3 tipos de microorganismos que se eliminan en función de si se encuentran en fase fluida o en superficie (biofilm)
| A0 = 600 en log | A0 = 3.000 en log | ||
|---|---|---|---|
| Microorganismos fáciles (Pseudomonas sp) | Fluido | 3 | 5 |
| Superficie | 0,5 | 3 | |
| Microorganismos medios (Flavobacterium sp) | Fluido | 1,5 | 5 |
| Superficie | Casi imposible | 1,5 | |
| Microorganismos difíciles (Exophilia sp) | Fluido | Casi imposible | 2,5 |
| Superficie | Casi imposible | 0,5 |
Fuente: adaptado de Nystrand et al.7.
Un aspecto importante que tener en cuenta en la planta de agua de HD es la particularidad de que el microorganismo puede ser hasta 5veces más resistente si se localiza adherido a una superficie que si se encuentra en fase fluida (tabla 2), lo que dificulta su eliminación13. Es importante tener en cuenta este aspecto y pensar que detectar, en los análisis periódicos que realizamos en nuestro medio, pequeñas concentraciones de microorganismos/endotoxinas, incluso consideradas aceptables según los estándares de calidad, no significa inexistencia de contaminación, ya que corresponden a la fase fluida y, por tanto, este mismo microorganismo puede encontrarse formando parte de un biofilm, lo que requiere mayores dosis de calor para su erradicación. De ahí la recomendación de mantener una actitud proactiva de prevención del crecimiento de gérmenes para evitar su adherencia a las superficies y la formación de biofilm13.
Experiencia en nuestro centroRealizamos un estudio observacional retrospectivo en las unidades de HD del Hospital Universitario Virgen del Rocío, tanto en la unidad de pacientes infectados por el virus de la hepatitis B (VHB) como en la unidad de HD infantil, y comparamos la desinfección térmica aplicada en 2períodos diferentes, con distintas programaciones de desinfección por calor. La unidad de HD de pacientes infectados por el VHB dispone de 12 puestos de diálisis, con una distancia hasta la planta de aguas de 60 m, mientras que la unidad de HD infantil dispone de 5 puestos, con una distancia hasta la planta de agua de 80 m y 2 m de altura.
En el primer período, comprendido entre enero del 2013 y mayo del 2014, se realizaba desinfección diaria del anillo a 65°C durante 120 min y una desinfección semanal a 90°C (incluyendo membranas a 85°C) durante 120 min. En el segundo período, comprendido entre junio del 2014 y marzo del 2016, utilizamos el concepto A0: con 12.000 A0 a diario y aplicando 90°C durante 120 min en anillo y membranas. Si bien las características de la instalación obligaron a extender esta temperatura más tiempo del teórico para garantizar que en todos los puntos se alcanzara una temperatura de 85°C durante 60min. Además, durante el segundo período se sustituyó un filtro de seguridad y los de 10, 5 y 1μ y en la unidad de pacientes infectados por VHB se sustituyeron 3 filtros de 10, 5 y 1μ.
Se realizó control de calidad de agua (microbiológico y de endotoxinas) de forma mensual según protocolo, y se obtuvieron las muestras de la salida del anillo, del retorno del anillo, 2tomas intermedias y de los monitores. El analisis microbiológico se realizó mediante cultivo reasoner's 2A agar (R2A) durante 14 días de incubación a 30-35°C y de endotoxinas (activación de lisado de amebocidos Limulus, LAL) con estándares de referencia para agua ultrapura4.
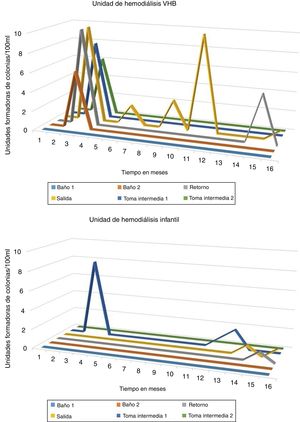
ResultadosEn la desinfección térmica realizada entre enero del 2013 y mayo del 2014 (desinfección diaria del anillo a 65°C durante 120 min y una desinfección semanal a 90°C), se observó el crecimiento de UFC en las distintas muestras tanto en la unidad de HD de pacientes infectados por el VHB como en la unidad de HD infantil; en ninguno de los casos superaba el estándar para agua ultrapura (ver figuras 1.1 y 1.2).
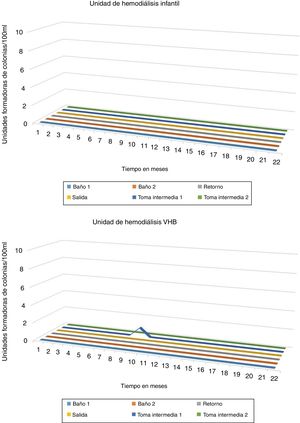
Mientras que, en la desinfección térmica realizada entre junio del 2014 y marzo del 2016, utilizando el concepto A0, (con 12.000 A0 a diario mediante la aplicación a 90°C durante 120 min en anillo y membranas) observamos solo 1UFC en la muestra de la toma intermedia 1 de la unidad de HD de pacientes infectados por el VHB: se trataba de una muestra aislada, por lo que probablemente se tratara de una contaminación, sin observarse ninguna UFC en las muestras correspondientes a la unidad de HD (ver figura 2.1 y 2.2).
Resultados del período comprendido entre junio del 2014 y marzo del 2016, con el concepto A0, que alcanzan 12.000 A0 a diario, aplicando 90°C durante 120 min en anillo y membranas. Se observa solo 1UFC en la muestra de la toma intermedia 1.
UFC: unidad formadora de colonias; VHB: virus de la hepatitis B.
Estos resultados muestran la efectividad de la desinfección diaria por calor; los equipos modernos se programan para arrancar el proceso de desinfección de forma automática, sin la intervención de personal, lo que permite una desinfección integral que incluye tanto el circuito como las membranas de la osmosis y los monitores. De esta manera, se puede aumentar fácilmente la frecuencia de la intervención y se evita el desarrollo de biofilm en el circuito, lo que permite mejorar la calidad del agua con la que dializamos a nuestros pacientes, como se puede comprobar en nuestros resultados.
Utilizar el concepto de A0 ofrece la ventaja de medir y programar el nivel de dosis aplicada, ajustarse a las características de las instalaciones y conseguir así una desinfección más eficiente y económica mediante combinaciones entre tiempo y temperatura, que encarecen el consumo energético. La aplicación de la dosis de calor de 12.000 A0 resulta en la eliminación de la actividad microbiológica en 2unidades de HD diferentes.
Conceptos claveLa guía de gestión de la calidad del líquido de diálisis de la Sociedad Española de Nefrología recomienda usar agua ultrapura en todas las unidades de HD.
La exposición crónica a una baja carga de contaminantes biológicos provoca un estado de inflamación crónica que se relaciona con el desarrollo de ateromatosis, estrés oxidativo, malnutrición, anemia y resistencia a la eritropoyetina.
La eficacia de los sistemas de desinfección estará determinada por la frecuencia de la desinfección y por la distribución. Es fundamental un diseño adecuado del circuito de distribución que evite zonas muertas y fondos de saco en el anillo.
Los parámetros que rigen la dosis de desinfección térmica están definidos y controlados por el valor A0, en el que una unidad de A0 significa un segundo a 80°C, que origina cierta desinfección. Un valor A0 se puede lograr con las diversas combinaciones entre temperatura y tiempo.
Utilizar el concepto de A0 ofrece la ventaja de medir y programar el nivel de dosis aplicada, consiguiendo una desinfección más eficiente y económica mediante conbinaciones entre tiempo y temperatura.
La dosis de calor de 12.000 A0 se muestra eficaz para asegurar la desinfección de una planta de tratamiento de aguas y del sistema de distribución de una unidad de HD estándar.
FinanciaciónExpresamos nuestro agradecimiento a Baxter por el apoyo a la publicación de este artículo.
Conflicto de interesesLos autores declaran que no tienen conflicto de intereses potenciales.