La presencia de malnutrición es bien conocida en la enfermedad renal crónica (ERC). El descubrimiento en los últimos 15 años de los mecanismos fisiopatológicos que desencadenan este proceso, tales como la anorexia, el aumento del catabolismo proteico y la inflamación, ha generado la necesidad de una nueva denominación por la Sociedad Renal Internacional de Nutrición y Metabolismo (ISRNM): protein energy wasting syndrome (PEW). Los objetivos de este documento son proponer la utilización del término «desgaste proteico energético» (DPE) como una traducción más fiel del término anglosajón y actualizar los mecanismos patogénicos implicados que son inherentes al DPE. Simultáneamente revisamos las últimas evidencias epidemiológicas que ponen de manifiesto la relevancia de la malnutrición y su impacto tanto en la mortalidad como en la morbilidad en la ERC. Por último, destacamos la necesidad de redefinir los criterios diagnósticos del DPE para que sean aplicables a la población española con ERC. Los criterios establecidos por la ISRNM creemos que no son extrapolables a diferentes poblaciones, como ocurre por ejemplo con las diferencias antropométricas interraciales.
The presence of malnutrition in chronic kidney disease (CKD) is well-known. The discovery in the last 15 years of pathophysiological mechanisms that lead to this process, such as anorexia, the increase of protein catabolism and inflammation, has created the need for a new name by the International Society of Renal Nutrition and Metabolism (ISRNM): protein-energy wasting syndrome (PEW). This document’s objectives are to propose the use of the term “desgaste proteico energético” (DPE) as a more accurate translation of the English term and to update the pathogenic mechanisms involved that are inherent to DPE (PEW). We simultaneously review the latest epidemiological evidence that highlight the relevance of malnutrition and its impact both on mortality and morbidity in CKD. Finally, we point out the need to redefine DPE (PEW) diagnostic criteria so that they are applicable to the Spanish population with CKD. We do not think that the criteria established by the ISRNM can be extrapolated to different populations, as is the case, for example, with interracial anthropometric differences.
INTRODUCCIÓN
La insuficiencia renal crónica se caracteriza por alteraciones nutricionales e inflamación sistémica que se acompaña de un aumento del catabolismo, lo que incrementa la morbimortalidad. Las alteraciones del estado nutricional se han descrito en la literatura con numerosos y confusos términos como malnutrición, sarcopenia, caquexia o síndrome de malnutrición-inflamación-aterosclerosis. Tales denominaciones describen una parte del problema, pero no engloban los múltiples mecanismos que influyen en la salud y el pronóstico del paciente. En 2008, la Sociedad Internacional de Nutrición Renal y Metabolismo (ISRNM) propuso la adopción del término protein-energy wasting (PEW) como nomenclatura unificadora y punto de partida hacia un mejor conocimiento y tratamiento de estos problemas en el paciente urémico. El término PEW no presenta una traducción fácil al castellano y desde el Grupo de Trabajo en Nutrición de la Sociedad Española de Nefrología (S.E.N.) proponemos la utilización del término «desgaste proteico energético» (DPE) como traducción más fiel del término anglosajón.
El síndrome de DPE es muy frecuente en el paciente renal, ocasiona un deterioro de su calidad de vida y acorta la supervivencia a corto plazo. Sin embargo, lamentablemente, muchos centros aún no incorporan medidas de valoración y monitorización del estado nutricional. Asimismo, la nutrición adecuada es una estrategia a veces olvidada en el manejo de los pacientes renales.
Podemos definir el síndrome de DPE como una entidad patológica única en donde confluyen alteraciones puramente nutricionales con condiciones catabólicas. Ambas están fisiopatológicamente relacionadas, potenciadas entre sí, y crean un círculo vicioso que dificulta en la práctica clínica diferenciar ambos componentes. El enfoque diagnóstico y terapéutico de los pacientes con DPE debe ser multifactorial, intentando tratar todos y cada uno de los factores que podamos identificar, ya que la repleción nutricional es insuficiente como único tratamiento, ya que no frena la proteólisis subyacente. Con la intención de ofrecer una visión actualizada del conjunto de alteraciones catabólicas englobadas en el síndrome de DPE, describimos los principales conceptos, mecanismos e implicaciones de este estado.
CONCEPTO Y TERMINOLOGÍA
El DPE1 se define como un estado patológico donde hay un descenso o desgaste continuado tanto de los depósitos proteicos como de las reservas energéticas, incluyendo pérdida de grasa y músculo. Antes de introducir en nuestra terminología este nuevo concepto, debemos detenernos brevemente en el concepto de malnutrición-desnutrición y su diferencia con otros términos como el síndrome de wasting o desgaste, para así poder entender el carácter unificador del término DPE.
El término «malnutrición» engloba los estados patológicos provocados tanto por exceso como por defecto de nutrientes. Sin embargo, generalmente se utiliza en la uremia para referirse a la desnutrición, es decir, a los trastornos derivados del déficit de macro y micronutrientes2.
Por «desnutrición» entendemos un trastorno de la composición corporal caracterizado por un exceso de agua extracelular, asociado con frecuencia a disminución del tejido muscular y grasa, hipoproteinemia y déficit de potasio, que interfiere con la respuesta normal del huésped a su enfermedad y tratamiento. La «desnutrición calórica-proteica» se produce cuando las necesidades diarias no son cubiertas por la dieta. Revierte en muchos casos con la recuperación de la ingesta y la resolución del problema de base. La desnutrición calórica-proteica puede dividirse en tres grandes síndromes clínicos:
La característica fundamental de la desnutrición es un descenso de peso. La supervivencia durante el ayuno se relaciona con el volumen de almacenamiento graso existente. Los cambios en la composición corporal se reflejan como un aumento relativo del agua extravascular, descenso de los depósitos grasos y descenso de la masa magra corporal. Es importante resaltar que el peso puede aumentar durante una enfermedad aguda grave, por paso de líquidos al tercer espacio. Las alteraciones presentes en la uremia reflejan en cierta manera una desnutrición mixta, aunque cursa con una intensidad moderada y no es el resultado de un proceso agudo intercurrente, sino de una inflamación crónica de baja intensidad.
El término de «caquexia» representa un complejo síndrome metabólico asociado a una enfermedad crónica y está caracterizado por pérdida gradual del tejido muscular, acompañado o no por pérdidas concomitantes de reservas grasas. La caquexia representa, sin embargo, un grado extremo de consunción que raramente se observa en la enfermedad renal crónica (ERC) avanzada.
El término «wasting» o «desgaste» fue propuesto por la Organización Mundial de la Salud en 19883 y se define como una pérdida involuntaria de peso superior al 10 % del basal en ausencia de infección oportunista, enfermedad tumoral o diarrea crónica. Es un síndrome multifactorial y en ocasiones es difícil conocer la causa principal. Se caracteriza por pérdida desproporcionada de masa magra debido a alteraciones específicas en el metabolismo, como parte de un mecanismo de defensa del organismo en respuesta a una situación de estrés. Esta situación mantenida conduce a una depleción de proteínas, sobre todo del músculo esquelético, y no se recupera con la ingesta, ya que todo el proceso es debido a cambios metabólicos celulares.
Es de gran importancia adoptar una terminología común en castellano, y el concepto de DPE consensuado por el Grupo de Nutrición de la S.E.N. pensamos que representa fielmente el espíritu de la nomenclatura PEW de la ISRNM. Este término describe los mecanismos implicados y de esa manera permite identificar dianas terapéuticas, utilizar los métodos apropiados de monitorización y elegir el abordaje terapéutico más eficaz. Reconocemos que el término «desgaste» conlleva menor gravedad clínica que el proceso de «emanciamiento» que puede ocurrir en los pacientes con enfermedad renal. Sin embargo, en la elección de términos y acrónimos debemos sopesar la ventaja de llegar, con un lenguaje más sencillo, a impactar en los profesionales sanitarios acerca de la necesidad de identificar y tratar estos desórdenes catabólicos. La terminología de DPE evita la inclusión de términos como malnutrición o catabolismo, con el fin de no dar más importancia a uno de los componentes. Y es que en estas alteraciones tanto la desnutrición como el catabolismo muscular confluyen y están fisiopatológicamente relacionados, por lo que es imposible diferenciar uno del otro en la práctica clínica. Así, DPE implica tanto la pérdida acelerada de proteína (músculo) como de energía (grasa).
MECANISMOS IMPLICADOS EN EL DESGASTE PROTEICO ENERGÉTICO
Las alteraciones implicadas en la malnutrición de la insuficiencia renal han sido recientemente revisadas por la ISRNM4. La anorexia5 y el aumento del catabolismo proteico6 dan lugar a un desequilibrio energético, con un resultado final de un aumento del gasto energético7 y del consumo de las fuentes de almacenamiento energético.
Otros mecanismos fisiopatológicos implicados en el DPE de la ERC son la acidosis metabólica8, las alteraciones endocrinas9,10, la inflamación11,12 y la activación del sistema ubiquitina-proteasoma (UPS)13,14. Simultáneamente, otros aspectos como la dieta restrictiva, la pérdida de aminoácidos y micro-macronutrientes15 por las técnicas de diálisis, la pérdida de sangre, la sobrecarga de volumen16 y otros factores psicosociales alteran el balance energético.
Pérdida de masa muscular (wasting)
El término sarcopenia define una situación de pérdida de masa y fuerza muscular importante y de etiología multifactorial, donde puede intervenir un déficit de ingesta, alteraciones hormonales, daño neuropático, alteraciones metabólicas y presencia de toxinas urémicas17. Representa un tipo de atrofia muscular crónica y en la ERC se asocia con DPE, limitando la autonomía del paciente y la calidad de vida. Produce compromiso de órganos vitales con deterioro respiratorio, músculo esquelético y del músculo cardíaco18. La disminución en la ingesta, la acidosis metabólica, la inactividad física, la diabetes y la sepsis son factores asociados en la ERC que aumentan la proteólisis muscular, mediante un aumento del catabolismo, activación de distintas señales intracelulares de apoptosis de la célula muscular y disminución en la síntesis. Varios estudios demuestran una atrofia significativa de las fibras musculares en la ERC19-21 (tabla 1).
Uno de los principales mecanismos por los que el DPE se asocia a la atrofia muscular en la uremia es el aumento del catabolismo proteico mediado por el UPS y la activación de la miostatina a nivel del músculo esquelético. El sistema UPS degrada proteínas musculares y la miostatina es un miembro de la familia factor de crecimiento transformante β que inhibe la proliferación celular y la síntesis de músculo22. La activación intracelular de la vía de las caspasas y la miostatina estimulan la degradación proteica proveyendo el sustrato para el sistema UPS y la apoptosis celular. El extenso tejido dañado lleva a una aumento de actina circulante que puede consumir gelsolina (proteína encargada del ensamblaje y desensamblaje de la actina) y otras proteínas como la vitamin D binding protein que tienen una función protectora23.
Niveles circulantes elevados de actina y bajos de gelsolina en pacientes en hemodiálisis se asocian con riesgo elevado de mortalidad. El aumento del catabolismo proteico y la acumulación de toxinas urémicas producirían una alteración en la síntesis de gelsolina, con pérdida de la capacidad de ensamblar actina, activación plaquetaria, disfunción endotelial e incremento de susceptibilidad a complicaciones infecciosas24.
Otro mecanismo recientemente descrito es la resistencia a la insulina. El factor de crecimiento insulínico tipo 1 activaría la vía de la fosfatidilinositol-3 quinasa alterando el metabolismo proteico, favoreciendo una sobrerregulación de la miostatina con disminución de la proliferación de las células musculares satélites25.
CRITERIOS DIAGNÓSTICOS DE DESGASTE PROTEICO ENERGÉTICO PROPUESTOS POR LA SOCIEDAD RENAL INTERNACIONAL DE NUTRICIÓN Y METABOLISMO
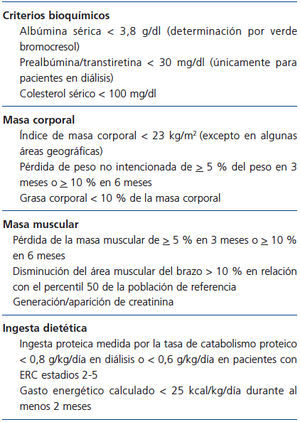
Un avance importante es la consideración del síndrome de DPE como una entidad patológica única en donde confluyen la desnutrición y el hipercatabolismo. El abordaje terapéutico eficaz del DPE no podrá llevarse solo a cabo con mera repleción nutricional, ya que persistirá la proteólisis. Un síndrome de origen multifactorial requerirá un criterio diagnóstico y una terapia integral. La ISRNM ha recomendado criterios diagnósticos (tabla 2). Se requiere cumplir al menos un criterio en tres de las cuatro categorías propuestas (criterios bioquímicos, masa corporal, masa muscular e ingesta)1 (tabla 2).
Estos criterios son inicialmente atractivos por su ámbito multifactorial (analítico, antropométrico y nutricional), pero cuando tratamos de aplicarlos a la práctica clínica diaria resultan confusos. Leinig et al.26 no encontraron ningún paciente que presentase alteraciones en tres de las cuatro categorías señaladas por la ISRNM y al redefinir el síndrome de DPE como alteración en dos de los cuatro compartimentos encontraron una prevalencia del 17 %, anormalmente baja si la comparamos con la prevalencia del 65 % al diagnosticarlo por encuesta de valoración global subjetiva (SGA). Otro ejemplo de la validez cuestionable de estos criterios lo hallamos en el trabajo de Drechsler et al.27, donde analizaron la relación entre DPE y mortalidad cardiovascular y de otras causas en una cohorte de 1255 pacientes diabéticos en hemodiálisis periódica. Observaron que ningún paciente cumplía los criterios de DPE propuestos por la ISRNM. En este caso los autores redefinieron los criterios de la ISRNM, considerando DPE si el índice de masa corporal (IMC), la albúmina y la creatinina sérica eran inferiores a la mediana de los pacientes estudiados. Este artículo tiene limitaciones derivadas de que toda la población estudiada era diabética, con la consecuente asociación a obesidad, por lo que tras los ajustes encuentran una prevalencia de DPE del 16 %.
Opinamos que los criterios de la ISRNM presentan limitaciones que debemos tener presentes. Estos criterios todavía deben demostrar en estudios prospectivos la superioridad a otras posibles combinaciones diagnósticas antes de generalizarse su implantación. Observaciones recientes ilustran este hecho al sugerir en una población de 570 pacientes en hemodiálisis que solo la presencia de hipoalbuminemia tenía un valor predictor de mortalidad similar o mayor que la suma de varios de los marcadores de malnutrición propuestos por la ISRNM28. Sin embargo, a menudo olvidamos que predicción de mortalidad no necesariamente se equipara a diagnóstico de malnutrición, y los puntos de corte sugeridos se basan en muchas ocasiones en análisis de supervivencia. En segundo lugar, los puntos de corte de los parámetros propuestos derivan de poblaciones americanas, planteando la duda de si son extrapolables a otras distribuciones geográficas y de estilo de vida, como Europa, Asia o, en el caso que nos ocupa, los países de la franja mediterránea. En tercer lugar, la población de diálisis cada vez es más anciana, y resulta difícil separar los cambios nutricionales y de composición corporal que ocurren con la edad de la malnutrición derivada de la uremia. Por todo ello, es lógico pensar que los criterios diagnósticos de DPE en la ERC deben adaptarse y variar en diferentes contextos demográficos (edad, raza), situaciones clínicas (obesidad, diabetes, ERC moderada, avanzada, diálisis y trasplante) y contextuales (hábitos de vida, situación geográfica y cultural)29.
En conclusión, si bien los criterios propuestos por la ISRNM refuerzan el carácter complejo del síndrome de DPE, se basan en unas determinaciones/mediciones que pueden ser cuestionables de forma individualizada30 y, por otro lado, todavía no han demostrado validez diagnóstica o pronóstica. Sin embargo, consideramos un paso importante el resaltar por vez primera en esta definición el carácter multifactorial del DPE y la necesidad del uso de diversos marcadores complementarios del estado nutricional.
PREVALENCIA DEL DESGASTE PROTEICO ENERGÉTICO
Las cifras tradicionales de prevalencia del DPE en la población de diálisis oscilan dentro de un amplio rango del 18-75 %26. Ciertamente, la imprecisión de estas cifras nos impide sacar conclusiones válidas. Uno de los problemas es la variedad de las herramientas de valoración y monitorización y de los puntos de corte que se han empleado para obtener estas cifras. En el caso de la hipoalbuminemia, se ha definido en la literatura con cifras de < 4, < 3,8 o < 3,5 g/dl, con la dificultad añadida de variar su estimación en función de la metodología empleada (bromocresol púrpura o bromocresol verde). Así, no es de extrañar que la prevalencia varíe en gran medida con la metodología empleada para su estimación. Una muestra de ello nos la dan dos estudios de Brasil26 y Europa28. La prevalencia de DPE varió entre un 23 % y un 74 %, dependiendo de si se definió por herramientas bioquímicas (albúmina, creatinina), antropométricas (perímetro del brazo, IMC) o nutricionales (SGA, ingesta energética/proteica). Lo mismo ocurre con otros estudios multicéntricos, como los realizados en Estados Unidos, donde describen una prevalencia del 38 %31. Por último, y no por ello menos importante, la prevalencia del DPE en distintos países será un reflejo de la situación económica, el grado de desarrollo y la prevalencia de la malnutrición en la población general, haciendo que sea imposible hablar de una prevalencia general a la población de diálisis. Esto también se aplica a la prevalencia en distintas regiones con más o menos recursos de una misma ciudad, provincia o país.
En España, los primeros estudios sobre prevalencia de malnutrición datan de 1994 y analizaron en 29 pacientes en hemodiálisis crónica el estado nutricional por medio de medidas antropométricas como el pliegue tricipital, la circunferencia muscular del brazo, el IMC, las proteínas viscerales (albúmina), la tasa de catabolismo proteico normalizado (nPCR) y la ingesta proteica32. Observaron que en una proporción considerable de pacientes (65 %) la reducción de las reservas de grasas y proteínas era más importante que lo que indicaba el peso corporal relativo (deficiente solo en el 38 % de ellos). En ese mismo año, se publicaron las primeras y únicas tablas de parámetros antropométricos de una población española en hemodiálisis (761 pacientes)33,34. En la muestra estudiada la prevalencia de malnutrición definida según parámetros antropométricos y marcadores bioquímicos (albúmina, transferrina, recuento de linfocitos) fue del 52 % en varones y del 46 % en mujeres. Los predictores de malnutrición fueron la edad avanzada, el índice de comorbilidad, el sexo masculino, el tiempo en hemodiálisis y la nPCR. El estudio multicéntrico Dialysis Outcomes and Practice Pattern Study (DOPPS) mostró importantes diferencias entre países en la monitorización de los parámetros nutricionales, siendo España uno de los más deficitarios en la recogida de estos parámetros35. Así, la nPCR se realizaba solo en el 20 % de las unidades de diálisis en España, en comparación con el 90 % en Alemania, y además solo había dietista en un 20 % de las unidades en España, comparado con un 85 % en el Reino Unido. A pesar de esto, no hubo diferencias significativas en los resultados de las cifras de albúmina sérica (3,98 g/dl), creatinina (9,1 mg/dl) e IMC (23,9 kg/m2) con el resto de los países europeos. Sin embargo, la prevalencia de malnutrición moderada según la escala SGA fue menor en España que en otros países como Francia (11 % frente a 18 %).
Debemos mencionar que los estudios hasta ahora citados incluyen pacientes estables, por lo que existe un sesgo al eliminar al paciente crítico o agudamente enfermo y que probablemente presente DPE. Este hecho nos conduce a pensar que la prevalencia de DPE puede ser incluso mayor de lo que aquí se reseña. Así, en un reciente análisis de nuestra unidad hemos observado una prevalencia de DPE según los criterios de la ISRNM del 37 %, que se incrementó al 41,1 % cuando los pacientes se siguieron durante dos años36. Aunque el tamaño muestral es relativamente pequeño, el estudio incluyó a todos los pacientes de la unidad de diálisis (sin exclusiones) y se usaron los criterios de DPE de la ISRNM.
Las últimas guías de la S.E.N. de nutrición en ERC avanzada publicadas en el año 200837 recomiendan valorar el estado nutricional mediante la determinación de marcadores nutricionales, bioquímicos, antropométricos y de ingesta energética y proteica.
IMPLICACIONES CLÍNICAS
La tasa de mortalidad de los pacientes con ERC, especialmente la cardiovascular, es más alta que en la población general38-41. Esta alta tasa de mortalidad persiste a pesar de corregir factores cardiovasculares tradicionales, como hipertensión, dislipemia, hipertrofia ventricular izquierda, y de mejorar las técnicas de diálisis42. El DPE se puede considerar un nuevo factor de riesgo que subyace al fenómeno de epidemiología inversa, donde marcadores que en la población general se asocian con menor probabilidad de eventos cardiovasculares como el descenso del IMC o niveles de colesterol bajos se asocian con mayor presencia de enfermedad cardiovascular y menor supervivencia en pacientes en diálisis43.
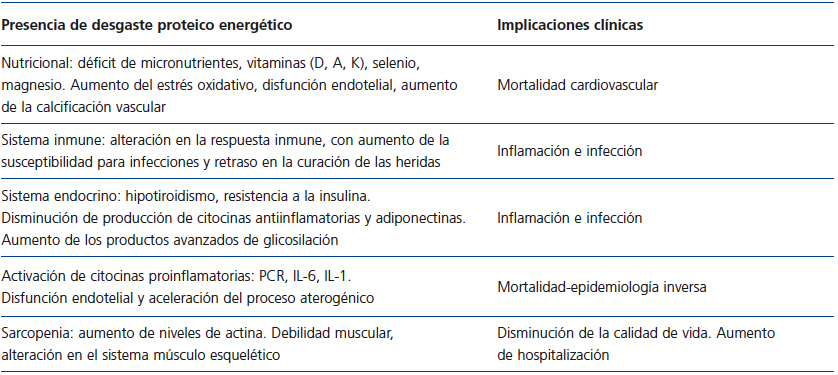
La presencia de DPE conlleva en el paciente renal la activación de mecanismos compensatorios y la desregulación de otros, lo que afecta a distintos órganos y sistemas, incluyendo sistema inmune, endocrino, músculo-esquelético, tejido adiposo, hematopoyético, gastrointestinal y mala adaptación a la activación de la cascada inflamatoria44,45, con lo que aumenta la mortalidad global (tabla 3).
Desgaste proteico energético y mortalidad cardiovascular
En pacientes con ERC avanzada, la malnutrición y la presencia de DPE se relacionan de forma importante con la mortalidad cardiovascular46,47. Los nutrientes son necesarios para el correcto funcionamiento del organismo. Las restricciones dietéticas en el paciente urémico para limitar la ingesta de potasio, fósforo o sodio, entre otros, pueden conducir a deficiencias en otros nutrientes esenciales si no existe consejo dietético por parte del personal sanitario. Los nutrientes esenciales son necesarios para la síntesis de tejido y producción de energía, al tiempo que son coenzimas en la mayoría de reacciones enzimáticas del organismo. Carencias nutricionales específicas como la deficiencia en selenio, magnesio o vitamina D, tan comunes en el paciente renal, tienen consecuencias negativas en la capacidad antioxidante y antiinflamatoria y en el metabolismo óseo mineral. Por ello, el DPE se asocia a un mayor riesgo de infecciones y de muerte por causas infecciosas29,48. El déficit de vitaminas A, K y D se asocia a mayor mortalidad cardiovascular en el paciente en hemodiálisis49,50. Hasta el 80 % de los pacientes en hemodiálisis tienen déficit de vitamina K debido a una ingesta insuficiente (140 µg/día frente a 200 µg/día en pacientes sanos). La deficiencia subclínica de vitamina K hepática aumenta las proteínas inactivas no-carboxiladas dependientes de vitamina K y puede contribuir a aumentar el riesgo de fracturas óseas y de calcificación vascular. Los suplementos de vitamina K (menaquinona-7) disminuyen las proteínas no-carboxiladas en pacientes en hemodiálisis y el tratamiento prolongado es capaz de aumentar la elasticidad vascular51-53.
El DPE propicia un aumento del catabolismo muscular en el paciente urémico, tanto por la falta de nutrientes circulantes como por el efecto combinado de la inflamación sistémica, la acidosis metabólica, las toxinas urémicas y otros factores. La consecuencia es una pérdida de masa muscular que también afecta al tejido muscular de las arterias y el corazón, encontrándose asociaciones directas entre malnutrición, rigidez arterial y alteraciones en la estructura miocárdica. La distensión vascular continuada como consecuencia de la sobrecarga hidrosalina agrava este proceso y propicia la hipertrofia ventricular. Un ejemplo de cómo la desnutrición pura conlleva alteraciones en el sistema cardiovascular data del experimento Minnesota, realizado en 1944 durante la II Guerra Mundial. El objetivo era conocer mejor la fisiopatología de la desnutrición a que se veían sometidos los judíos en los campos de concentración. Se sometió a 36 voluntarios a una disminución controlada de la ingesta que resultó en la pérdida total del 25 % del peso. La desnutrición produjo una disminución del volumen cardíaco del 17 %, con disminución del gasto cardíaco, bradicardia, hipotensión, y disminución de la oxigenación periférica y de la contractilidad miocárdica54.
La hipoalbuminemia es el biomarcador más común y frecuentemente usado para medir el DPE en diálisis y es un potente marcador pronóstico de morbimortalidad55,56. Además, la hipoalbuminemia se ha asociado con el desarrollo de novo y recurrencia de insuficiencia cardíaca congestiva en pacientes en hemodiálisis y en diálisis peritoneal57. En el estudio 4D realizado en una cohorte de 1255 pacientes diabéticos en hemodiálisis se investigó el efecto del DPE sobre la mortalidad a los cuatro años. La presencia de DPE (definido como IMC 26,7 kg/m2, albúmina sérica < 3,8 g/dl y creatinina < 6,8 mg/dl) duplicó el riesgo de mortalidad global, de muertes debidas a infecciones y de muerte súbita de origen cardíaco, pero no se relacionó con mayor incidencia de infartos de miocardio. La presencia de enfermedad cardiovascular no arteriosclerótica en este estudio tuvo más relevancia en los pacientes con DPE como causa de los eventos cardiovasculares27.
Las alteraciones hormonales asociadas a la uremia como el hipotiroidismo subclínico58 o el síndrome de T3 baja59 se asocian a inflamación y malnutrición60 y pueden contribuir a la enfermedad cardiovascular. Así, se ha observado una asociación independiente entre hipotiroidismo y mortalidad cardiovascular en pacientes en hemodiálisis61,62. En pacientes con insuficiencia e hipotiroidismo subclínico la administración de T3-sintético mejoró el perfil neuroendocrino con descenso significativo en los niveles de noradrenalina y péptido natriurético tipo B (pro-BNP) en comparación con placebo. Además, se observó un aumento del volumen telediastólico del ventrículo izquierdo con aumento del gasto cardíaco, sin observarse un aumento de la precarga63. La disminución en la síntesis de otras hormonas anabólicas como la testosterona64 también se asocia a una mayor pérdida muscular65, disfunción endotelial66, anemia, resistencia a la eritropoyetina67 y mortalidad68.
DESGASTE PROTEICO ENERGÉTICO E INFECCIÓN Y HOSPITALIZACIÓN
La uremia se considera un estado de inmunodeficiencia adquirida69 y los pacientes con ERC tienen un alto riesgo de infección70. En el estudio HEMO la infección fue la primera causa de muerte (23 %) y el riesgo de mortalidad asociado a una infección durante el ingreso hospitalario fue del 15 %. Los factores que predisponen a la infección en el paciente con ERC según el estudio HEMO fueron la edad avanzada, la hipoalbuminemia, la terapia inmunosupresora y los catéteres como acceso vascular71. Paralelamente, en el estudio DOPPS29 la infección fue la causa del 55 % de las muertes en pacientes en hemodiálisis y se relacionó con hipoalbuminemia, bajo nPCR y caquexia.
La definición de estatus de malnutrición según el concepto de DPE conlleva una deficiencia en el sistema inmune y una alteración en la respuesta del huésped, por lo que se asocia a mayor susceptibilidad a las infecciones y a una lenta recuperación de las heridas72. El déficit de ciertos micro-macronutrientes favorece el estado de inmunodeficiencia. Algunos aminoácidos como la arginina y la glutamina intervienen y favorecen la respuesta inmune73. Un déficit grave de cinc, vitamina B6 (piridoxina), vitamina C y acido fólico74-76 altera la respuesta inmune, disminuye la producción de anticuerpos, causa disfunción de los leucocitos polimorfonucleares o linfocitos y retrasa la cicatrización y curación de las heridas. El paciente en hemodiálisis con DPE estará expuesto a un mayor riesgo de infecciones y a sus complicaciones, aumentando la mortalidad77. Por ejemplo, en la infección del virus de la hepatitis C la presencia de hipoalbuminemia y de un resultado elevado de la escala MIS (malnutrition inflammation score) se asocia independientemente con infección activa y mayor replicación viral78.
En pacientes hospitalizados un estado nutricional deficiente retrasa la recuperación, prolonga la estancia hospitalaria, incrementa la tasa de infecciones y de reingresos, y aumenta la dependencia al alta y la necesidad de institucionalización. En pacientes en diálisis con estancias hospitalarias prolongadas y complicadas, se produce un rápido descenso de la albúmina y pérdida de peso, sobre todo en aquellos que presentan una desnutrición previa, edad avanzada, comorbilidad y anorexia79. Las recomendaciones de las guías de prevención y manejo de la desnutrición hospitalaria pueden ser muy útiles en los pacientes con ERC hospitalizados, puesto que incluyen el uso de suplementos y nutriciones parenterales para mejorar la situación nutricional80.
DESGASTE PROTEICO ENERGÉTICO E INFLAMACIÓN
Varios estudios han observado una asociación independiente entre procesos inflamatorios, comúnmente medidos por el aumento de Proteína C reactiva (PCR), IL6, IL1 y TNF-α, con el riesgo de mortalidad cardiovascular en los pacientes en hemodiálisis81 y en la población general82.
La inflamación se asocia tanto con anorexia como con un aumento del catabolismo proteico83,84 y parece ser el nexo de unión que explica la relación entre DPE y mortalidad en la ERC.
La relación entre malnutrición e inflamación en pacientes con ERC puede ser una de las causas de mortalidad asociada a la malnutrición. Por otro lado, el DPE también puede ser consecuencia de estados inflamatorios crónicos en los pacientes con insuficiencia renal85,86.
DESGASTE PROTEICO ENERGÉTICO Y CALIDAD DE VIDA
Un aspecto a veces poco apreciado por el nefrólogo, pero que cada vez tiene más relevancia en la práctica clínica, es la repercusión de la enfermedad en el grado de funcionalidad del paciente. El impacto de la ERC sobre el funcionamiento global del paciente se puede recoger en encuestas de calidad de vida como PROs (patient–reported outcomes) y QoL (health related quality of life), que evalúan el estado mental y funcional del paciente. La ERC se asocia a un pobre QoL y este conlleva un mayor riesgo de mortalidad87. Igualmente se ha relacionado QoL con marcadores de malnutrición, donde peores valores de QoL se asocian con niveles bajos de albúmina, creatinina plasmática, pérdida de LBM (tejido magro, principalmente muscular) y alto porcentaje de grasa88. La mejoría de QoL se ha convertido en uno de los objetivos en los pacientes en diálisis.
La prevalencia de estados mentales de depresión y ansiedad es alta en los pacientes en diálisis89. Estos se enfrentan a situaciones como hospitalizaciones, ansiedad frente a los cambios en diálisis, restricciones en la dieta y agua, y a la adaptación de la diálisis a sus vidas cotidianas. El miedo a la incapacidad, la minusvalía y a una menor esperanza de vida son el origen de estas alteraciones del estado de ánimo. Se están desarrollando nuevos métodos y herramientas para medir la depresión y la ansiedad y se ha apreciado que la ansiedad está infradiagnosticada90.
EPIDEMIOLOGÍA INVERSA EN LA INSUFICIENCIA RENAL: IMPLICACIONES DEL ESTADO NUTRICIONAL
En la evaluación de los factores de riesgo para morbimortalidad de los pacientes con ERC a menudo se observan tendencias paradójicamente opuestas a las observadas en la población general. Un claro ejemplo es la obesidad, que en estudios observacionales aparece como un factor protector de mortalidad en los estadios finales de la ERC. Es lo que se conoce como fenómeno de epidemiología inversa o paradoja de la obesidad urémica. La causa de estos fenómenos de epidemiología inversa se debe al efecto devastador que tiene el DPE sobre la supervivencia a corto plazo, no dejando tiempo suficiente a otros factores de riesgo tradicionales a actuar en la mortalidad a largo plazo91. Entre los ejemplos más llamativos encontramos el caso de la hipercolesterolemia, que se asocia de manera inversa a la mortalidad en el paciente urémico. Cuando se segrega a los pacientes en función de si presentan o no DPE, se puede observar que en presencia de DPE la hipercolesterolemia es un factor protector, mientras que en ausencia de DPE la hipercolesterolemia es un factor de riesgo. Ante el proceso de consunción energética que afronta el paciente, el colesterol en este caso se convierte temporalmente en un marcador de las reservas de grasa del organismo y, a mayor grasa, el paciente puede resistir esta consunción energética más tiempo.
El mismo razonamiento se aplica a la paradoja de la obesidad. Los pacientes en diálisis, independientemente de la modalidad elegida, presentan una relación inversamente proporcional entre IMC y mortalidad92, difiriendo de la población general, en donde esta relación tiene forma de U (ambos extremos, malnutrición y obesidad, presentan un incremento de la mortalidad)93. En este caso, la obesidad supone un estado de exceso energético que ayuda a que el paciente resista el DPE. Sin embargo, la obesidad a largo plazo supone un factor de riesgo relacionado con inflamación, aterosclerosis y calcificación, por mencionar algunos94. Ello es debido al carácter endocrino del adipocito y a la capacidad de modular estos procesos mediante la secreción de citocinas y adipocitocinas95. La grasa endocrinológicamente activa, primordialmente la acumulada en el abdomen, propicia estos procesos. Por ello, la cantidad de grasa total (reflejo del bienestar de reservas energéticas) y la grasa abdominal (participante del riesgo asociado a la obesidad) pueden tener efectos opuestos sobre el riesgo del paciente96.
Otra explicación a la epidemiología inversa del IMC en la uremia es la incapacidad del IMC de diferenciar masa muscular, distribución corporal de grasa (abdominal frente a periférica) e hipervolemia. Así, pudimos observar recientemente que un IMC > 30 kg/m2 no era capaz de discriminar un exceso de grasa corporal en un 65 % de los pacientes en diálisis43. Estudios recientes señalan que el tipo y distribución de la grasa, más que el total de esta, es un determinante factor de riesgo97. En concreto, el acúmulo de grasa abdominal es un factor de riesgo y se asocia a una mayor secreción de adiponectinas proinflamatorias98. Se ha descrito que tanto la leptina como la visfatina son activadores de la enfermedad cardiovascular y factores de riesgo de disfunción endotelial99,100. Estudios observacionales basados en la cinética de la creatinina sugieren que el efecto protector del IMC en los pacientes en hemodiálisis es debido a que indica una mayor masa muscular101. Posiblemente en los pacientes en diálisis es necesaria la conservación de ambos tejidos, grasa y músculo. En este sentido, un percentil bajo de circunferencia muscular del brazo, como indicador de masa muscular, y un percentil bajo de pliegue tricipital, como indicador de tejido graso, se relacionan en igual medida con mayor mortalidad en pacientes en hemodiálisis102. Por último, el riesgo de mortalidad aumenta cuando el IMC, la creatinina y el peso disminuyen progresivamente, pero, si disminuye el peso y aumenta la creatinina, el riesgo de mortalidad se reduce103.
CONCLUSIÓN
El término desgaste proteico energético o DPE intenta aunar en una sola entidad patológica las múltiples alteraciones nutricionales y catabólicas que acontecen en la ERC y que conllevan la pérdida gradual y progresiva de masa tanto muscular como grasa. Es un síndrome común, especialmente a partir del estadio 4-5 de ERC, que está presente en el 30-60 % de los pacientes en diálisis. Las consecuencias clínicas del DPE pueden ser graves y reclaman un tratamiento rápido y efectivo, puesto que se asocia a un incremento de la mortalidad tanto global como cardiovascular, del número de infecciones e ingresos, y a otras muchas comorbilidades. El efecto devastador del DPE origina paradojas epidemiológicas que se explican por la competitividad entre los factores de riesgo a corto y a largo plazo.
AGRADECIMIENTOS
ISCIII-RETIC REDinREN/RD06/0016 y 12/0021, PIE13/00051, Sociedad Española de Nefrología, Swedish Research Council, programa Intensificación Actividad Investigadora (ISCIII).
Conflictos de interés
Los autores declaran que no tienen conflictos de interés potenciales relacionados con los contenidos de este artículo.
PUNTOS CLAVE
- El término desgaste proteico energético se define como un estado patológico donde hay un descenso o desgaste continuado tanto de los depósitos proteicos como de las reservas energéticas.
- Los mecanismos fisiopatológicos implicados en el DPE son anorexia y aumento del catabolismo proteico, que dan lugar a un desequilibrio energético, con el resultado final de un aumento del gasto energético.
- Para un correcto diagnóstico del DPE se requiere la valoración de marcadores bioquímicos y de la composición corporal, y calcular la pérdida de músculo y la ingesta dietética.
- La presencia de DPE se asocia a un aumento en el riesgo cardiovascular, de infección, de hospitalización y de mortalidad, a la inflamación, y a una peor calidad de vida.
- La presencia de DPE explica el conocido fenómeno de epidemiología inversa, donde los factores de riesgo tradicionales aparecen como factores de protección.
Tabla 1. Causas de desarrollo de desgaste proteico energético en la enfermedad renal crónica
Tabla 2. Criterios diagnósticos para el desgaste proteico energético propuestos por la Sociedad Renal Internacional de Nutrición y Metabolismo1
Tabla 3. Repercusiones clínicas subyacentes al síndrome de desgaste proteico energético que implican una mayor mortalidad