Introducción: La hemodiafiltración (HDF) con altos volúmenes de reinfusión es la técnica más eficaz en la depuración de toxinas urémicas. Existen distintas modalidades dependiendo del lugar donde se administra el volumen de sustitución en el circuito extracorpóreo: predilucional, mixta o mid-dilucional y posdilucional, en las que la infusión se realiza pre, de forma simultánea pre y pos, y posdilucional, respectivamente. Objetivo: Comparar la depuración de moléculas pequeñas, medianas y unidas a proteínas y el volumen convectivo administrado en HDF en línea (HDF-OL) con infusión posdilucional y mixta (pre-posdilucional). Material y métodos: Estudio prospectivo, aleatorizado y cruzado, comparando HDF-OL posdilucional y mixta. Los pacientes (n = 8) fueron asignados aleatoriamente para recibir 6 sesiones en cada técnica. Se realizaron 89 sesiones, de las cuales 68 fueron a tiempo programado (TP) y 21 a tiempo efectivo (TE). Se determinaron los porcentajes de reducción (RR) de distintas sustancias y los volúmenes de infusión. El estudio de los RR se realizó con TE. Resultados: El KT obtenido fue mayor con HDF-OL posdilucional [68 (8,1) frente a 64,9 (8,8) litros] (p = 0,009) cuando los pacientes se dializaron a TP. Esta diferencia desaparecía cuando la diálisis se realizaba a TE. La diferencia entre el TP-TE fue mayor en la HDF mixta con respecto a la HDF posdilucional [10,3 (7,4) frente a 6,5 (3,1) minutos, p = 0,02]. No encontramos diferencias en los RR de las sustancias analizadas. Conclusión: La HDF-OL mixta no es inferior a la posdilucional ni en la depuración de moléculas pequeñas y medianas ni en las unidas a proteínas a igual TE.
Introduction: Haemodiafiltration (HDF) with high reinfusion volumes is the most effective technique for clearing uraemic toxins. There are various modalities depending on the location where the replacement volume is administered in the extracorporeal circuit: pre-dilution, mixed or mid-dilution and post-dilution, in which the infusion is carried out pre-dilution, pre- and post-dilution simultaneously and post-dilution, respectively. Objective: Compare the clearance of small, medium-sized and protein-bound molecules and the convective volume administered in online HDF (OL-HDF) in post-dilution and mixed (pre-post-dilution) infusion. Material and method: A prospective, randomised, crossover study comparing post-dilution and mixed OL-HDF. Patients (n=8) were randomly assigned to receive 6 sessions in each technique. We conducted 89 sessions, of which 68 were at a scheduled time (ST) and 21 at an effective time (ET). We determined the reduction rate (RR) percentages for various substances and the infusion volumes. The RR study was performed using ET. Results: The KT value obtained was greater with post-dilution OL-HDF [68 (8.1) compared to 64.9 (8.8) litres] (P=.009) when patients were dialysed at ST. This difference disappeared when dialysis was performed at ET. The difference between ST and ET was greater in mixed HDF than in post-dilution HDF [10.3 (7.4) compared to 6.5 (3.1) minutes, P=.02]. We found no differences in the RR of the substances analysed. Conclusion: Mixed OL-HDF is not inferior to post-dilution OL-HDF either in the clearance of small and medium-sized molecules or in the clearance of protein-bound molecules at the same ET.
INTRODUCCIÓN
La hemodiafiltración (HDF) con altos volúmenes de reinfusión es la técnica más eficaz en la depuración de toxinas urémicas, en especial las moléculas medias, cuya eliminación es significativamente superior con las técnicas convectivas. Diversos estudios han mostrado que la HDF mejora algunas de las complicaciones de los pacientes en hemodiálisis (HD) como la hiperfosforemia1, la desnutrición2, el crecimiento en los niños3, la respuesta a la eritropoyetina4 y a la vitamina D5 y la amiloidosis asociada a la diálisis, entre otras6. También en el momento actual existen evidencias que demuestran una mejor supervivencia de los pacientes que son sometidos a diálisis con HDF en línea (HDF-OL) respecto a los que lo hacen en HD7-10, como se comentará más adelante. Los buenos resultados obtenidos en estos estudios quedan condicionados por el volumen de transporte convectivo alcanzado, en general por encima de 20-24 l por sesión.
Existen diferentes modalidades de HDF-OL, dependiendo del lugar donde se administra el volumen de sustitución en el circuito extracorpóreo. En la HDF predilucional el líquido es infundido antes de la entrada de la sangre en el dializador, lo que conlleva una hemodilución y una disminución del transporte difusivo. En la HDF posdilucional el líquido de sustitución es administrado después del dializador, de forma que no interfiere en el transporte difusivo, pero produce una hemoconcentración en el dializador que puede aumentar las presiones y producir problemas de coagulación. La HDF posdilucional se considera la forma más eficiente. Además de estas dos modalidades más habituales, encontramos otras dos formas de HDF-OL en las que la infusión se realiza simultáneamente pre y posdilucional: la HDF-OL mixta y la HDF-OL mid-dilución. En la HDF-OL mixta el líquido de sustitución se infunde de forma simultánea pre y posdilución, regulándose el porcentaje de infusión pre y posdilución de forma automática mediante un feedback presión transmembrana (PTM) y ultrafiltración (UF). La mid-dilución requiere de un dializador especial, donde la sangre entra por un haz de fibras centrales y regresa, en sentido contrario, por fibras periféricas. El líquido de reinfusión se incorpora en la mitad de los dos tramos del dializador; así, en el primer tramo se produce una HDF posdilucional y en el segundo tramo una HDF predilucional. Estas formas mixtas de HDF-OL son una buena alternativa, ya que en teoría evitan las desventajas descritas para la HDF-OL pre y posdilucional. La elección entre una y otra modalidad va a depender de las características hemorreológicas y del flujo sanguíneo con que se dialice al paciente.
Los beneficios citados de la HDF están basados en resultados de la HDF-OL posdilucional. La cantidad de volumen convectivo administrado parece ser decisiva en la mejora de la supervivencia. Dicho volumen por sesión fue de 15 l en el European Dialysis Outcomes and Practice Pattern Study (DOPPS)7, 17,4 l en el estudio turco8, 21,9 l en el Convective Transport Study (CONTRAST)9 y 23,1 l en el Estudio de Supervivencia de Hemodiafiltración On line (ESHOL)10 (tabla 1). Estos estudios ponen en evidencia la necesidad de alcanzar volúmenes convectivos altos para reducir la mortalidad.
A pesar de la importancia de la cantidad de volumen convectivo mostrada en estos estudios, no se conoce la equivalencia del volumen de infusión entre las diferentes modalidades de HDF-OL. Recientemente el grupo EUDIAL11 ha aconsejado utilizar un factor de dilución en la HDF-OL cuando el volumen sea total o parcialmente infundido antes del dializador (modalidades predilucional, mid-dilucional y mixta). También insisten en la importancia de la medida del volumen convectivo efectivo ajustado a la superficie corporal para cuantificar la eficacia de la HDF-OL.
La cantidad de volumen convectivo administrado se ha relacionado de forma directa con la depuración de moléculas medias12,13. Los estudios que han analizado la eficacia en la eliminación de solutos comparando las técnicas convectivas muestran que la infusión posdilucional es la forma más eficaz para depurar moléculas tanto pequeñas como medianas y grandes14-16. Solo Pedrini17 ha estudiado la infusión mixta pre-posdilucional, y ha encontrado un mayor porcentaje de reducción de la β2-microglobulina (β2m) con HDF mixta en comparación con la infusión predilucional y resultados similares a la infusión posdilucional (72,1 % en mixta, 69,2 % en pre y 74,7 % en HDF posdilucional).
OBJETIVO
Comparar la depuración de moléculas pequeñas, medianas y unidas a proteínas y el volumen convectivo administrado de la HDF-OL con infusión posdilucional y mixta (pre-posdilucional) en pacientes en tratamiento con HDF-OL, para determinar los litros de volumen convectivo requeridos con ambas técnicas para lograr igual eficiencia depurativa.
MATERIAL Y MÉTODOS
Diseño
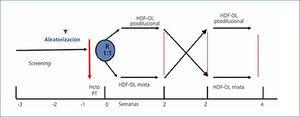
Estudio prospectivo, aleatorizado y cruzado, comparando HDF-OL posdilucional y mixta (figura 1). Los pacientes fueron asignados aleatoriamente para recibir 6 sesiones consecutivas en HDF-OL posdilucional, seguida o precedida por otras 6 sesiones de HDF-OL mixta.
Cada paciente sirvió como control de sí mismo y no se realizaron modificaciones de la pauta de diálisis ni del tratamiento farmacológico durante el estudio.
Dado que los monitores modernos de diálisis interrumpen el procedimiento por autochequeos que incrementan la seguridad haciendo que el tiempo efectivo (TE) o real de tratamiento sea inferior al tiempo programado (TP) o prescrito por el médico, se tuvieron en cuenta estas variables. Se siguió la pauta habitual de trabajo dializando a TP en las sesiones 1, 3, 4 y 6, mientras que las sesiones 2 y 5 se realizaron a TE, prolongándose lo necesario para que el tiempo real fuera el programado.
Para evaluar la eficacia de la técnica se midieron la depuración de moléculas mediante el porcentaje de reducción de dichas sustancias y la cantidad de volumen convectivo administrado.
Pacientes y técnica de diálisis
Los criterios de inclusión fueron: pacientes mayores de 18 años en tratamiento con diálisis trisemanal y con un mínimo de tres meses en tratamiento con HDF-OL.
Los criterios de exclusión fueron: presencia de inestabilidad hemodinámica con hipotensiones frecuentes, contraindicación para el uso de heparina, presencia de función renal residual (FRR) definida como un aclaramiento medio de urea y creatinina mayor de 1 ml/min o tener un flujo sanguíneo (Qs) inferior a 250 ml/min.
Todos los pacientes firmaron un consentimiento informado en el momento de la inclusión.
Se realizaron todas las sesiones con un monitor de diálisis: ST5008 (Fresenius, FMC, Bad Homburg, Germany) y utilizando el dializador FXCorDiax1000 (Fresenius, FMC, Bad Homburg, Germany).
Características del dializador: membrana de helixona, superficie de 2,3 m2 y coeficiente de UF: 76 ml/h/mmHg.
En la unidad de diálisis se utiliza líquido de diálisis ultrapuro18 definido por unos niveles de unidades formadoras de colonias/ml inferiores a 0,1 y niveles de endotoxinas inferiores a 0,03 UE/ml.
El modo de infusión posdilucional fue controlado por el monitor teniendo en cuenta los valores de proteínas totales, el hematocrito y la permeabilidad hidráulica del dializador.
El modo de infusión mixta es controlado por feedback PTM-UF. Este feedback ajusta de forma automática la tasa y el lugar de infusión (pre/posdilucional) a la máxima fracción de filtración teniendo en cuenta las condiciones del flujo, las presiones internas y la permeabilidad hidráulica del dializador y sus interacciones. El sistema regula el grado de infusión pre/pos por medio de dos bombas de infusión independientes cuya velocidad de infusión es modulada por un software interno en función del valor de PTM, con el objetivo de mantener la PTM entre 250-300 mmHg19,20. La PTM se calcula instantáneamente según las presiones en cuatro puntos mediante la fórmula:
PTMm = 0,5 x [(P entrada sangre dializador + P salida sangre dializador) - (P entrada líquido diálisis + P salida líquido diálisis)]
Determinaciones analíticas
Setenta y dos horas antes del inicio del estudio (última sesión previa al inicio del estudio) se determinaron el hematocrito y las proteínas totales (valores que se introdujeron en el monitor en la HDF-OL posdilucional).
El día intermedio de la semana (sesiones 2 y 5) los pacientes se dializaron a TE y se obtuvieron muestras de sangre prediálisis extraídas de la línea arterial inmediatamente antes de iniciar la técnica y posdiálisis de la línea arterial después de disminuir el QS a 50 ml/min durante 60 segundos.
En sangre se determinaron distintas toxinas urémicas, que en función de la clasificación21 se definen como moléculas pequeñas (peso molecular [PM] inferior a 500 Da): urea (60 Da), fósforo (95 Da), creatinina (113 Da) y ácido úrico (168 Da); como moléculas medias (PM superior a 500 Da): β2m (11 818 Da), mioglobina (17 200 Da), y moléculas unidas a proteínas: proteína transportadora del retinol (PTR) (21 200 Da).
En el dializado se determinó la concentración de albúmina, recogiéndose las muestras a los 30, 60 y 120 minutos de iniciada la sesión de HDF-OL mediante un dispositivo colocado en el tubo de drenaje.
La β2m se determinó mediante inmunoturbidimetría utilizando el inmunoensayo Immulite® 2000 (Siemens), y la PTR por inmunonefelometría, utilizando el método BN ProSpec® System (Siemens). El hematocrito se determinó mediante el autoanalizador ADVIA 2120/2120, y el resto de las determinaciones bioquímicas, incluida la albúmina en el dializado, se determinaron con un autoanalizador (ADVIA® 2400 Chemistry System, Bayer).
Parámetros demográficos y de diálisis recogidos
Se recogieron una serie de parámetros demográficos: edad, enfermedad de base, tiempo en HD y HDF-OL, el tipo de acceso vascular: fístula y catéter.
Los parámetros de diálisis: Qs, flujo del líquido de diálisis, tiempos: TP y TE, conductividades de sodio y bicarbonato, temperatura del líquido, tipo y dosis de heparina, volúmenes de infusión (total, pre y posdilución), PTM media, el KT medido automáticamente por el biosensor OCM (on-line clearance monitoring), la UF por sesión y la tensión arterial (TA) pre y pos-HDF.
Cálculos
Los porcentajes de reducción (RR) se calcularon con la fórmula: RR (%) = [(Cpre – Cpos)/Cpre] x 100.
Donde Cpre y Cpos son las concentraciones de las sustancias analizadas pre y posdiálisis.
Para las sustancias unidas a proteínas y la β2m las concentraciones al finalizar la sesión fueron corregidas para la hemoconcentración por un factor de corrección (FC) basado en la concentración de proteínas plasmáticas (PT):
FC = PTpre/PTpos22
Donde PTpre y PTpos son las concentración de proteínas totales prediálisis y posdiálisis.
Análisis estadístico
El análisis estadístico se realizó con el programa SPSS 15.0 (SPSS INC., Chicago IL, USA). Los datos descriptivos se presentan como la media y la desviación estándar (DE).
Para la comparación de dos variables continuas independientes se utilizó el test de la t de Student para muestras apareadas. Para la comparación de más de dos variables cuantitativas se utilizó el ANOVA. La p < 0,05 fue considerada como estadísticamente significativa.
RESULTADOS
Se incluyeron 8 pacientes en el estudio, 5 varones y 3 mujeres; edad media: 66 (14) [39-83] años; con un tiempo medio en tratamiento renal sustitutivo de 14,5 (10) [3-28] años; tiempo medio en HDF-OL de 30,8 (30,9) [4-99] meses. La etiología de la enfermedad renal crónica fue glomerulonefritis (3 pacientes), poliquistosis (2 pacientes), nefritis intersticial (1 paciente) y desconocida (2 pacientes). Un paciente no finalizó el estudio, pues completó únicamente las primeras 6 sesiones. Se incluyeron los datos de un total de 89 sesiones de HDF.
En la tabla 2 se muestran las características de los parámetros de diálisis. La dosis de anticoagulación no se modificó a lo largo del estudio, se utilizó enoxaparina en 2 pacientes (dosis media por sesión: 60 [28,2] mg) y heparina sódica al 1 % en 6 pacientes (dosis media por sesión: 53,7 [25,6] mg).
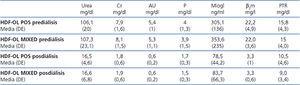
En la tabla 3 se muestran los valores prediálisis y posdiálisis de las distintas moléculas analizadas, entre las que no encontramos diferencias significativas.
En la figura 2 están representados los RR de las sustancias analizadas, no habiendo encontrado diferencias significativas en las moléculas analizadas entre la HDF-OL posdilucional y la HDF-OL mixta.
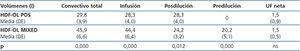
En la tabla 4 se muestran los volúmenes de infusión obtenidos con ambas técnicas, siendo como era de esperar la diferencia entre ellos estadísticamente significativa para todos los volúmenes, salvo para el volumen de UF.
En la tabla 5 se muestran los resultados del KT obtenido a TP y TE en función de la técnica. Como puede observarse, encontramos una diferencia estadísticamente significativa en el KT obtenido en ambas técnicas (p = 0,009) cuando los pacientes se dializaron a TP. Sin embargo, esta diferencia desaparecía cuando la diálisis se realizaba a TE.
La diferencia entre el TP-TE fue mayor en la HDF mixta con respecto a la HDF posdilucional (10,3 [7,4] frente a 6,5 [3,1] minutos), alcanzado significación estadística (p = 0,02).
No encontramos diferencias en los valores de TA sistólica ni diastólica antes y después de la realización de ambas técnicas (TA sistólica prediálisis: 139,7 [14,4] frente a 140,7 [20,4] mmHg, TA diastólica prediálisis: 66,5 [11,5] frente a 63,8 [14,7] mmHg, TA sistólica posdiálisis: 128 [15] frente a 132,1 [17,1] mmHg y TA diastólica posdiálisis: 64,7 [11,8] frente a 62,9 [1,9] mmHg para la HDF-OL posdilucional y mixta, respectivamente).
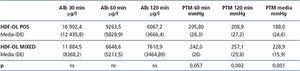
La PTM media en ambas técnicas fue diferente: 188,3 (37,3) frente a 229,6 (26,7) mmHg en la HDF-OL posdilucional y mixta, respectivamente (p = 0,002) (la medida de la PTM se realiza de forma diferente). No encontramos diferencias en la concentración de albúmina en el dializado en los tiempos analizados (30, 60 y 120 minutos) (tabla 6).
DISCUSIÓN
Este estudio compara la eficacia de depuración de toxinas urémicas de dos modalidades de HDF-OL, la posdilucional y la mixta (pre-posdilucional), y encontramos que en el RR de las moléculas analizadas no existen diferencias significativas en ninguna de ellas. La mayoría de los estudios han comparado la eficacia de la HDF posdilucional con la HDF predilucional y han mostrado que la HDF-OL posdilucional es más eficaz en la depuración de moléculas tanto pequeñas como medianas14,23. Esto se atribuye al hecho de que en la HDF predilucional se disminuye el transporte difusivo. Por ello, la HDF posdilucional se considera el tratamiento convectivo más eficiente y nuestro trabajo muestra por primera vez, midiendo la eliminación de múltiples moléculas, la no inferioridad de la HDF-OL mixta frente a esta, cuando el TE es idéntico con ambas técnicas.
Pedrini et al.17 han comparado la eficacia de la HDF mixta con otras formas de HDF, observando una mayor depuración de solutos con esta modalidad en comparación con la infusión predilucional y, al igual que nosotros, tampoco encontraron diferencias con infusión posdilucional, aunque su estudio solo muestra resultados de β2m. Los RR de β2m fueron inferiores a los obtenidos en nuestro estudio, 85,3 % y 85,4 % en HDF posdilucional y mixta, respectivamente, debido posiblemente a las distintas características de los dializadores y flujos utilizados.
Estudios que comparan la eficacia de la HDF-OL posdilucional con otra forma de infusión pre-posdilucional, la mid-dilución24,25, aunque realizadas con distintas membranas y superficies, encuentran que los porcentajes de reducción de moléculas pequeñas como la urea y la creatinina son ligeramente superiores en HDF-OL posdilucional, mientras que moléculas de mayor tamaño como la β2m, mioglobina, prolactina y PTR presentaron un porcentaje de reducción mayor con mid-dilución. Queremos destacar que los RR de PTR que hemos conseguido (del 39 % y del 43,2 % en HDF-OL posdilucional y mixta, respectivamente) son muy superiores a los de otros estudios (inferiores al 31 %). Este es un hallazgo de gran interés, ya que la PTR es una molécula unida a proteínas26 y estas moléculas han sido identificadas como unas de las toxinas urémicas responsables de las complicaciones crónicas de los pacientes con ERC, y caracterizadas por ser difíciles de eliminar con HDF, ya que solo se elimina la fracción libre de ellas27. Los buenos resultados obtenidos en nuestro trabajo pueden explicarse por las características de la membrana utilizada que obtiene aclaramientos elevados, gracias a su mayor superficie (2,3 m2) y los altos Qs utilizados. En la práctica clínica, para medir la eficacia de la HDF-OL se analiza la β2m, considerada representativa de las moléculas medias y que además se relaciona con algunas de las complicaciones, como la amiloidosis dialítica. El volumen de transporte convectivo se ha relacionado con la tasa de reducción de β2m28, ya que su depuración es significativamente mayor en las técnicas con alto transporte convectivo, como la HDF-OL29.
Recientemente, Sakurai30 ha sugerido la conveniencia de utilizar para evaluar la eficiencia de la HDF un biomarcador o sustancia de PM más elevado que la β2m. Basa su recomendación en que esta molécula puede ser depurada de forma eficaz mediante difusión si se utilizan dializadores de alto flujo, y por ello propone la α1 microglobulina (α1-MG), que tiene un PM de 33 000 Da y se elimina por convección, como más representativa de la HDF. Lamentablemente nosotros no hemos analizado la α1-MG, pero sí la PTR, que también tiene un PM alto (21 200 Da), obteniendo unos RR elevados.
En relación con los resultados obtenidos con los volúmenes de infusión, en nuestro estudio hemos conseguido volúmenes de infusión elevados con ambas técnicas, una cantidad muy superior a la que los distintos estudios mencionados han mostrado que disminuye la mortalidad. El volumen medio de infusión alcanzado fue de 28,3 y 44,4 litros en las HDF-OL posdilucional y mixta, respectivamente. En HDF-OL mixta se obtuvieron 24,2 litros en posdilución (4 litros menos que con la HDF-OL posdilucional) y 20,2 litros en predilución. Aunque los litros en posdilución no son equivalentes en ambas técnicas, habiendo obtenido RR similares podríamos inferir de nuestro estudio que se necesitan unos 5 litros de volumen de infusión predilucional por cada litro de menos de infusión posdilucional que se consiguen con la HDF-OL mixta respecto a la HDF-OL posdilucional, o que al menos el volumen en posdilución de la HDF-OL mixta sea un 54 % del volumen total alcanzado.
El Qs, el hematocrito y la concentración de proteínas son importantes determinantes de la cantidad de volumen de infusión en la HDF posdilucional. De forma que en la HDF posdilucional se recomienda que la tasa de infusión en relación con el Qs real no sea superior al 25-30 %, ya que proporciones más altas pueden conllevar una hemoconcentración elevada que provoque complicaciones. En pacientes con Qs limitados, como en el caso de portadores de catéter, esta tasa máxima puede comprometer la consecución de volúmenes de infusión elevados en un tiempo limitado. La HDF-OL mixta es una técnica más versátil, que puede ser utilizada en pacientes en los que la HDF-OL posdilucional no consigue alcanzar volúmenes de infusión adecuados, bien por tener hematocritos o proteínas elevadas o un acceso vascular que no permita un Qs apropiado. Esto tiene especial relevancia en el momento actual debido al progresivo aumento de la proporción de pacientes portadores de catéteres permanentes31.
El tercer resultado para distinguir en nuestro trabajo es la importancia de tener en consideración el TE o real de diálisis. El tiempo de diálisis es un parámetro fundamental que determina no solo la adecuación, sino también otros aspectos como el control del fósforo, la presión arterial y, más importante aún, la mortalidad32-34. En un estudio previo realizado sobre 2162 sesiones de diálisis que incluía tanto HD como HDF-OL, encontramos una diferencia estadísticamente significativa entre el TP y el TE (p < 0,001). Esta diferencia era proporcional al TP; en concreto, para las sesiones de 240 minutos fue de 9,7 (12,7) minutos35. Por ello, en el diseño del estudio consideramos necesario dializar a TE para poder comparar con mayor rigor ambas modalidades de HDF-OL. De hecho, el KT a TP fue superior en la HDF-OL posdilucional, resultado que no se mantuvo al dializar a TE. Esto se explica por la diferencia encontrada entre TP y TE en ambas técnicas, ya que en la HDF-OL mixta cuando se dializa a TP el TE era menor, perdiéndose 10,3 (7,4) frente a 6,5 (3,1) en mixta y posdilucional, respectivamente. Ello se debe al mayor número de interrupciones del procedimiento por autochequeos o controles realizados por el monitor de diálisis. En nuestro conocimiento, este es el primer estudio que compara la eficacia de la HDF-OL teniendo en cuenta el TE de diálisis. De no haber sido así, nuestra conclusión sería que la HDF-OL posdilucional consigue KT superiores, y sí es así cuando dializamos a TP. No podemos afirmar que el porcentaje de reducción de las sustancias analizadas también hubiera sido superior, ya que solo se realizaron sus determinaciones en las cuatro sesiones hechas en el día intermedio de la semana (sesiones 2 y 5 de ambas modalidades posdilucional y mixta), y en estas los pacientes se dializaron a TE. En cambio, sí podemos concluir que es muy importante individualizar el tiempo de diálisis no solo a la superficie corporal, existencia de FRR, TA, etc., sino también al tipo de técnica. Más aún, en la práctica clínica diaria deberíamos conocer cuál es el tiempo real que se dializan nuestros pacientes y adecuar la prescripción a él.
Por último, es importante recalcar que la mejor depuración de moléculas de mayor tamaño no debe ser en detrimento de la pérdida excesiva de sustancias útiles como la albúmina. En nuestro trabajo no hemos encontrado diferencias en las concentraciones de albúmina en las muestras del ultrafiltrado analizadas entre ambas técnicas. Aunque el coeficiente de cribado del dializador utilizado no permite un gran paso de albúmina al ultrafiltrado para poder aseverar que no existen diferencias entre ambas técnicas, deberíamos haber realizado la medición en el volumen total de ultrafiltrado. Esta es una limitación de nuestro estudio.
La principal limitación de nuestro estudio es el escaso número de pacientes incluidos, pero el hecho de tener un diseño cruzado reafirma los resultados.
En conclusión, la HDF-OL mixta a igual TE no es inferior a la HDF-OL posdilucional ni en la depuración de moléculas pequeñas y medianas ni en las unidas a proteínas. Esta modalidad de HDF-OL, al administrar el líquido de infusión pre y posdilucional de forma simultánea, obvia algunas desventajas presentes en otras formas de HDF-OL y puede utilizarse en pacientes con problemas de flujo y/o hemoconcentración.
Agradecimientos
Al personal del enfermería de la Unidad de Diálisis del Hospital Universitario Infanta Leonor por su colaboración en el estudio.
Conflictos de interés
Los autores declaran conflictos de interés potenciales.
Honorarios por ponencias: La Dra. P. de Sequera, la Dra. M. Albalate y el Dr. R. Pérez García han participado como ponentes en reuniones organizadas por Gambro® y Fresenius®.
Tabla 1. Principales estudios que analizan el efecto de la hemodiafiltración en línea sobre la mortalidad de los pacientes en diálisis
Tabla 2. Características de la hemodiálisis
Tabla 3. Valores prediálisis y posdiálisis de las sustancias analizadas en ambas técnicas
Tabla 4. Volúmenes en ambas técnicas
Tabla 5. KT a tiempo programado y efectivo en función de la técnica
Tabla 6. Diferencias en función de la técnica
Figura 1. Diseño del estudio.
Figura 2. Porcentajes de reducción de las sustancias analizadas en hemodiafiltración en línea posdilucional y mixta.