ÍNDICE
¿ Presentación del estudio
¿ Objetivos
¿ Metodología
¿ Resultados
¿ Conclusiones
¿ Anexos
PRESENTACIÓN DEL ESTUDIO
Se ha pretendido conocer el estado de opinión del colectivo de nefrólogos con actividad en el trasplante renal, intentando dar respuesta a una serie de cuestiones diagnósticas y terapéuticas que carecen de un importante nivel de evidencia.
Las encuestas y el análisis estadístico de los datos han sido realizados por Prex con el patrocinio de Novartis.
El aval científico de los contenidos corresponde al Grupo FITI (Foro de Individualización de Terapia Inmunosupresora):
Comité Científico:
Dr. Manuel Arias
Dr. Josep M.ª Campistol
Dr. Josep M.ª Grinyó
Dr. Domingo Hernández
Dr. José M.ª Morales
Dr. Federico Oppenheimer
Dr. Daniel Serón
OBJETIVOS
El objetivo general de este estudio de ámbito nacional ha sido conocer el estado de opinión del colectivo de nefrólogos españoles acerca de cuestiones diagnósticas y terapéuticas relacionadas con el trasplante renal sin un nivel de evidencia adecuado en aras de optimizar los resultados a través de la individualización de la inmunosupresión.
Objetivos generales
Conocer la práctica clínica referente a la individualización de la inmunosupresión en el campo del trasplante renal.
Describir el estado de opinión acerca de los factores de riesgo en los pacientes trasplantados y su repercusión en la evolución del trasplante renal.
Precisar la metodología diagnóstica y terapéutica empleada y conocer la actitud de los especialistas ante situaciones clínicas determinadas.
Detectar el grado de utilización de medidas preventivas.
Definir estrategias para nuevas líneas de investigación.
Se han estructurado las preguntas siguiendo criterios de aspectos generales, asistenciales, diagnósticos y terapéuticos.
En resumen, se trata de un corte transversal en el proceso clínico del trasplante renal mediante la colaboración de un amplio colectivo de nefrólogos especialistas en trasplante con aportación de su experiencia y opiniones en los temas planteados. Es importante resaltar el carácter voluntario de la participación y aportación en las encuestas de recogida de datos.
METODOLOGÍA
Tipo de estudio
Se trata de un estudio observacional de ámbito nacional, prospectivo, transversal, descriptivo y analítico.
Criterios de selección
Se seleccionó a priori una población de 314 nefrólogos con actividad profesional en el campo del trasplante renal o su seguimiento. Es importante destacar que, no habiéndose realizado muestreo, las respuestas son voluntarias y que, por tanto, la muestra de la primera y segunda oleada no es superponible. Habiendo sido estrictamente anónimas y confidenciales las encuestas, no se puede conocer el porcentaje de repetición de participantes.
Muestra
Los especialistas participantes han sido, en la primera oleada, 79, y en la segunda, 61.
Recogida de información
La ejecución logística se ha realizado mediante dos oleadas de encuestas que se han planteado durante 2006; la primera oleada de preguntas, en el primer trimestre, y la segunda, en el último. La explotación estadística se ha realizado al finalizar cada uno de los dos procesos de toma de datos. A cada uno de los nefrólogos, en cada una de las oleadas se le hizo llegar una carta de presentación del estudio, un cuestionario en papel y la dirección URL de la página web con el mismo cuestionario en formato electrónico, pudiendo elegir la vía de respuesta en cualquiera de los dos formatos.
Las preguntas fueron formuladas y preparadas por el Comité Científico.
Los cuestionarios (Anexo 1 y Anexo 2) contenían 29 y 36 preguntas respectivamente, algunas relacionadas con el ejercicio profesional del especialista y la mayoría relativas a su opinión o a su práctica clínica acerca de aspectos diagnósticos y terapéuticos. Dado que en la primera oleada las respuestas tendían a ser académicas, se insistió en la segunda oleada en que la orientación fuese eminentemente práctica.
Las respuestas se recogían en forma de variables cuantitativas, cualitativas, de respuesta múltiple o en forma de ordinales según la preferencia del especialista.
Análisis de datos
El análisis estadístico ha sido diseñado para poder cruzar los resultados más allá de la descripción de respuestas, a través de técnicas estadísticas de comparación y relación univariantes y bivariantes. El análisis de datos se ha enriquecido con el cruce a posteriori de todas las variables de las encuestas clasificadas según la actitud terapéutica individualizadora del especialista.
Estratificación
Se realizó una estratificación a posteriori de la muestra que permitiese establecer una variable de comparación de resultados entre subgrupos muestrales. De acuerdo con los objetivos del sondeo, fue la actitud terapéutica individualizadora la variable elegida. Siendo muestras diferentes y no superponibles las de las dos oleadas, hay que tener en cuenta, en primer lugar, que el tamaño muestral de la primera oleada es superior, por lo que en las comparaciones realizadas se han encontrado algunos resultados significativos, mientras que en la segunda no se han encontrado diferencias significativas; y en segundo lugar, parece que el perfil individualizador/no individualizador ha estado más equilibrado en cuanto a número de respondedores en la primera oleada, mientras que en la segunda eran más frecuentes los individualizadores, lo que supone también un sesgo diferente entre ambas oleadas.
Explotación
Los datos, una vez recogidos y procesados, se han analizado mediante técnicas estadísticas automatizadas, utilizando SPSS 12.0. Se han elaborado informes preliminares con todos los resultados descriptivos de variables cualitativas, cuantitativas y ordinales, así como resultados analíticos comparativos y de relación a través de cruces de variables.
Las pruebas estadísticas utilizadas han sido:
- Descriptiva de frecuencias.
- Índices cuantitativos y de posición.
- Gráficos estadísticos.
- Test de normalidad (Kolmogorov-Smirnof).
- Test de asociación de caracteres (Chi cuadrado).
- Comparación de medias independientes (t de Student para muestras independientes).
- Comparación de medias no paramétrica (U de Mann-Whitney)
Comunicación
En la fase de comunicación de la información se pretende proporcionar a los especialistas cuantos resultados y conclusiones, provisionales y definitivos pueda aportar este estudio para un mayor conocimiento de la evidencia científica y su grado de aplicación en la práctica clínica. Estos objetivos podrán ampliarse en sucesivos estudios o aplicarse en forma de procesos informativos o formativos.
RESULTADOS
Descripción de la muestra de especialistas que han respondido a las encuestas
Descripción geográfica por ciudades de la muestra
Para la población seleccionada de 314 nefrólogos, el número de respuestas fue de 79 (25,2%) en la primera encuesta y de 61 (19,4%) en la segunda.
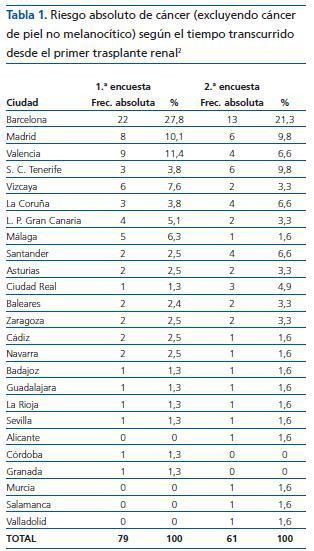
En la tabla 1 se muestra la distribución de respuestas obtenidas, clasificadas por ciudades, en cada una de las dos encuestas. La ciudad con mayor tasa de respuestas en ambas es Barcelona, con un 27,8 y un 21,3% de los totales, seguida por Madrid (10,1 y 9,8%) y Valencia (11,4 y 6,6%).
¿ ¿Se hace trasplante renal en tu hospital?
La mayoría de los encuestados trabaja en centros donde se realizan trasplantes (86,1 y 90,2% en la primera y segunda encuesta, respectivamente), mientras que en el resto (13,9 y 9,8%) únicamente se realiza el seguimiento de los pacientes trasplantados.
¿ ¿En cuál de estas áreas dedicas principalmente tu labor asistencial de pacientes trasplantados renales?
Los resultados de las dos encuestas muestran que los nefrólogos ven pacientes preferentemente en consultas externas (40,5 y 42,6%) o simultaneándolos con la planta (40,5 y 36,1%), mientras que tan sólo un 19 y un 21,3% trabajan únicamente en planta.
¿ Número de trasplantes que se realizan anualmente en tu hospital
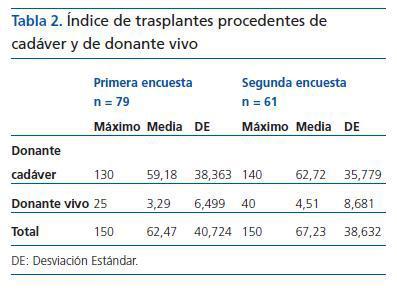
En la tabla 2 se muestran los índices del número de injertos procedentes de cadáver y de donante vivo y la suma de ambos (total) obtenidos en las dos encuestas.
¿ ¿Cuáles crees que son las áreas más importantes que deberíamos analizar en el campo del trasplante renal? Por favor, ordena de mayor a menor importancia (1-6) según tu criterio:
El orden de preferencia y la puntuación media obtenida por cada concepto ha sido:(ver tabla 20)
El área que ha quedado en primer lugar, la nefropatía crónica del injerto, ha obtenido la puntuación máxima (6) en el 51,9% de los casos y la segunda puntuación (5) en el 20,3%, representando ambas opciones en conjunto un 72,2% del total.
Caracterización de los especialistas en función de su carácter individualizador de la terapia inmunosupresora
¿ ¿Crees que está justificada actualmente la individualización de la inmunosupresión en el campo del trasplante renal?
En la primera oleada se reparten las respuestas de forma equilibrada entre la opción «Sí, en todos los casos» (53,2%) y la condicionada a la evolución clínica o a las características del donante/receptor (45,6%). Las respuestas «No, en ningún caso» y «Sólo en casos excepcionales» representaron el 0 y el 1,3%, respectivamente. En la segunda oleada el carácter individualizador se manifiesta en cifras en torno al 80% de los encuestados.
¿ Carácter individualizador
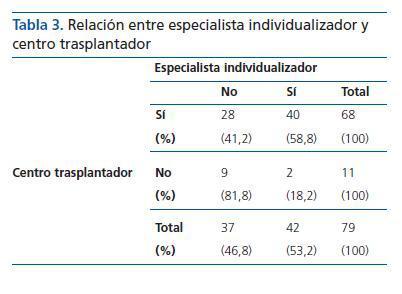
Con el fin de relacionar la tendencia terapéutica hacia la individualización del tratamiento inmunosupresor, se cruzó esta característica con el carácter trasplantador del centro, encontrándose una relación significativa (p <0,05) tan sólo en la primera encuesta.
Los nefrólogos que afirman utilizar la individualización trabajan principalmente en centros trasplantadores (58,8%), mientras que los que no la utilizan trabajan preferentemente en centros no trasplantadores (81,8%) (tabla 3).
En la segunda encuesta, sin embargo, no se ha encontrado relación significativa.
Tampoco se encuentra relación entre el carácter individualizador y el número de trasplantes que se realizan en el centro.
¿ ¿Aproximadamente en qué porcentaje de pacientes estás realmente individualizando la inmunosupresión en trasplante renal de novo?
El porcentaje de casos en que los nefrólogos afirman individualizar en trasplantes de novo se distribuye equitativamente en tercios aproximados: el 32,9% individualiza menos del 25%, el 30,4% lo hace entre un 25 y un 50%, y el 32,9% por encima del 50%.
Al cruzar la información teórica con la práctica se detecta una asociación significativa p <0,05 (p = 0,03), interpretándose como coherencia interna de la encuesta y del proceso terapéutico la opinión favorable a la terapia individualizadora y el porcentaje de pacientes tratados consecuentemente. Los individualizadores reconocen individualizar mayoritariamente a más de la mitad de sus pacientes, mientras que los que se identifican como individualizadores condicionales, lo hacen con menos de la mitad de sus pacientes.
¿ ¿En qué fase del trasplante crees que debería individualizarse la inmunosupresión?
La mayoría de los especialistas (68,4%) refiere adoptar la individualización de la inmunosupresión de forma secuencial a lo largo del trasplante. El 19% dice hacerlo en los primeros 6-12 meses, con cambios significativos a partir de entonces (p. ej. retirar esteroides, retirar anticalcineurínico, etc.). Un 8,9% sólo ante cambios significativos de la función renal, perfil de riesgo vascular del receptor y/o disfunciones inmunológicas. Y el 3,8% lo haría en el postrasplante inmediato, manteniendo la misma inmunosupresión del principio y haciendo solamente ajustes de dosis a lo largo del tiempo (p. ej. reducir inhibidor de anticalcineurina, reducir esteroides, etc.).
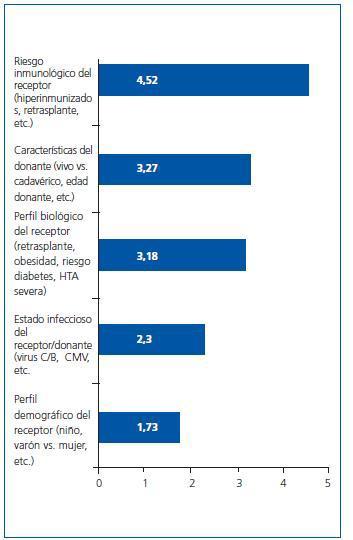
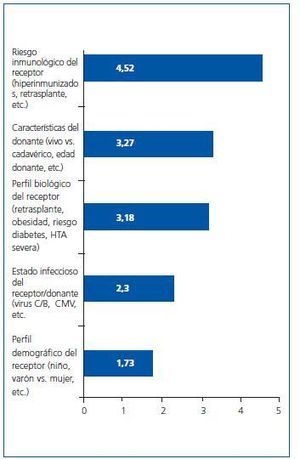
¿ ¿Qué criterios o grupos de riesgo crees que deben acogerse a la individualización de la inmunosupresión? Por favor, ordena de mayor a menor importancia (1-5) según tu criterio:
El orden de preferencia y la puntuación media obtenida por cada concepto ha sido (figura 1):
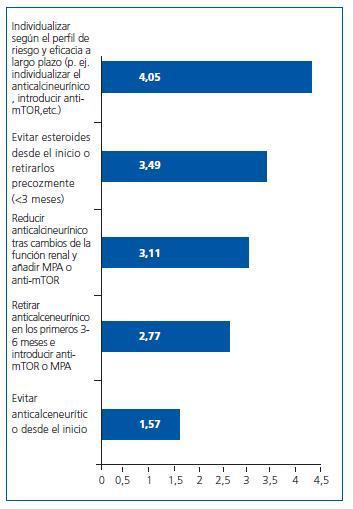
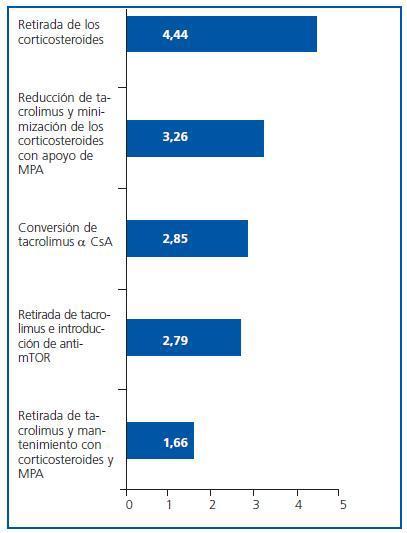
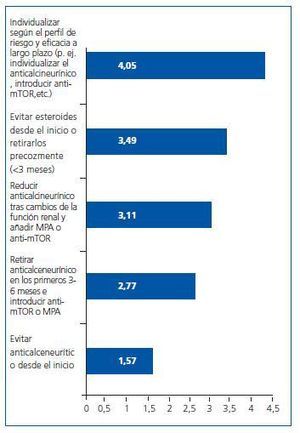
¿ Globalmente, ¿qué estrategia terapéutica crees que es más importante a la hora de individualizar la inmunosupresión en pacientes sin riesgo inmunológico? Por favor, ordena de mayor a menor importancia (1-5) según tu criterio:
Igualmente, se presenta el listado de criterios por orden de importancia y la puntuación media obtenida por cada uno de ellos (figura 2).
La estrategia preferida en primer lugar fue elegida como primera opción por el 49,4% de los especialistas.
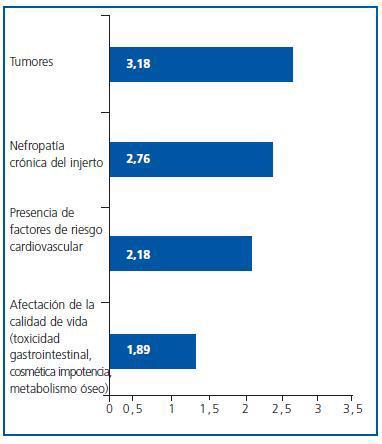
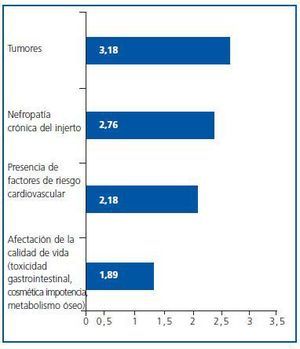
¿ ¿En cuál de estas situaciones te plantearías la individualización de la inmunosupresión en un paciente en fase de mantenimiento? Por favor, ordena de mayor a menor importancia (1-4) según tu criterio:
Los tumores han mostrado ser el principal factor para plantearse la individualización de la inmunosupresión en la fase de mantenimiento de los pacientes, opción elegida como más importante por el 55,7% de los encuestados.
¿ Si tienes que realizar un cambio en la inmunosupresión con el propósito de individualizar, ¿cómo crees que debes monitorizar esta actitud?
Más de la mitad (54,4%) de los encuestados (n = 79) respondió que realizarían una biopsia antes de hacer un cambio en la inmunosupresión con el propósito de individualizar. El 31,6% monitorizaría solamente con parámetros clínicos y analíticos; el 13,9% realizaría una biopsia antes del cambio y otra después de cierto tiempo para comprobar el efecto del tratamiento; y ninguno de los encuestados respondió que mediría el filtrado glomerular con un método isotópico.
¿ ¿La biopsia de protocolo te ayudaría a individualizar la inmunosupresión?
El 46,8% de los nefrólogos participantes (79) opina que la biopsia de protocolo sólo ayuda para individualizar y realizar cambios de la inmunosupresión. Un 32,9% cree que siempre debería llevarse a cabo como práctica clínica de rutina y un 19% considera que sólo se debería biopsiar ante cambios confirmados de la función renal. Tan sólo el 1,3% de los participantes opina que no tiene utilidad.
¿ ¿Individualizas la inmunosupresión teniendo en cuenta el riesgo cardiovascular pretrasplante (cardiópatas, hipertensión grave, hiperlipidemia, síndrome metabólico, etc.)?
La mayoría de los nefrólogos (78,7%, n = 61) individualiza en la práctica clínica tomando en consideración los factores de riesgo cardiovascular pretrasplante.
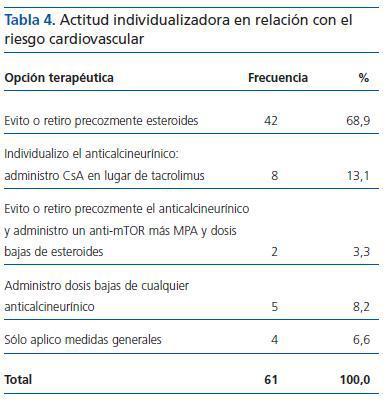
¿ En caso de individualizar la inmunosupresión teniendo en cuenta el riesgo cardiovascular, ¿qué actitud tomas en pacientes con síndrome metabólico pretrasplante y riesgo de desarrollar diabetes postrasplante?
La mayoría de los encuestados (68,9%) optó por evitar o retirar precozmente los esteroides (tabla 4).
Es significativa la asociación con el carácter individualizador con una probabilidad de error p <0,05 (p = 0,033), prefiriendo los individualizadores las respuestas 1 y 2, mientras que los no individualizadores prefieren la 3, 4 y 5.
Aspectos clínicos, diagnósticos y terapéuticos
¿ ¿Crees que debería individualizarse la inmunosupresión en los pacientes con virus C sin riesgo inmunológico?
La mayoría de los nefrólogos (65%, n = 79) cree que sí.
Existe asociación significativa p <0,05 entre la opinión contestada y el carácter individualizador de los especialistas, eligiendo mayoritariamente los individualizadores la respuesta afirmativa, mientras que los no individualizadores prefieren la negativa.
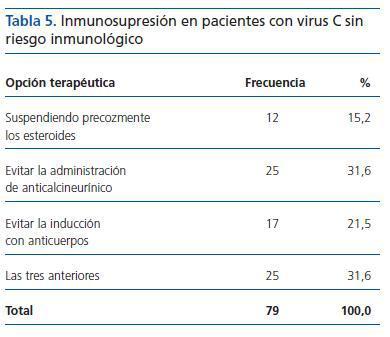
¿ En caso de haber contestado afirmativamente la pregunta anterior, ¿cuál crees que debería ser la inmunosupresión a utilizar en pacientes con virus C sin riesgo inmunológico?
Se ha encontrado una tasa de respuestas equilibrada entre varias opciones, ya que estando la opción «Evitar la administración de anticalcineurínico», con un 31,6% de respuestas favorables, empatada con la última alternativa, también con un 31,6%, ésta contempla las otras tres, por lo que aparece una cierta yuxtaposición de opciones. A su vez, las otras dos alternativas de suspensión precoz de esteroides y evitar la inducción con anticuerpos también están valoradas independientemente, con un 15,2 y un 21,5%, respectivamente (tabla 5).
¿ ¿Crees que está justificada la inducción con anticuerpos anti-CD25 en pacientes sin riesgo inmunológico?
Más de la mitad (51,9%) de los encuestados (79) refiere que la inducción con anticuerpos en pacientes sin riesgo inmunológico sólo está justificada en pacientes que reciben órganos de donantes de edad avanzada para retrasar o minimizar el uso de los anticalcineurínicos, y un 15,2% piensa que estaría justificada sólo en circunstancias especiales como retrasplantes o cuando se evitan los esteroides. Por el contrario, un 22,8% cree que está justificada siempre, para tratar de disminuir las cifras de rechazo agudo postrasplante y disminuir dosis de anticalcineurínicos, y un 10,1% no lo considera justificado.
Existe asociación significativa (p <0,05) entre las respuestas y el carácter individualizador de los especialistas, de forma que los individualizadores apoyan preferentemente el uso de anticuerpos anti-CD25 en pacientes que reciben órganos de donantes de edad avanzada para retrasar o minimizar el uso de los anticalcineurínicos, mientras que los no individualizadores se decantan por su uso en circunstancias especiales (como retrasplantes o cuando se evitan los esteroides), o bien creen que no está justificado. La opción cuarta, que justifica siempre el uso de anti-CD25 se valoró de igual manera en ambos subgrupos.
¿ ¿Crees que está justificada la inducción con anticuerpos policlonales?
La mitad de las respuestas (51,9%) se orientó hacia pacientes de riesgo inmunológico y en los que se precise retrasar la administración de anticalcineurínicos. El 41,8% contestó afirmativamente sólo en pacientes con riesgo inmunológico. Un 6,3% apoyó su uso para retrasar o minimizar el uso de anticalcineurínicos en situaciones especiales, como donantes añosos. Ningún encuestado se decantó por su uso siempre en pacientes con y sin riesgo inmunológico para disminuir las tasas de rechazo agudo.
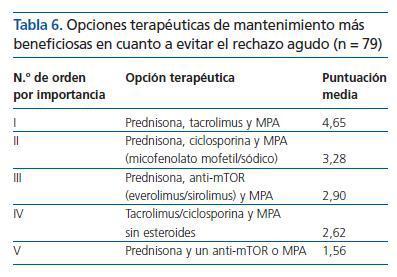
¿ En pacientes sin riesgo inmunológico, ¿qué inmunosupresión de mantenimiento crees que aporta más beneficios en cuanto a evitar el rechazo agudo? Por favor, ordena de mayor a menor importancia (1-5) según tu criterio:
En la tabla 6 se presenta el listado de opciones terapéuticas por orden de importancia, mostrando la puntuación media obtenida por cada una de ellas:
La opción que ha conseguido mayor puntuación ha sido la combinación de prednisona, tacrolimus y MPA, que ha sido votada en primer lugar por el 77,2% de los participantes.
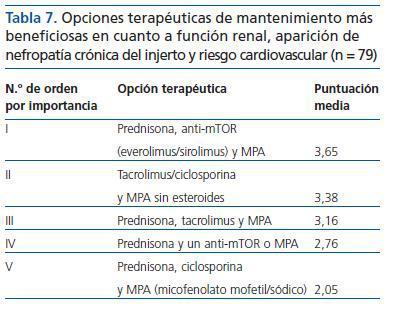
¿ En pacientes sin riesgo inmunológico, ¿qué inmunosupresión de mantenimiento crees que aporta más beneficios en cuanto a función renal, aparición de nefropatía crónica del injerto y riesgo cardiovascular? Por favor, ordena de mayor a menor importancia (1-5) según tu criterio:
La tabla 7 muestra el listado de opciones terapéuticas por orden de importancia y la puntuación media obtenida por cada una de ellas:
La opción con más puntuación es la triple terapia combinada de prednisona, anti-mTOR (everolimus/sirolimus) y MPA; ha sido elegida en primer lugar por un 34,2% de los encuestados y en segundo lugar por un 26,6%, lo que entre ambos suma un 60,8%.
¿ ¿Con qué criterios defines la nefropatía crónica del injerto?
Más de la mitad (53,2%) opta por los criterios histológicos (clasificación de Banff), mientras que un 35,4% prefiere el criterio funcional del deterioro de la función renal con o sin proteinuria. Los criterios histológicos incluyendo la tinción con C4d y/o determinación de anticuerpos donante-específicos han sido elegidos por el 10,1%, y tan sólo un 1,3% ha optado por la función renal con creatinina elevada aunque no exista evidencia de deterioro progresivo de la función renal.
¿ ¿Crees que es necesaria la biopsia renal después de tratar un rechazo agudo?
La mayoría de los encuestados (68,4%) responde que sólo cuando no se recupera ad integrum la función renal. Un 17,7% opta por la biopsia incondicional en todos los casos (para identificar lesiones histológicas subsidiarias de un cambio en la inmunosupresión), y el 13,9% sólo ante la aparición o persistencia de proteinuria. Ningún encuestado opina que no debe hacerse nunca.
¿ ¿Determinas la proteinuria en cada revisión ambulatoria de los pacientes con trasplante renal?
La mayoría (84,8%) contestó que lo hace siempre. La revisión periódica cada dos o tres meses fue elegida por el 15,2%, y el resto de opciones (nunca, sólo ante la sospecha de nefropatía crónica del injerto y sólo ante cambios de la función renal o sospecha de rechazo agudo) fueron rechazadas.
¿ Ante un enfermo con proteinuria leve ( 0,5 g/día), ¿qué actitud terapéutica tomarías? (sólo una respuesta válida)
La opción terapéutica mayoritaria fue la administración de IECA/ARA, con un 59,5%. El 19% eligió sólo vigilancia y monitorización periódica. Un control más estricto de los lípidos, tensión arterial y glucemia fue la opción del 13,9%, y la biopsia en todos los casos la del 7,6%. Ningún participante apoyó la intensificación de la inmunosupresión.
Se detecta una relación significativa (p <0,05) entre las respuestas y el carácter individualizador del especialista. Los perfiles individualizadores eligieron mayoritariamente la administración de IECA/ARA y la biopsia en todos los casos, mientras que los no individualizadores prefirieron las otras dos opciones.
¿ En un paciente añoso (>60 años) con hipertensión arterial pretrasplante y lesión en órganos diana y/o calcificaciones vasculares, ¿qué actitud tomas?
Se observaron proporciones similares (n = 61) entre la reducción de dosis de anticalcineurínico más anti-mTOR o micofenolato (27,9%) y la evitación o retirada precoz de esteroides (26,2%). La adopción de medidas generales y tratamiento específico de la HTAtambién fue considerada por un 21,3% de los especialistas.
Las opciones «Evito la CsA y en su lugar doy tacrolimus + MPA» y «No administro anticalcineurínicos o los retiro precozmente. En su lugar, doy un anti-mTOR más MPA y dosis bajas de esteroides » fueron elegidas por 13,1 y el 11,5%, respectivamente.
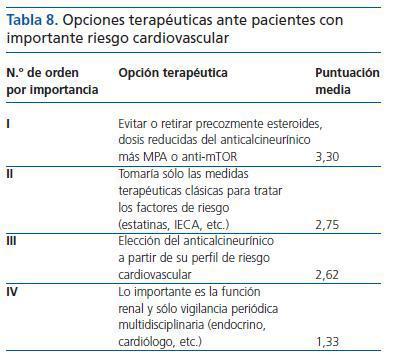
¿ Ante un enfermo con importante riesgo cardiovascular pretrasplante (cardiópatas, hipertensos graves, hiperlipidemia, diabéticos, síndrome metabólico, etc.), ¿qué actitud terapéutica tomarías? Por favor, ordena de mayor a menor importancia (1-4) según tu criterio:
Las respuestas (n = 79) mostraron el siguiente orden de preferencia (tabla 8).
La opción más puntuada fue también la más valorada, considerada la primera preferencia en un 54,4%.
Se han detectado diferencias significativas p <0,05 en cuanto a la elección del anticalcineurínico a partir de su perfil de riesgo cardiovascular entre los subgrupos de individualización vs. no individualización, de forma que los rangos de puntuación fueron significativamente superiores en el primer grupo.
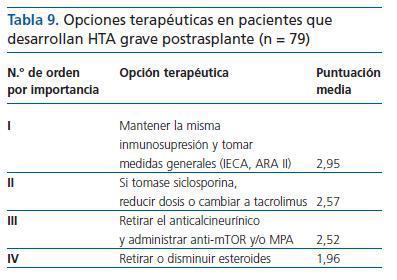
¿ Ante un enfermo que desarrolla HTA grave postrasplante, cuyo origen no es una causa corregible como las estenosis vascular, ¿qué harías? Por favor, ordena de mayor a menor importancia (1-4) según tu criterio (tabla 9):
Se obtuvieron puntuaciones equilibradas, favorables al mantenimiento de la inmunosupresión y adopción de medidas generales, opción elegida en primer lugar por el 50,6% de los participantes.
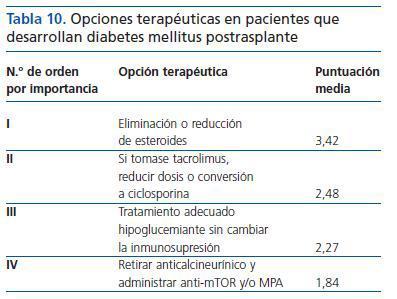
¿ Ante un enfermo que desarrolla diabetes mellitus postrasplante, ¿qué actitud terapéutica tomarías? Por favor, ordena de mayor a menor importancia (1-4) según tu criterio:
La eliminación o reducción de esteroides fue elegida mayoritariamente, por un 59,5% de los participantes (n = 79), como primera opción (tabla 10).
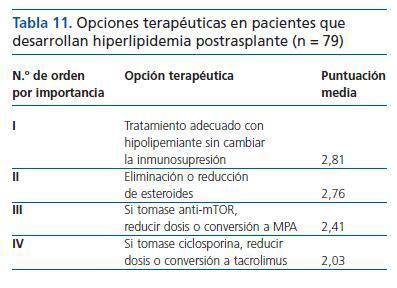
¿ Ante un enfermo que desarrolla hiperlipidemia importante postrasplante, ¿qué actitud terapéutica tomarías?
Se han obtenido puntuaciones equilibradas, aunque ligeramente superiores en la opción «Tratamiento adecuado con hipolipemiante sin cambiar la inmunosupresión», que fue elegida en primer lugar por el 45,6% de los participantes (tabla 11).
Se detectaron diferencias significativas p = 0,001 en la opción «Si tomase ciclosporina, reducir dosis o conversión a tacrolimus», más puntuada en el grupo de individualizadores que en el de no individualizadores.
¿ En un paciente joven (<45 años) con hipertensión grave pretrasplante renal, ¿qué actitud tomas?
Prácticamente la mitad (45,9%) de los encuestados (n = 61) evita CsA y, en su lugar, da tacrolimus más micofenolato. El 19,7% sólo adopta medidas generales. Un 16,4% da dosis reducidas de cualquier anticalcineurínico más MPA, el 11,5% evita esteroides o hace una reducción rápida, y sólo un 6,6% hace una inmunosupresión con dosis bajas de esteroides, un antimTOR y MPA.
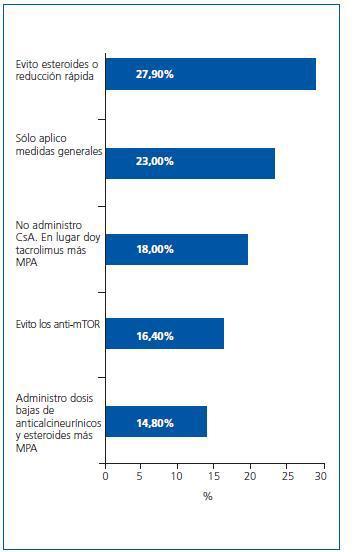
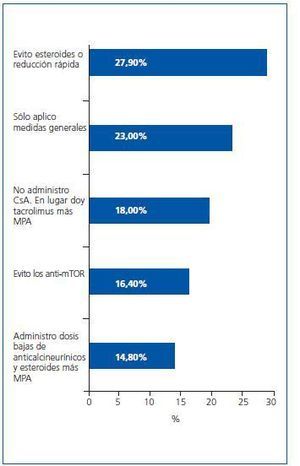
¿ Ante un enfermo con hiperlipemia pretrasplante, ¿qué actitud tomas?
Los nefrólogos distribuyen sus opciones terapéuticas de forma equilibrada entre todas las presentadas, con un ligero predominio de la evitación o reducción rápida de esteroides (figura 4).
¿ ¿Individualizas o modificas la inmunosupresión en pacientes que desarrollan complicaciones cardiovasculares o metabólicas postrasplante?
El desarrollo de complicaciones cardiovasculares o metabólicas postrasplante es motivo de individualización o modificación de la inmunosupresión en un 88,5% de los especialistas (n = 61).
Se han encontrado diferencias significativas p <0,001 en la asociación del carácter individualizado del especialista y su respuesta a esta pregunta, contestando mayoritariamente de forma afirmativa los individualizadores (87,0%) y de forma negativa los no individualizadores (85,7%).
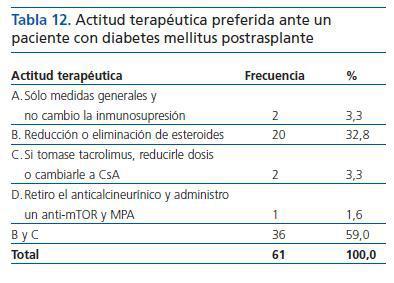
¿ Ante un enfermo que desarrolla diabetes mellitus postrasplante, ¿qué actitud tomas?
La combinación de las respuestas B y C es la elección preferida por un 59,0% de los encuestados, siendo la opción de reducción o eliminación de esteroides la única opción individual relevante (32,8%) (tabla 12).
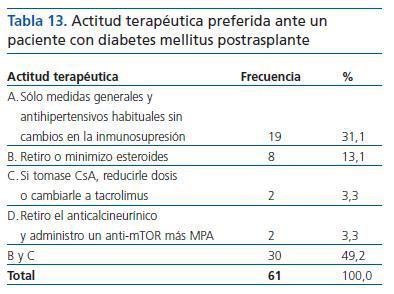
¿ Si individualizas la inmunosupresión en pacientes con complicaciones metabólicas o vasculares postrasplante, ¿qué actitud tomas inicialmente en un enfermo que desarrolla hipertensión arterial grave no condicionada por una estenosis de la arteria del injerto renal?
Como es habitual en respuestas combinadas, la opción elegida por prácticamente la mitad de los encuestados (49,2%) es la suma de B y C. La segunda opción considerada (31,1%) es la adopción de medidas generales y antihipertensivos habituales, sin cambios en la inmunosupresión (tabla 13).
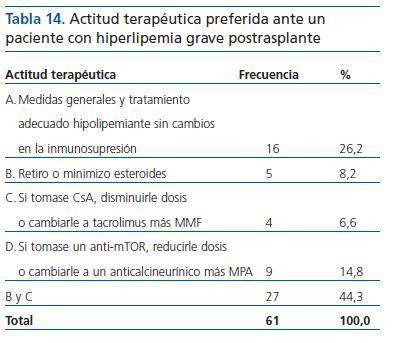
¿ En un enfermo que desarrolla hiperlipemia grave postrasplante, ¿qué actitud tomas?
Vuelve a ser mayoritaria (44,3%) una combinación de opciones, la B y C. La alternativa de opción individual (26,2%) es la adopción de medidas generales y tratamiento hipolipemiante, sin cambios en la inmunosupresión (tabla 14).
¿ En un enfermo que sufre un infarto agudo de miocardio postrasplante renal, ¿qué actitud tomas en la práctica clínica?
De forma casi equiparable, un 31,1% adoptaría medidas generales posinfarto sin cambios en la inmunosupresión (opción A); un 27,9% minimizaría o retiraría los esteroides (opción B); y un 29,5% optaría por la respuesta combinada B y C, que incluye la minimización o retirada de los esteroides y, en caso de que el paciente tomase CsA, cambiarle a tacrolimus más MMF por su mejor perfil cardiovascular. Tan sólo el 9,8% optaría por retirar el anticalcineurínico y administrar un antimTOR más MPA.
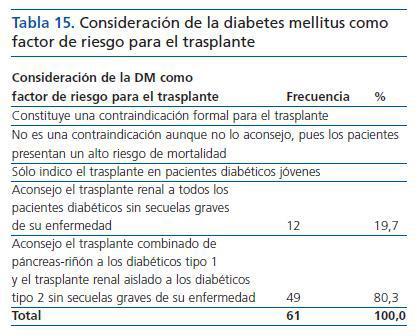
¿ ¿Qué importancia te merece la diabetes mellitus como factor de riesgo para la indicación del trasplante?
Las tres primeras opciones no han sido elegidas en ningún caso, siendo la mayoritaria (80,3%) la última alternativa, de trasplante combinado (tabla 15).
¿ ¿Individualizas la inmunosupresión teniendo en cuenta los antecedentes de diabetes mellitus?
La mayoría (80,3%) de los nefrólogos (n = 61) tiene en cuenta los antecedentes de diabetes de cara a la individualización.
Se encuentra relación significativa p <0,001 entre el carácter individualizador y las respuestas a esta pregunta, respondiendo «sí» mayoritariamente los individualizadores (97,9%) y respondiendo «no» los no individualizadores (84,6%).
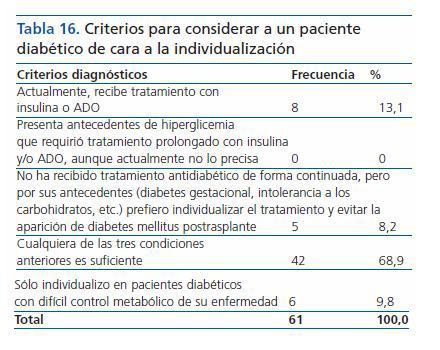
¿ Si así fuera, en los pacientes que acuden a trasplantarse, ¿cuál es tu criterio para considerar a un paciente como diabético a los efectos de individualizar el tratamiento?
La opción de cualquiera de las tres primeras es la preferida (68,9%) (tabla 16).
Se encuentra relación significativa p <0,05 entre las respuestas y el carácter individualizador: los especialistas no individualizadores escogieron preferentemente las opciones 1 y 5, mientras que los individualizadores prefirieron las opciones 3 y 4.
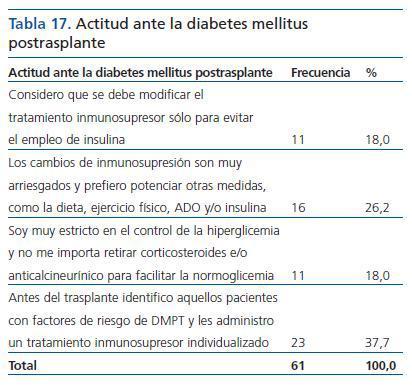
¿ ¿Cuál de estas afirmaciones refleja mejor tu actitud ante la DMPT?
Hay reparto de opiniones, siendo la preferida la administración de un tratamiento inmunosupresor individualizado (tabla 17).
Se encuentra asociación significativa p <0,01 (p = 0,008) con el carácter individualizador respondiendo preferentemente los no individualizadores la opción 2 y los individualizadores las opciones 1, 3 y 4.
¿ ¿Cuál de estos fármacos te parece que es más diabetogénico en pacientes trasplantados?
Sólo han obtenido respuestas positivas los corticosteroides (55,7%) y el tacrolimus (44,3%). El ácido micofenólico, la ciclosporina y los inhibidores de mTOR (sirolimus/everolimus) no fueron elegidos por ningún encuestado.
¿ En los pacientes con diabetes mellitus en el momento del trasplante, ¿cuál es tu actitud respecto a una posible individualización del tratamiento inmunosupresor?
La mayoría (70,5%) afirmó dar corticosteroides, pero retirándolos de forma precoz. El 14,8% respondió que sus pacientes diabéticos reciben el mismo tratamiento inmunosupresor que el resto de pacientes. Un 6,6% evita los corticosteroides, el 4,9% da ciclosporina sólo en pacientes mayores y tacrolimus en los diabéticos jóvenes, y el 3,3% da ciclosporina pero no tacrolimus.
¿ Señala cuál es para ti el régimen inmunosupresor ideal en fase de mantenimiento para el paciente con antecedentes de diabetes mellitus
Sólo un 3,3% seleccionó la opción de AMF en monoterapia. El resto se repartió entre las tres opciones que incluían AMF sin corticosteroides: el 37,7% asociado a anti-mTOR, un 31,1% a tacrolimus, y el 27,9% a ciclosporina. Ningún participante eligió la opción de anti-mTOR en monoterapia.
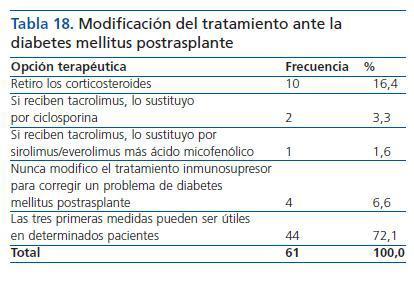
¿ En los pacientes sin antecedentes de diabetes mellitus pero que desarrollan diabetes mellitus postrasplante, ¿cuál es tu actitud respecto a una posible codificación del tratamiento inmunosupresor que mejore el control metabólico?
Un 6,6% nunca modifica el tratamiento inmunosupresor para corregir un problema de diabetes mellitus postrasplante. El 72,1% consideró que cualquiera de las demás medidas podría ser útil (tabla 18).
Se encontró asociación significativa p = 0,001 con el carácter individualizador. Los especialistas no individualizadores respondieron preferentemente las opciones 1 y 4 y los individualizadores las opciones 2, 3 y 5.
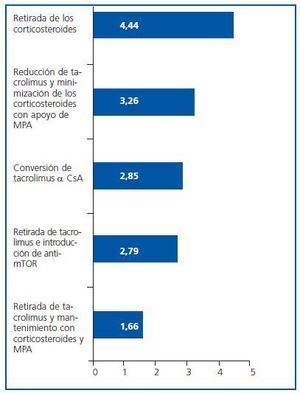
¿ Señala en qué orden (1-5) según tus preferencias adoptas las posibles medidas encaminadas a corregir la diabetes mellitus postrasplante en pacientes que reciben terapia triple tacrolimus-ácido micofenólicocorticosteroides:
La opción más valorada fue la retirada de corticosteroides, elegida en primer lugar por el 67,2% de los participantes (n = 61) (figura 5).
Se han encontrado diferencias significativas en las respuestas 3 y 5, otorgando una mayor puntuación con p <0,05 en la 3 los individualizadores, mientras que en la 5 son los no individualizadores los que puntúan más alto, con p = 0,010.
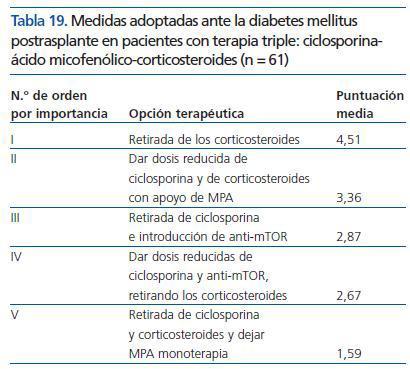
¿ Señala en qué orden (1-5) según tus preferencias adoptas las posibles medidas encaminadas a corregir la diabetes mellitus postrasplante en pacientes que reciben terapia triple ciclosporina-ácido micofenólico-corticosteroides
La opción más valorada fue la retirada de los corticosteroides, elegida como primera opción por el 72,1% de los participantes (tabla 19).
Se han encontrado diferencias significativas en las puntuaciones de las respuestas I y II, con p <0,05 en ambas, siendo en la I mayores las de los individualizadores y en la II las de los no individualizadores. En las respuestas IV y V se encuentran diferencias casi significativas (p <0,1).
¿ Para tu práctica diaria en trasplante renal, ¿cómo valoras la importancia del cáncer en tus pacientes?
El 59% de los nefrólogos considera el cáncer como un problema muy importante para sus pacientes. El 34,4% lo considera importante y el 6,6% poco importante. Ningún participante contestó que no le preocupa el tema del cáncer.
Se encuentran diferencias significativas con p <0,05 (p = 0,023) en las respuestas en individualizadores, que han respondido preferentemente «Muy importante» o «Importante», mientras que los no individualizadores han respondido mayoritariamente «Poco importante».
¿ ¿Consideras que el tratamiento inmunosupresor participa de manera directa en el desarrollo de cáncer en los pacientes trasplantados renales?
La respuesta ha sido «Sí» de forma unánime (100%).
¿ De los siguientes fármacos inmunosupresores, ¿cuál consideras que tiene un impacto más negativo en el desarrollo de cáncer?
Los fármacos peor conceptuados por tener un impacto más negativo en el desarrollo del cáncer son los inhibidores de la calcineurina (85,2%). Azatioprina fue elegida por el 11,5%, y MMF por el 3,3%. Ningún participante seleccionó los esteroides ni los inhibidores de mTOR.
¿ ¿Cuál de los siguientes procesos neoplásicos observas con mayor frecuencia en tu consulta diaria?
De entre las opciones que se ofrecían:
- Cáncer de piel.
- Sarcoma de Kaposi.
- Cáncer de pulmón.
- Cáncer de colon.
Sólo se ha respondido el cáncer de piel (100%).
¿ Respecto al papel etiopatogénico del tratamiento inmunosupresor en el desarrollo de cáncer, ¿cuál de los siguientes factores consideras de mayor importancia?
De las distintas opciones ofrecidas:
- Tipo de inmunosupresión.
- Dosis de inmunosupresión.
- Tratamiento acumulado.
El 90,2% respondió que «Todas las respuestas son correctas».
¿ ¿Consideras que los inhibidores de m-TOR tienen un papel preventivo en el desarrollo de cáncer?
El 73,8% de los nefrólogos respondió afirmativamente, aunque sólo en algunos cánceres, y el 19,7% respondió que sí en todos los casos. Un 4,9% contestó que no y sólo un 1,6% se abstuvo.
¿ ¿Consideras que el tratamiento con inhibidores de m-TOR puede jugar algún papel en el tratamiento de los procesos neoplásicos?
El 67,2% de los nefrólogos respondió afirmativamente, aunque sólo en algunos cánceres, y el 29,5% respondió que sí en todos los casos.
¿ Cuando algún paciente en tu consulta presenta el desarrollo de un cáncer, ¿lo conviertes automáticamente a un inhibidor de m-TOR?
Las respuestas son mayoritariamente afirmativas: un 50,8% lo hace en algunas ocasiones, y un 45,9% siempre. Sólo un 3,3% lo hace excepcionalmente.
¿ ¿Consideras que los inhibidores de m-TOR podrían disminuir el tiempo de exclusión de lista de espera a los pacientes con cáncer?
Sólo el 1,6% contestó que siempre. La mayoría (68,9%) respondió que sí, en algunos casos, y un 29,5% dijo que nunca.
¿ ¿Cuál de los siguientes fármacos de inducción consideras relacionado con el desarrollo de cáncer?
El OKT3 se considera el de mayor riesgo (60,7%) seguido del ATG (37,7%). Los anticuerpos anti-IL-2R y el rituximab fueron prácticamente descartados.
CONCLUSIONES
Encuesta de trasplante renal
1. Las áreas que más preocupan en el campo del trasplante son la NCI, la enfermedad CV y la individualización de la inmunosupresión.
2. Está justificada la individualización de la IS (para un 50% siempre).
3. Sólo un 30% de los encuestados lleva a cabo la individualización en >50%.
4. La individualización debe realizarse secuencialmente (68%) a lo largo de las diferentes fases del trasplante, priorizando en la eficacia a largo plazo y en el perfil de riesgo vascular.
5. Los criterios a seguir deben ser escalonados por orden de importancia: riesgo inmunológico, características del donante y perfil del receptor.
6. Debe individualizarse la IS en pacientes con VHC: reducción de esteroides, reducción del AC, no anticuerpos.
7. Anticuerpos mono y policlonales sólo justificados en pacientes de riesgo inmunológico y riesgo de función renal retrasada.
8. Mayor eficacia
¿ Rechazo agudo: P más TAC más MAP
¿ NCI, supervivencia y riesgo vascular: P más anti-mTOR más MPA.
9. En fase de mantenimiento, diferentes criterios para individualizar: NCI, riesgo.
10. Biopsia del injerto para definir NCI, realizar un cambio de IS o no recuperación de la función renal tras Rx.
11. La proteinuria se determina regularmente, e IECA/ARA tratamiento de inicio.
12. Ante riesgo vascular pretrasplante o complicaciones postrasplante (HTA, diabetes, lípidos), en un 75% de los casos ¿ individualizar la IS.
Individualización de la inmunosupresión en la enfermedad cardiovascular
1. Se debería individualizar la terapia inmunosupresora en función del riesgo cardiovascular pretrasplante, principalmente evitando o reduciendo precozmente los corticoides (80% resp).
2. En pacientes jóvenes con HTA grave pretrasplante la práctica clínica habitual es la administración de tacrolimus más MPA, evitando CsA.
3. Igualmente, se debería individualizar la inmunosupresión en pacientes con complicaciones cardiovasculares o metabólicas postrasplante. Las prácticas clínicas más habituales son:
- Diabetes mellitus: retirada/minimización de esteroides, con o sin cambio tacrolimus ¿ CsA.
- HTA(no estenosis arteria renal): retirada/minimización esteroides, con o sin cambio CsA¿ tacrolimus.
- Hiperlipemia grave: retirada/minimización esteroides, con o sin cambio CsA¿ tacrolimus.
- IAM: retirada/minimización esteroides, con o sin cambio CSA tacrolimus más MMF.
Individualización de la inmunosupresión en la diabetes
Se aconseja el trasplante combinado páncreas-riñón a los diabéticos tipo 1 y el trasplante renal aislado a los diabéticos tipo 2 sin secuelas graves de la enfermedad.
Se sigue un perfil individualizador en la inmunosupresión (80% resp.) en los pacientes en tratamiento actual con insulina/ADO, o que hayan tenido antecedentes previos (tratamientos previos prolongados con insulina/ADO, diabetes gestacional, intolerancia carbohidratos, etc.).
Los corticoides son los fármacos más diabetogénicos (56% resp.), seguidos por el tacrolimus (44% resp.). No obstante, la práctica más habitual es la continuación del uso de corticoides en el tratamiento individualizador de la inmunosupresión (70% resp.).
DMPT retirada de los corticoides, con o sin retirada/sustitución de tacrolimus (CsA, sirolimus/everolimus más AMF).
Individualización de la inmunosupresión en el cáncer
El cáncer es un problema muy importante para la práctica del trasplante renal (59% resp.). Se considera que la inmunosupresión participa directamente en su desarrollo.
Los inhibidores de la calcineurina son los fármacos que tienen un impacto más negativo en el desarrollo del cáncer.
El cáncer de piel es el más frecuente en las consultas.
Los inhibidores de m-TOR tienen un papel preventivo en algunos cánceres (78% resp). La práctica clínica habitual es la introducción de inhibidores de m-TOR en pacientes con cáncer postrasplante. Adicionalmente, se considera que los inhibidores de m-TOR pueden disminuir el tiempo de exclusión de la lista de espera.
El OKT3 es el fármaco que está más relacionado con el desarrollo de cáncer.
Figura 1.
Figura 2.
Figura 3.
Figura 4.
Figura 5.
Tabla 1. Riesgo absoluto de cáncer (excluyendo cáncer de piel no melanocítico) según el tiempo transcurrido desde el primer trasplante renal
Tabla 2. Índice de trasplantes procedentes de cadáver y de donante vivo
Tabla 3. Relación entre especialista individualizador y centro trasplantador
Tabla 4. Actitud individualizadora en relación con el riesgo cardiovascular
Tabla 5. Inmunosupresión en pacientes con virus C sin riesgo inmunológico
Tabla 6. Opciones terapéuticas de mantenimiento más beneficiosas en cuanto a evitar el rechazo agudo (n = 79)
Tabla 7. Opciones terapéuticas de mantenimiento más beneficiosas en cuanto a función renal, aparición de nefropatía crónica del injerto y riesgo cardiovascular (n = 79)
Tabla 8. Opciones terapéuticas ante pacientes con importante riesgo cardiovascular
Tabla 9. Opciones terapéuticas en pacientes que desarrollan HTA grave postrasplante (n = 79)
Tabla 10. Opciones terapéuticas en pacientes que desarrollan diabetes mellitus postrasplante
Tabla 11. Opciones terapéuticas en pacientes que desarrollan hiperlipidemia postrasplante (n = 79)
Tabla 12. Actitud terapéutica preferida ante un paciente con diabetes mellitus postrasplante
Tabla 13. Actitud terapéutica preferida ante un paciente con diabetes mellitus postrasplante
Tabla 14. Actitud terapéutica preferida ante un paciente con hiperlipemia grave postrasplante
Tabla 15. Consideración de la diabetes mellitus como factor de riesgo para el trasplante
Tabla 16. Criterios para considerar a un paciente diabético de cara a la individualización
Tabla 17. Actitud ante la diabetes mellitus postrasplante
Tabla 18. Modificación del tratamiento ante la diabetes mellitus postrasplante
Tabla 19. Medidas adoptadas ante la diabetes mellitus postrasplante en pacientes con terapia triple: ciclosporinaácido micofenólico-corticosteroides (n = 61)
Tabla 20.
Anexo
Cuestionario