■ Tipo de diseño y seguimiento
Ensayo clínico en fase 2, un brazo de tratamiento, realizado y analizado independientemente en 2 países: Estados Unidos y Polonia. Los pacientes fueron seguidos al menos 12 meses.
■ Asignación
No aleatoria.
■ Enmascaramiento
No existente.
■ Ámbito
Seis centros distintos en Estados Unidos y Polonia.
■ Pacientes
Se incluyen pacientes con insuficiencia renal crónica estadio 5D, mayores de 18 años, que fueron excluidos para implantación de fístula arteriovenosa (FAV) nativa (FAVn). Se excluyen pacientes con una FAV protésica (FAVp) previa o antecedentes de enfermedad vascular periférica en la extremidad seleccionada, conocimiento o sospecha clínica de obstrucción de troncos venosos superiores, insuficiencia cardíaca clase funcional III o IV (NYHA), infarto de miocardio o accidente vasculocerebral en los 6 meses previos, taquicardia ventricular o angina inestable, neoplasia activa en el último año o expectativa de vida < 12 meses. En los centros de Estados Unidos también se excluyeron los pacientes en lista de espera para trasplante renal.
■ Intervención
Se obtuvieron vasos humanos descelularizados de 6 mm de diámetro y 35-42 cm de longitud mediante técnica de bioingeniería humana. En todos los casos se implantaron los accesos vasculares arteriovenosos en la extremidad superior de los pacientes a modo de loop, según técnica quirúrgica convencional: 59 humeroaxilares y 1 axiloaxilar.
■ Variables de resultado principales
– Análisis de la aparición de rechazo inmunológico o infección del injerto, aneurismas, fallo mecánico o técnico e incidencia de efectos adversos durante el seguimiento.
– Análisis de las permeabilidades: primaria, primaria asistida y secundaria a los 6 meses del estudio.
° Permeabilidad primaria: tiempo que transcurre con acceso vascular funcionante hasta algún tipo de intervención necesaria para mantener la permeabilidad (angioplastia con catéter-balón o trombectomía endovascular).
° Permeabilidad primaria asistida: tiempo transcurrido hasta la trombosis del acceso vascular.
° Permeabilidad secundaria: tiempo transcurrido desde la implantación quirúrgica del acceso hasta su pérdida o abandono.
■ Variables secundarias
Análisis de las permeabilidades y aparición de eventos adversos a los 12, 18 y 24 meses del estudio.
■ Tamaño muestral
No se ha realizado análisis del tamaño muestral, dado que no es un estudio comparativo sino una fase 2 de un ensayo clínico. Se incluyeron un total de 60 pacientes (20 de Estados Unidos y 40 de Polonia).
■ Promoción o patrocinio
La empresa productora de estos injertos (Humacyte) ha diseñado el estudio, ha recolectado, analizado e interpretado los datos, y ha escrito el artículo.
■ RESULTADOS PRINCIPALES
Las características de los 2 grupos de estudio fueron similares con una edad media de 61 ± 8 años en Estados Unidos y 59 ± 10 años en Polonia; sin embargo, la proporción de mujeres y la incidencia de diabetes, enfermedad cardiovascular, ictus y vasculopatía periférica resultaron mayores en la población americana. En ambos estudios, los pacientes tenían antecedentes de accesos vasculares previos (rango, 1-9). La media de seguimiento resultó de 16 ± 7,6 meses y 8 pacientes fueron censurados (4 muertes, 1 trasplante renal y 3 retiradas del consentimiento). Los pacientes tomaron aspirina 75-325 mg/día vía oral después del procedimiento quirúrgico durante el período de seguimiento.
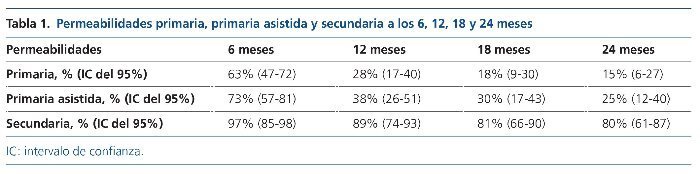
En la tabla 1 se resumen las distintas permeabilidades (primaria, primaria asistida y secundaria) obtenidas en el grupo de estudio. La media del flujo vascular medido por ecografía fue de 1.000 ml/min, manteniéndose estable a lo largo de todo el período de seguimiento. Se inició la canulación del acceso vascular entre las 4 semanas (10 pacientes polacos) y las 8 semanas tras la implantación quirúrgica (20 pacientes americanos y 30 polacos).
La media de intervenciones para mantener la permeabilidad del acceso durante el período de seguimiento fue de 1,89 por paciente-año. Durante el estudio se dejaron de utilizar 10 accesos vasculares (media 2 a 85 semanas tras la implantación), 5 dentro del primer año, 2 por deterioro del vaso tras angioplastia transluminal percutánea con catéter-balón de 8 mm (alteración estructural), 1 ligadura secundaria a neuropatía isquémica monomiélica y 7 estenosis refractarias con trombosis asociada. Se objetivaron un total de 4 muertes no relacionadas con las variables del estudio. No se objetivó ningún caso de infección aguda en el postoperatorio inmediato. A pesar de ello, durante el período de seguimiento se evidenciaron 3 episodios de infección en las zonas de canulación, 1 hematoma resuelto con antibioterapia, 1 caso que precisó reconstrucción quirúrgica de la anastomosis venosa y 1 caso que requirió exéresis quirúrgica por presentar celulitis y cultivos positivos.
Durante el período de seguimiento se reportaron un total de 155 eventos adversos en 33 pacientes para mantener la permeabilidad del acceso vascular. Se constataron un total de 14 seudoaneurismas en 10 pacientes asociados a las zonas de canulación, de los cuales 2 precisaron de reparación quirúrgica.
No se evidenció ningún caso de rechazo inmunológico o respuesta inflamatoria secundaria a los vasos descelularizados obtenidos mediante bioingeniería humana. Sin embargo, 5 pacientes presentaron elevación de anticuerpos IgG que no se correlacionaron con maniobras de repermeabilización y 3, un panel positivo para el complejo mayor de histocompatibilidad clases I y II a los 6 meses de la implantación (2 casos por reducción del tratamiento inmunosupresor a un trasplante renal previo y 1 por causa desconocida). En el estudio histológico del vaso obtenido a las 16 semanas, los autores constatan algunos marcadores positivos (CD 68+, actina de músculo liso) que se podrían correlacionar con un proceso de remodelado vascular (repoblación) con células del huésped.
■ CONCLUSIONES DE LOS AUTORES
Los vasos humanos descelularizados obtenidos mediante técnicas de bioingeniería humana presentan una buena tolerancia con escasa respuesta inmunogénica por parte del huésped. A pesar de que resultan necesarios futuros estudios prospectivos y aleatorizados, podrían representar una alternativa con una buena resistencia a las canulaciones repetidas (> 1 año), baja tasa de aneurismas, buena permeabilidad secundaria y escasas complicaciones infecciosas.
■ COMENTARIOS DE LOS REVISORES
La FAVn representa el acceso vascular de elección sobre la base de la mayor supervivencia, menores complicaciones y mejor coste-efectividad1. A pesar de los peores resultados de las FAVp (con politetrafluoroetileno [PTFE]), su implantación ha aumentado dadas las crecientes comorbilidades asociadas y mayor longevidad de la población actual con insuficiencia renal crónica en programa de hemodiálisis2. Entre las complicaciones asociadas a los injertos cabe destacar la hiperplasia neointimal venosa, fundamentalmente a nivel de la anastomosis venosa, la trombosis y la infección. Según algunos estudios, hasta el 90% de los pacientes que presentan trombosis de su FAVp tiene hiperplasia de la neoíntima venosa que condiciona la presencia de estenosis significativa3.
El equipo de Lawson JH y Humacyte tratan de buscar una mejor alternativa a los injertos protésicos de PTFE. No es el primer intento; se han publicado otras alternativas (homoinjertos arteriales y venosos, aloinjertos, conductos de tejido autólogo diseñados con bioingeniería, etc.), pero todas ellas han fracasado al intentar mejorar los resultados del PTFE, y sobre todo han demostrado dilataciones y degeneraciones tisulares en el seguimiento. Sin embargo, los resultados preliminares de este estudio muestran algo esperanzador: obtienen una permeabilidad primaria similar al PTFE y una permeabilidad secundaria superior (el 89 frente al 55-65% a 1 año)3,4, con una menor tasa de infecciones (el 1,3% paciente-año), similar a las FAVn5.
Existen numerosas limitaciones en el estudio. Los autores no reportan la aplicación de ningún método específico para la monitorización del acceso vascular, cuando es conocido el impacto negativo de la angioplastia preventiva en la aparición de la hiperplasia neointimal venosa acelerada, con el riesgo de trombosis y pérdida del acceso6 (nuevas guías de acceso vascular del GEMAV 2017). Los 2 países participantes empezaron a incluir pacientes en períodos diferentes, con protocolos de tratamiento y seguimiento algo distintos, pacientes no homogéneos (más comórbidos y con peores permeabilidades en Estados Unidos) y protocolos sin criterios similares de trombectomía del injerto tras una oclusión (trombectomía simple, y stent tras trombosis repetida en Polonia y trombectomía más stent inicialmente en Estados Unidos), con lo que curiosamente los pacientes americanos sufren menos procedimientos por año. En el título y en el estudio se describen 2 ensayos fase 2 aparentemente independientes, como cabría esperar ante estos grupos y protocolos distintos y según su registro NCT independiente, pero finalmente los resultados se analizan conjuntamente (ensayo clínico fase 2 multicéntrico). El tamaño muestral (60 pacientes) es algo escaso para un ensayo fase 2, y no aporta análisis de costes.
Pero, a pesar de las múltiples limitaciones, este estudio ofrece una salida esperanzadora en un campo con grandes limitaciones con los materiales actualmente disponibles, por lo que estaremos esperando ansiosamente los resultados de estudios fase 3 comparando estos injertos con los habituales de PTFE.
■ CONCLUSIONES DE LOS REVISORES
La obtención de vasos humanos descelularizados mediante técnicas de bioingeniería humana puede representar una alternativa futura en el campo del acceso vascular. Sin embargo sería necesario el diseño de futuros estudios clínicos multicéntricos y aleatorizados que analicen sus ventajas, así como su coste-efectividad respecto a las FAVp convencionales tipo PTFE.
■ CLASIFICACIÓN
Subespecialidad: Fracaso renal crónico
Tema: Acceso vascular para hemodiálisis
NIVEL DE EVIDENCIA: Baja
GRADO DE RECOMENDACIÓN: Débil