En nuestro país, existe una larga tradición para diseñar y mantener registros de las enfermedades renales más prevalentes y entre ellas, se encuentran las glomerulonefritis (GN) y las patologías diagnosticadas mediante biopsia renal. Así, para situar temporalmente el inicio de los estudios sobre la epidemiología de las enfermedades renales biopsiadas en España, especialmente las patologías glomerulares, hay que remontarse al año 1986 cuando se describió, de forma independiente, la disminución de la incidencia de la GN membranoproliferativa (GNMP) en dos hospitales de Madrid1,2. Con motivo de estas publicaciones, se insistió en una publicación en la revista Nefrología, en la necesidad de aunar esfuerzos y crear grupos multicéntricos de estudio de cara a obtener resultados multicéntricos para obtener datos más consistentes y fiables3. Poco después, en 1987, se hicieron las primeras publicaciones que confirmaban este hecho, tanto en la población infantil (1.364 casos)4 como en la adulta (8.545 casos)5,6, donde se revisaban los resultados de las biopsias renales realizadas entre 1970 y 1986. Estas publicaciones, realizadas por el Grupo de Estudio de la SEN marcan el comienzo de un trabajo continuado y productivo a nivel nacional, hecho que fue favorablemente comentado y estimulado por el entonces director de Nefrología7. Unos años más tarde, en 1990, se publicó un estudio multicéntrico, con 2.123 biopsias renales, realizadas en 1987 y 1988, que consolidó el denominado «Registro Español de Glomerulonefritis (REGN)» 8. Este registro hizo, en la década de los 90, varias publicaciones dando cuenta de los resultados de las biopsias renales a nivel nacional, con un porcentaje de participación significativo por parte de los Servicios o Unidades de Nefrología de nuestro país9–15. A partir de 1994, se introdujeron dos novedades en la recogida de datos: a) cumplimentación individualizada de cada paciente para facilitar el procesamiento estadístico y b) inclusión de patología no glomerular. Con la información recogida con un registro para cada biopsia renal, se hizo la primera publicación en Nephrology Dialysis and Transplantation en 200216, que tuvo un elevado índice de impacto. En resumen, se han publicado 23 manuscritos4,8–27: 12 en Nefrología4,8–15,25 y 11 en revistas internacionales16,26,27. Como prueba de su eficacia y fiabilidad se han detallado resultados acerca de datos generales sobre la incidencia y prevalencia de las distintas formas histológicas renales6,8,10–13,15,16,25, así como sus correlaciones con la clínica18, tanto en la población infantil4 como en la anciana14,20. Además, y de forma más detallada se ha profundizado sobre determinados síndromes clínicos como: insuficiencia renal aguda19, hematuria26 y síndrome nefrótico9. Por otro lado, se ha analizado varias entidades renales como nefropatía IgA27, GN extracapilar24, GN membranoproliferativa4,5,17, nefropatía lúpica21, amiloidosis23 y nefritis tubulointersticial aguda22. Por otro lado, desde 1988 se vienen presentado estos datos en la sesión anual de Registros en los congresos de la SEN, posteriormente descargables en la página web de la SEN28. Para facilitar la participación, desde hace unos 15 años, los datos se están enviando de forma telemática a través de la página web de la SEN. Y como última novedad, ha contribuido mediante un enlace al envío de material al Biobanco de la SEN (https://www.senefro.org/modules.php?name=webstructure&idwebstructure=30) de cara a colaborar con investigación aplicada utilizando técnicas de biología molecular y avanzar en medicina de precisión.
Con estos datos se confirma que el REGN en uno de los más numerosos y fiables a nivel mundial, como se ha reconocido en varias ocasiones, ya que los manuscritos mencionados se incluyen en las referencias de los trabajos que tratan sobre la epidemiología de las enfermedades renales biopsiadas29,30.
Es bien sabido que los registros de las enfermedades renales aportan información clave en la práctica clínica por múltiples razones, entre las que destacan el conocimiento de las patologías más frecuentes, con datos reales acerca de la incidencia y prevalencia de las mismas29, así como la puesta en marcha de protocolos de prevención y tratamiento, así como servir de base para estudios y ensayos clínicos multicéntricos. Uno de los puntos fundamentales en cada registro es la colaboración a nivel nacional, con un formulario previamente acordado31, así como una política uniforme acerca de las indicaciones de biopsia renal32,33, para responder a las preguntas no resueltas acerca de la prevención y tratamiento de las enfermedades renales34 y estos fueron los motivos de la creación y desarrollo del REGN, tal y como comentamos en una publicación anterior35. Otra de las razones para disponer de un registro de enfermedades renales biopsiadas es que muchas patologías, especialmente las glomerulares, solo pueden ser diagnosticadas con certeza mediante biopsia renal30. Un buen ejemplo de ello es el valor de la biopsia renal en el fracaso renal agudo36 o el estudio de la patología glomerular en pacientes ancianos37–39. Finalmente, la información suministrada puede contribuir a la sobrecarga que estas enfermedades tienen sobre el sistema sanitario derivadas del número de hospitalizaciones, progresión hacia la insuficiencia renal avanzada y fallecimientos40,41.
Los estudios de un solo centro dan información relevante pero insuficiente. No obstante, se han publicado numerosas publicaciones, como los estudios realizados en un solo centro de referencia, como los siguientes en Springfield y Minnesota en EE. UU.42,43, Colombia44, Irlanda45, Helsinki46, Bélgica47, Alemania48,49, Porto (Portugal)50, Macedonia51, Serbia52, Polonia53, India54, Japón55, China56, Corea57, Tailandia58,59, Egipto60,61, Sudáfrica62, Asia del Sur63, Pakistán64. Además, se han publicado datos locales acerca de determinados síndromes renales, como síndrome nefrótico en Chicago65, China66 y Pakistán67, fracaso renal agudo en Chicago68 e India69 y alteraciones urinarias en Serbia70. Y también acerca de entidades concretas como referentes acerca de la NIgA en Kentucky y en 24 estados del sur y medio oeste de
EE. UU.71,72, GSF en EE. UU.73,74 y Brasil75, GN primarias en Sao Paulo (Brasil)76 y Reino Unido77, nefropatía membranosa en Reino Unido78, vasculitis renales en Norfolk (Reino Unido)79, GN extracapilar-pauciinmune en Estocolmo80 y Estonia81, y membrana basal fina en Limburgo (Holanda)82. Y finalmente, algunos estudios se han centrado en determinados grupos de edad como en población infantil en China83 y Sur de Asia63 o en ≥ 60 años en Chicago68, ≥ 65 en Irlanda45, Japón84 y Turquía85 y en ≥ 80 años en Japón86 y EE. UU.87.
Los registros nacionales o multicéntricos son los más fiables de cara a conocer la epidemiología de las enfermedades renales biopsiadas y permiten las comparaciones entre ellos. En la tabla 1, se indican la mayoría de ellos, entre los que se encuentran los realizados en Reino Unido88–91, Francia92,93, Nueva Caledonia94, Italia95–101, India102, Emiratos Árabes Unidos103, Japón104–118, Dinamarca119,120, Singapur121, Perú122, Australia123, Corea124, China125, República Checa 126,127, Hungría128, Croacia129, Uruguay130, Rumanía131,132, Brasil133–136, Líbano137, Estados Unidos138, Lituania139, Turquía140, Colombia141, Noruega142–144 y Polonia145, entre los más importantes. Como se puede deducir, la NIgA es la nefropatía más frecuente en Europa y Asia, mientras que en USA la GSF puede estar aumentando42,73,74,146.
Publicaciones multicéntricas sobre patología renal biopsiada
| Autores | País | Núm. biopsias | Comentarios |
|---|---|---|---|
| Johnston et al 88 | 599 | Datos de NIgA | |
| Johnston et al 90 | Reino Unido | 255 | Datos SN en ancianos |
| Hedger et al 89 | 241 | Datos vasculitis renales | |
| McQuarrie et al 91 | 2.480 | Variaciones de incidencia en Escocia | |
| Simon et al 92 | 942 | NIgA como la más frecuente | |
| Simon et al 93 | Francia | 1742 | NIgA como la más frecuente |
| Painter et al 94 | Nueva Caledonia | 275 | NIgA y GSF como las más frecuentes |
| Stratta et al 95 | 1.926 | NIgA como la más frecuente | |
| Schena et al 96 | 15.461 | NIgA y NM como las más frecuentes | |
| Coppo et al 97 | Italia | 432 | NIgA y nefropatía púrpura de Henoch–Schönlein en niños |
| Vendemia et al 98 | 2.511 | NM y proliferativa extracapilar en ≥ 65 años | |
| Gesualdo et al 34 | 14.607 | NIgA y nefroangiosclerosis como las más frecuentes | |
| Lupo et al 99 | 816 | NIgA como la más frecuente en GN primarias | |
| Zaza et al 100 | 2.680 | NIgA como la más frecuente | |
| Zaza et al 101 | 1.185 | NIgA, GSF y membranosa en pacientes con insuficiencia renal avanzada | |
| Chugh et al 102 | India | 2.947 | Elevada prevalencia de síndrome nefrótico: cambios mínimos, amiloidosis (lepra y otras infecciones) |
| Yahya et al., 103 | Emiratos Árabes Unidos | 490 | Predominio de GN proliferativas y NM |
| Research Group on Progressive Chronic Renal Disease 149 | |||
| Iseki et al 105 | 1.850 | Elevada prevalencia de NIgA | |
| Imai et al 106 | Japón | 2.832 | Supervivencia renal según resultados de biopsia renal |
| Sugiyama et al 107 | 281 | Revisión amiloidosis | |
| Yokoyama et al 108 | Japón | 2400 | Prevalencia de NIgA y NM |
| Yokoyama et al 109 | 2.082 | Datos en ≥ 65-83 años (predominio de vasculitis ANCA+) | |
| Kawamura et al 110 | 3073 | Datos en ancianos | |
| Sugiyama et al 111 | 79 | Datos de NM | |
| Yokoyama et al 112 | 4016 | Datos de GNMP | |
| Yokoyama et al 113 | 438 | Prevalencia de NIgA y NM | |
| Nakashima et al 114 | 328 | Datos síndrome nefrótico en ≥65 años | |
| Hiromura et al 115 | 47 | Datos nefritis por fármacos | |
| Nishi et al 116 | 331 | Datos de enfermedad asociada a IgG-4 | |
| Komatsu et al 117 | 281 | Datos de NL | |
| Nakagawa et al 118 | 152 | Datos de amiloidosis | |
| 593 | Datos de nefritis por Henoch-Schönlein en ≥65 años | ||
| Datos de GNMP | |||
| Heaf et al.119,120 | Dinamarca | 2.380 | Elevada prevalencia de GN proliferativa mesangial y de CM |
| Woo et al.121 | Singapur | 2.102 | Elevada prevalencia de GN proliferativa mesangial y de CM. Papel de antígenos ambientales |
| Hurtado et al.122 | Perú | 1.263 | Prevalencia de NL y GNMP |
| Briganti et al. 123 | Australia | 2.030 | Prevalencia de NIgA y GSF |
| Choi et al 124 | Corea | 4.514 | Prevalencia de CM y NIgA |
| Li et al 125 | China | 13.519 | Prevalencia de NIgA y NL |
| Rychlik et al 126 | República Checa | 4.004 | Prevalencia de NIgA y CM |
| Maixnerova et al 127 | 10.472 | Prevalencia de NIgA, NM, NL y CM | |
| Horvatic et al 129 | Croacia | 922 | Prevalencia de NIgA, GSF y NM |
| Sipiczki et al 128 | Hungría | 798 | Prevalencia de NIgA y membranosa |
| Mazzuchi et al 130 | Uruguay | 2.058 | Prevalencia de GSF y NL |
| Covic et al 131 | Rumanía | 635 | Prevalencia de GNMP y mesangioproliferativa |
| Gusbeth-Tatomir et al 132 | 336 | Prevalencia de GNMP y mesangioproliferativa | |
| Malafonte et al 133 | 2.086 | Prevalencia de GSF y NM | |
| Polito et al 134 | Brasil | 9.617 | Prevalencia de GSF y NM |
| Costa et al 135 | 1.151 | Prevalencia de GSF y GNMP | |
| Machado et al 136 | Brasil | 582 | Prevalencia de GSF, CM y NIgA |
| Karnib et al 137 | Líbano | 1.327 | Prevalencia de GN mesangioproliferativa y GSF |
| Layton et al 138 | Estados Unidos | 217 | Dificultad para clasificar resultados de biopsia renal |
| Brazdziute et al 139 | Lituania | 5.368 | Prevalencia de NIgA y GSF |
| Fidan et al 140 | Turquía | 3.982 | Datos población infantil: predominio de GSF y púrpura de Henoch-Schönlein |
| Barrera et al., 141 | Colombia | 12.613 | Predominio de glomerulosclerosis, NIgA y NL |
| Norby et al 142 | 178 | Datos de NL | |
| Bjorneklett et al 143 | Noruega | 81 | Datos de vasculitis renales ANCA+en ancianos |
| Bjorneklett et al 144 | 357 | Evolución vasculitis renales ANCA+según género | |
| Perkowska-Ptasinska et al., 145 | Polonia | 3.934 | Prevalencia de NIgA y GSF |
CM: cambios mínimos; GN: glomerulonefritis; GNMP: glomerulonefritis membranoproliferativa;GSF: glomerulosclerosis segmentaria y focal; NIgA: nefropatía IgA; NL: nefropatía lúpica; NM: nefropatía membranosa; SN: síndrome nefrótico.
El REGN, que cuenta con más de 28.000 biopsias renales en 2018, solo es comparable a los registros de Italia34 y Japón118 que tienen registrados, al menos hasta sus últimas publicaciones, entre 15.000 y 26.000 biopsias, respectivamente.
En esta publicación queremos resumir los resultados a grandes rasgos de nuestro registro REGN, reflexionar sobre su futuro, los datos actuales en 2019, así como las innovaciones necesarias para mantener su vigencia.
Presente: datos actualizadosEn los últimos 26 años (desde 1994 hasta la 2019) se han recogido 27.116 biopsias renales de riñones nativos (92% primera biopsia), con una media de 1.042 biopsias anuales. En total han participado 157 Unidades de Nefrología, cuyo listado se indica en el Anexo.
Los años de estudio se han agrupado de 5 apartados de 5 años cada uno (excepto el último de ellos que comprende 6 años): 1994-1998, 1999-203, 2004-2008, 2009-2013 y 2014-2019. Las edades en el momento de la biopsia se han separado en 4 intervalos: <15 años, 15-65 años, 65-80 años y >80 años. Los diagnósticos histológicos se han agrupado en 5 apartados: GN primarias, GN secundarias, nefropatías tubulointersticiales y nefropatías vasculares. El resto (hereditarias o de difícil clasificación) se han etiquetado como «otras».
En la tabla 2 se indica el número y porcentaje de biopsias realizadas en cada intervalo de tiempo según el grupo de edad.
Número y proporción de biopsias renales por periodos de tiempo
| 1994-1998n(%)* | 1999-2003n(%)* | 2004-2008n(%)* | 2009-2013n(%)* | 2014-2019n(%)* | Totaln(%)* | |
|---|---|---|---|---|---|---|
| <15 años | 487(8,5) | 292(6,1) | 188(3,2) | 116(2,2) | 148(2,9) | 1.231(4,6%) |
| 15-65 años | 4.107(71,8) | 3.355(70,5) | 4.236(73,0) | 3.683(70,6) | 3.471(67,1) | 18.852(70,7) |
| 65-80 años | 1.058(18,5) | 1.012(21,3) | 1.252(21,6) | 1.232(23,6) | 1.331(25,7) | 5.885(22,1) |
| >80 años | 70(1,2) | 100(2,1) | 124(2,1) | 185(3,5) | 224(4,3) | 703(2,6) |
| Total | 5.722 | 4.759 | 5.800 | 5.216 | 5.174 | 26.671** |
Las medianas de edad y creatinina en el momento de la biopsia renal de toda la población son 50 años y 1,6mg/dl, respectivamente (ambas no tienen distribución gaussiana). Los varones predominan sobre las mujeres, con una ratio de 1,5. La prevalencia de hipertensión es 55%. En la tabla 3 se indican estos valores en cada grupo de edad.
Edad, género, hipertensión y función renal según grupos de edad
Respecto al método de estudio, el 74,7% de las biopsias tenían estudio simultáneo con microscopio óptico e inmunofluorescencia, el 17,8% con estas técnicas y microscopio electrónico, mientras que el 7% solo tenían estudio con microscopio óptico y el 0,5% restante solo inmunofluorescencia.
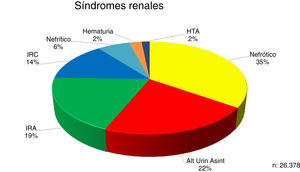
Las proporciones de los síndromes renales en el momento de la biopsia renal se indican en la figura 1.
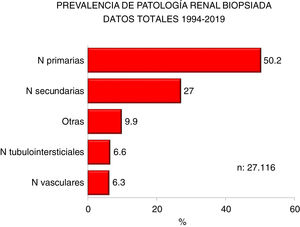
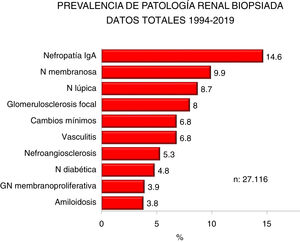
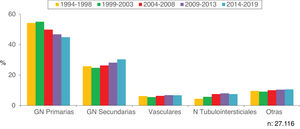
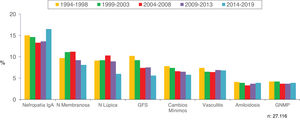
En las figuras 2 y 3 se indican las prevalencias globales de todas las biopsias renales agrupadas y por diagnósticos concretos, respectivamente.
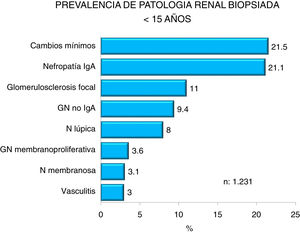
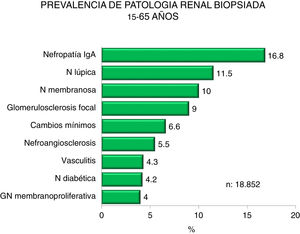
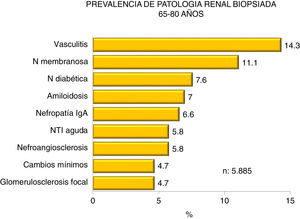
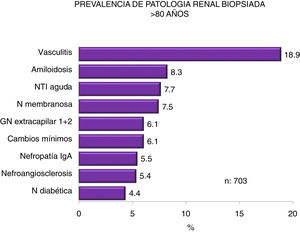
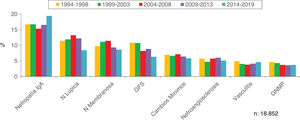
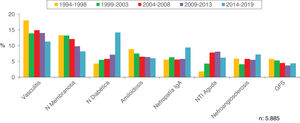
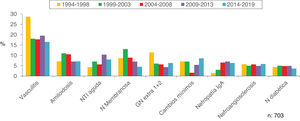
En las figuras 4-7 se resumen las prevalencias en los diferentes intervalos de edad.
En las figuras 8 y 9 se representa la tendencia de las patologías renales más frecuentes, agrupadas y por diagnósticos histológicos, respectivamente.
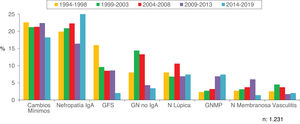
En las figuras 10-13 se indican las tendencias de las patologías biopsiadas en cada intervalo de edad, <15 años, 15-65 años, 65-80 años y>80 años, respectivamente.
En las tablas 4 y 5 se resumen las conclusiones de todos estos resultados.
Resumen de los datos del Registro de Glomerulonefritis (1994-2019). Datos generales
| Predominio de varones en todos los grupos de edad |
| La mediana de edad es 50 años |
| Elevada presencia de hipertensión arterial e insuficiencia renal en adultos y ancianos |
| El síndrome nefrótico es la indicación más frecuente de biopsia renal, seguido por alteraciones urinarias asintomáticas |
| Las nefropatías primarias son la mitad de todos los diagnósticos |
| La nefropatía IgA, membranosa y lúpica son las más frecuentes (1/3 del total) |
| Hay cambios en las tendencias temporales de los diagnósticos en general: |
| Aumento de GN secundarias y nefropatías tubulointersticiales y disminución de las GN primarias |
| Aumento de la prevalencia de nefropatía IgA y disminución de glomerulosclerosis, cambios mínimos nefropatía membranosa y lúpica; con estabilización de vasculitis, amiloidosis y GN membranoproliferativa |
Resumen de los datos del Registro de Glomerulonefritis (1994-2019). Datos y tendencias según grupos de edad
| <15 años: |
| Predominio de cambios mínimos, nefropatía IgA y glomerulosclerosis focal |
| Aumento de nefropatía IgA y GN membranoproliferativa y disminución de la prevalencia de cambios mínimos y glomerulosclerosis |
| 15-65 años: |
| Predominio de nefropatía IgA, lúpica y membranosa |
| Aumento de nefropatía IgA y disminución de glomerulosclerosis y lúpica |
| 65-80 años: |
| Predominio de vasculitis, nefropatía membranosa y diabética |
| Aumento de nefropatía IgA, nefropatía diabética y nefritis intersticial aguda, con disminución de vasculitis, N. membranosa, amiloidosis y glomeruloesclerosis; sin cambios en nefroangiosclerosis |
| >80 años: |
| Predominio de vasculitis, amiloidosis y nefritis tubulointersticial aguda |
| Aumento de nefritis intersticial aguda, cambios mínimos y nefropatía IgA, con disminución de vasculitis y membranosa; sin modificaciones de nefroangiosclerosis y nefropatía diabética |
La Nefrología ha experimentado numerosos cambios en los últimos años y las enfermedades renales que requieren biopsia no han sido ajenas a estas modificaciones. Entre ellas, destaca la irrupción de nuevas entidades (GN C3, entre otras) así como un nuevo enfoque para la clasificación y emisión de informes de las GN 147,148. Por tanto, los registros deben adaptarse a estos cambios de cara a recoger los datos de forma más uniforme y actual. Sin duda, el REGN precisa algunos cambios, entre los que se encuentran:
- a)
Modificación de la ficha de cumplimentación de datos, con ampliación de los síndromes clínicos que indican la biopsia renal (ej.: síndrome nefrótico+insuficiencia renal aguda; alteraciones urinarias+hipertensión).
- b)
Posibilidad de seleccionar varias patologías detectadas en la biopsia renal (ej.: NIgA+nefroangiosclerosis; nefropatía diabética+GN extracapilar).
- c)
Mejorar la recogida de datos para conocer la incidencia de las diferentes patologías p.m.p según población de referencia del centro que realiza las biopsias renales.
- d)
Adecuar la clasificación de la patología renal acorde con el nuevo sistema propuesto en la Clínica Mayo 147.
- e)
Aumentar la participación, especialmente en los Centros de Nefrología Infantil.
- f)
Promover estudios multicéntricos y promover estudios o ensayos clínicos en base a los datos obtenidos.
- g)
Mantener el análisis de los datos y su publicación posterior, de cara a analizar cambios de prevalencia e incidencia, así como estudiar correlaciones entre síndromes clínicos y el sustrato histológico.
- h)
Incorporar información sobre comorbilidad asociada, para poder establecer el diagnóstico de formas secundarias (ej. infecciones virales o de otro tipo, tumores, entre otros), dada la aparición de nuevos biomarcadores 78.
Finalmente, el REGN debe mantenerse activo, dados los logros, experiencia acumulada y número de biopsias. Dado que se trata de uno de los registros más amplios y fiables del mundo debe seguir aportando datos para la mejoría de la práctica clínica y para el desarrollo de la investigación clínica. Conociendo la calidad y cantidad de centros participantes –pese a la ausencia de algunos de ellos– es seguro que su actividad no decaerá en próximos años.
Hospitales participantes y su provincia (por orden alfabético)
| Ciudad Sanitaria Virgen de la Nieves (Granada) |
| Clínica Quirón (Madrid) |
| Clínica Ruber (Madrid) |
| Clínica Universidad de Navarra (Navarra) |
| Clínica Vistahermosa (Alicante) |
| Complejo Asistencial de Palencia (Palencia) |
| Complejo Asistencial Universitario de Burgos (Burgos) |
| Complejo Asistencial Universitario de León (León) |
| Complejo Asistencial Universitario de Salamanca (Salamanca) |
| Complejo Hospitalario Arquitecto Marcide Novoa Santos Ferrol (A Coruña) |
| Complejo Hospitalario de Navarra (Pamplona) |
| Complejo Hospitalario Nuestra Sra. de la Candelaria (Tenerife) |
| Complejo Hospitalario Princesa de España (Jaén) |
| Complejo Hospitalario San Millán y San Pedro (La Rioja) |
| Complejo Hospitalario San Pedro de Alcántara (Cáceres) |
| Complejo Hospitalario Universitario A Coruña (A Coruña) |
| Complejo Hospitalario Universitario de Santiago (A Coruña) |
| Complejo Hospitalario Universitario Reina Sofía (Córdoba) |
| Complejo Universitario San Carlos (Madrid) |
| Consorci Corporació Sanitaria Parc Taulí de Sabadell (Barcelona) |
| Consorci Hospitalari de Terrassa (Barcelona) |
| Consorcio Hospital General Universitario de Valencia (Valencia) |
| Fundació Althaia Manresa (Barcelona) |
| Fundación Hospital Alcorcón (Madrid) |
| Fundación Hospital Manacor (Mallorca) |
| Fundación Puigvert (Barcelona) |
| Hospital 12 de Octubre Infantil (Madrid) |
| Hospital Arnau de Vilanova (Valencia) |
| Hospital Central de Asturias Infantil (Asturias) |
| Hospital Clinic i Provincial (Barcelona) |
| Hospital Clínico Universitario de Valencia (Valencia) |
| Hospital Clínico Universitario de Valladolid (Valladolid) |
| Hospital Clínico Universitario de Zaragoza (Zaragoza) |
| Hospital Clínico Universitario Virgen de la Victoria (Málaga) |
| Hospital Comarcal de Melilla (Melilla) |
| Hospital Comarcal Francesc De Borja (Valencia) |
| Hospital Costa del Sol Marbella (Málaga) |
| Hospital Cristal Piñor (Orense) |
| Hospital de Basurto (Bilbao) |
| Hospital de Bellvitge (Barcelona) |
| Hospital de Cruces (Bilbao) |
| Hospital de Cruces Infantil (Bilbao) |
| Hospital de Jerez (Cádiz) |
| Hospital de la Cruz Roja (Madrid) |
| Hospital de la Santa Creu i Sant Pau (Barcelona) |
| Hospital de León (León) |
| Hospital de Manises (Valencia) |
| Hospital de Navarra (Pamplona) |
| Hospital de Palamós (Gerona) |
| Hospital de Poniente El Ejido (Almería) |
| Hospital de Sagunto (Valencia) |
| Hospital de San Agustín Avilés (Asturias) |
| Hospital de Torrevieja Alicante (Alicante) |
| Hospital de Villajoyosa-Benidorm (Alicante) |
| Hospital de Zumárraga (Guipúzcoa) |
| Hospital del Aire (Madrid) |
| Hospital del Henares (Madrid) |
| Hospital del Mar (Barcelona) |
| Hospital del Mollet (Barcelona) |
| Hospital del Sureste (Madrid) |
| Hospital del Tajo (Madrid) |
| Hospital General de Elda (Alicante) |
| Hospital General de Especialidades Ciudad de Jaén (Jaén) |
| Hospital General de Granollers (Barcelona) |
| Hospital General de la Marina Alta de Denia (Alicante) |
| Hospital General de Segovia (Segovia) |
| Hospital General de Soria (Soria) |
| Hospital General Universitario de Albacete (Albacete) |
| Hospital General Universitario de Alicante (Alicante) |
| Hospital General Universitario de Castellón (Castellón) |
| Hospital General Universitario de Ciudad Real (Ciudad Real) |
| Hospital General Universitario de Elche (Alicante) |
| Hospital General Universitario de Guadalajara (Guadalajara) |
| Hospital General Universitario de Málaga Adultos (Málaga) |
| Hospital General Universitario de Málaga Infantil (Málaga) |
| Hospital General Universitario Gregorio Marañón Adultos (Madrid) |
| Hospital General Universitario Gregorio Marañón Infantil (Madrid) |
| Hospital Gral. Univ. Reina Sofía (Murcia) |
| Hospital GU Santa Lucía de Cartagena Infantil (Murcia) |
| Hospital Infanta Cristina (Madrid) |
| Hospital Infanta Elena (Madrid) |
| Hospital Infanta Leonor (Madrid) |
| Hospital Infanta Sofía (Madrid) |
| Hospital Militar de Zaragoza (Zaragoza) |
| Hospital Militar Gómez Ulla (Madrid) |
| Hospital Montecelo (Pontevedra) |
| Hospital Nuestra Señora de Sonsoles (Ávila) |
| Hospital Nuestra Señora del Prado de Talavera (Toledo) |
| Hospital Obispo Polanco (Teruel) |
| Hospital Provincial de Pontevedra (Pontevedra) |
| Hospital Público Lluis Alcanys de Xátiva (Valencia) |
| Hospital Público Virgen de los Lirios (Alicante) |
| Hospital Rafael Méndez (Murcia) |
| Hospital Regional de Málaga Infantil (Málaga) |
| Hospital Rey Juan Carlos, Móstoles (Madrid) |
| Hospital San Joan de Deu (Barcelona) |
| Hospital San Jorge (Huesca) |
| Hospital Santa María del Rosell (Murcia) |
| Hospital Santiago Apóstol (Vitoria) |
| Hospital Son Llàtzer (Mallorca) |
| Hospital Universitari de Girona Doctor Josep Trueta (Gerona) |
| Hospital Universitari Germans Trias i Pujol (Barcelona) |
| Hospital Universitario 12 de Octubre Adultos (Madrid) |
| Hospital Universitario Araba (Álava) |
| Hospital Universitario Central de Asturias (Oviedo) |
| Hospital Universitario de Badajoz (Badajoz) |
| Hospital Universitario de Cabueñes Gijón (Asturias) |
| Hospital Universitario de Canarias (Tenerife) |
| Hospital Universitario de Fuenlabrada (Madrid) |
| Hospital Universitario de Galdakao (Vizcaya) |
| Hospital Universitario de Getafe (Madrid) |
| Hospital Universitario de Gran Canaria Dr. Negrín (Gran Canaria) |
| Hospital Universitario de Granada (Granada) |
| Hospital Universitario de la Princesa (Madrid) |
| Hospital Universitario de Puerto Real (Cádiz) |
| Hospital Universitario Doctor Peset (Valencia) |
| Hospital Universitario Donostia (Guipúzcoa) |
| Hospital Universitario Fundación Jiménez Díaz (Madrid) |
| Hospital Universitario Infantil Niño Jesús (Madrid) |
| Hospital Universitario Insular de Las Palmas (Gran Canaria) |
| Hospital Universitario Joan XXIII (Tarragona) |
| Hospital Universitario Juan Ramón Jiménez (Huelva) |
| Hospital Universitario La Fe Adultos (Valencia) |
| Hospital Universitario La Fe Infantil (Valencia) |
| Hospital Universitario La Paz (Madrid) |
| Hospital Universitario La Paz Infantil (Madrid) |
| Hospital Universitario Lucus Augusti (Lugo) |
| Hospital Universitario Marqués de Valdecilla (Santander) |
| Hospital Universitario Miguel Servet (Zaragoza) |
| Hospital Universitario Miguel Servet Infantil (Zaragoza) |
| Hospital Universitario Nuestra Señora de Candelaria (Tenerife) |
| Hospital Universitario Nuestra Señora de Valme (Sevilla) |
| Hospital Universitario Príncipe de Asturias (Madrid) |
| Hospital Universitario Puerta de Hierro (Madrid) |
| Hospital Universitario Puerta del Mar (Cádiz) |
| Hospital Universitario Ramón y Cajal (Madrid) |
| Hospital Universitario Ramón y Cajal Infantil (Madrid) |
| Hospital Universitario Río Hortega (Valladolid |
| Hospital Universitario San Agustín (Oviedo) |
| Hospital Universitario Severo Ochoa (Madrid) |
| Hospital Universitario Son Espases (Mallorca) |
| Hospital Universitario Torrecárdenas (Almería) |
| Hospital Universitario Vall d’Hebrón (Barcelona) |
| Hospital Universitario Vall Hebrón Infantil (Barcelona) |
| Hospital Universitario Virgen de la Arrixaca (Murcia) |
| Hospital Universitario Virgen del Rocío (Sevilla) |
| Hospital Universitario Virgen Macarena (Sevilla) |
| Hospital Valle Del Nalón (Asturias) |
| Hospital Virgen de la Concha (Zamora) |
| Hospital Virgen de la Luz (Cuenca) |
| Hospital Virgen de la Salud (Toledo) |
| Hospital Virgen del Rocío Infantil (Sevilla) |
| Hospital Vithas Xanit Internacional Benalmádena (Málaga) |
| Hospital Xeral Cíes (Pontevedra) |
| Policlínica Miramar (Mallorca) |
| Policlínico de Vigo, SA (Pontevedra) |
| Sanatorio Perpetuo Socorro (Alicante) |