INTRODUCCIÓN
La enfermedad renal crónica se acompaña en la mayoría de los casos de hipertensión arterial (HTA) y es un importante factor de morbilidad y mortalidad en estos pacientes. Diversos fármacos pueden emplearse en su control y algunos han demostrado la posibilidad de disminuir o enlentecer la progresión del fallo renal y/o de la proteinuria. Los inhibidores de la enzima de conversión de angiotensina (IECAs) se han utilizado con éxito en la HTA de pacientes con nefropatía de etiología diabética y no diabética, reduciendo la proteinuria y con un efecto favorable sobre la progresión de la insuficiencia renal1-5. Se ha descrito algunos efectos secundarios con estos fármacos, entre los cuales la tos persistente es uno de los más frecuentes, y un problema añadido en pacientes con enfermedad renal crónica avanzada estadío 4 (ERCA 4)6, es que los IECAs pueden contribuir al empeoramiento de la función renal expresada por un incremento de la creatinina sérica hasta un 30-35% y producir hiperpotasemia7,8. También los fármacos bloqueantes de los receptores de angiotensina II (ARA II) han demostrado su efecto sobre la proteinuria y progresión de la función renal en pacientes con nefropatía diabética9-12 y con menores efectos adversos que los IECAs, pero existen muy pocos ensayos sobre su eficacia en la hipertensión, proteinuria, y progresión de la función renal de los pacientes con nefropatía no diabética13,14 o con ERCA establecida de causa no diabética15,16.
El irbesartan es un fármaco de la familia de los ARA II que ha demostrado su eficacia en el tratamiento de la HTA, incluso en pacientes con ERCA o en diálisis15,17. Es un fármaco que se absorbe rápidamente tras la administración oral, excretándose principalmente por vía hepática (78%) y en menor cantidad por vía renal (22%) con una vida media de 11 a 15 h18, no siendo necesario ajustar dosis en la ERCA19. Irbesartan ha mostrado efectos antiproteinúrico y de enlentecimiento de la progresión de la nefropatía diabética9,11.
En este trabajo realizamos un estudio de los efectos del tratamiento con irbesartan en pacientes con ERCA no diabéticos, analizando la eficacia antihipertensiva, acción sobre la proteinuria y la progresión de la enfermedad renal, y efectos sobre algunos parámetros bioquímicos, comparándolos con el tratamiento con IECAs en el mismo tipo de pacientes y con el mismo grado de afectación renal.
PACIENTES Y MÉTODOS
Pacientes
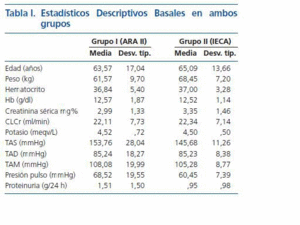
En el estudio longitudinal, no aleatorizado, se incluyeron 43 pacientes con ERCA de causa no diabética, en estadio IV de NKF-DOQI (aclaramiento de creatinina (CLCR) < de 30 ml/min), de forma prospectiva durante un año. Se trataron con irbesartan 21 pacientes (grupo I), a dosis iniciales de 150 mg una vez al día, aumentando a 300 mg también en monodosis cuando fue preciso para mejorar control de TA. En los pacientes que a dosis plenas de irbesartan (300 mg/día) no se conseguía el control de tensión arterial adecuado, se añadieron otros fármacos no ARA II y no IECAs. La edad media era de 6317 años, 12 mujeres y 9 hombres, con CLCR medio al comienzo del tratamiento de 22,1 (8,0) ml/min. El grupo II lo constituyen 22 pacientes que fueron tratados con IECAs (enalapril en 9, captopril en 7, perindopril en 6), comenzando con dosis diarias de 5 mg, 50 mg, y 2 mg respectivamente, e incrementando a dosis máximas de 20 mg, 100 mg, y 4 mg de enalapril, captopril y perindopril. En los pacientes que a esas dosis no se obtenía un control adecuado de la TA, se añadieron otros fármacos no IECAs, no ARA II. La edad media de los pacientes del grupo II era de 6513 años, 8 mujeres y 14 hombres, con CLCR inicial de 22,3 (7,0) ml/min. Los datos epidemiológicos basales de ambos grupos se muestran en la tabla I, sin diferencias estadisticas entre los dos grupos. No se incluyeron en ninguno de los dos grupos pacientes en tratamiento con diálisis, ni con sospecha de estenosis de arteria renal. Las causas de enfermedad renal en ambos grupos se muestran en la tabla II.
En ninguno de los grupos los pacientes habían recibido previamente medicación antihipertensiva con IECA o ARAII, ni tampoco medicación con resinas de intercambio iónico, o anti-inflamatorios no esteroideos durante el estudio. Un paciente en cada grupo tomaba alopurinol previamente al comienzo del estudio y continúo con la medicación. Tres pacientes (14%) en el grupo I y cuatro (18%) en el grupo II recibieron diuréticos, y el 14% en el GI y 13,6% en el GII recibieron calcio-antagonistas dihidropiridínicos como medicación antihipertensiva añadida a lo largo del estudio.
Métodos
En el diseño del estudio no se incluyó la aleatorización ni se calculó el tamaño muestral debido a que en la consulta externa acude un número reducido de pacientes de las características requeridas, lo que consideramos unas limitaciones del estudio y por tanto con sesgo observador dependiente, realizándose la práctica clínica diaria de aplicación de las guías clínicas.
Se realizó un seguimiento a un año con un control basal que incluía exploración física, con toma de TA arterial por la mañana en posición sentada, medida de presión de pulso, y estudio analítico. Durante el primer mes se realizaron controles quincenales de tensión arterial y ajuste de la medicación antihipertensiva. En los meses 3, 6, 9 y 12 se repitió el mismo esquema que en la visita basal. El incremento de dosis de irbesartan o IECAs a las dosis máximas marcadas se basó en la obtención de tensión arterial sistólica ≤ 140 mmHg y diastólica < 90 mmHg. Las determinaciones analíticas incluyeron creatinina, acido úrico y potasio séricos, y creatinina y proteinuria en orina de 24 horas (solo se hizo seguimiento de la proteinuria en los pacientes con ≥ 0,5 g/día en el control basal). Se calculó el ritmo de progresión de la insuficiencia renal en ml/min/mes de CLCR en ambos grupos. La tolerabilidad del tratamiento se comprobó con la aparición de reacciones adversas o alteraciones analíticas en cada visita.
El estudio estadístico se realizo con SPSS 11.5 (Chicago, Ill). Se comparan los resultados de la evaluación basal con los obtenidos a los 12 meses de seguimiento, con t-Student, Chicuadrado y test de Mann-Whitney según fue adecuado. La hipótesis nula fue rechazada cuando p < 0,05.
RESULTADOS
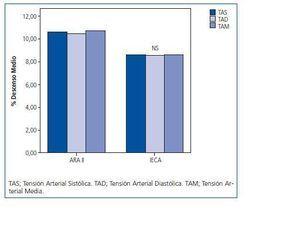
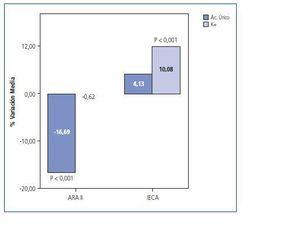
Todos los pacientes completan los 12 meses de tratamiento, sin que ninguno de los pacientes sea incluido en diálisis en el periodo de estudio. A los 12 meses de seguimiento, la TA se controló en el 57% de pacientes del grupo I solo con la administración de irbesartan frente al 39% de pacientes del grupo II solo tratado con IECAs, sin embargo el objetivo de control de tensión arterial establecido al comienzo del estudio se alcanzó en los dos grupos sin diferencias significativas tanto en la TAS, TAD y tensión arterial media (TAM), como se muestra en la figura 1. A los 12 meses con Irbesartan la tensión arterial sistólica media se reduce de 154 a 138 mm de Hg y la diastólica de 138 a 77 mm de Hg. Con IECAs se observa una disminución de la TAS de 146 a 133 mm de HG y de la TAD de diastólica de 85 a 77 mm de Hg. La TAM se reduce un 10,7% con irbesartan y un 8,5% con IECAs. La presión de pulso desciende igualmente en el grupo de irbesartan y en el tratado con IECAs sin diferencia entre ambos (7,2% vs 8,3%). En la figura 2 se muestra el comportamiento de los niveles séricos de K que no se modifican desde sus valores básales en el grupo I, con un incremento de un 10% en el grupo II (p < 0,001). El AC. Úrico aumenta un 4% respecto a sus valores basales en el grupo tratado con IECAs, mientras que se reduce en un 17% en los pacientes incluidos en tratamiento con irbesartan (p < 0,001) (fig. 2). No se observaron diferencias en la reducción de la función renal, progresando la insuficiencia renal por igual en los dos grupos. El descenso del CLCR a lo largo del estudio fue de 0,23 ml/min/mes en el grupo I y 0,21 ml/min/mes en el grupo II (NS).
La excreción media de proteínas en 24 h desciende a los 12 meses en los pacientes tratados con irbesartan de 2,1 g/día a 1,3 gr/día, con diferencia significativa respecto al grupo de IECAs donde apenas se reduce la proteinuria 1,35 g/día a 1,33 g/día (p = 0,041).
El tratamiento con irbesartan y con IECAs ha sido bien tolerado por los pacientes, sin que ningún paciente tuviera que ser retirado del estudio por reacciones adversas, alteraciones bioquímicas importantes o alcanzar valores de CLCR que hicieran preciso su inclusión en diálisis. Los incrementos moderados en los niveles de K sérico en alguna de las analíticas de los controles periódicos no obligo al abandono del estudio en ningún paciente. En un paciente del grupo II que meses antes había sido tratado con captopril y al que se le suspendió el fármaco por tos persistente, la tos continuo tras la retirada de la medicación y al comenzar el estudio fue incluido en el grupo de enalapril, con persistencia de la tos, sin que se pudiera valorar su relación con la toma del IECA. Dos pacientes más del grupo II presentaron tos no intensa y prefirieron continuar con el tratamiento. TAS inferiores a 100 mm de Hg se objetivaron en alguna toma en 2 pacientes del grupo I y en 1 del grupo II sin repercusión clínica que obligase a suspender los fármacos en estudio.
DISCUSIÓN
La mayoría de los estudios realizados con ARA II en pacientes hipertensos y con afectación renal se han hecho en nefropatía diabética9-12. Los resultados sobre el control de la HTA, así como sobre la proteinuria y progresión de la nefropatía han sido tan favorables como los reportados con IECAs en pacientes diabéticos y no diabéticos1-5. En nuestro trabajo se demuestra la eficacia antihipertensiva de un ARA II de vida media larga como el irbesartan en pacientes no diabéticos con hipertensión leve-moderada y enfermedad renal crónica avanzada seguidos en una consulta específica, con resultados similares a los obtenidos con IECAs en pacientes con iguales características y con mayor efecto sobre los niveles séricos de a. úrico, potasio y proteinuria que estos. En un uno de los pocos estudios publicados donde de incluye un subgrupo de pacientes con ERCA de etiología no diabética tratados con irbesartan y seguidos durante 3 meses, se obtienen resultados similares a los nuestros respecto a control tensional y descenso de la proteinuria, incluso en monoterapia15.
El nuestro es un estudio realizado en un solo centro con pacientes procedentes de la consulta de enfermedad crónica avanzada, con la dificultad que supone el reclutamiento de pacientes con ERCA próximos a su inclusión en técnicas de diálisis y que puedan ser seguidos un periodo largo para ver la eficacia del tratamiento antihipertensivo, y de ahí las limitaciones del estudio. A pesar de estas limitaciones, el seguimiento de 12 meses nos ha permitido analizar la evolución de la progresión de la insuficiencia renal y comprobar que no es diferente con el empleo de IECAs o de irbesartan (-0,21 y -0,23 ml/min/mes respectivamente) y similares a las ya publicadas. Tasas de progresión de enfermedad renal de -0,46 ml/min/mes de CLCR se han descrito en pacientes con enfermedad renal crónica no diabética tratados con medicación antihipertensiva estándar20. Esta tasa de progresión se reduce hasta -0,23/ml/min/mes cuando, de forma randomizada, se trata con fármacos como captopril o nifedipino20. Nuestros resultados, parecen indicar que la reducción en la progresión de la insuficiencia renal que se obtiene con IECAs o con un ARA II como el irbesartan se produce también cuando la enfermedad renal se encuentra en grados muy avanzados como es el caso de los pacientes incluidos en este estudio, en los que en los 12 meses de seguimiento ningún paciente preciso tratamiento con diálisis. Es posible que la falta de diferencia en la progresión de la enfermedad renal en uno y otro grupo este en relación con el pequeño número de pacientes de la muestra.
El irbesartan ha demostrado un efecto antiproteinúrico en nefropatía diabética en estudios amplios como el IRMA9 o el IDNT11, de forma similar a otros ARA II como el losartan (estudio RENAAL)10 o el valsartan (estudio MARVAL)12. En la nefropatía no diabética, estudios con menor numero de pacientes, han demostrado este mismo efecto sobre la proteinuria con losartan14,21. Todos estos estudios incluían pacientes con grados leves de insuficiencia renal y en la mayoría de ellos el beneficio sobre la función renal era independiente del control de tensión arterial10,12,14,21. La mayor respuesta sobre la proteinuria del irbesartan frente a IECAs observada en nuestros pacientes, tiene la peculiaridad de darse en sujetos no diabéticos con ERCA. En un grupo de pacientes de las mismas características, evaluados a tres meses, De Rosa y cols.15, describen la disminución de la proteinuria con irbesartan respecto a valores basales.
El conocido efecto de elevación de los niveles de potasio sérico en algunos pacientes con fallo renal tratados con IECAs, se ha extendido a los ARA II por la inhibición del sistema renina-angiotensina que se produce con ambas familias de fármacos8. Nuestros resultados muestran el diferente comportamiento respecto al potasio sérico empleando IECAs o irbesartan en enfermos con ERCA, observándose un incremento del 10% con los primeros frente a un mantenimiento de los valores de potasio con el ARA II. Bakris y cols.22 han descrito resultados semejantes al comparar Lisinopril (IECA) con valsartan (ARA II) en pacientes con filtrado glomerular inferior a 60 ml/min, relacionando la elevación significativa del potasio producida por el lisinopril con una relativamente menor reducción de la aldosterona plasmática con el ARA II. No sabemos si en nuestros pacientes con mayor afectación de la función renal seria aplicable esta hipótesis. Las dosis de IECAs y ARA II empleadas en nuestros pacientes son dosis habituales, no muy elevadas en razón del grado de su enfermedad renal, pero ya hay trabajos utilizando grandes dosis de candersartan (5 veces más altas que las máximas habituales) en enfermedad renal crónica sin que se modifiquen los valores basales de potasio sérico23. Otro de los hallazgos de nuestro estudio es la reducción en el tiempo de los niveles séricos de ácido úrico con irbesartan que no se obtienen en el grupo de pacientes tratados con IECAs. Existen varios trabajos que han descrito el descenso del ácido úrico con el empleo de losartan24-26. Esta acción del losartan parece ser temporal y en relación con un efecto uricosúrico. En un estudio donde se compara losartan con enalapril en sujetos sanos, el IECA no demuestra efectos en el aclaramiento fraccional de ácido úrico y si lo hace el ARA II24. La comparación del efecto uricosúrico del losartan frente a otros ARA II ofrece resultados controvertidos, y mientras en el trabajo de Wurzner y cols.25 con pacientes hiperuricémicos (comparando losartan con irbesartan) se obtiene un descenso del ácido úrico solo con el primero. en otro estudio26 con pacientes con HTA leve o moderada, el losartan comparado con eprosartan incrementa la excreción urinaria de ácido úrico pero ninguno de los dos ARA II producen cambios en los niveles séricos de ácido úrico. Nuestro estudio no incluye datos sobre la excreción renal de acido úrico, que pueda aclarar la causa de la reducción de los niveles séricos con la toma de irbesartan, aunque el seguimiento de los pacientes se ha realizado a más largo plazo que en los estudios mencionados y en pacientes con afectación importante de la función renal.
En conclusión, nuestros resultados, con las correspondientes limitaciones enumeradas, muestran que con una eficacia antihipertensiva similar y un comportamiento semejante en la evolución de la función renal, irbesartan reduce la proteinuria en mayor grado que IECAs, sin elevación del potasio sérico y con una disminución significativa de los valores de ácido úrico en pacientes con enfermedad renal crónica avanzada de etiología no diabética.
Tabla 1.
Figura 1.
Figura 2.