La viruela del mono es una infección zoonótica previamente endémica en África, que se ha ido extendiendo a otros continentes en los últimos meses. La transmisión ocurre a través del contacto directo con la piel lesionada, las mucosas, las gotas respiratorias y a través de fómites contaminados. Las manifestaciones clínicas más habituales incluyen fiebre, lesiones cutáneas y linfadenopatías. Debe sospecharse en un paciente con lesiones compatibles y factores de riesgo epidemiológicos, y la confirmación se realiza mediante la detección de ADN viral con la técnica de reacción en cadena de la polimerasa (PCR)1. El manejo principal se basa en proporcionar medidas de soporte y tratamiento sintomático. Sin embargo, en determinados pacientes pueden emplearse antivirales como tecovirimat. Presentamos el caso de un paciente trasplantado renal diagnosticado de infección por viruela del mono con afectación grave.
Se trata de un varón de 26 años, trasplantado renal en enero de 2021, con una creatinina basal de 2,3-2,6mg/dL sin proteinuria. Su nefropatía de base es secundaria a un síndrome hemolítico urémico atípico (SHUa), en tratamiento con eculizumab. Desde el trasplante el paciente ha presentado dos episodios de rechazo humoral agudo en el primer y sexto mes, por mala adherencia al tratamiento. Actualmente se encuentra en tratamiento con tacrolimus, micofenolato mofetilo y prednisona.
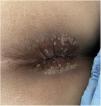
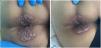
Acude a Urgencias por fiebre de 4 días de evolución, dolor en región anal y diarrea sin productos patológicos. Refiere haber mantenido relaciones sexuales por vía anal sin utilizar preservativo. Presenta lesiones papulares en la región perianal (fig. 1), en el tronco y en el abdomen. No presenta adenopatías palpables ni dolor abdominal. En los análisis realizados se objetiva leucocitosis con neutrofilia y elevación de los reactantes de fase aguda (RFA): proteína C reactiva 29,7mg/dL y procalcitonina 5,7mg/dL. Se solicita PCR de viruela del mono en exudado cutáneo y sangre, siendo ambas positivas. Decidimos reducir a la mitad la dosis diaria de micofenolato e ingresar al paciente, pero cursa alta voluntaria 48h después.
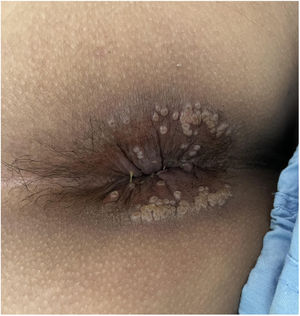
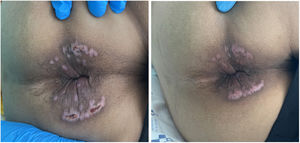
Al cabo de 4 semanas acude nuevamente a Urgencias por diarrea y rectorragia franca. Presenta lesiones ulceradas exudativas en todo el margen perianal (fig. 2), mientras que las del resto de localizaciones están en proceso de resolución. Dada la mala evolución clínica y la sospecha de proctosigmoiditis se cursa una solicitud a la AEMPS (Agencia Española de Medicamentos y Productos Sanitarios) para iniciar tratamiento con tecovirimat, que es aprobada.
Tras 7 días de tratamiento se realiza una colonoscopia en la que se observan dos lesiones equimóticas y úlceras cubiertas con fibrina en el canal anal en proceso de cicatrización. Las lesiones de la región perianal se encontraban en fase de resolución (fig. 2) y la rectorragia había cedido. Se realiza nueva PCR de viruela del mono en las muestras obtenidas, que es negativa. Dada la buena evolución y la falta de disponibilidad del fármaco al tratarse de medicación extranjera, el paciente completa 7 días de tratamiento con tecovirimat en lugar de los 14 días habitualmente recomendados y es dado de alta.
Se describe el primer caso en nuestro centro de un paciente trasplantado renal con infección por viruela del mono, no habiendo encontrado en la literatura otros casos publicados a día de hoy. Dada la mala evolución clínica se administró tratamiento con tecovirimat tras ser aprobada la solicitud por la AEMPS. Se trata del fármaco de elección para el tratamiento de la viruela del mono2. A pesar de no disponer de ensayos clínicos que determinen la eficacia en humanos, los estudios en primates han demostrado una mayor supervivencia en aquellos que recibieron tecovirimat en comparación con los que recibieron placebo, incluso cuando el fármaco se administraba tras la aparición de complicaciones graves. Los efectos secundarios más frecuentes son cefalea, náuseas y dolor abdominal. Se administró a aproximadamente 360 voluntarios humanos en un ensayo de seguridad ampliado, que encontró un perfil de efectos adversos similar al del placebo3. No se puede descartar que disminuya los niveles de tacrolimus, al actuar como inductor del citocromo CYP3A4, si bien en el caso de nuestro paciente los niveles en sangre permanecieron estables durante el tratamiento.
Como fármaco de segunda línea se encuentra el cidofovir. Aunque tiene actividad in vitro contra la viruela símica y ha demostrado ser eficaz en modelos animales, no hay datos clínicos sobre su eficacia en humanos en el momento actual y su uso puede estar asociado con eventos adversos significativos, como la nefrotoxicidad y/o hepatotoxicidad4. El brincidofovir es una modificación que también ha mostrado actividad in vitro y en ensayos con primates. Las ventajas radican en su administración por vía oral y en su reducida nefrotoxicidad5.
En el caso descrito, el paciente presentó una evolución clínica satisfactoria sin efectos secundarios y sin interacciones con el tacrolimus durante todo el tratamiento.