El líquido de diálisis (LD), elemento esencial en la hemodiálisis (HD), se fabrica in situ mezclando 3 componentes: agua tratada, concentrado de bicarbonato y concentrado ácido. Para evitar la precipitación de carbonato cálcico y magnésico que se produce en el LD por la adición de bicarbonato, es necesario añadir un ácido. Existen 2 concentrados ácidos según contengan acetato (LDA) o citrato (LDC) como estabilizante.
ObjetivoComparar el efecto agudo de la HD con LDC vs. LDA sobre el metabolismo del calcio, fosforo y magnesio, el equilibrio ácido base, la coagulación, inflamación y la estabilidad hemodinámica.
MétodosEstudio prospectivo, multicéntrico, aleatorizado y cruzado, de 32 semanas de duración, en pacientes en HD trisemanal, monitor AK-200-Ultra-S o Artis, 16 semanas con LDA SoftPac®, elaborado con 3mmol/l de acetato, y 16 semanas con LDC SelectBag Citrate®, con 1mmol/l de citrato. Se incluyeron pacientes mayores de 18 años en HD durante un mínimo de 3 meses mediante fístula arteriovenosa. Se recogieron datos epidemiológicos, de diálisis, bioquímica pre- y posdiálisis, episodios de hipotensión arterial, y scores de coagulación mensualmente durante los 8 meses de estudio. Se extrajeron pre- y posdiálisis: gasometría venosa, calcio (Ca), calcio iónico (Cai), fósforo (P), magnesio (Mg) y hormona paratiroidea (PTH), entre otros.
ClinicalTrials.gov NCT03319680.
ResultadosSe incluyeron 56 pacientes, 47 (84%) hombres y 9 (16%) mujeres de edad media: 65,3 (16,4) años, técnica HD/HDF: 20 (35,7%)/36 (64,3%).
Encontramos diferencias (p<0,05) cuando utilizamos el LD con citrato (C) frente a acetato (A) en los valores posdiálisis de bicarbonato [C: 26,9 (1,9) vs. A: 28,5 (3) mmol/l], Cai [C: 1,1 (0,05) vs A: 1,2 (0,08) mmol/l], Mg [C. 1,8 (0,1) vs A: 1,9 (0,2) mg/dl] y PTH [C: 255 (172) vs. 148 (149) pg/ml]. No encontramos diferencias en ninguno de los parámetros medidos prediálisis. Se registraron menos episodios de hipotensión arterial durante las sesiones con el LDC; de las 4.416 sesiones de HD, 2.208 en cada grupo, cursaron con hipotensión 311 sesiones (14,1%) con LDA y 238 (10,8%) con LDC (p<0,01). También fue menor la caída de volumen sanguíneo máximo medido por biosensor Hemoscan® [−3,4(7,7) vs. −5,1 (8,2)], aunque sin significación estadística.
ConclusiónLa diálisis con citrato produce de forma aguda menor alcalemia posdiálisis y modifica de forma significativa el Ca, el Mg y la PTH. El LDC tiene un impacto positivo sobre la tolerancia hemodinámica.
Dialysis fluid (DF), an essential element in hemodialysis (HD), is manufactured in situ by mixing three components: treated water, bicarbonate concentrate and acid concentrate. To avoid the precipitation of calcium and magnesium carbonate that is produced in DF by the addition of bicarbonate, it is necessary to add an acid. There are 2 acid concentrates that contain acetate (ADF) or citrate (CDF) as a stabilizer.
ObjectiveTo compare the acute effect of HD with CDF vs. ADF on the metabolism of calcium, phosphorus and magnesium, acid base balance, coagulation, inflammation and hemodynamic stability.
MethodsProspective, multicenter, randomized and crossed study, of 32 weeks duration, in patients in three-week HD, AK-200-Ultra-S or Artis monitor, 16 weeks with ADF SoftPac®, prepared with 3mmol/L of acetate, and 16 weeks with CDF SelectBag Citrate®, with 1mmol/L of citrate. Patients older than 18 years were included in HD for a minimum of 3 months by arteriovenous fistula. Epidemiological, dialysis, pre and postdialysis biochemistry, episodes of arterial hypotension, and coagulation scores were collected monthly during the 8 months of the study. Pre and post-dialysis analysis were extracted: venous blood gas, calcium (Ca), ionic calcium (Cai), phosphorus (P), magnesium (Mg) and parathyroid hormone (PTH) among others.
ClinicalTrials.gov NCT03319680.
ResultsWe included 56 patients, 47 (84%) men and 9 (16%) women, mean age: 65.3 (16.4) years, technique HD/HDF: 20 (35.7%)/36 (64.3%).
We found differences (p<0.05) when using the DF with citrate (C) versus acetate (A) in the postdialysis values of bicarbonate [C: 26.9 (1.9) vs. A: 28.5 (3) mmol/L], Cai [C: 1.1 (0.05) vs. A: 1.2 (0.08) mmol/L], Mg [C: 1.8 (0.1) vs A: 1, 9 (0.2) mg/dL] and PTH [C: 255 (172) vs. 148 (149) pg/mL]. We did not find any differences in any of the parameters measured before dialysis. Of the 4,416 sessions performed, 2,208 in each group, 311 sessions (14.1%) with ADF and 238 (10.8%) with CDF (p<0.01), were complicated by arterial hypotension. The decrease in maximum blood volume measured by Hemoscan® biosensor was also lower [−3.4 (7.7) vs −5.1 (8.2)] although without statistical significance.
ConclusionDialysis with citrate acutely produces less postdialysis alkalemia and significantly modifies Ca, Mg and PTH. CDF has a positive impact on hemodynamic tolerance.
El líquido de diálisis (LD) es un elemento esencial en la diálisis, ya que durante la misma se producen distintas transferencias entre líquido y paciente. Por ello, la composición física, microbiológica y química del LD es fundamental para el éxito o fracaso del tratamiento. Las recomendaciones de pureza y calidad del LD se recogen en las Guías de gestión de calidad del líquido de diálisis de la Sociedad Española de Nefrología1.
Desde el punto de vista técnico, para evitar la precipitación de carbonato cálcico y magnésico que se produce en el LD al añadir bicarbonato, es necesario añadir un ácido, de forma que se utiliza un sistema de generación de LD con 2 concentrados, uno con el bicarbonato y el otro con el ácido. El ácido utilizado habitualmente es el acético, a unas concentraciones que oscilan entre los 3 y 10mmol/l. Esta pequeña cantidad hace que se transfiera acetato al paciente durante la hemodiálisis (HD), elevando su concentración en sangre, ya que el LD tiene concentraciones 30-40 veces superiores a los valores normales en sangre (0,1mmol/l). Esta exposición al acetato aumenta en técnicas de hemodiafiltración online (HDF-OL)2 debido a la mayor cantidad de líquido infundido. Entre los efectos secundarios descritos con el acetato cabe destacar, por su importancia durante la HD, la inestabilidad hemodinámica producida por la vasodilatación mediada por la liberación de óxido nítrico3 y la activación de citoquinas proinflamatorias por la hipoxia4. Aun comparado con un LD con pequeñas concentraciones de acetato (3mmol/l), se ha descrito un menor riesgo de complicaciones hemodinámicas cuando los pacientes se dializan con LD libre de acetato5.
Por ello, desde hace años se han buscado otros ácidos como estabilizantes del LD. Los primeros intentos de sustitución del acetato se realizaron con ácido clorhídrico. Con ese LD se modificaba la relación concentración de sodio y conductividad, produciendo cambios en los iones séricos de modo que era necesario cambiar las conductividades total y parcial de bicarbonato no estando su forma de uso claramente estandarizada.
El LD con citrato (LDC) fue desarrollado para mejorar la biocompatibilidad sustituyendo el ácido acético por otro más fisiológico, el cítrico. El citrato es un quelante del calcio (Ca) que se usa por su efecto anticoagulante al disminuir el calcio iónico (Cai). Se estima que produce una disminución de un 10% del Cai, por ello la mayoría de los autores recomiendan, cuando se utiliza citrato como ácido, suplementar el calcio del LD para corregir estas diferencias. Según demostraron Steckiph et al.6, por cada mmol de citrato, la concentración de calcio debe aumentar 0,15mmol/l para mantener el balance de calcio durante el tratamiento y prevenir la hipocalcemia. La utilización del LDC está aumentando y es hoy en día, al menos en España, una opción terapéutica. Existen 2 LDC, uno exento de acetato, que es con el que hemos realizado este trabajo, el SelectBag Citrate®, con 1mmol/l de citrato, y otro con pequeñas cantidades de acetato, el Citrasate®, que contiene 0,3mmol/l de acetato y 0,8mmol/l de citrato. Aunque el LDC está comercializado desde hace más de 15 años, inicialmente en EE.UU.7 la información sobre los posibles efectos tanto metabólicos como de coagulación o hemodinámicos basados en estudios aleatorizados es limitada. Se han descrito varios efectos beneficiosos a largo plazo en relación con el citrato, como son una menor trombogenicidad8, mejoría de los aclaramientos9,10, de la inflamación11, nutrición12, tolerancia13, y del control ácido-base con menor acidosis prediálisis14. Nuestro estudio multicéntrico, aleatorizado y controlado tiene como objetivo aportar evidencia a algunas de estas cuestiones.
El citrato es usado como anticoagulante en otras terapias distintas a la HD, como son las terapias continuas. Monchi et al.15 concluyen que la anticoagulación con citrato se mostró superior a la heparina en el tiempo de vida del dializador y en los requerimientos transfusionales de los pacientes de Cuidados Intensivos tratados con terapias sustitutivas continuas, en las que la concentración de citrato es mucho mayor que la utilizada en el LD. No obstante, el citrato del LD se une al calcio circulante en plasma, reduciendo el calcio necesario para la cascada de la coagulación, pudiendo precisarse menos dosis de heparina8 y favoreciendo que el dializador mantenga su superficie útil obteniendo un mejor aclaramiento y una mejor eficacia dialítica. Conviene pues constatar tanto los potenciales beneficios de este efecto anticoagulante como el impacto del LDC en la tolerancia hemodinámica, equilibrio ácido base y metabolismo fosfocálcico.
ObjetivoComparar el efecto agudo de la HD con LDC vs. LDA sobre el equilibrio ácido base, el metabolismo del calcio, fosforo y magnesio, la eficacia dialítica, la coagulación, la inflamación y la estabilidad hemodinámica.
Material y métodosDiseño del estudioEstudio prospectivo, multicéntrico, aleatorizado y cruzado, realizado en 8 Unidades de Hemodiálisis españolas. Todos los pacientes firmaron el consentimiento informado. El protocolo de estudio fue aprobado por el Comité de investigación Clínica de la Comunidad de Madrid y de los centros participantes, y se llevó a cabo de acuerdo con la Declaración de Helsinki (ClinicalTrials.gov, NCT03319680).
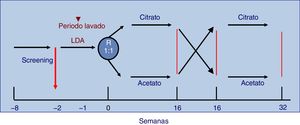
Estudio de 32 semanas de duración, en pacientes en HD trisemanal, monitor AK-200-Ultra-S o Artis. Los pacientes fueron asignados aleatoriamente para recibir 16 semanas consecutivas con LDC, SelectBag Citrate®, con 1mmol/l de citrato, seguida o precedida por otras 16 semanas con LDA, SoftPac®, elaborado con 3mmol/l de acetato. Antes del proceso de aleatorización todos los pacientes se dializaron durante 2 semanas con LDA. Cada paciente sirvió como control de sí mismo y no se realizaron modificaciones de la pauta de diálisis durante el estudio a excepción del LD, siguiéndose la pauta habitual de trabajo. El diseño del estudio se muestra en la figura 1.
Se incluyeron pacientes mayores de 18 años en HD durante un mínimo de 3 meses mediante fístula arteriovenosa (nativa o protésica), que firmaron el consentimiento informado. Los criterios de exclusión fueron alergia o intolerancia al citrato, enfermedades inflamatorias intercurrentes, HD mediante catéter y deterioro cognitivo. En el diseño del estudio, dado que uno de los objetivos era valorar la eficacia dialítica y la duración del estudio de 32 semanas, se decidió excluir a los pacientes con catéter por la posibilidad de disfunción del mismo y la posible pérdida.
Las características del líquido dializante con citrato y acetato se muestran en la tabla 1. Se utilizaron dos concentraciones de calcio, en función de las concentraciones que en condiciones de práctica clínica habitual se utilizara en el paciente antes del inicio del estudio: si calcio previo en el LDA de 1,25 o 1,50mmol/l, se utilizaron concentraciones de calcio mayores con LDC, siendo de 1,50 y 1,65mmol/l, respectivamente. Se recogieron:
Características del líquido dializante con citrato y acetato
| Acetato | Citrato | |
|---|---|---|
| Sodio, mEq/l | 140 | 140 |
| Potasio, mEq/l+ | 1,5/2 | 2 |
| Calcio, mmol/l* | 1,25/1,50 | 1,50/1,65 |
| Magnesio, mEq/l | 0,50 | 0,50 |
| Cloro, mEq/l, | 109,5 | 106,5 |
| Citrato, mEq/l | 0 | 1 |
| Acetato, mEq/l | 3 | 0 |
| Bicarbonato, mEq/l | 34 | 34 |
Parámetros demográficos y de diálisis: edad, enfermedad de base, peso, tiempo en tratamiento renal sustitutivo (TRS) y la función renal residual (FRR) definida previamente16, técnica de diálisis: HD de alto flujo (HD-HF) o hemodiafiltración en línea (HDF-OL), flujo sanguíneo (Qb), conductividades de sodio y bicarbonato, temperatura del líquido, volúmenes de infusión en HDF-OL (posdilución), el Kt medido automáticamente por el biosensor Diascan®, ganancia de peso interdiálisis (GID), caída máxima de volumen sanguíneo (CMVS) durante la sesión, medida mediante el biosensor Hemoscan®, la ultrafiltración (UF) por sesión y la presión arterial (PA) pre- y posdiálisis.
También se recogieron el número de hipotensiones definidas como toda disminución aguda de la presión arterial que precise la intervención del personal de enfermería.
Determinaciones analíticas. Todas las muestras de sangre se realizaron en el día intermedio de la semana, obtenidas a través de la línea arterial del acceso vascular, las prediálisis extraídas inmediatamente antes de iniciar la técnica y posdiálisis después de disminuir el Qb a 50ml/min durante 60 segundos en el momento de finalizar la sesión.
En sangre se determinaron: parámetros ácido-base mediante gasometría venosa (pH, bicarbonato y exceso de base en el líquido extracelular (BEecf)); parámetros bioquímicos [sodio (Na), cloro (Cl), Ca (calcio total), Cai (calcio iónico), fósforo (P), hormona paratiroidea (PTH), urea, beta2 microglobulina (β2m), albúmina y prealbúmina]; hemograma y coagulación.
Los métodos utilizados fueron los habituales en los laboratorios de los distintos centros, no modificándose ningún método durante el estudio.
Para evaluar el estado nutricional, además de las determinaciones se analizó la composición corporal mediante bioimpedancia multifrecuencia (BCM®). Las medidas se realizaron inmediatamente antes del inicio de la sesión de diálisis en la sesión intermedia (miércoles o jueves). Para ello, los pacientes permanecieron en decúbito supino durante 10min, sin objetos metálicos. Los electrodos se colocaron en el hemicuerpo contralateral al acceso vascular. Se recogieron los datos de hidratación (OH) y de composición corporal: índice de tejido graso (FTI) e índice de tejido magro (LTI), definidos respectivamente como tejido graso y magro ajustado a la superficie corporal del paciente (kg/m2).
Para evaluar el estado de inflamación los niveles de proteína C reactiva (PCR) y el índice de resistencia a eritropoyetina (equivalente a EPOalfa) (IRE) mediante la fórmula: IRE=Dosis de EPO(U/kg/sem)/Hb(g/dl).
Para estudiar el efecto del LDC sobre la coagulación se incluyeron dos scores de coagulación. Una escala visual del dializador que tenía el personal de enfermería con 5 grados en función del porcentaje de fibras coaguladas al final de la sesión de diálisis: 0 si no se observaban, 1 si eran menores del 25%, 2 del 25 al 50%, 3 del 50 al 75% y 4 si la coagulación de las fibras del dializador era del 75-100% con imposibilidad para continuar la diálisis. El score de coagulación de las cámaras tenía 4 grados: 0 si estaban limpias, 1 si la coagulación era mínima (anillo de fibrina), 2 cuando aparecía un coágulo (hasta 5cm) pero la diálisis era posible, y 3 cuando se producía una oclusión completa que impedía la diálisis. Los scores de coagulación de cámaras y dializador se representan en la figura 2. También se recogió el tiempo de hemostasia, cuantificándose los minutos que se precisaban para la coagulación del acceso vascular.
Análisis estadísticoEl análisis estadístico se realizó con el programa SPSS 15.0 (SPSS INC., Chicago IL, EE.UU.). Los datos descriptivos se presentan como la media y desviación estándar (DE).
Para la comparación de dos variables continuas independientes se utilizó el test de la t de Student para muestras apareadas. Para la comparación de más de dos variables cuantitativas se utilizó el ANOVA. La p<0,05 fue considerada como estadísticamente significativa.
El estudio fue registrado en ClinicalTrials.gov NCT03319680.
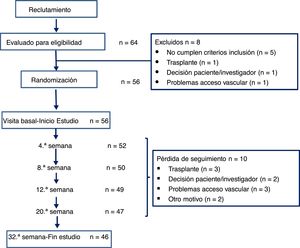
ResultadosDe 64 pacientes evaluados inicialmente en 8 Unidades de Hemodiálisis españolas en 2015, se incluyen 56 pacientes en HD que cumplían los criterios de inclusión. El diagrama de flujo que ilustra el progreso de los pacientes durante el ensayo se representa en la figura 3. Su edad media era 65,3 (16,4) [23-93] años, 47 hombres y 9 mujeres, con un índice de Charlson ajustado de 6,2 (2,5). La etiología de la ERC era en 16 glomerulonefritis, en 10 diabetes, en 9 enfermedad vascular, en 4 hereditarias, en 4 nefritis intersticial, en 9 otras causas y en 4 etiología desconocida. De los pacientes incluidos, 51 (91,1%) se dializaban con fístula arteriovenosa (FAV) nativa y 5 (8,9%) con FAV protésica.
Se dializaban en HDF-OL 36 y 20 en HD-HF.
La aleatorización asignó 29 pacientes al LDA y 27 al LDC; a las 16 semanas los pacientes cambiaron de LD durante otras 16 semanas. En la tabla 2 se describen las características basales de los pacientes según el grupo al que fueron asignados.
Características basales de los pacientes según el grupo al que fueron asignados en la aleatorización LDA/LDC (N=56)
| Características | LDA (29 pacientes) | LDC (27 pacientes) | p |
|---|---|---|---|
| Demográficas | |||
| Edad (años) (DT) | 63,5 (18,3) | 67,1 (14,1) | 0,409 |
| Sexo (H/M) | 22/7 | 25/2 | 0,089 |
| Peso (kg) | 67,1 (12,5) | 72,1 (11,9) | 0,133 |
| Estatura (cm) | 163,6 (8,3) | 167,8 (8,2) | 0,056 |
| Diabetes (n.o) | 4 | 6 | |
| Charlson ajustado | 6,2 (2,6) | 6,2 (2,4) | 0,934 |
| Tiempo en TRS (meses) | 100,0 (134,9) | 95,7 (101,1) | 0,894 |
| Parámetros de HD | |||
| Acceso vascular (FAV%) | 100% | 100% | 1 |
| HD / HDF-OL | 10 / 19 | 10 / 17 | 0,531 |
| PAS preHD (mmHg) | 137,1 (24,1) | 132,9 (24,7) | 0,524 |
| PAD preHD (mmHg) | 73,7 (14,4) | 68,2 (11,4) | 0,122 |
| Kt (l) | 53,0 (7,6) | 53,9 (8,8) | 0,689 |
| Qb (ml/min) | 394,7 (47,1) | 387,4 (52,3) | 0,587 |
| Qd (ml/min) | 514,8 (45,6) | 514,8 (36,2) | 1 |
| Bioimpedancia | N=20 | N=18 | |
| LTI (kg/m2) | 12,1 (2,8) | 13,9 (3,2) | 0,055 |
| FTI (kg/m2) | 12,6 (5,5) | 12,7 (4,7) | 0,96 |
| V (medido en l) | 37,3 (4,2) | 37,1 (4,3) | 0,92 |
| VEX (l) | 15,5 (3,9) | 16,0 (5,0) | 0,73 |
FAV: fistula arteriovenosa; FTI: índice de masa grasa; HD: hemodiálisis; HDF-OL: hemodiafiltración en línea; LDA: líquido de diálisis con acetato; LDC: líquido de diálisis con citrato; LTI: índice de masa magra; PAD: presión arterial diastólica; PAS: presión arterial sistólica; Qb: flujo sanguíneo; Qd: flujo del líquido de diálisis; TRS: tratamiento renal sustitutivo; V: volumen del agua corporal; VEX: volumen extracelular.
Los resultados que vamos a presentar corresponden al efecto agudo del LD, que nosotros consideramos como el que se produce durante la sesión de diálisis, como son las hipotensiones o la coagulación, y en el caso de las determinaciones analíticas, a la diferencia en los valores pre- y posdiálisis analizados. Para ello hemos tomado los resultados de la visita basal que corresponden a los valores pre/posdiálisis después del periodo de lavado con acetato, una vez realizada la aleatorización y que corresponde a 56 pacientes. Comentaremos posteriormente en alguno de los resultados estos valores pre/post a lo largo del estudio.
En la tabla 3 figuran los valores prehemodiálisis de los parámetros del equilibrio ácido base, bioquímicos, PTH, y hematológicos en los dos grupos LDA y LDC. Así mismo, se muestran los valores posthemodiálisis de los parámetros del equilibrio ácido base, algunos bioquímicos y PTH.
Datos de laboratorio, pre- y posthemodiálisis, en 56 pacientes con LDA o LDC
| Prehemodiálisis | Posthemodiálisis | Significación | ||||
|---|---|---|---|---|---|---|
| LDA | LDC | LDA | LDC | LDA-LDC | LDA-LDC | |
| Bicarbonato, mmol/l | 23,0 (1,87) | 22,8 (2,20) | 28,5 (3,0) | 26,9 (1,9) | 0,668 | 0,032 |
| Delta bicarbonato | −5,4 (2,7) | −4,1 (2,4) | 0,073 | |||
| pH | 7,37 (0,05) | 7,38 (0,03) | 7,45 (0,045) | 7,45 (0,036) | 0,448 | 0,883 |
| pCO2 | 40,6 (4,3) | 38,9 (4,3) | 40,2 (6,1) | 39,0 (4,4) | 0,153 | 0,424 |
| Calcio++, mmol/l | 1,11 (0,06) | 1,12 (0,08) | 1,23 (0,086) | 1,11 (0,05) | 0,573 | 0,000 |
| Calcio total, mg/dl | 9,04 (0,52) | 8,92 (0,63) | 10,0 (0,62) | 9,6 (0,69) | 0,452 | 0,117 |
| Magnesio, mg/dl | 2,29 (0,39) | 2,23 (0,32) | 1,98 (0,20) | 1,85 (0,018) | 0,505 | 0,035 |
| Fósforo, mg/dl | 4,32 (1,07) | 4,30 (0,86) | 1,9 (0,52) | 2,0 (0,72) | 0,918 | 0,531 |
| iPTH, pg/ml | 276,8 (154,2) | 311,1 (214,2) | 148,4(148,8) | 255,1 (171,9) | 0,510 | 0,040 |
| Na, mmol/l | 139,2 (1,8) | 139,8 (2,9) | 138,9 (1,6) | 139,3 (1,6) | 0,394 | 0,347 |
| K, mmol/l | 5,3 (0,7) | 5,2 (0,5) | 3,4 (0,5) | 3,6 (0,4) | 0,331 | 0,407 |
| Cl, mmol/l | 99,6 (3,6) | 100,7 (4,6) | 99,3 (2,9) | 100,4 (2,9) | 0,324 | 0,228 |
| Anion gap, mmol/l | 16,6 (4,6) | 16,7 (4,0) | 10,4 (4,6) | 12,1 (3,4) | 0,951 | 0,183 |
| Proteínas totales, g/dl | 6,5 (0,34) | 6,4 (0,6) | 7,1 (0,78) | 6,8 (0,89) | 0,376 | 0,281 |
| Albúmina, g/dl | 3,8 (0,5) | 3,7 (0,5) | 0,173 | |||
| Prealbúmina, mg/dl | 30,7 (7,1) | 26,5 (8,3) | 0,113 | |||
| Colesterol, mg/dl | 145,5 (40,7) | 139,8 (31,5) | 0,577 | |||
| Triglicéridos, g/dl | 134,9 (86,0) | 128,4 (56,7) | 0,749 | |||
| Creatinina, mg/dl | 8,4 (2,0) | 8,3 (2,7) | 2,4 (0,88) | 3,0 (1,29) | 0,843 | 0,066 |
| Urea, mg/dl | 121,0 (26,6) | 120,6 (31,9) | 27,3 (14,4) | 32,6 (14,7) | 0,953 | 0,188 |
| Glucosa, mg/dl | 131,1 (64) | 115,1 (49,7) | 49,71867 | 0,311 | ||
| β2 microglobulina, mg/l | 24,3 (6,9) | 22,2 (7,1) | 6,1 (3,2) | 7,1 (5,3) | 0,289 | 0,427 |
| Leucocitos ×103/ml | 6,3 (2,1) | 6,5 (1,8) | 0,595 | |||
| Linfocitos % | 20,1 (8,7) | 17,7 (12,8) | 0,425 | |||
| Plaquetas ×103/ml | 185,8 (63,5) | 181,6 (53,6) | 0,793 | |||
| Hb, g/dl | 11,5 (1,2) | 11,8 (1,2) | 0,270 | |||
| IRE (UI/kg/sem) (g/dl) | 884,54 (479,8) | 1.246,45 (815,4) | 0,119 | |||
| IST % | 27,3 (10,0) | 25,5 (6,8) | 0,450 | |||
| Ferritina | 376 (228) | 358 (218) | 0,770 | |||
| PCR, mg/l | 2,8 (3,8) | 4,7 (7,3) | 0,253 | |||
Cl: cloro; Hb: hemoglobina; iPTH: hormona paratiroidea intacta; IRE: índice de resistencia a la eritropoyetina; IST: índice de saturación de transferrina; K: potasio; LDA: líquido de diálisis con acetato; LDC: líquido de diálisis con citrato; Na: sodio; pCO2: presión parcial de dióxido de carbono; PCR: proteína C reactiva.
En negrita, los resultados que alcanzaron la significación estadística.
En los parámetros del equilibrio ácido base, destacan unos niveles de bicarbonato posdiálisis significativamente más bajos con el LDC, sin diferencias en el delta de bicarbonato.
Respecto al efecto sobre el metabolismo mineral, se objetiva un menor aumento del Cai y Mg posthemodiálisis con el LDC respecto al LDA, con un aumento de la iPTH (tabla 3).
No se objetivaron diferencias con LDA o LDC en la eficacia dialítica valorada por la urea pre y posthemodiálisis (tabla 4). Tampoco cuando se analizaron por grupo de tratamiento (HD vs. HDF). El Kt en HD fue de 52,7 (9)l vs. 48,7 (10,6)l, y en HDF de 53,1 (7,2)l vs. 57 (5,9)l los LDA y LDC, respectivamente.
Efecto del líquido de diálisis (LDC respecto al LDA), sobre la eficacia dialítica: Kt, Kt sc y eKt/V
| Media | Desviación típica | Mínimo | Máximo | p | |
|---|---|---|---|---|---|
| Kt (l) | |||||
| LDA | 53,0 | 7,5 | 40,00 | 67,6 | |
| LDC | 53,9 | 8,8 | 34,5 | 74,0 | 0,689 |
| Total | 53,5 | 8,1 | 34,5 | 74,0 | |
| Kt sc | |||||
| LDA | 54,4 | 2,0 | 47,9 | 56,5 | |
| LDC | 54,5 | 2,2 | 47,9 | 56,5 | 0,0832 |
| Total | 54,4 | 2,1 | 47,9 | 56,5 | |
| eKt/V | |||||
| LDA | 1,41 | 0,18 | 1,12 | 1,75 | 0,843 |
| LDC | 1,39 | 0,29 | 0,83 | 1,87 | |
| Total | 1,40 | 0,25 | 0,83 | 1,87 | |
K: aclaramiento fraccional de urea; t: tiempo; Kt sc: Kt ajustado a la superficie corporal; eKt/V: aclaramiento fraccional de urea por volumen.
Las dosis de heparina permanecieron estables durante el estudio. En ningún caso de las 56 sesiones de HD basales hubo problemas importantes de coagulación del dializador o de la cámara venosa. Se analizó como parámetro de la coagulación el tiempo de tromboplastina, pero solo se analizó prehemodiálisis, no encontrándose diferencias entre ambos grupos (p=0,388).
No hubo diferencias significativas en el score de coagulación de las cámaras entre las HD realizadas con LDA y LDC, que fue de 0 (ausentes) o 1 (mínimos) en el 80% de las sesiones. Tampoco encontramos diferencias al analizar por la técnica de diálisis. El tiempo de hemostasia fue 1,4 (2,7)min mayor con LDC que con LDA, p<0,05.
No encontramos diferencias significativas (p=0,253) en los valores de proteína C reactiva, con el LDA y LDC [2,8 (3,8) vs. 4,7 (7,3), respectivamente].
En relación con el objetivo de evaluar el efecto del LDC sobre la tolerancia a las sesiones de HD, se registraron menos episodios de hipotensión arterial durante las sesiones de la visita basal con el LDC (1 vs. 3) (p=0,04), y también fue menor la CMVS medida por biosensor Hemoscan® [−3,4(7,7) vs. −5,1 (8,2)], aunque sin significación estadística. Estos datos se mantienen cuando consideramos el total de las sesiones del estudio. Los 46 pacientes que completaron el estudio realizaron 4.416 sesiones de HD, 2.208 con LDA y 2.208 con citrato LDC. Con LDA, 311 sesiones (14,1%) cursaron con hipotensión y 238 (10,8%) con LDC (p<0,01).
En los 29 pacientes a quienes se realizó bioimpedancia prehemodiálisis, no encontramos diferencias significativas en el agua extracelular total ni en la sobrehidratación relativa [sobrehidratación global ajustada al agua extracelular, medida en % (OH/AEC)], siendo los valores de 2,06 (1,25)l vs. 1,7 (1,19)l y 12,4% y 11,15% con el LDA y LDC, respectivamente.
DiscusiónComo en algunos estudios previos17, en nuestro estudio se objetiva que el LDC mejora el control del equilibrio ácido base, evitando/disminuyendo la alcalosis posdiálisis. Otros autores como Kuragano et al.18 encuentran una mayor alcalinización durante la diálisis con citrato frente al acetato (7,38 a 7,50 y 21 a 29,2 mmol/l vs. 7,39 a 7,45 y 22,4 a 24,3 para los valores de pH y bicarbonato con LDC y LDA, respectivamente). Schmitz et al.19 también encontraron menos hipercorrección de la acidosis posdiálisis (bicarbonato >32mmol/l) con el LDC con respecto al LDA. La alcalemia aguda inducida por el aporte de bicarbonato durante la diálisis es un problema de considerable trascendencia clínica, ya que se ha relacionado con importantes efectos adversos como la inestabilidad hemodinámica20-22, arritmias cardíacas, parestesias-calambres23, disminución del flujo sanguíneo cerebral, depresión respiratoria24,25, cefalea y un efecto procalcificante26. Finalmente, también una mayor concentración de bicarbonato en el LD se ha asociado con aumento de la mortalidad27, lo que llevó a la FDA28 a alertar a los médicos sobre la misma y a considerar el impacto del acetato y otras fuentes de álcali cuando se prescribe el LD. No obstante, a pesar de encontrarse una menor alcalemia posdiálisis con LDC, el delta de bicarbonato no fue estadísticamente diferente: −5,4 (2,7) vs. −4,1 (2,4) para LDA vs. LDC, respectivamente. Y los niveles de bicarbonato posthemodiálisis, aunque con diferencias estadísticamente significativas, en ninguno de los grupos fue muy elevado (28,5 vs. 26,9 en LDA vs. LDC). Esto probablemente esté en relación con un ajuste fino de la concentración de bicarbonato del LD que se realizó de forma protocolizada previamente a la aleatorización.
Esta menor alcalemia podría explicarse por la química del citrato, cuyo metabolismo es fundamentalmente hepático y también muscular, metabolizándose para generar bicarbonato y energía. A diferencia de lo que ocurre con el acetato, esta metabolización es incompleta durante la diálisis, ya que el metabolismo hepático y muscular ocurre en parte después de finalizar la técnica. Además, hay pacientes metabolizadores rápidos y lentos del mismo dependiendo de la función hepática y de la masa muscular, factores que también deben tenerse en cuenta. En pacientes a los que se les infunde citrato como anticoagulación regional los niveles de citrato en plasma son de 1mmol/l, y los pacientes en HD presentan niveles similares a los que tienen función renal normal29; no así los pacientes con insuficiencia hepática en los que el aclaramiento de citrato se reduce en un 50%30.
En relación con el metabolismo fosfocálcico, con el LDC encontramos valores de Cai y Mg posthemodiálisis significativamente inferiores a los prehemodiálisis, y valores de PTH más elevados. Esto no ocurría con el LDA. Como se ha comentado previamente, el citrato es un quelante del calcio y como tal su uso provoca alteraciones de las concentraciones de este ion. Por otro lado, se sabe que un calcio bajo en diálisis favorece la hipocalcemia en plasma, que estimula la PTH, el recambio óseo y la aparición de calambres, arritmias y el aumento de riesgo de episodios hipotensivos, y por ello, cuando los pacientes se trataban con LDC aumentamos la concentración de Ca del LD. Pese a esta corrección, los resultados muestran un Cai posdiálisis menor cuando se emplea LDC. No obstante, otros autores no han encontrado estos resultados. Gabutti et al.9, al suplementar de calcio el baño no aprecian diferencias significativas entre los valores de Cai prediálisis y posdiálisis en los tratados con LDC, mientras que en los tratados con LDA se produce un sensible aumento del calcio posdiálisis, lo cual puede tener consecuencias inhibitorias en la PTH. Aunque se ha descrito la aparición de hipomagnesemia en la anticoagulación regional con citrato31, esta es la primera vez que se describe en relación con el LDC. Este resultado, aunque no descrito, era esperable, ya que el citrato puede quelar otros iones como el Mg. Una fórmula de LDC con una concentración superior a la utilizada habitualmente (0,5mEq/l) solventaría este problema.
Nosotros no hemos encontrado diferencias en la eficacia dialítica medida por Kt, Ktsc ni eKt/V entre los dos LD. No obstante, otros autores como Ahmad et al. encontraron una mejoría de la adecuación de diálisis medida por Kt/V en el grupo con citrato (1,23±0,19 a 1,34±0,20, p=0,01) en un estudio sobre 25 pacientes7, al igual que Kossman et al.10 en un estudio sobre 146 pacientes (1,51±0,01 a 1,57±0,01, p<0,0001). Aunque no se conoce el mecanismo último que lo origina, algunos autores lo ponen en relación con el efecto anticoagulante del citrato que evitaría la coagulación de las fibras del dializador como causa de la mejora en la eficacia dialítica.
En relación con la coagulación, no encontramos diferencias en los scores de coagulación, pero sí en el tiempo de hemostasia, que fue 1,4 (2,7)min mayor con el LDC. Una posible explicación para la ausencia de diferencias en los scores de coagulación podría ser que la dosis de heparina utilizada sea elevada y pequeñas diferencias en la coagulación no tengan por ello repercusión en los scores analizados, que mostraron ausencia o mínimas alteraciones en el 80% de las sesiones. Si bien el tiempo de hemostasia es una medida grosera de la coagulación, este resultado está en consonancia con el descrito por la mayoría de los autores y es debido al efecto anticoagulante del citrato.
Por último, el resultado que a los investigadores del estudio nos parece más importante es el efecto sobre la estabilidad hemodinámica, registrándose menos episodios de hipotensión arterial con el LDC. Y sin diferencias significativas en el agua extracelular total ni en la sobrehidratación relativa. También fue menor la CMVS medida por biosensor Hemoscan®, aunque sin significación estadística. Daimon et al.13 describen una reducción en la frecuencia de episodios hipotensivos en una muestra de 44 pacientes durante la fase de LDC, especialmente en los episodios más sintomáticos y graves. Gabutti et al.9 describen una mayor estabilidad hemodinámica, con una reducción significativa de las resistencias periféricas y de la presión arterial sistólica. Sin embargo, otros estudios32 han encontrado variaciones significativas en la tolerancia. Este efecto nos parece relacionado con la ausencia de acetato, que produce vasodilatación mediada por la liberación de óxido nítrico3 y la activación de citoquinas proinflamatorias por la hipoxia4. Smith et al.33 encontraron un aumento ligero y constante de los valores de acetato en torno a 1mmo/l en la sangre obtenida después de dializar a pacientes con concentraciones de acetato en el LD de 4 y 8mEq/l.
A modo de resumen, no solo de nuestros resultados sino también de los publicados previamente, algunas situaciones en las que los pacientes podrían beneficiarse de utilizar LDC se han detallado en la tabla 5. Los pacientes que podrían perjudicarse de utilizar un LDC se podrían resumir en pacientes con hipocalcemia, hipomagnesemia e hiperparatiroidismo secundario no controlado.
Situaciones en las que los pacientes en hemodiálisis podrían beneficiarse de utilizar LDC
| • Inestabilidad hemodinámicaa |
| • PTH baja o enfermedad ósea adinámicaa |
| • Hipercalcemiaa |
| • Calcificaciones vascularesa |
| • Pacientes con indicación de reducir la heparina o diálisis sin heparina |
| • Alcalosis metabólica posthemodiálisis a |
| Sintomatología asociada a aumento de la concentración de bicarbonato intra o posthemodiálisis o que se agravan con la alcalemia posthemodiálisisa: |
| -→ Insuficiencia respiratoria con retención de carbónico |
| -→ Hepatopatía crónica avanzada |
| -→ Cefalea |
| • Hipermagnesemiaa |
| • Dificultad para alcanzar la dosis de diálisis prescrita |
| • Malnutricióna |
LDC: líquido de diálisis con citrato; PTH: hormona paratiroidea.
Queremos destacar como limitaciones del estudio el tamaño muestral y el sesgo de selección que viene dado por la definición de uno de los criterios de inclusión: pacientes que se dializan a través de una FAV. Así, la etiología de la ERC de los pacientes incluidos en el estudio no es representativa de la población en diálisis, ya que la primera causa fueron las glomerulonefritis, seguidas de la diabetes, mientras que tanto en la población española como en la mayoría de los países la primera causa de ERC en pacientes en diálisis es la diabetes. Esto se debe al sesgo de seleccionar a los pacientes portadores de FAV, que ha excluido a un porcentaje de pacientes diabéticos que se dializan con catéter.
ConclusionesEn conclusión, los resultados del presente trabajo muestran que la diálisis con citrato consigue un mejor control de equilibrio ácido base posdiálisis disminuyendo/evitando la alcalemia posdiálisis. Los niveles de Cai y Mg posdiálisis disminuyen con el LDC y aumenta la PTH. Estos resultados, junto con una menor alcalemia, apoyan un perfil menos calcificante del LDC. Comparado con el LDA, el LDC ofrece una mayor estabilidad hemodinámica produciendo menos hipotensiones.
Conflicto de interesesP de S, RPG, MM han recibido honorarios por participación como ponentes en reuniones de Fresenius y Baxter-Gambro y patrocinios de congresos científicos por Nipro, Fresenius y Baxter-Gambro.
Al personal de enfermería de las Unidades de Diálisis de los Hospitales participantes en el estudio por su inestimable colaboración.
El promotor del estudio ha sido la Fundación de la Sociedad Española de Nefrología (SENEFRO) y la financiación por una beca de investigación independiente de Baxter.
P. de Sequera Ortiz (Servicio de Nefrología, Hospital Universitario Infanta Leonor, Madrid).
R. Pérez García (Servicio de Nefrología, Hospital Universitario Infanta Leonor, Madrid).
M. Molina Nuñez (Hospital General Universitario Santa Lucía, Cartagena).
R.I. Muñoz González (Hospital Galdakao,Vizcaya).
G. Álvarez Fernández (Servicio de Nefrología, Hospital Universitario Infanta Leonor, Madrid).
E. Mérida Herrero (Hospital Universitario Doce de Octubre, Madrid).
M.J Camba Caride (Complexo Hospitalario Universitario de Ourense).
L.A. Blázquez Collado (Hospital Universitario de Guadalajara).
M.P. Alcaide Lara (Hospital Universitario Virgen del Rocío, Sevilla).
R. Echarri Carrillo (Hospital Universitario Infanta Sofía, Madrid).
I. Gallardo (Hospital Galdakao,Vizcaya).
E. Hernández Martínez (Hospital Universitario Doce de Octubre, Madrid).
A. Otero González (Complexo Hospitalario Universitario de Ourense).
M. Sánchez Heras (Hospital Universitario de Guadalajara).
G. de Arriba de la Fuente (Hospital Universitario de Guadalajara).
L. Gil Sacaluga (Hospital Universitario Virgen del Rocío, Sevilla).
A. Cirugeda García (Hospital Universitario Infanta Sofía, Madrid).
V. Barrio Lucía (Hospital Universitario Infanta Sofía, Madrid).