Se ha comunicado una disminución de los valores de glicosaminoglicanos (GAG) en el riñón y otros órganos en modelos experimentales de diabetes y en humanos. La administración a largo plazo de heparina y otros GAG previene las alteraciones morfológicas y funcionales del riñón en ratas diabéticas. Evaluamos el efecto del pentosán polisulfato de sodio (PPSNa), un mucopolisacárido semisintético similar a los GAG y de baja actividad anticoagulante, sobre la función renal y los cambios estructurales en ratas diabéticas. La diabetes fue inducida a ratas Sprague-Dawley mediante la administración i.v. de estreptozotocina (STZ). Los animales fueron distribuidos al azar en tres grupos (C = control, STZ y STZ + PPSNa = pretratados con 15 mg/kg/día de PPSNa s.c.). Después de 3 meses se tomaron muestras de sangre y de orina de 24 horas; los animales fueron sacrificados y los riñones extraídos mediante microdisección para el análisis morfométrico. Los animales del grupo STZ presentaron un incremento importante de la excreción de albúmina en orina (C = 0,26 ± 0,03 frente a STZ = 7,75 ± 1,8 mg/24 h), que fue parcialmente revertido por el pretratamiento con PPSNa (3,7 ± 0,7 mg/24 h), sin afectar al control metabólico, HbA1c (C = 3,6 ± 1,7; STZ = 8,82 ± 0,47; STZ + PPSNa = 8,63 ± 0,54). En las micrografías electrónicas se observan las lesiones renales habituales descritas en la diabetes experimental (grupo STZ). La administración de PPSNa previene el engrosamiento de la membrana basal tubular y la pérdida de la citoarquitectura inducida por la diabetes. Nuestros resultados demuestran que la administración de PPSNa previene parcialmente el daño renal en este modelo experimental y sugieren un potencial uso terapéutico de este compuesto.
Decreased levels of glycosaminoglycans (GAGs) have been observed in the kidney and other organs, in human and animal models of diabetes. Long-term administration of heparins and other glycosaminoglycans has demonstrated a beneficial effect on morphological and functional kidney abnormalities in diabetic rats. We assessed the effect of pentosan polysulfate sodium (PPS), a semi-synthetic glycosaminoglycan with low anticoagulant activity, on kidney involvement in streptozotocin diabetic rats. Diabetes was induced in male Sprague-Dawley rats by i.v. administration of streptozotocin (STZ). Animals were randomly allocated to three groups: C = control, STZ and STZ + PPS = pretreated with PPS (15mg/kg, s.c.). After three months of follow-up, blood and 24 h-urine samples were obtained, the animals were sacrificed and the kidney microdissected for morphometric analysis. Urinary albumin excretion was markedly increased in untreated diabetic rats (C = 0.26 ± 0.03 vs STZ = 7.75 ± 1.8 mg/24 h) and PPS treatment partially prevented the albumin rise (3.7 ± 0.7 mg/24 h), without affecting the metabolic control HbA1c (C = 3.6 ± 1.7; STZ = 8.82 ± 0.47; STZ + PPS = 8.63 ± 0.54). Electron microscope observation revealed typical renal lesions described in experimental diabetes (STZ group). PPS administration prevents the tubular basement membrane thickening and the loss of cytoarchitecture induced by experimental diabetes. Our data demonstrate that long-term administration of PPS has a favourable effect on morphological and functional abnormalities in kidneys of diabetic rats and suggests a potential therapeutic use for this compound.
INTRODUCCIÓN
La eficacia de los glicosaminoglicanos (GAG) para disminuir la excreción de albúmina en orina en la nefropatía diabética ha sido ampliamente demostrada en diferentes estudios experimentales y en humanos1-3, lo que ha estimulado la investigación clínica con estos compuestos no sólo en esta patología sino también en otras complicaciones microvasculares de la diabetes4,5 y en diferentes tipos de glomerulonefritis6.
Se han realizado estudios con moléculas modificadas, tratando de obtener preparaciones con poca actividad anticoagulante para mejorar el perfil de seguridad. Las moléculas modificadas derivadas de heparina presentan una efectividad similar al dermatán sulfato para disminuir la excreción de albúmina y para inhibir la expresión del TGFb1, demostrando que la fracción heparina no es indispensable para la actividad7. Igualmente, se han realizado estudios con moléculas con diferente grado de sulfatación8, con proteoglicanos que unen TGFb como el decorin9, y GAG con cadena similar al heparán sulfato, como el danaparoid sódico10, obteniéndose resultados diversos. Sin embargo, la mayor experiencia clínica se ha obtenido con el uso de la sulodexida, un GAG compuesto de una fracción de heparina de migración rápida y dermatán sulfato11-15.
El pentosán polisulfato de sodio (PPSNa) es un mucopolisacárido semisintético con estructura similar a los GAG, que ha sido ampliamente utilizado en el tratamiento de la cistitis intersticial, mostrando eficacia en el control de la sintomatología y un perfil de seguridad y una tolerancia adecuados en el rango de dosis utilizado16-18.
El PPSNa presenta cierta similitud de efectos con la sulodexida. Así, ambos tienen efecto fibrinolítico y activan la lipoproteina lipasa y la lipasa de triglicéridos hepática19-22, efectos que serían beneficiosos en el paciente diabético. La actividad anticoagulante del PPSNa es muy baja, unas 15 veces menor que la de la heparina; presenta un mejor perfil de absorción por vía oral que los GAG16 y se ha demostrado en estudios in vitro que inhibe la proliferación celular mediada por factores de crecimiento que unen heparina23.
Los estudios farmacocinéticos en ratas, mediante la administración de PPSNa radiomarcado, demuestran que se concentra principalmente en los riñones y en el tracto urinario24, lo que sugiere un posible papel funcional en estas estructuras.
La posibilidad de que el PPSNa prevenga o disminuya la excreción de albúmina en la nefropatía diabética no ha sido evaluada. Para ello, nos proponemos evaluar si el PPSNa disminuye la excreción de albúmina en orina en ratas hechas diabéticas mediante la administración de estreptozotocina (STZ) y si puede prevenir los cambios morfológicos inducidos por la diabetes en el riñón.
MATERIALES Y MÉTODOS
Animales
Los animales de experimentación fueron ratas albinas, machos, de la cepa Sprague-Dawley, de 6 a 7 semanas de edad, con un peso comprendido entre 220 y 250 g, provenientes del bioterio de la Escuela José María Vargas, Facultad de Medicina, UCV, Caracas, las cuales fueron mantenidas con períodos alternos de luz y oscuridad, permitiéndoles libre acceso al agua y a la comida (comida estándar para ratas de laboratorio, que contiene aproximadamente un 20% de proteína).
Las ratas fueron asignadas al azar a dos grupos, un grupo control y otro al que se le indujo diabetes. Todos los experimentos fueron realizados siguiendo las buenas prácticas para el manejo de animales de laboratorio25, y fue aprobado por el Comité de Bioética de la Escuela de Medicina José María Vargas.
Inducción de la diabetes experimental
La diabetes fue inducida mediante la administración de una inyección única de STZ (Sigma Chemical Co., St. Louis, MO), a una dosis de 60 mg/kg de peso, en la vena caudal. La inducción de la diabetes fue confirmada a los 2 y 7 días posteriores a la administración de STZ, mediante la determinación de los valores sanguíneos de glucosa utilizando un método enzimático (Glucose HK Reagent, Bayer). Se mantuvo un grupo control al que no se le indujo diabetes, al que sólo se le administró solución salina en la vena caudal. A los 7 días, los animales controles y aquellos a los cuales se les indujo diabetes fueron distribuidos al azar los siguientes grupos de tratamiento:
Control
Solución salina o vehículo.
STZ-control
STZ.
STZ-PPSNa
STZ + 15 mg/kg de peso/día de PPSNa por vía subcutánea, durante 3 meses.
El PPSNa fue administrado por vía subcutánea durante 5 días a la semana (de lunes a viernes). Los animales no recibieron insulina durante el experimento. Durante el período de seguimiento a los animales se les determinaron mensualmente el peso, la presión arterial y los valores de glucosa capilar. Al finalizar el período de tratamiento se obtuvieron muestras de sangre de la vena caudal de la cola para la determinación de la glicemia y de la HbA1c, y los animales fueron colocados en jaulas metabólicas para recolectar orina durante 24 horas para determinar la albuminuria. Posteriormente fueron sacrificados, y se extrajeron los riñones mediante microdisección para el análisis morfométrico.
La glicemia fue determinada en muestras de sangre mediante una prueba enzimática utilizando un equipo comercial (Glucose HK Reagent, Bayer). La HbA1c y la excreción de albúmina en orina se determinaron empleando equipos comerciales (DCA 2000®, Bayer).
Determinación de la presión arterial
El registro de la presión arterial se realizó en ratas conscientes, utilizando un método no invasivo mediante el uso de un pletismógrafo digital de cola (LE 5000, LETICA Scientific Instrument, Barcelona, España).
Para producir la vasodilatación de los vasos periféricos, las ratas fueron sometidas a calentamiento (42 ºC) durante 15 minutos, utilizando para ello una estufa (Memmert, 854 Schawabach, Alemania)26. Posteriormente fueron inmovilizados en un cepo, y se les colocó en la cola el dispositivo para determinación de la presión arterial conectado a un transductor de pulso, que permite el registro de este parámetro. Los valores que comunicamos son el promedio de tres registros sucesivos.
Análisis ultraestructural y morfométrico
Se extrajeron muestras de corteza renal de 2 mm de diámetro. Las muestras fueron fijadas en un 3% de glutaraldehído y en un 1% de OsO4 en tampón fosfato de Millonig (pH = 7,4, 320 mOsmol). Posteriormente fueron deshidratadas en concentraciones crecientes de etanol e incluidas en epón. Después de la inclusión, fueron seccionadas en un ultramicrotomo Porter-Blum MT2-B, contrastadas con acetato de uranilo y citrato de plomo y observadas en un microscopio electrónico de transmisión JEM-1011, con un voltaje de aceleración de 80 kV.
El registro digital de las imágenes fue analizado con un programa de morfometría (Image-Tool versión 3.0), con el cual se midió el diámetro de la membrana basal (n = 16/cada tratamiento).
Análisis estadístico
Los resultados se representan como la media ± error estándar de la media (EEM) y fueron graficados y analizados mediante los programas GraphPad Prism versión 4.1. y STATICS, versión 7. La comparación entre las medias aritméticas de los grupos fue realizada mediante análisis de varianza (ANOVA). Los valores con p <0,05 fueron considerados estadísticamente significativos.
RESULTADOS
En la tabla 1 se exponen los valores del peso, la glicemia y el volumen urinario de los grupos estudiados. Los grupos a los cuales se le indujo diabetes muestran un incremento significativo en la glicemia y el volumen urinario excretado en 24 h, así como un menor peso comparado con el grupo control a los 3 meses de tratamiento.
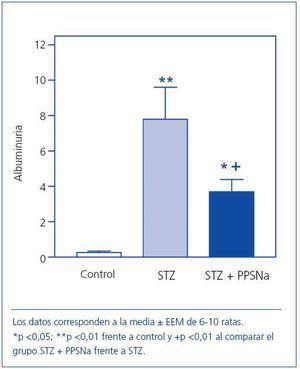
La inducción de diabetes con STZ produjo un incremento significativo de la excreción urinaria de albúmina con respecto al grupo control (C = 0,26 ± 0,03; STZ = 7,8 ± 1,8 mg/24 h). El tratamiento durante 3 meses con PPSNa previno parcialmente este incremento (STZ + PPSNa = 3,7 ± 0,70 mg/24 h), disminuyendo la excreción de albúmina un 52,5% con respecto al grupo diabético no tratado (figura 1).
Los valores de HbA1c en los grupos de tratamiento fueron: C = 3,6 ± 1,7; STZ = 8,8 ± 0,47 y STZ + PPSNa = 8,65 ± 0,54%, evidenciándose que el tratamiento con PPSNa no modifica el incremento en los valores de HbA1c característicos de este modelo de diabetes. Además, se observa que no existen diferencias significativas entre los valores de la presión arterial media entre los diferentes grupos de tratamiento (C = 122,8 ± 5,1; STZ = 134,6 ± 12 y STZ + PPSNa = 110 ± 5,7 mmHg).
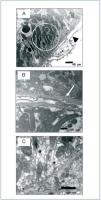
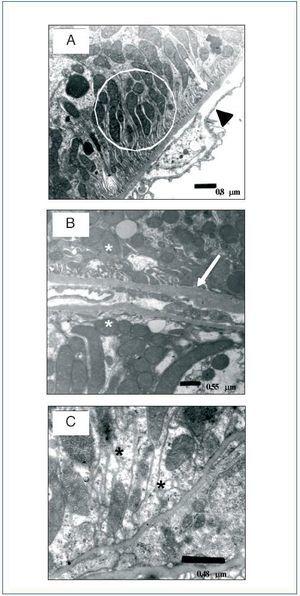
En las micrografías electrónicas (figura 2) se observa la apariencia normal de los túbulos renales en las ratas controles (A), con una disposición adecuada de las interdigitaciones y una membrana basal de grosor normal. Destaca que el capilar muestra un endotelio uniforme y de escaso grosor. Por el contrario, en el grupo STZ (B) se observa un importante daño tubular con pérdida de la citoarquitectura evidenciada por la desaparición de las interdigitaciones y engrosamiento de la membrana basal. El tratamiento con PPSNa (C) previene parcialmente la implantación del daño tubular, ya que se observa mayor número de interdigitaciones que en STZ, pero están dispuestas irregularmente y no se corresponden con el número de mitocondrias.
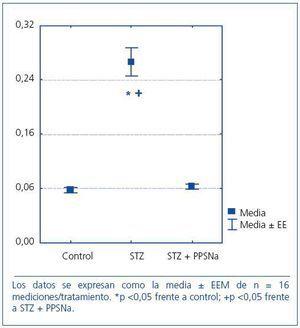
El análisis morfométrico del grosor de las membranas basales tubulares para los diferentes grupos de tratamiento (figura 3) revela los siguientes valores: C = 0,077 ± 0,003; STZ = 0,266 ± 0,021 y STZ + PPSNa = 0,082 ± 0,04 µm. El grosor de la membrana basal se incrementa de manera significativa en el grupo STZ al compararlo con el control, mientras que en el grupo de ratas con diabetes que recibe tratamiento con PPSNa el engrosamiento de la membrana basal es mucho menor, no presentando diferencia significativa con el grupo control y sí es estadísticamente diferente al grupo STZ.
DISCUSIÓN
Los GAG, principalmente el heparán sulfato, son sintetizados en las células endoteliales y mesangiales, y después de un proceso de sulfatación en el aparato de Golgi, son incorporados en la matriz extracelular del glomérulo y de las grandes arterias, donde contribuyen a mantener la integridad estructural de la membrana basal y de la pared vascular27.
En la diabetes se ha referido una reducción generalizada de las cargas negativas de la matriz extracelular y de las membranas plasmáticas, asociada con una disminución del contenido de heparán sulfato o con cambios en su grado de sulfatación28-31. Esta alteración en la carga de la membrana basal se traduciría en la pérdida de selectividad por carga y facilitaría una eliminación incrementada de proteínas en la orina30,32.
Así, en modelos experimentales de diabetes en ratas y en ratones, se ha encontrado una disminución en la síntesis de proteoglicanos en el glomérulo y disminución del contenido de proteoglicanos unidos a heparán sulfato en la membrana basal33,34. Asimismo, se ha comunicado que el contenido de GAG está disminuido en los riñones y en la íntima de las aortas obtenidas por autopsia en pacientes diabéticos35,36, lo que sugiere que las alteraciones del metabolismo del heparán sulfato no están restringidas al riñón y pueden participar en patogenia de otras complicaciones de la diabetes.
Se ha demostrado que las alteraciones en el metabolismo de los GAG, producidas en un modelo de diabetes experimental en ratas, son susceptibles de ser modificadas mediante la administración exógena de los mismos, con la consiguiente restauración del funcionamiento normal del riñón1,2.
Nuestros resultados coinciden con lo referido en la bibliografía médica, ya que las alteraciones renales inducidas por la diabetes son parcialmente prevenidas por la administración de PPSNa durante los 3 meses posteriores a la administración de STZ en ratas.
La administración de PPSNa por vía subcutánea durante 3 meses previene el incremento en la excreción renal de albúmina en este modelo experimental, lo que coincide con lo comunicado previamente en la bibliografía médica1,2, y se corresponde con el efecto de disminución de la excreción renal de albúmina demostrado en pacientes con diabetes mellitus, mediante la administración de otros GAG12,14,15,37-39, entre los que el más estudiado es la sulodexida.
De igual manera, el tratamiento con PPSNa protege al riñón de los cambios estructurales inducidos por la diabetes, previniendo el engrosamiento de la membrana basal y la pérdida de la citoarquitectura. Esto coincide con lo comunicado por otros autores que han demostrado que la administración de heparina y otros GAG previene la nefropatía diabética en ratas manteniendo el grosor normal de la membrana basal y la densidad de cargas aniónicas, retrasando paralelamente el inicio de la microalbuminuria1-3.
En pacientes con nefropatía diabética, se ha demostrado una correlación entre la albuminuria y el contenido de heparán sulfato de la membrana basal del glomérulo40. Asimismo, se ha observado una importante reducción de la microalbuminuria o de la macroalbuminuria en pacientes diabéticos que han sido tratados con GAG11,37-39.
Estos hallazgos señalan que los GAG pueden cumplir un papel importante en la fisiopatología de la nefropatía diabética, y que un metabolismo anormal de los GAG podría ser la causa de esta patología1,41.
El mecanismo por el cual los GAG ejercen este efecto protector en la nefropatía diabética no está completamente dilucidado. Inicialmente se propuso que su efecto se limitaría a restituir la permeselectividad glomerular al reponer las cargas negativas, disminuyendo de esta forma la excreción de albúmina en orina y recuperando la funcionalidad3,32,42. Sin embargo actualmente se sabe que los GAG pueden modular la síntesis proteica en la matriz extracelular, efecto que puede contribuir a su utilidad terapéutica.
La administración de heparina de bajo peso molecular y de dermatán sulfato previene el engrosamiento de la membrana basal, la reducción de cargas aniónicas y el inicio de la albuminuria en ratas con diabetes inducida mediante la administración de STZ1. Además, se ha demostrado que la administración de la heparina disminuye la sobreexpresión de colágeno, posiblemente interfiriendo la vía mediada por el TGFb1 que está activada en la nefropatía diabética2,7. Recientemente Lewis y Xu (2008) han demostrado que los GAG inhiben la enzima heparanasa, que es estimulada por la hiperglicemia, previniendo de esta manera la degradación del heparán sulfato31. En conjunto, estos efectos contribuyen a que los GAG puedan prevenir las alteraciones estructurales y funcionales, principalmente mesangiales, que se presentan en la nefropatía diabética.
El PPSNa ha demostrado, en ratas nefrectomizadas, que es capaz de prevenir la atrofia de las células epiteliales y disminuir el infiltrado inflamatorio en el intersticio43, y que inhibe la proliferación de la matriz extracelular, disminuyendo el colágeno tipos I y IV en cultivo de células mesangiales44, y en células de músculo liso vascular obtenidas de pacientes en los que ha fallado el implante para obtener el acceso vascular para la hemodiálisis45. Además, reduce la nefropatía inducida por ciclosporina en ratas sometidas a depleción de sal, lo que se evidencia por la disminución del número de arteriolas afectadas y de las lesiones túbulo-intersticiales46. Estos hallazgos, conjuntamente con nuestros resultados, evidencian el papel nefroprotector del PPSNa.
La similitud de efectos del PPSNa con la sulodexida, a saber, efecto fibrinolítico y activación la lipoproteina lipasa y la lipasa de triglicéridos hepática19-22, así como la similitud estructural con los GAG, pueden explicar nuestros hallazgos. Asimismo, la acción antinflamatoria del PPSNa desempeña un papel en su efectividad para el tratamiento de la cistitis intersticial47,48, y podría partcicipar en el efecto nefroprotector. Así, en modelos de de ratas nefrectomizadas, el efecto nefroprotector del PPSNa evidenciado por la disminución de la esclerosis y la dilatación tubular se asocia con la reducción en el infiltrado de linfocitos y macrófagos, de manera similar a los efectos referidos para el losartán43,49.
En este modelo experimental de nefropatía diabética se demuestra que el PPSNa previene parcialmente el daño renal, observándose concordancia entre los hallazgos fisiológicos y ultraestructurales, lo que sugiere un potencial uso terapéutico de este compuesto.
Agradecimientos
Al personal del Bioterio de la Escuela José María Vargas, Laboratorios CLINIFAR, al Laboratorio de Microscopia Electrónica de la Escuela de Medicina José María Vargas y a Laboratorios IVAX por la donación del pentosán polisulfato de sodio. Este trabajo fue subvencionado por el proyecto N.º PG09-11-5102-2003 y PG0911-5102-2007 del Consejo de Desarrollo Científico y Humanístico de la Universidad Central de Venezuela.
Tabla 1. Parámetros evaluados a los 3 meses
Figura 1. Excreción urinaria de albúmina en 24 h en las ratas control, diabéticas (STZ) y diabéticas tratadas con pentosán polisulfato de sodio (STZ + PPSNa).
Figura 2.
Figura 3. Diámetro de la membrana basal.