INTRODUCCIÓN
La incidencia de infección por citomegalovirus (CMV) en los primeros meses del trasplante renal es alta, especial-mente en receptores con serología IgG CMV negativa que reciben un injerto de un donante con serología positiva (D+/R-). En estos casos, el 40-60% de los pacientes desarrollan enfermedad por CMV (ECMV). Además de su morbilidad inherente, la infección CMV favorece el desarrollo del rechazo del órgano trasplantado, la sobreinfección por gérmenes oportunistas y la aparición de otros efectos indirectos1.
Para prevenir o minimizar la patología ligada a la infección CMV, se han utilizado diferentes estrategias. La profilaxis con fármacos antivirales y/o inmunoglobulinas constituye una de las vías de actuación. Otra alternativa es la terapia anticipada, basada en la monitorización de la replicación viral e inicio del tratamiento antiviral en caso de infección activa2.
En esta edición del Proyecto Prometeo, centrada en la infección CMV en el trasplante renal, nuestro Grupo ha trabajado en el apartado «Estrategias de Prevención y Tratamiento de la Enfermedad por CMV», analizando la bibliografía existente y proponiendo recomendaciones de actuación de práctica clínica.
METODOLOGÍA
Los coordinadores del Proyecto dirigieron la búsqueda inicial de la bibliografía en las bases biomédicas PubMed, Medline, Embase y Cochrane Database. Nuestro Grupo recibió 115 referencias, con sus resúmenes correspondientes, relacionadas con la prevención y el tratamiento de la ECMV en el trasplante renal, con la posibilidad de añadir nuevas citas aportadas por los miembros del Grupo. Con posterioridad, el portavoz del Grupo, con el consenso del mismo, seleccionó los artículos originales que según los resúmenes ofrecían inicialmente una mayor calidad metodológica. En esta fase se seleccionaron un total de 28 artículos: 6 revisiones sistemáticas, 12 ensayos clínicos (EC) aleatorizados, 8 estudios clínicos controlados y 2 estudios observacionales relevantes.
A cada miembro del Grupo se le asignaron dos artículos para realizar el resumen estructurado y una evaluación crítica de los mismos. La calidad de la evidencia de los artículos se jerarquizó siguiendo los criterios del modelo GRADE en cuatro niveles: alto, moderado, bajo y muy bajo3. Asimismo, todos los miembros del Grupo recibieron los artículos de revisión y las guías clínicas publicadas sobre este tema en los últimos años4,5. En una fase posterior se fue estructurando la información evaluada y perfilando las recomendaciones de actuación. Finalmente, en una reunión presencial de todos los Grupos del Proyecto y Expertos en el tema, se debatió el trabajo realizado y se elaboró el documento final.
RESULTADOS
1. Profilaxis
La inmunoglobulina CMV y los antivirales aciclovir, valaciclovir, ganciclovir y valganciclovir son los fármacos que han sido utilizados en pacientes con trasplante renal y otros órganos sólidos, con una duración y posología variables, como tratamiento preventivo de la ECMV. Diferentes estudios han evaluado su eficacia y seguridad.
Profilaxis frente a placebo o no tratamiento
Bonaros et al.6 valoran la utilidad preventiva de la inmunoglobulina CMV en pacientes con trasplante de órgano sólido. En su revisión incluyen 11 EC aleatorizados, publicados entre 1987 y 2003, con un total de 698 pacientes con trasplante de órgano sólido; 6 de los estudios reclutaron 302 trasplantes renales. El análisis de los resultados mostró que el tratamiento no modificó la incidencia de infección CMV, pero sí disminuyó la incidencia de ECMV. En los pacientes con trasplante renal se redujo dicha enfermedad del 46,2% en el grupo con placebo o no tratados al 31,5% en los que recibieron inmunoglobulina [riesgo relativo (RR) 0,70, intervalo de confianza (IC 95%) 0,56-0,87]. También se observó una reducción en la mortalidad, tanto global como la asociada a ECMV, en pacientes con trasplante de órgano sólido, aunque dicho descenso no fue estadísticamente significativo en el trasplante renal. Los EC evaluados fueron heterogéneos en cuanto al tratamiento, serología CMV y procedimientos diagnósticos, factores que limitan la validez de los resultados. Actualmente es una terapia que está en desuso, superada por los fármacos antivirales.
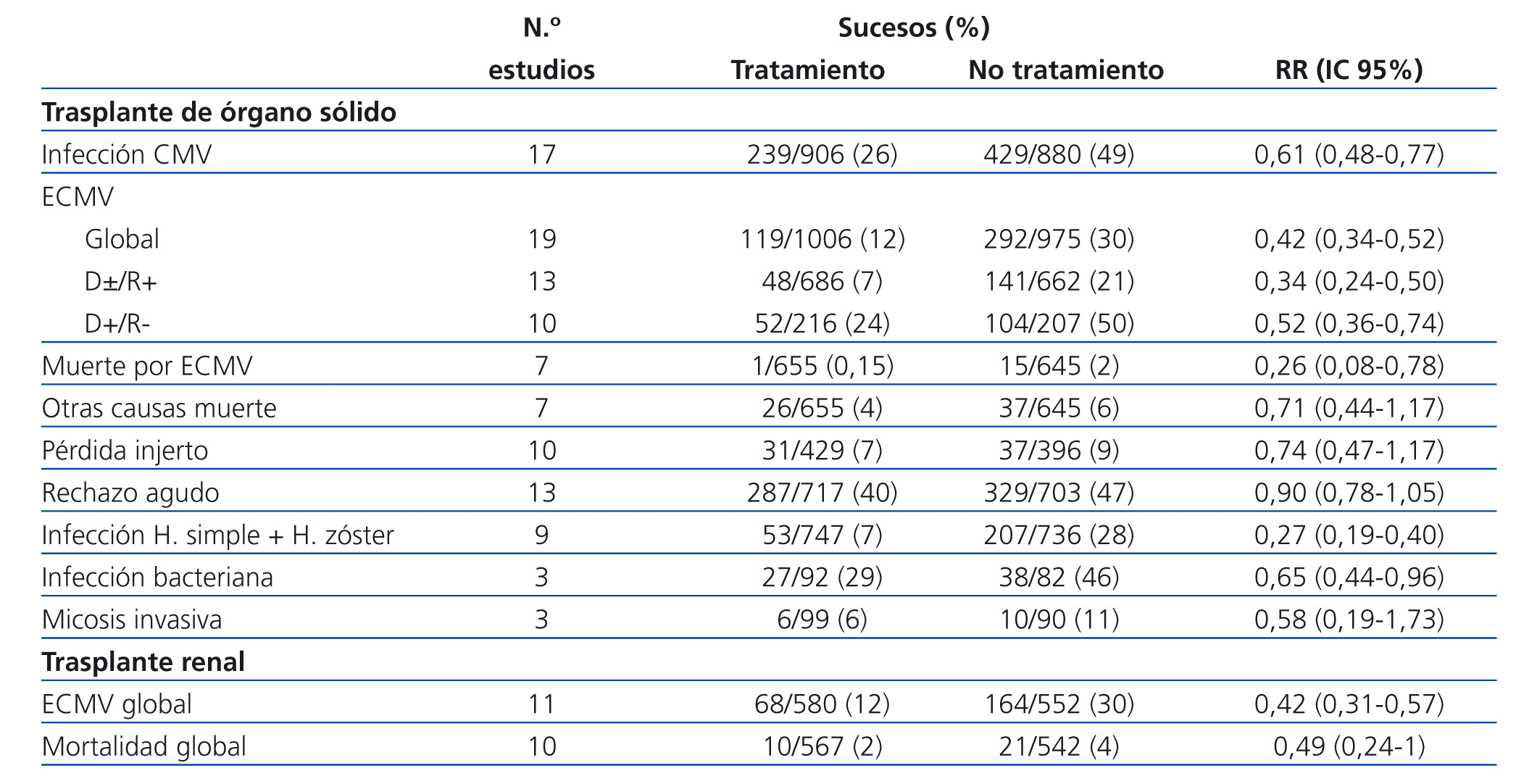
Hodson et al.7 realizan una revisión sistemática de la eficacia y la seguridad de los fármacos antivirales en la prevención de la ECMV en pacientes con trasplante de órgano sólido. En el estudio incluyen 19 EC publicados entre 1989 y 2002, 11 realizados en pacientes con trasplante renal, y comparan de forma conjunta la profilaxis con los fármacos antivirales aciclovir, valaciclovir, ganciclovir y valganciclovir, frente a pacientes no tratados o que recibieron placebo. La tabla 1 muestra un resumen de los resultados de los metaanálisis realizados. Los fármacos antivirales redujeron la infección y la ECMV tanto en pacientes D±/R+ como en D+/R-. También disminuyeron la muerte por ECMV y las infecciones, especialmente las causadas por los virus herpes simple y zóster.
Otro hecho objetivado fue el retraso en la presentación de la ECMV en los pacientes tratados. Entre los EC analizados, el realizado por Lowance et al.8 fue el que reclutó más pacientes; 306 trasplantados renales recibieron profilaxis con valaciclovir durante 90 días y 310 placebo. Un total de 208 pacientes eran D+/R- y 102 recibieron profilaxis antiviral. En este grupo, el descenso de ECMV fue especialmente relevante en el grupo con valaciclovir: un 16% frente al 45% en el grupo placebo. La incidencia de rechazos agudos confirmados con biopsia en los seis primeros meses del trasplante también fue menor en los pacientes tratados con valaciclovir: un 26% frente al 52% en el grupo placebo. Se trata de una observación clínicamente relevante, pero hay que señalar que son pacientes tratados con ciclosporina y azatioprina; sólo el 5% recibieron tacrolimus o micofenolato.
Estudios comparativos entre diferentes fármacos antivirales
Diferentes EC han abordado la comparación de la eficacia y la seguridad de los fármacos antivirales utilizados en la prevención de la infección CMV.
La revisión de Hodson et al.7 aporta varios metaanálisis de dichos estudios. En estos análisis, el ganciclovir fue más eficaz que el aciclovir en la prevención de la ECMV, sin otras diferencias clínicas relevantes [RR (IC 95%) 0,37 (0,23-0,60)].
Reischig et al.9 comparan la eficacia de ganciclovir y valaciclovir. Este estudio, con 83 pacientes reclutados, no mostró diferencias en la incidencia de infección y ECMV. El grupo con valaciclovir presentó una menor incidencia de rechazos agudos confirmados con biopsia.
Paya et al.10 comparan 245 pacientes con trasplante renal de órgano sólido tratados con el valganciclovir oral y 127 con ganciclovir oral durante 100 días, todos ellos D+/R-. Los resultados clínicos obtenidos fueron similares en ambos grupos en todas las variables analizadas. Un 17% de los pacientes tratados con valganciclovir y un 18% del grupo ganciclovir presentaron ECMV al año del trasplante.
La biodisponibilidad de ganciclovir a partir de valganciclovir es aproximadamente del 60%, entre 8 y 10 veces superior a la del ganciclovir oral. Actualmente, el valganciclovir es el fármaco más utilizado en la prevención de ECMV, con indicación en ficha técnica restringida a pacientes D+/R-. La dosis recomendada es de 900 mg/día, ajustada a filtrado glomerular.
Duración de la profilaxis
La duración del tratamiento preventivo de la infección CMV ha sido variable en los estudios publicados. Se han utilizado pautas cortas de menos de 6 semanas, pero en general la pauta más habitual ha sido la de 3 meses/100 días, sin estudios comparativos entre ambas.
El reciente EC de Humar et al.11 plantea la conveniencia de ampliar dicha duración de 100 a 200 días. Se trata de un EC multicéntrico realizado en 326 trasplantados renales D+/R- que compara la eficacia y la seguridad de valganciclovir administrado durante 100 días frente a 200 días postrasplante. Los pacientes tratados con la pauta larga presentaron una menor incidencia de infección y ECMV a lo largo del primer año del trasplante. Un total de 25 pacientes (16,1%, IC 95% 10,7-22,9%) de los tratados 200 días presentaron ECMV en el primer año del trasplante frente a 60 (36,8%, IC 95% 29,4-44,7%) en el grupo tratado 100 días. La incidencia de rechazo agudo y efectos adversos fueron similares en ambos grupos. Este estudio, por su implicación en la duración del tratamiento con valganciclovir, ha desencadenado un importante debate clínico. Por el momento impera la cautela; la Guía de la Sociedad Internacional de Trasplantes5 recomienda que la duración de la profilaxis CMV en pacientes trasplantados renales D+/R- sea de 3-6 meses, aconsejando 6 meses en pacientes que reciben mayor inmunosupresión, como es el caso de los tratados con anticuerpos antilinfocitarios.
2. Terapia anticipada
Esta estrategia supone monitorizar la replicación del CMV, carga viral por PCR o Ag pp65 en los primeros meses del trasplante y, en caso de infección, tratar con ganciclovir i.v./valganciclovir de forma similar a lo realizado en pacientes con ECMV.
Terapia anticipada frente a placebo o no tratamiento
Tres revisiones sistemáticas12-14 analizan los resultados de los EC realizados en pacientes con trasplante de órgano sólido que comparan la terapia anticipada frente a la diferida, en la que los pacientes son tratados cuando desarrollan ECMV. Incluyen ocho EC, cuatro realizados en trasplante renal, con un total de 282 pacientes. Los resultados muestran una disminución de ECMV en el grupo con terapia anticipada: 11/142 frente a 43/146 en el grupo con terapia diferida [RR (IC 95%) 0,29 (0,11-0,80)]13. No detectan diferencias claras en la incidencia de rechazo agudo ni en la mortalidad, pero la potencia estadística del estudio es baja.
Terapia anticipada frente a tratamiento profiláctico
En varios EC se compara la eficacia de ambas terapias preventivas. Reisching et al.15 incluyen 70 pacientes (10 D+/R-) con trasplante renal; de ellos, 34 recibieron profilaxis con valaciclovir y 36 tratamiento anticipado con valganciclovir. Khoury et al.16 aportan 98 trasplantados renales (29 D+/R-), 49 con profilaxis de valganciclovir durante 100 días y 50 tratamiento anticipado. Kliem et al.17 reclutan 144 pacientes con trasplante renal (44 D+/R-); 70 recibieron profilaxis con ganciclovir oral durante 90 días y 65 tratamiento anticipado con ganciclovir. En todos los estudios, los tratados con profilaxis antiviral tuvieron una menor incidencia de infección CMV, un 3033% absoluto menos, y su presentación fue más tardía que en los pacientes con terapia anticipada. En el estudio de Kliem et al.17, los pacientes con terapia anticipada presentaron una mayor incidencia de enfermedad invasiva por CMV que los que recibieron profilaxis, 4/73 (5,5%) frente a 12/65 (18,5%). La supervivencia de los injertos a los cuatro años también fue mejor en los pacientes con profilaxis, un 92,2% frente al 78,3% en pacientes con terapia anticipada.
Ambas estrategias reducen la incidencia de ECMV, cada una con sus fortalezas y debilidades. La profilaxis introduce el costo económico y los efectos secundarios de la medicación. La terapia anticipada no evita la replicación inicial del CMV y sus posibles efectos, reduce la medicación administrada pero impone una logística de monitorización que tiene implicaciones económicas y organizativas, variables de unos centros a otros. Todos ellos son aspectos a tener en cuenta a la hora de decidir la elección de una de las dos terapias.
3. Tratamiento de la enfermedad por citomegalovirus
El ganciclovir i.v. ha sido el tratamiento de referencia de la ECMV en pacientes con trasplante de órgano sólido. En el EC multicéntrico internacional de Asberg et al.18,19 se incluyeron 321 pacientes adultos con trasplante de órgano sólido, el 73,8% trasplantes renales, que presentaban ECMV: 164 recibieron valganciclovir 900 mg dos veces al día y 157 pacientes ganciclovir i.v. 5 mg/kg dos veces al día. En ambos casos se administró dicha medicación, ajustada a filtrado glomerular, durante 21 días, continuando con valganciclovir 900 mg/día hasta el día 49, con seguimiento de un año. El 45,1% de los pacientes con valganciclovir negativizaron su viremia a los 21 días del tratamiento y un 67,1% a los 49 días. Estos resultados fueron similares a los conseguidos en el grupo con ganciclovir, un 48,8% y un 70,1%, respectivamente. Las tasas de recurrencia clínica y virológica fueron similares en ambos grupos.
Los autores concluyen que la eficacia del valganciclovir no es inferior a la del ganciclovir i.v. En este estudio fueron excluidos los pacientes con afectación grave y los trasplantes pediátricos, situaciones en las que no se pueden extra-polar los resultados obtenidos, tal como indican los autores del estudio.
PREVENCIÓN Y TRATAMIENTO DE LA ENFERMEDAD POR CITOMEGALOVIRUS EN PACIENTES CON TRASPLANTE RENAL. RECOMENDACIONES DE CONSENSO DEL GRUPO PROMETEO
Tras la evaluación de la bibliografía realizada y la valoración de los consensos recientes KDIGO y la Sociedad Internacional de Trasplantes, recomendamos:
1. Prevención
Pacientes D+/R-
- Profilaxis con valganciclovir 900 mg/día, ajustado a filtrado glomerular, durante 3-6 meses.
- Recomendación fuerte.
Pacientes D±/R+
Se aceptan las dos estrategias:
1. Tratamiento anticipado con monitorización de la replicación viral mediante antigenemia pp65 o PCR CMV.
2. Profilaxis con valganciclovir durante 3 meses. Uso especial/experimental profilaxis con valganciclovir.
- Recomendación de consenso.
Pacientes D-/R-
No es necesario un abordaje preventivo.
- Recomendación de consenso.
Pacientes que reciben anticuerpos antilinfocitarios
Administrar profilaxis con valganciclovir durante 1-3 meses en los pacientes que no lo estén recibiendo.
- Recomendación de consenso.
Pacientes pediátricos
No existen estudios controlados específicos en la prevención de la infección-ECMV en la población pediátrica con trasplante renal.
La dosificación de los fármacos antivirales se ajusta en relación con el filtrado glomerular y la superficie corporal.
- Recomendación de consenso.
2. Tratamiento
- Administrar valganciclovir, 900 mg/12 horas, ajustado a filtrado glomerular.
- Recomendación fuerte.
- En pacientes adultos con ECMV grave y en pacientes pediátricos, administrar inicialmente ganciclovir i.v., 5 mg/kg/12 horas, ajustado a filtrado glomerular.
- Recomendación fuerte.
- Se establece una duración mínima del tratamiento de tres semanas y prolongar el tratamiento hasta reducir la replicación viral < 500 copias/ml. Una vez finalizado el tratamiento, controlar la replicación viral cada semana en dos ocasiones o iniciar profilaxis secundaria durante 1-3 meses.
- Recomendación de consenso.
- En pacientes con infección activa asintomática, tratar con valganciclovir 450-900 mg/12 horas, ajustado a filtrado glomerular, con la misma duración y controles anteriores.
- Recomendación de consenso.
- Ajustar de forma individualizada el tratamiento inmunosupresor según el estado clínico y el grado de inmunosupresión. Reducir/suspender el ácido micofenólico en pacientes leucopénicos.
- Recomendación de consenso.
- Valorar conversión a m-TOR en pacientes con ECMV recurrente.
- Recomendación de consenso.
- En pacientes con mala respuesta al tratamiento con valganciclovir, valorar la monitorización de sus niveles y la posible aparición de resistencias.
- Recomendación de consenso.
Conflictos de interés
Los autores declaran que no tienen conflictos de interés potenciales relacionados con los contenidos de este artículo.
Tabla 1. Resultados de los metaanálisis de los ensayos clínicos que comparan la eficacia de la profilaxis frente a la infección de citomegalovirus con tratamiento viral frente a placebo o no tratamiento