Navaneethan SD, Nigwekar SU, Sehgal AR, Strippoli GF. Aldosterone antagonists for preventing the progression of chronic kidney disease: a systematic review and meta-analysis. Clin J Am Soc Nephrol 2009;4:542-51.
Delimitación del tema en estudio
Evaluar los beneficios sobre la proteinuria y función renal, así como los efectos secundarios de los antagonistas de la aldosterona (AA), en pacientes con enfermedad renal crónica (ERC) y proteinuria con independencia de los inhibidores de la enzima de conversión de angiotensina (IECA) o antagonistas de los receptores de angiotensina (ARA) II.
Criterios de selección de estudios
Se incluyeron los ensayos aleatorios y cuasi aleatorios controlados de AA, selectivos y no selectivos, usados solos o en combinación con ARA II, IECA o ambos para la prevención de la progresión de la ERC en pacientes con albuminuria o proteinuria y ERC, usados al menos durante 4 semanas. No hubo ningún estudio que comparara AA solo con placebo. Se incluyeron pacientes con ERC en estadios 1 a 4, de acuerdo con las guías K/DOQI, con albuminuria o proteinuria. De los 11 estudios incluidos que englobaron a 991 pacientes, 10 fueron publicados en forma de artículos, con 776 pacientes, y uno en forma de resumen, que incluyó a 215 pacientes.
Fuentes de datos
MEDLINE (1966 hasta agosto 2008), EMBASE (1980 hasta agosto 2008), Renal Health Library (n.º 2, 2008) y referencias de artículos y libros de texto. No hubo restricción idiomática.
Extracción de datos
Dos investigadores realizaron la extracción de los datos y un tercero resolvió las discrepancias.
Evaluación de la calidad
Se evaluó la cal idad de los estudios mediante la ocultación de la asignación, el anál isis por intención de tratar, completitud del periodo de seguimiento y el enmascaramiento de los investigadores, participantes y evaluadores del desenlace.
Tratamiento de los resultados
Para las variables dicotómicas se calcularon los riesgos relativos (RR) con su intervalo de confianza (IC) del 95%, mediante modelos de efectos aleatorios. Para variables continuas se calcularon las diferencias ponderadas de medias y sus IC. La heterogeneidad fue evaluada con la prueba de la ji al cuadrado y mediante la prueba I2. Se efectuaron análisis separados para los AA selectivos y no selectivos.
También se l levó a cabo un estudio de subgrupos post hoc para comparar la incidencia de hiperpotasemia en pacientes que recibían espironolactona más dos inhibidores del sistema renina-angiotensina-aldosterona (RAA) frente a dos inhibidores RAS solos, y en pacientes que recibían espironolactona más un inhibidor RAS, ( IECA o ARA I I ) frente a IECA o ARA I I aislados.
Promoción
Se señala explícitamente la ausencia de soporte financiero y de conflicto de intereses de los autores.
RESULTADOS PRINCIPALES
De los 133 estudios inicialmente seleccionados, 111 fueron excluidos por diferentes motivos: no ser ensayos aleatorios controlados, investigaciones solapadas, revisiones irrelevantes, artículos de revisión. De los 17 incluidos, 6 fueron descartados en una segunda selección por ser revisiones y estudios retrospectivos.
Finalmente, 11 estudios, con 991 pacientes, cumplieron los requisitos de inclusión.
ANÁLISIS BASAL DE LOS GRUPOS
De los 11 estudios, ocho incluyeron a pacientes diabéticos, uno a pacientes con varios tipos de glomerulopatías y los otros dos incluyeron a pacientes no diabéticos con mayoría de nefropatía IgA. Todos los estudios excluyeron a los pacientes con un filtrado glomerular renal <30 ml/min/1,73m2. La proteinuria basal osciló entre 0,8 y 3,6 g/día. De los 9 estudios que analizaron la eficacia de los AA no selectivos, 3 compararon espironolactona + IECA con monoterapia con IECA y 6 compararon espironolactona más IECA y/o ARA II con IECA y/o ARA II solo. En todos los estudios la dosis de espironolactona fue de 25 mg, excepto en uno que utilizó entre 25 y 50 mg/día. El periodo de seguimiento osciló entre 2 y 20 meses y el tamaño de la muestra varió entre 18 y 256 pacientes; ningún estudio tuvo el poder suficiente para detectar los efectos adversos primarios de evolución, incluyendo mortalidad o la evolución renal a largo plazo.
La ocultación de la asignación fue adecuada en cinco y poco clara en seis ensayos. En ninguno de los estudios hubo enmascaramiento de los participantes, investigadores o evaluadores de la evolución. Solamente 1 de los 11 ensayos se analizó por intención de tratar. La tasa de abandono varió entre 0-15%, no siendo diferente entre el grupo de tratamiento y el grupo control.
- AA no selectivos: No se demostró heterogeneidad significativa para la variación del filtrado glomerular, presión arterial sistólica o diastólica. Sí, en cambio, para la variación de la proteinuria.
- AA selectivos: En comparación con placebo, la asociación de eplerenona a IECA en los dos ensayos analizados redujo la proteinuria y las presiones arteriales sistólica y diastólica a las 12 semanas de tratamiento, sin variación en el filtrado glomerular renal.
- Efectos secundarios: Globalmente, la espironolactona aumentó el riesgo de hiperpotasemia cuando se asoció a algún inhibidor del sistema renina-angiotensina (8 estudios, 436 pacientes RR 3,06, IC 95%: 1,26 a 7,41). Por separado, la espironolactona asociada a dos inhibidores del sistema renina angiotensina produjo hiperpotasemia (4 estudios, 149 pacientes, RR 4,30, IC 95%: 1,12 a 16,51), no así si se asoció a un solo inhibidor (5 estudios, 277 pacientes, RR 2,41, IC 95%: 0,79 a 7,31). La ginecomastia sólo se describió en 6 casos de un estudio de 83 pacientes, que no necesitaron suspender la medicación.
No se demostró heterogeneidad significativa para la variación del filtrado glomerular, presión arterial sistólica o diastólica. Sí, en cambio, para la variación de la proteinuria.
- AA selectivos: En comparación con placebo, la asociación de eplerenona a IECA en los dos ensayos analizados redujo la proteinuria y las presiones arteriales sistólica y diastólica a las 12 semanas de tratamiento, sin variación en el filtrado glomerular renal. Efectos secundarios
- Globalmente, la espironolactona aumentó el riesgo de hiperpotasemia cuando se asoció a algún inhibidor del sistema renina-angiotensina (8 estudios, 436 pacientes, RR 3,06, IC 95%: 1,26 a 7,41). Por separado, la espironolactona asociada a dos inhibidores del sistema renina-angiotensina produjo hiperpotasemia (4 estudios, 149 pacientes, RR 4,30, IC 95%: 1,12 a 16,51), no así si se asoció a un solo inhibidor (5 estudios, 277 pacientes, RR 2,41, IC 95%: 0,79 a 7,31). La ginecomastia sólo se describió en 6 casos de un estudio de 83 pacientes, que no necesitaron suspender la medicación. La eplerenona asociada a IECA no aumentó de forma significativa el riesgo de hiperpotasemia (2 estudios, 509 pacientes, RR 1,62, IC 95%: 0,66 a 3,95). (ver tabla 1)
CONCLUSIONES DE LOS AUTORES
Del análisis de los estudios incluidos, los antagonistas selectivos y no selectivos de aldosterona, añadidos al bloqueo del sistema renina-angiotensina-aldosterona en pacientes con ERC, reducen la proteinuria de 24 horas y la presión arterial, pero sin afectar al filtrado glomerular. En comparación con la inhibición aislada del sistema renina-angiotensina, la espironolactona, en mayor grado que la eplerenona, aumenta la incidencia de hiperpotasemia.
En pacientes con ERC estadio I-III y proteinuria persistente a pesar de recibir dosis máximas de IECA y/o ARA II, los AA pueden reducir la proteinuria. Sin embargo, estos fármacos deberían añadirse en dosis bajas con vigilancia estrecha del potasio sérico durante el tratamiento.
COMENTARIOS
La gran limitación de esta revisión sistematizada, que los propios autores reconocen, es el número insuficiente de casos, la variabilidad en el diseño de los estudios, su incapacidad para evaluar objetivos primarios, como el efecto de los AA sobre la mortalidad, su heterogeneidad y la alta tasa de abandono en los estudios originales.
El amplio uso de los inhibidores RAS en pacientes con ERC ha determinado una significativa reducción de la progresión de la ERC en torno a un 20-30%. Aunque los IECA/ARA II inhiben el sistema RAA, no disminuyen de forma eficaz los niveles de aldosterona, por lo que la adición de un antagonista de la aldosterona constituye una estrategia de tratamiento efectiva y segura. El uso de AA, tanto selectivos como no selectivos, añadidos a terapia con IECA y/o ARA II, puede tener una acción clínica beneficiosa en pacientes con ERC y proteinuria, sean o no diabéticos.
El hecho de que la aldosterona pueda contribuir a la progresión de la enfermedad renal y no solamente en el fenómeno de escape, es analizado en una revisión editorial recientemente publicada por Becker et al.1, en donde la adición de un AA no selectivo a inhibidores RAS redujo la proteinuria en un 54%, sin modificación de la presión arterial, un hallazgo también observado en pacientes diabéticos tipo 2.
Desde un punto de vista fisiopatológico, tiene interés el posible papel nocivo de la aldosterona en el riñón por vía inflamatoria o profibrótica a través del estrés oxidativo, la activación del NF-κ-B, AP-1, ICAM, VCAM y otros2,3.
Finalmente, hacen falta ensayos clínicos a largo plazo que analicen los efectos de los AA sobre el filtrado glomerular renal, la necesidad de tratamiento renal sustitutivo y la mortalidad.
CONCLUSIONES DE LOS REVISORES
La adición de AA selectivo o no selectivo a un IECA y/o ARA I I parece eficaz en los pacientes con ERC con FG >30 ml /min/1,73 m2 con proteinuria e hipertensión. Dosis bajas de espironolactona o eplerenona son eficaces en pacientes con nefropatía diabética. Como efectos secundarios, los AA producen hiperpotasemia y ginecomastia. Estos hallazgos sugieren la necesidad de diseñar ensayos controlados y aleatorizados con mayor número de pacientes, con diferentes tipos de enfermedad renal, con o sin proteinuria, y con variables de resultado clínicas.
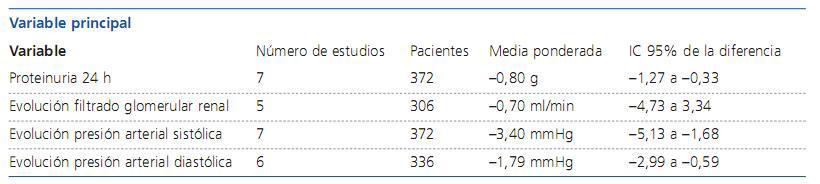
Tabla 1. Variable principal