La enfermedad renal crónica (ERC) es una condición prevalente que requiere herramientas fiables para predecir la progresión a enfermedad renal crónica terminal (ERCT). La ecuación KFRE, validada internacionalmente, permite estimar el riesgo de progresión a 2 y 5 años. Sin embargo, no ha sido validada en población española. Este estudio tiene como objetivo evaluar la capacidad predictiva de la KFRE en una cohorte de pacientes españoles.
MétodosEstudio multicéntrico, observacional y retrospectivo, en pacientes con GFRe<30ml/min seguidos en consultas de nefrología entre enero de 2016 y 2021. Se incluyeron 602 pacientes con datos clínicos y demográficos. La capacidad predictiva de la KFRE, en sus versiones de 4 y 8 variables, se evaluó mediante análisis de regresión de Cox y curvas ROC.
ResultadosDe los 602 pacientes incluidos el 60% eran varones. La diabetes fue la principal etiología. El 37% de los pacientes que iniciaron TRS lo hicieron a los 2 años y el 70% mediante hemodiálisis. Los pacientes que iniciaron TRS (50,6%) eran más jóvenes, con peor GFRe y mayor albuminuria basal. La ecuación KFRE de 4 variables mostró un AUC de 0,7639 (IC 95%: 0,71-0,81) y precisión superior al modelo de 8 variables.
ConclusionesLa ecuación KFRE, especialmente en su versión de 4 variables, demuestra ser útil para predecir la progresión a ERCT en población española. No obstante, es necesaria su recalibración para mejorar la precisión en este contexto.
Chronic kidney disease (CKD) is a prevalent condition that requires reliable tools to predict its progression to end-stage renal disease (ESRD). The KFRE equation, internationally validated, allows for estimating the risk of progression at 2 and 5 years. However, it has not been validated in the Spanish population. This study aims to evaluate the predictive capacity of the KFRE in a cohort of Spanish patients.
MethodsThis is a multicenter, observational, and retrospective study conducted in patients with an estimated glomerular filtration rate (eGFR) <30ml/min who were followed in nephrology clinics between January 2016 and 2021. A total of 602 patients with clinical and demographic data were included. The predictive capacity of the KFRE, in its 4-variable and 8-variable versions, was evaluated using Cox regression analysis and ROC curves.
ResultsOf the 602 patients included, 60% were male. Diabetes was the main etiology. Among the patients who started renal replacement therapy (RRT), 37% did so within two years, and 70% began with hemodialysis. Patients who initiated RRT (50.6%) were younger, had a lower eGFR, and exhibited higher baseline albuminuria. The 4-variable KFRE equation showed an AUC of 0.7639 (95% CI: 0.71-0.81) and demonstrated superior accuracy compared to the 8-variable model.
ConclusionsThe KFRE equation, particularly in its 4-variable version, proves to be useful in predicting the progression to ESRD in the Spanish population. However, recalibration is necessary to improve its accuracy in this context.
La enfermedad renal crónica (ERC) representa un importante problema de salud pública global, con una prevalencia del 15% en España1,2. Esta condición está asociada a un aumento del inicio de terapia renal sustitutiva (TRS) del 23%, con variaciones significativas entre comunidades autónomas, siendo más alta en Canarias y la Comunidad Valenciana, y más frecuente en hombres y personas mayores de 75 años2.
La progresión de la ERC a ERC terminal (ERCT) conlleva un impacto sustancial en la supervivencia y los costes sanitarios asociados al inicio de la TRS. Por ello, la identificación temprana de pacientes en riesgo es crucial para optimizar el manejo clínico y planificar adecuadamente el inicio de la TRS3,4.
En respuesta a estas necesidades, se han desarrollado modelos de predicción del riesgo como la Kidney Failure Risk Equation (KFRE), la cual estima el riesgo de progresión a ERCT en 2 y 5 años mediante variables demográficas y analíticas básicas. Las guías internacionales como KDIGO 2024 destacan el uso de estas herramientas para mejorar la estratificación del riesgo en pacientes con ERC avanzada, permitiendo intervenciones más oportunas y eficientes3.
Sin embargo, los protocolos de remisión a nefrología varían ampliamente entre guías internacionales3,5–7. Una remisión prematura puede resultar en intervenciones innecesarias en pacientes de bajo riesgo, mientras que una tardía podría retrasar el inicio adecuado de la TRS en aquellos con alto riesgo de progresión8. Aunque parámetros como el filtrado glomerular estimado (GFRe) y la albuminuria son útiles para clasificar la ERC, su capacidad para predecir progresión a ERCT de manera aislada es limitada9.
Para abordar estas limitaciones, modelos predictivos como la KFRE, desarrollada por Tangri et al., se han incorporado en guías clínicas como ERBP y KDIGO para estimar el riesgo de progresión a ERCT en periodos de 2 y 5 años3,10,11. La KFRE se ha desarrollado en diferentes versiones, que varían en el número de variables incluidas y en su aplicabilidad a distintas poblaciones.
Existen 2 principales versiones de la KFRE según la cantidad de variables consideradas:
- 1.
KFRE de 4 variables: es la versión más utilizada y la más sencilla para su implementación en la práctica clínica. Incluye las variables edad, sexo, GFRe y relación albúmina/creatinina en orina (ACR). Su simplicidad permite su integración en herramientas de estratificación del riesgo sin necesidad de pruebas de laboratorio adicionales.
- 2.
KFRE de 8 variables: además de los parámetros anteriores, incorpora valores séricos de calcio, fosfato, bicarbonato y albúmina. Aunque ofrece una mayor precisión predictiva en algunos contextos, su uso es menos común en la práctica diaria debido a la necesidad de disponer de análisis bioquímicos más específicos.
En cuanto a su desarrollo y validación, la KFRE tiene 2 enfoques principales:
- •
KFRE original: derivada y validada en cohortes canadienses, con coeficientes de regresión ajustados a esta población. Ha mostrado una excelente capacidad discriminativa en diferentes estudios, pero su calibración puede verse afectada cuando se aplica a poblaciones con características clínicas y demográficas distintas11.
- •
KFRE pooled: desarrollada mediante un metaanálisis de datos individuales de múltiples cohortes internacionales para mejorar la generalización del modelo en distintas poblaciones. Aunque mantiene la estructura de la ecuación original, sus coeficientes han sido recalibrados para reflejar un riesgo basal más ajustado a diferentes regiones. Estudios previos han demostrado que la versión pooled mejora la calibración en cohortes no norteamericanas, reduciendo la sobreestimación del riesgo observada con la ecuación original12.
La ecuación KFRE ha sido validada en cohortes norteamericanas, europeas y asiáticas, mostrando buena capacidad predictiva12–14.
No obstante, la KFRE no ha sido validada en población española. Dado que los factores demográficos, clínicos y sociales pueden influir en su rendimiento, es esencial evaluar y, si es necesario, recalibrar esta herramienta para garantizar su aplicabilidad en nuestro contexto. Este estudio multicéntrico tiene como objetivo validar la capacidad predictiva de la KFRE en pacientes españoles con ERC avanzada.
Material y métodosObjetivoEl objetivo del estudio es validar la aplicabilidad de la ecuación KFRE de 4 y 8 variables en la población española mediante la valoración del área bajo la curva (AUC) resultante de la clasificación generada por la KFRE (alto o bajo riesgo de fallo renal) y la realidad clínica del paciente.
Diseño del estudioEstudio observacional retrospectivo multicéntrico que incluyó, de forma consecutiva, a todos los pacientes adultos mayores de 18 años en seguimiento en consultas de nefrología de los hospitales participantes, con GFRe<30ml/min/1,73m2 (estadio 4 de ERC) medido por la fórmula del Chronic Kidney Disease Epidemiology Collaboration (CKD-EPI). Los pacientes fueron atendidos desde el 1 de enero de 2016 hasta completar 5 años de seguimiento o el inicio de TRS, trasplante renal o muerte de causa renal.
El tamaño muestral calculado para estimar un AUC superior a 0,9 (excelente clasificación), con un intervalo de confianza al 95% y un error de 0,05, fue de 628 pacientes, distribuidos en 314 pacientes que iniciaron TRS antes de la finalización del seguimiento de 5 años y 314 pacientes que completaron el seguimiento sin precisar el inicio de TRS.
PacientesCriterios de inclusión:
- •
Edad>18años.
- •
GFRe<30ml/min/1,73m2 al inicio del seguimiento en la consulta ERCA y que, siendo candidatos a TRS, no hayan iniciado dicha terapia al finalizar el seguimiento (5 años).
- •
GFRe<30ml/min/1,73m2 al inicio del seguimiento en consulta ERCA que hayan iniciado TRS o fallecido de causa renal antes de finalizar el seguimiento (5 años).
Criterios de exclusión:
- •
GFRe<10ml/min/1,73m2, trasplante renal previo o requerimiento previo de TRS al inicio del seguimiento.
- •
No disponibilidad de al menos 2 mediciones con un intervalo de 3 meses de GFRe o albuminuria basal.
- •
Pérdida de seguimiento antes de la finalización del estudio.
- •
Embarazo.
- •
Fallecimiento antes de la finalización del seguimiento de 5 años por causas no renales.
- •
Pacientes no candidatos a TRS.
Todos los pacientes requerían al menos 2 mediciones de GFRe y albuminuria medida por cociente albúmina/creatinina (CAC) con un intervalo de 3 meses.
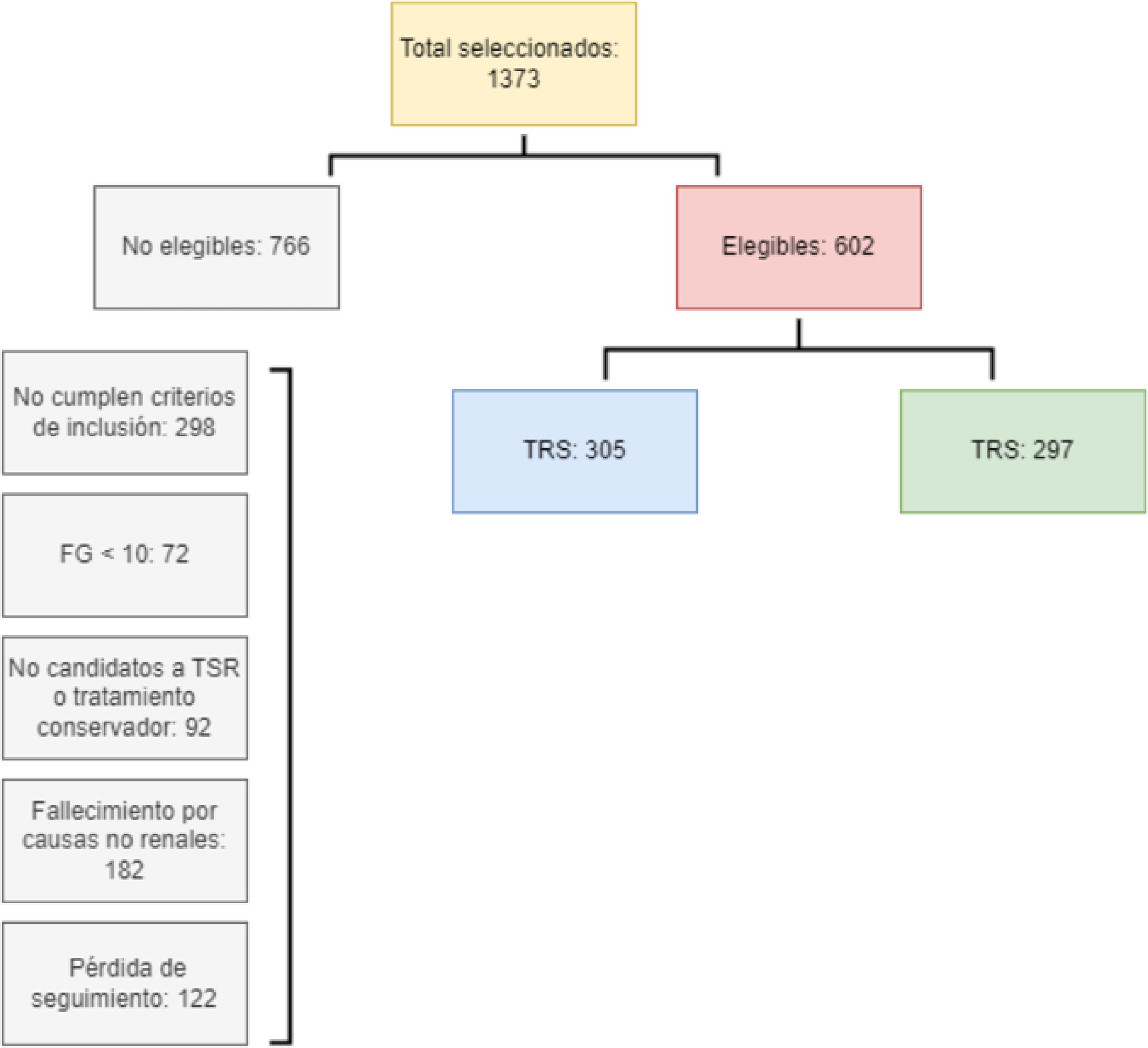
La figura 1 muestra el proceso de selección de pacientes en el estudio. De los 1.373 pacientes iniciales, 766 fueron excluidos por diversos criterios. Finalmente, 602 pacientes fueron considerados elegibles, de los cuales 305 recibieron TSR y 297 no.
VariablesSe recogieron variables demográficas y resultados de laboratorio: edad, sexo y etnicidad. El GFRe se estimó utilizando la ecuación de creatinina del CKD-EPI 2009. La albuminuria se representó como una relación ACR transformada logarítmicamente. Otras medidas de excreción de proteínas en orina se transformaron a ACR usando ecuaciones previamente desarrolladas15. Se obtuvieron valores basales de albúmina sérica, fósforo, calcio y bicarbonato de cada paciente. Se excluyeron del análisis a los participantes cuyos datos basales no estaban disponibles.
La variable principal fue el cálculo de KFRE de 4 y 8 variables basales, a los 2 y a los 5 años de seguimiento. Las variables secundarias fueron la enfermedad renal de base, la modalidad de TRS iniciada y el tipo de inicio (urgente o programado), así como la causa del mismo y, en su caso, la muerte de causa renal.
La elegibilidad para TRS en este estudio se basó en la decisión clínica del médico tratante en consenso con el paciente, sin criterios unificados debido a la naturaleza retrospectiva del estudio. Esto refleja la práctica real, donde la indicación de TRS no depende solo de parámetros biológicos, sino también de la toma de decisiones compartida.
Definición de muerte de causa renal: fallecimiento con ERCT sin inicio de hemodiálisis, sin que exista otra causa de muerte, o cuando el tratamiento de diálisis se suspendió o no se inició por futilidad terapéutica o por rechazo del paciente o la familia.
Análisis estadísticoLas variables categóricas se describieron como número total y porcentaje para cada categoría. Las variables continuas se expresaron como media±desviación estándar. Las comparaciones entre variables continuas se realizaron con la prueba «t» de Student y las variables categóricas con la prueba de Chi-cuadrado.
La recalibración de la ecuación KFRE para la población española se realizó utilizando un modelo de riesgos proporcionales de Cox, manteniendo las mismas variables del modelo original (edad, sexo, GFRe y ACR). Para adaptar la ecuación al contexto español se implementaron 3 enfoques de calibración del riesgo a 2 y 5 años (material suplementario 1):
- 1.
KFRE original: modelo predictivo desarrollado en cohortes canadienses, basado en variables clínicas y de laboratorio, con alta capacidad discriminativa para estimar el riesgo de progresión a insuficiencia renal terminal en 2 y 5 años.
- 2.
KFRE calibrada (Regional Calibrated-non-North America): variante de la ecuación original ajustada mediante un factor de calibración regional, corrigiendo la sobreestimación del riesgo observada en algunas cohortes fuera de América del Norte, optimizando así su precisión predictiva en poblaciones específicas.
- 3.
KFRE ponderada (pooled): modelo derivado de un metaanálisis de múltiples cohortes internacionales, en el que los coeficientes de regresión son estimados mediante métodos de efectos aleatorios, permitiendo una mayor generalización y aplicabilidad global del modelo.
Para comparar el rendimiento de cada modelo se calcularon el Brier Score, el sesgo y la precisión en la predicción del riesgo a 2 y 5 años. La ecuación con menor puntuación en el Brier Score se consideró la más precisa. Asimismo, se evaluó la capacidad discriminatoria de cada modelo mediante el cálculo del AUC utilizando curvas ROC.
Además, se realizaron análisis estratificados en función del nivel basal de GFRe, diferenciando entre pacientes con GFRe≤20ml/min y GFRe>20ml/min para evaluar la validez del modelo en distintos subgrupos.
Todos los cálculos se realizaron mediante el paquete estadístico SAS versión 9.4 (SAS Institute).
Aprobación éticaEste estudio fue aprobado por el comité de ensayos clínicos del Hospital Universitario de Canarias —número de aprobación (CHUC_2021_67 [KFRESPAÑA])—.
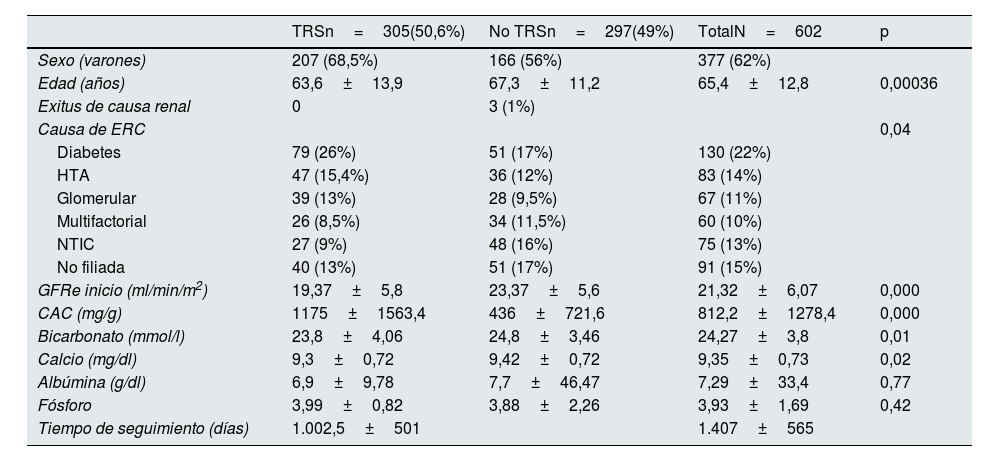
ResultadosCaracterísticas basalesSe incluyeron un total de 602 pacientes en el estudio, de los cuales aproximadamente el 60% eran varones en ambas cohortes. En la tabla 1 se muestran las características basales de los pacientes a los 2 y 5 años.
- •
Los pacientes que iniciaron TRS eran más jóvenes (63,6±13,9años, p<0,0003) y presentaban un peor GFR (19,37±5,8ml/min, p<0,000) y mayor albuminuria basal (1175±1563mg/g, p<0,000).
- •
La principal causa de enfermedad renal en ambos grupos fue la diabetes, seguida de la hipertensión.
- •
La media de seguimiento global fue de 1407±565días.
Características basales
| TRSn=305(50,6%) | No TRSn=297(49%) | TotalN=602 | p | |
|---|---|---|---|---|
| Sexo (varones) | 207 (68,5%) | 166 (56%) | 377 (62%) | |
| Edad (años) | 63,6±13,9 | 67,3±11,2 | 65,4±12,8 | 0,00036 |
| Exitus de causa renal | 0 | 3 (1%) | ||
| Causa de ERC | 0,04 | |||
| Diabetes | 79 (26%) | 51 (17%) | 130 (22%) | |
| HTA | 47 (15,4%) | 36 (12%) | 83 (14%) | |
| Glomerular | 39 (13%) | 28 (9,5%) | 67 (11%) | |
| Multifactorial | 26 (8,5%) | 34 (11,5%) | 60 (10%) | |
| NTIC | 27 (9%) | 48 (16%) | 75 (13%) | |
| No filiada | 40 (13%) | 51 (17%) | 91 (15%) | |
| GFRe inicio (ml/min/m2) | 19,37±5,8 | 23,37±5,6 | 21,32±6,07 | 0,000 |
| CAC (mg/g) | 1175±1563,4 | 436±721,6 | 812,2±1278,4 | 0,000 |
| Bicarbonato (mmol/l) | 23,8±4,06 | 24,8±3,46 | 24,27±3,8 | 0,01 |
| Calcio (mg/dl) | 9,3±0,72 | 9,42±0,72 | 9,35±0,73 | 0,02 |
| Albúmina (g/dl) | 6,9±9,78 | 7,7±46,47 | 7,29±33,4 | 0,77 |
| Fósforo | 3,99±0,82 | 3,88±2,26 | 3,93±1,69 | 0,42 |
| Tiempo de seguimiento (días) | 1.002,5±501 | 1.407±565 |
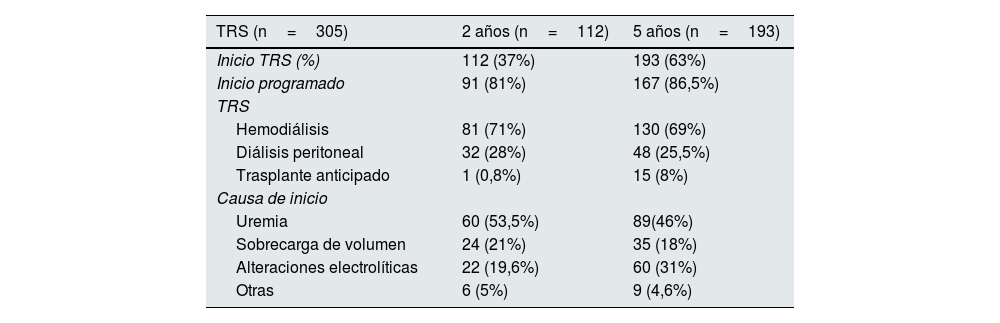
De los 305 pacientes que iniciaron TRS 112 (37%) lo hicieron a los 2 años y 193 (63%) a los 5 años (tabla 2). La hemodiálisis fue la principal técnica de inicio en ambos grupos (70%), con un inicio programado en aproximadamente el 80% de los pacientes. La principal causa de inicio fue la aparición de clínica urémica (50%), seguida de sobrecarga de volumen (20%).
Características basales del grupo de terapia renal sustitutiva
| TRS (n=305) | 2 años (n=112) | 5 años (n=193) |
|---|---|---|
| Inicio TRS (%) | 112 (37%) | 193 (63%) |
| Inicio programado | 91 (81%) | 167 (86,5%) |
| TRS | ||
| Hemodiálisis | 81 (71%) | 130 (69%) |
| Diálisis peritoneal | 32 (28%) | 48 (25,5%) |
| Trasplante anticipado | 1 (0,8%) | 15 (8%) |
| Causa de inicio | ||
| Uremia | 60 (53,5%) | 89(46%) |
| Sobrecarga de volumen | 24 (21%) | 35 (18%) |
| Alteraciones electrolíticas | 22 (19,6%) | 60 (31%) |
| Otras | 6 (5%) | 9 (4,6%) |
Para valorar el riesgo de TRS y compararlo con la tasa de evento real, se analizaron los modelos con menor sesgo, así como lo descrito en el material suplementario 2.
- •
Evento a los 2 años: la ecuación KFRE ponderada de 4 variables mostró una mejor capacidad predictiva con un AUC de 0,766, Brier Score de 0,196, sesgo de 0.,29 y precisión de 0,84, frente a la KFRE original. La ecuación KFRE ponderada de 8 variables también presentó menor sesgo (0,35), mayor precisión (0,89) y un AUC de 0,68 frente a la KFRE original (tabla 1 del material suplementario 2).
- •
Evento a los 5 años: la ecuación KFRE ponderada mostró menor sesgo tanto en la versión de 4 variables (sesgo de 0,01, precisión de 0,64) como en la de 8 variables (sesgo de 0,07, precisión de 0,72) (tabla 1 del material suplementario 2).
Para identificar el modelo con mejor capacidad discriminativa se compararon los modelos de KFRE ponderado de 4 y 8 variables a los 2 y 5 años (tabla 2 del material suplementario 2):
- •
A los 2 años: la KFRE ponderada de 4 variables presentó un mayor AUC (0,763; IC 95%: 0,71-0,81) frente a la KFRE ponderada de 8 variables (AUC 0,682; IC 95%: 0,62-0,73) (p<0,0001).
- •
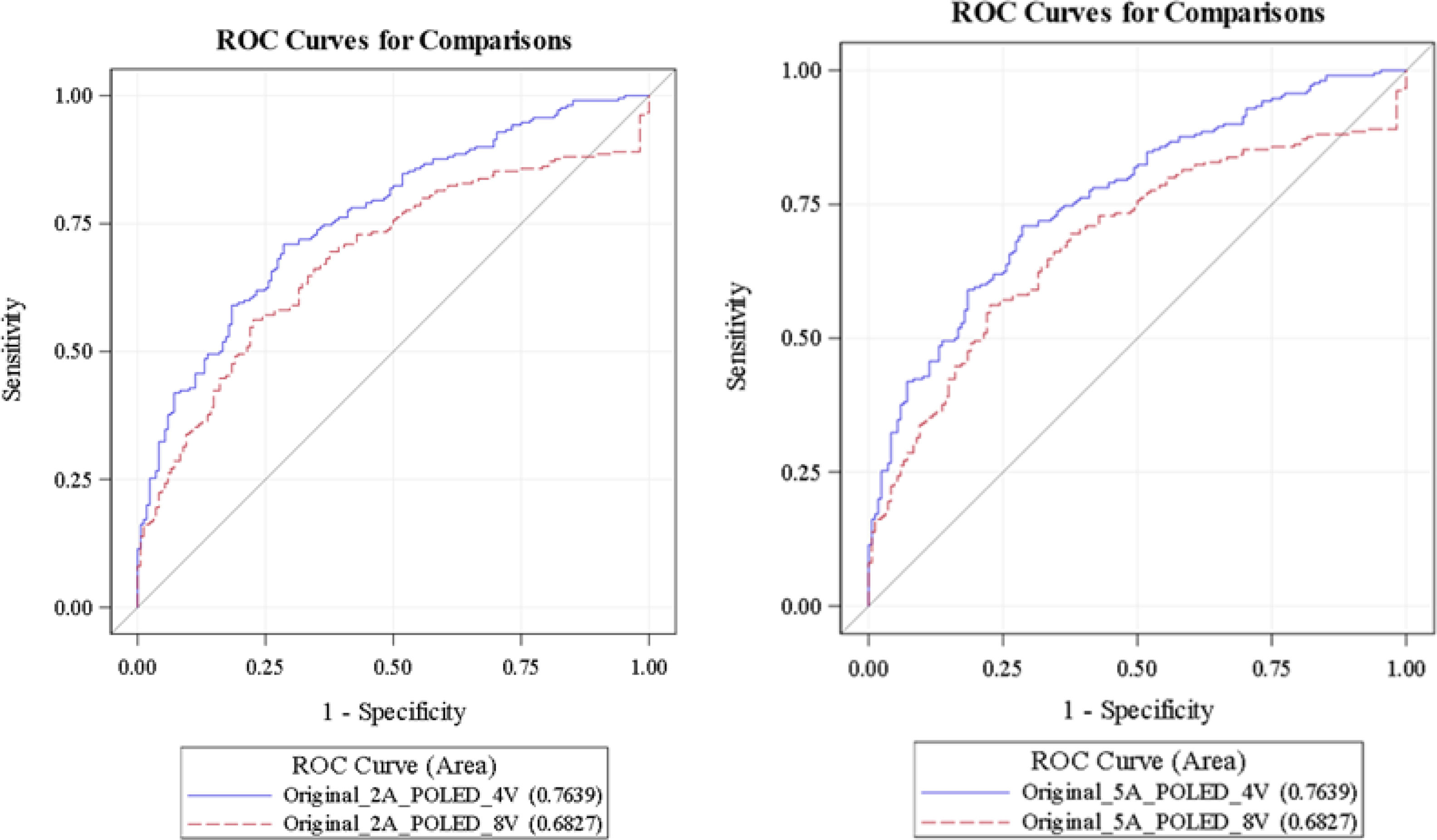
A los 5 años: de manera similar, la KFRE ponderada de 4 variables mostró un mayor AUC (0,7639; IC 95%: 0,71-0,81) comparado con la KFRE ponderada de 8 variables (0,682; IC 95%: 0,62-0,73) (p<0,001) (fig. 2).
GFR<=20ml/min:
- •
Evento a los 2 años: la KFRE ponderada de 4 variables mostró una mejor capacidad predictiva (AUC 0,733, Brier Score 0,202, sesgo 0,29 y precisión 0,84) frente a la KFRE original. La KFRE ponderada de 8 variables también presentó menor sesgo (0,35), mayor precisión (0,89) y un AUC de 0,656 frente a la KFRE original.
- •
Evento a los 5 años: la KFRE ponderada mostró menor sesgo en la versión de 4 variables (sesgo de 0,01, precisión de 0,64) y en la de 8 variables (sesgo de 0,07, precisión de 0,72). La KFRE ponderada de 4 variables presentó un mayor AUC (0,752; IC 95%: 0,682-0,823) frente a la KFRE ponderada de 8 variables (AUC 0,656; IC 95%: 0,578-0,736) (p=0,0017).
GFR>20ml/min:
- •
Evento a los 2 años: la KFRE ponderada de 4 variables presentó una mejor capacidad predictiva (AUC 0,673, Brier Score 0,277, sesgo 0,29 y precisión 0,84) frente a la KFRE original. La KFRE ponderada de 8 variables también mostró menor sesgo (0,35), mayor precisión (0,89) y un AUC de 0,662 frente a la KFRE original.
- •
Evento a los 5 años: La KFRE ponderada mostró menor sesgo tanto en la versión de 4 variables (sesgo de 0,01, precisión de 0,64) como en la de 8 variables (sesgo de 0,07, precisión de 0,72). No se observaron diferencias significativas en cuanto al AUC de ambos modelos en los eventos a los 2 y 5 años (p=1,000).
El análisis de las curvas ROC mostró una capacidad predictiva superior del modelo KFRE de 4 variables en comparación con el de 8 variables, tanto a los 2 como a los 5 años. A los 2 años el área bajo la curva (AUC) fue mayor en el modelo de 4 variables (0,7639; IC 95%: 0,71-0,81) frente al de 8 variables (0,682; IC 95%: 0,62-0,73), lo que sugiere que el modelo de 4 variables discrimina mejor entre los pacientes que progresarán a ERCT en este periodo. Este patrón se mantuvo a los 5 años, con una diferencia consistente en las AUC (0,7639 frente a 0,682).
DiscusiónEste estudio valida la capacidad predictiva de la fórmula KFRE de 4 variables en pacientes españoles con ERCA, demostrando un mejor desempeño en comparación con el modelo de 8 variables. La curva ROC mostró un AUC de 0,7639, tanto a los 2 como a los 5 años, lo que refuerza la utilidad del modelo simplificado como herramienta práctica y eficiente para la estratificación del riesgo de progresión a TRS. Este hallazgo coincide con estudios previos que evaluaron el desempeño del modelo KFRE en otras poblaciones, como el análisis del Reino Unido, donde se observó un AUC superior a 0,9, pero con necesidad de recalibración para ajustar la sobreestimación del riesgo en pacientes de bajo riesgo14. De manera similar, en la cohorte portuguesa el modelo de 4 variables presentó un AUC elevado (0,903 a 2 años), aunque se identificaron desafíos en términos de especificidad en grupos específicos16.
En nuestra población española, la capacidad predictiva global de la KFRE fue limitada, reflejada en un AUC inferior a 0,8, lo que subraya la importancia de recalibrar la fórmula para ajustarla a las características de cada población17,18. Además, en pacientes con ERCA (GFRe<20ml/min/1,73m2), aunque útil, la fórmula KFRE no captura completamente factores clínicos, sociales y emocionales que influyen en la decisión de iniciar TRS, como la presencia de síntomas urémicos o sobrecarga de volumen19. Esto es consistente con observaciones previas de que la KFRE tiende a sobreestimar el riesgo en pacientes ancianos debido al riesgo competitivo de muerte antes de alcanzar insuficiencia renal20,21.
La toma de decisiones compartida (SDM, por sus siglas en inglés) se identifica como un enfoque esencial, integrando no solo factores biomédicos, sino también preferencias del paciente, calidad de vida y metas personales. Herramientas como la KFRE podrían complementarse con medidas personalizadas, como el índice Bansal, para guiar decisiones individualizadas, especialmente en pacientes ancianos frágiles donde la calidad de vida puede prevalecer sobre la prolongación de esta19. Un estudio japonés de Okada et al. sugirió que incluir biomarcadores dinámicos, como cambios anuales en FG y proteinuria, mejora significativamente la predicción, indicando una dirección para futuras investigaciones17. Además, enfoques basados en inteligencia artificial (IA), como los propuestos por Bai et al., han mostrado un desempeño comparable o superior al KFRE, permitiendo integrar múltiples variables clínicas y biomarcadores dinámicos, lo que podría abordar limitaciones actuales de sensibilidad y especificidad en subgrupos específicos22.
Implicación y planificación del inicio de terapia renal sustitutivaUn aspecto positivo de este estudio es que más del 80% de los pacientes iniciaron TRS de manera programada, lo que resalta la efectividad de las consultas de ERCA en la planificación del tratamiento. Este hallazgo es crucial, ya que el inicio planificado, especialmente en pacientes que comienzan con hemodiálisis, se asocia con mejores resultados clínicos, como menor uso de catéteres temporales y mayor preparación de acceso vascular permanente. Este resultado coincide con la revisión de Smart et al., que evidenciaron que la derivación temprana a nefrología reduce significativamente el inicio con acceso vascular temporal (RR 0,47, IC 95%: 0,45-0,50)23.
La proporción de inicios programados en nuestra cohorte supera los estándares internacionales, donde las tasas de inicio no programado oscilan entre el 24% y el 49%24,25. Esto subraya la importancia de implementar herramientas predictivas como la KFRE, junto con estrategias proactivas para optimizar la preparación del paciente y los resultados clínicos. Sin embargo, también es evidente la necesidad de incorporar variables adicionales, como factores psicosociales o contextuales, para mejorar su precisión. Estudios prospectivos serán esenciales para validar estos ajustes en la población española y explorar enfoques avanzados, como modelos de aprendizaje automático, que aborden la complejidad del manejo clínico en ERCA.
Fortalezas y limitaciones del estudioFortalezas:
- •
Validación en población española: este es uno de los primeros estudios en validar la KFRE en una cohorte multicéntrica de pacientes con enfermedad renal crónica avanzada en España, lo que aporta datos específicos y relevantes para esta población.
- •
Enfoque clínicamente relevante: la selección de pacientes candidatos a TRS refleja la práctica habitual en nefrología, asegurando que los hallazgos sean aplicables en el contexto clínico real.
- •
Evaluación comparativa: se han analizado diferentes versiones de la ecuación KFRE (4 y 8 variables) y se han realizado análisis por subgrupos según el filtrado glomerular estimado, lo que permite una evaluación más detallada de su rendimiento predictivo.
- •
Uso de medidas robustas de rendimiento predictivo: se incluyeron métricas como el Brier Score, el sesgo y la precisión, además del AUC de la curva ROC, lo que refuerza la validez de los resultados.
Limitaciones:
- •
Naturaleza retrospectiva del estudio: la inclusión de pacientes en función de registros clínicos puede haber introducido sesgos de selección y limitaciones en la estandarización de criterios para la indicación de TRS.
- •
Exclusión de pacientes fallecidos antes del seguimiento: esto puede haber generado un sesgo de supervivencia, subestimando el impacto de la mortalidad en la progresión de la enfermedad renal.
- •
Ausencia de criterios objetivos para la indicación de TRS: la decisión clínica de iniciar TRS fue tomada por el médico tratante en consenso con el paciente, sin un protocolo unificado, lo que podría afectar la comparación con estudios previos.
- •
Necesidad de recalibración del modelo: aunque la ecuación KFRE mostró un buen desempeño, los valores de AUC en esta población fueron inferiores a los reportados en estudios internacionales, lo que indica la necesidad de ajustes adicionales para mejorar su precisión en pacientes españoles.
- •
Falta de integración de eventos competitivos: la mortalidad como desenlace alternativo no fue considerada en los análisis principales, lo que podría haber limitado la evaluación completa del riesgo en esta población.
La fórmula KFRE de 4 variables demostró ser una herramienta útil y práctica para la estratificación del riesgo de progresión a TRS. Sin embargo, su implementación en la práctica clínica requiere ajustes para maximizar su aplicabilidad en el contexto español. Este estudio resalta tanto las fortalezas como las limitaciones del modelo, subrayando la necesidad de combinarlo con estrategias clínicas integrales en las consultas de ERCA.
FinanciaciónEl estudio fue financiado en parte por subvenciones del Instituto de Salud Carlos III, Madrid, España (ICI21/00042 y Red RICORS RD21/0005/0012), FONDOS FEDER y FIISC (PFIISC23/12).
AutoríaBeatriz Escamilla y Marco Montomoli comparten la autoría principal de este estudio.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.