Caso clínico
Varón de 68 años, exfumador (dosis acumulada 20 paquetesaño), con antecedentes personales de hiperuricemia, hipertensión arterial de larga evolución e insuficiencia renal crónica atribuida a nefroangioesclerosis con creatininas habituales en torno a 2,7 mg/dL.
Consulta por angina de esfuerzo realizándose coronariografía que mostró enfermedad de dos vasos (coronaria derecha y circunfleja). Se efectuó un intervencionismo coronario percutáneo mediante angioplastia y colocación de stent en descendente proximal y coronaria derecha. A las 48 horas de la intervención presenta insuficiencia renal aguda (pico máximo de creatinina en el cuarto día: 4,8 mg/dL), sin presentar síntomas y con diuresis mantenida. La ecografía mostró riñones disminuidos de tamaño, sin dilatación de la vía excretora. Hemograma, bioquímica, complemento y autoinmunidad normales. Recuperación progresiva de la función renal, adquiriendo a los 12 días sus cifras basales de creatinina (2,47 mg/dL).
Tras 25 días consulta por cuadro consistente en astenia y edemas progresivos a nivel de extremidades inferiores, presentando nuevo episodio de insuficiencia renal aguda sin factor desencadenante aparente.
Exploración física: PA 145/85 mmHg; FC 80 lpm; Tª 36,2ºC. Auscultación cardio-pulmonar: sin hallazgos. Extremidades: Edema bimaleolar leve. Pulsos periféricos presentes y simétricos. Abdomen anodino. No alteraciones cutáneas.
Analítica: Creatinina 6,8 mg/dL; Sodio 137 mEq/L; Potasio 4,6 mEq/L; Leucocitos 9.300 (73% Ne; 10% Li; 8,8% Eo); Hematocrito 28%; Hemoglobina 9,5 g/dL; VCM 95 fL; Plaquetas 262.000. Complemento normal. Autoinmunidad normal.
Orina: Leucos 11-20 por campo (ausencia de eosinófilos); Hematíes 10 por campo. Proteinuria 500 mg/24horas.
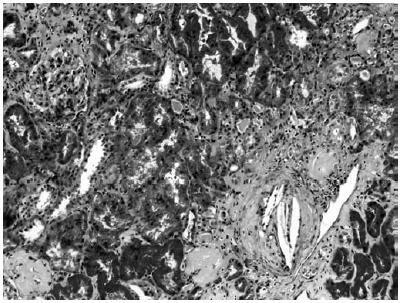
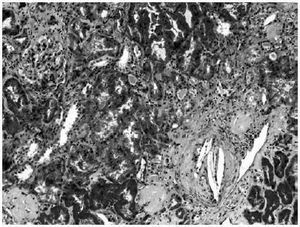
La ecografía abdominal muestra riñones disminuidos de tamaño, con cortical de grosor discretamente disminuida (12 mm), sin dilatación de la vía excretora. Fondo de ojo sin lesiones. Ante la presencia de un deterioro de la función renal y eosinofilia, se decide la retirada de fármacos potencialmente causantes de nefritis intersticial aguda (omeprazol y alopurinol) y la realización de una biopsia renal que muestra nefroangioesclerosis (9 glomérulos esclerosados de un total de 13), así como la presencia de cristales de colesterol ocluyendo la luz de varias arterias de pequeño tamaño (Imagen 1). El paciente no recupera la función renal y se incluye en programa de hemodiálisis periódicas.
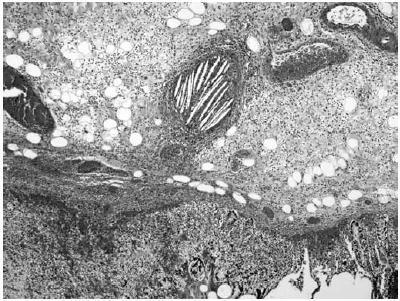
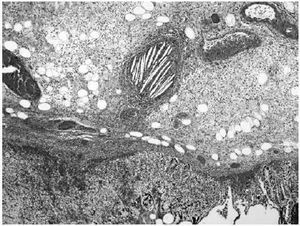
Consulta nuevamente un mes después por dolor abdominal agudo, destacando importante distensión abdominal y ausencia de peristaltismo. La TAC evidenció isquemia arterial mesentérica con signos de infarto en colon derecho, procediéndose a la realización de hemicolectomía con anastomosis difetermino-terminal. La biopsia de la pieza quirúrgica mostró ateroembolia intestinal (Imagen 2). Buena evolución clínica posterior siendo dado de alta sin nuevas incidencias.
Discusión
En el caso presentado nos encontramos con la aparición de un primer episodio de insuficiencia renal aguda tras 48 horas de la realización de un cateterismo cardíaco, con diuresis mantenida y recuperación de la función renal basal a los 12 días. Ante dicha situación debemos realizar el diagnóstico diferencial entre las entidades más frecuentes: la nefropatía por contraste, la enfermedad ateroembólica, lesión isquémica por bajo gasto cardiaco y la nefritis intersticial aguda por hipersensibilidad (NIA).
El paciente se encontraba hemodinámicamente estable, con buen estado de hidratación por lo que la lesión isquémica se descartó. No había cambios en la medicación habitual del paciente. Esto, junto con la ausencia de rash cutáneo, fiebre, eosinofilia y eosinofiluria hacen poco probable la NIA. La recuperación espontánea tras dos semanas, recuento de eosinófilos y complemento normales y la falta de evidencia de embolismos de colesterol en otros territorios van en contra de la EAE. Así pues, nuestro paciente cumple la definición más reconocida para la nefropatía por contraste, consistente en un aumento absoluto ≥ a 0,5 mg/dL o un incremento relativo ≥ 25% de los niveles basales de creatinina plasmática en las 48-72 horas posteriores a la administración de un medio de contraste, sin identificar otros desencadenantes1. Siendo ésta generalmente no-oligúrica y transitoria, recuperando valores basales de creatinina tras 14 días de la administración del contraste.
Basados en la definición descrita, la incidencia global de NC es baja (1,6-2,3%), siendo mayor en pacientes que reciben la administración intraarterial de contraste, particularmente en las intervenciones coronarias percutáneas (1,5-13%)2. Además, se ha descrito que la NC supone la tercera causa de insuficiencia renal aguda hospitalaria y está asociada con un aumento en la estancia hospitalaria y las tasas de mortalidad a largo plazo. Los principales factores de riesgo para su desarrollo son la insuficiencia renal crónica pre-existente, la diabetes mellitus, la depleción de volumen, edad avanzada (>65-70 años), insuficiencia cardiaca congestiva, contrastes iónicos de alta osmolalidad, la dosis de los mismos y la corta duración entre dos administraciones (< 72 horas)3,4.
Por todo ello, ante pacientes con factores de riesgo para la NC debemos plantear alternativas como la angiografía con dióxido de carbono (aunque ésta no nos permitiría el intervencionismo). Y en caso de ser necesario la administración de contraste, utilizar los contrastes no iónicos de baja osmolalidad o bien iso-osmolales, con la mínima dosis posible y evitando varias exploraciones en poco tiempo. En cuanto a la prevención, según los diferentes estudios realizados, parece clara la importancia de asegurar un correcto estado de hidratación del paciente. En este sentido, el bicarbonato sódico sería superior al suero salino isotónico (Incidencia de NC del 1,7% vs 13,6% respectivamente, P = 0.02)5. Algo más controvertido parece la administración de antioxidantes como la N-acetilcisteina (NAC), pese a la existencia de un estudio esperanzador a dosis superiores de las ensayadas hasta la fecha (Incidencia NC del 33% con placebo; 15% con NAC 600 mg ev pre-angioplastia y 600 mg/12h hasta las 48 horas post; 8% con NAC 1200 mg ev pre-angioplastia y 1200 mg/12h hasta las 48 horas post-angioplastia; P < 0.001)6.
En nuestro caso, un segundo episodio de insuficiencia renal aguda tuvo lugar 25 días después de la intervención. Se realizó una ecografía abdominal que descartó un proceso obstructivo. En este punto, la presencia de insuficiencia renal aguda y eosinofilia debe hacernos plantear el diagnóstico diferencial, entre otras causas, con la nefropatía intersticial aguda, las vasculitis sistémicas y la enfermedad ateroembólica.
El estudio autoinmunitario resultó negativo. La ausencia de manifestaciones en otros territorios y el complemento normal irían en contra de la EAE, aunque el antecedente de la coronariografía y la eosinofilia no permitirían descartarla. Pese a que el paciente no experimentó síntomas de hipersensibilidad, la eosinofilia y el deterioro renal acompañando la introducción, desde el último ingreso, de omeprazol y alopurinol, sugerían que la NIA fuese la responsable del cuadro. En consecuencia, retiramos los fármacos descritos y realizamos una biopsia renal para completar el estudio. Ésta permitió el diagnóstico de enfermedad ateroembólica renal en paciente afecto de nefroangioesclerosis. Tras 25 días del intervencionismo coronario consulta de nuevo por cuadro de isquemia intestinal aguda, observándose la presencia de émbolos de colesterol en el territorio intestinal resecado.
La embolización por cristales de colesterol se produce tras el desprendimiento de una placa de ateroma, ocluyendo de forma parcial o total pequeñas arteriolas. Puede ser iatrogénica (precipitada por una arteriografía, angioplastia, cirugía vascular, anticoagulantes, y fibrinolíticos entre otras) o espontánea7, y suele afectar a pacientes añosos con ateroesclerosis difusa. Por detrás de la afectación cutánea, la renal es la segunda en frecuencia, pudiendo también aparecer manifestaciones gastrointestinales, neurológicas o coronarias.
La enfermedad ateroembólica renal es debida no sólo a la oclusión de pequeñas arterias por los cristales de colesterol, sino también a una reacción a cuerpo extraño que produce proliferación intimal, formación de células gigantes y la consecuente oclusión de la luz vascular. Puede manifestarse de tres formas clínicas diferentes: Aguda, de inicio tras 1-2 semanas del evento desencadenante. Subaguda, en que la disfunción renal ocurre de forma progresiva y escalonada, separada por periodos de estabilidad en la función renal. Generalmente aparece semanas después del posible insulto como consecuencia de la combinación de embolismos recurrentes y la reacción a cuerpo extraño descrita. Y por último la presentación en forma de alteración renal estable y crónica. La EAE suele acompañarse de eosinofilia, eosinofiluria e hipocomplementemia en las fases activas de la enfermedad. No existe un tratamiento específico para la misma y su pronóstico es malo, con un significativo aumento de la mortalidad aguda intrahospitalaria (16%)8 y a largo plazo (hasta del 80%)9. Pese a no disponer de tratamiento efectivo, en los pacientes con EAE deben suspenderse los posibles agentes desencadenantes (anticoagulantes, trombolítico, etc) y realizarse de forma agresiva prevención secundaria cardiovascular consistente en un buen control de la presión arterial, de las glucemias en pacientes diabéticos, así como el uso de antiagregantes y estatinas.
Resumen
El intervencionismo intravascular percutáneo puede ser responsable de insuficiencia renal aguda por varias causas, entre ellas las presentadas por nuestro paciente: nefropatía por contraste y enfermedad ateroembólica. Ambas entidades aumentan la morbilidad y la mortalidad de los pacientes afectos sin que exista un tratamiento específico para ellas. Por tanto, debemos afinar al máximo las indicaciones y ofrecer una adecuada profilaxis a los pacientes con factores de riesgo.
Figura 1. Parénquima renal con fibrosis intersticial focal y algunos glomérulos esclerosados. En la esquina inferior derecha se observa una arteria de pequeño calibre con la luz ocluida por cristales de colesterol (Tricrómico de Masson x100)
Figura 2. Imagen de la pared intestinal con extensa necrosis y una arteria rellena de material ateroembólico. (H&E x40)