Revisión del artículo: Hladunewich MA, Cattran D, Beck LH, Odutayo A, Sethi S, Ayalon R, et al. A pilot study to determine the dose and effectiveness of adrenocorticotrophic hormone (H.P. Acthar® Gel) in nephrotic syndrome due to idiopathic membranous nephropathy. Nephrol Dial Transplant 2014;29:1570-7.
¿Tipo de diseño
Estudio piloto fase Ib/II, no ciego, de optimización de dosis, en pacientes con glomerulonefritis membranosa idiopática (GNMI) aleatorizados a recibir ACTH (hormona adrenocorticotropa; Acthar® Gel, purificada de origen porcino) en dos dosis de 40 u 80 U subcutáneas durante 12 semanas con evaluación basal y a 1, 3, 6 y 12 meses.
¿Asignación
Aleatorizado 1:1. Método no especificado.
¿Enmascaramiento
No ciego.
¿Ámbito
Pacientes reclutados en dos centros: Mayo Clinic y Universidad de Toronto.
¿Pacientes
Criterios de inclusión: adultos > 18 años con GNMI demostrada mediante biopsia en los 36 meses anteriores en la que no existía más del 30 % de glomeruloesclerosis y/o fibrosis intersticial, que presentaban síndrome nefrótico definido por proteína orina/creatinina en orina ≥ 4,0 en una muestra de orina de 24 h, con función renal estimada por MDRD-4 ≥ 40 ml/m. Todos requerían tratamiento previo al menos tres meses con bloqueo del sistema renina-angiotensina (SRA) en dosis crecientes hasta la máxima dosis tolerada, con objetivo de conseguir una tensión arterial (TA) < 130/75 en el 75 % de las lecturas antes de iniciar tratamiento, dieta baja en sal y estatina. Podían incluirse pacientes no resistentes, pero con remisiones parciales y/o intolerancia a otros tratamientos, siempre que existiera un período de más de seis meses sin inmunosupresión. En todos se realizó anti-PLA2-R basal, que fue positivo en 15.
Criterios de exclusión: pacientes con resistencia documentada a inmunosupresión clásica (inhibidores de calcineurina con o sin esteroides, agentes citotóxicos con o sin esteroides). Infección activa. Causas secundarias de glomerulonefritis membranosa, diabetes tipo I y tipo II, pacientes anticoagulados, embarazo, lactancia.
Intervenciones:
– Grupo de 11 pacientes en dosis de 80 U durante 12 semanas.
– Grupo de 9 pacientes en dosis de 40 U durante 12 semanas. En este grupo se dio opción a los que no respondieron a las 12 semanas (9/9) a un segundo tratamiento de 12 semanas con la dosis de 80 U, que completaron 5/9. En 2 pacientes sin respuesta se optó por tratamiento inmunosupresor.
En la evaluación al año solo 4 pacientes habían mantenido la dosis de 40 U y 16 habían recibido un tratamiento completo con 80 U.
¿Variables de resultado
Variables principales: cambios en proteinuria, albúmina sérica, colesterol, documentación de efectos secundarios.
Variables secundarias: proporción de pacientes que consiguen una remisión completa (RC) al año definida como proteinuria < 0,3 g/día, una remisión parcial (RP) definida como reducción de proteinuria en un 50 % con una proteinuria final < 3,5 g/día, pero mayor de 0,3 g/día, y no respuesta (NR) definida como reducción de proteinuria < 50 % o empeoramiento de la proteinuria.
¿Estadística
Análisis por intención de tratar en población de pacientes que recibe un tratamiento completo de 12 semanas y análisis al año por dosis total acumulada. Variables continuas expresadas como media ± desviación estándar, y categóricas como porcentajes. Cambios en el tiempo estimados con test pareados. Test exacto de Fisher para comparar proporciones. Análisis de varianza para comparar respuesta a dosis con test Newman-Keuls. Correlación para evaluar relación entre respuesta a tratamiento, disminución de proteinuria y variación de los niveles de anti-PLA2R. Se utilizó SAS versión 9.1 (SAS Institute, Cary, NC, USA).
¿Promoción
Estudio financiado por Questor Pharmaceuticals, que proporcionó la medicación. Los autores no declaran conflicto de interés y afirman que la empresa no ha participado ni en el diseño ni en la evaluación de los resultados ni en la elaboración del manuscrito.
¿ RESULTADOS PRINCIPALES
Características basales
Expresadas de los 20 pacientes. De ellos, 7 habían recibido inmunosupresión previa con recidiva posterior, pero tenían un intervalo sin medicación de más de seis meses. Población caucásica 58 %, varones 63 %, edad 51 ± 15 años. Todos estables, con TA controlada con monoterapia (14) o doble bloqueo del SRA (5), sin cambios en la proteinuria. Población nefrótica con proteinuria de 9,1 + 3,4 g; función renal con filtrado glomerular estimado 77 ± 30 ml/m, albúmina sérica 2,9 + 0,83 g/dl, colesterol ligado a lipoproteínas de baja densidad (LDL) 182 + 85 mg/dl. Glucosa 93 + 11 mg/dl y cortisol 11 + 3 μg/dl normales. Nos dicen que no había diferencias entre el grupo con 40 U (9 pacientes) y el de 80 U (11 pacientes), pero estos datos no están expresados.
Variable principal
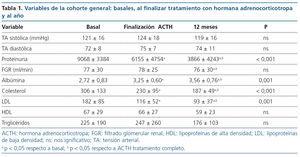
Cambios en proteinuria, albúmina sérica y colesterol: existe una disminución significativa de la proteinuria, el colesterol total y el colesterol LDL, con un aumento de la albúmina plasmática al fin del tratamiento con ACTH y que sigue mejorando en el control al año. La TA se mantuvo controlada y no existieron variaciones de la función renal (tabla 1).
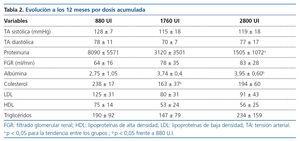
Dosis y respuesta: los autores hacen un análisis de la tendencia a la disminución de la proteinuria en función de la dosis total recibida, encontrando una relación significativa (tabla 2).
Efectos secundarios
Buena tolerancia, ningún paciente suspendió el tratamiento por efectos secundarios. Se detectó:
– Elevación aguda de los niveles de ACTH sérica y cortisol en suero y orina en las dos dosis, con tendencia a un mayor aumento en la dosis de 80 U, si bien se normaliza a la basal a las 24 h.
– Aumento de peso menor o igual a 7 kg en 5 pacientes, con edema transitorio en 3.
– Cushing en 3.
– Cambios dermatológicos: acné (3), enrojecimiento (2), pigmentación (2).
– Cambios psicológicos fluctuantes con irritabilidad o inestabilidad en 6. Insomnio en 6.
– Temblor (3), ronquera (2), mareo (5), dolor muscular (5), cefalea (5), síntomas gastrointestinales (7), visión borrosa (2), sensación de debilidad y fatiga (9), aunque no se relacionaban claramente con el tratamiento.
– Picor en el punto de inyección en 5.
– Elevaciones de la glucemia en 13/20 pacientes tras la administración de ACTH, sin diferencias entre las dos dosis. Elevación transitoria de glucosa por encima de 130 mg en 5, pero solo en un caso se mantuvo y respondió a tratamiento con dieta.
Variables secundarias
Remisiones: existía reducción de la proteinuria de un 50 % en 10/20, que mejoró a 13/20 al año (65 %). De estos 13, 2 consiguieron RC, 10 RP y 1 disminuyó de 18 g a 8 g sin cumplir criterios de RP. Siete pacientes no mejoraron o progresaron.
Respuesta a las 12 semanas de tratamiento:
– De los pacientes con 40 U, ninguno presentó mejoría (9/9 sin respuesta).
– De los pacientes con 80 U, mostraron una disminución del 30 % 5/11, con mejoría progresiva en los siguientes controles.
Respuesta a los 12 meses:
– Pacientes con 40 U (4 pacientes): 1 presenta RP y 3 no responden.
– Pacientes con 80 U (al final 16 pacientes recibieron 80 U: 11 iniciados en 80 U y 5 iniciados en 40 U con posterior aumento a 80 U): 11/16 hacen remisión, siendo RC en 2 y RP en 9.
Variaciones de anti-PLA2R: en los 15 pacientes basalmente positivos el anticuerpo desapareció en 3 y disminuyó en 4. Esta disminución precedió a la de la proteinuria en 5 o se produjo paralelamente en 2. En los no respondedores el anticuerpo no se modificó. Existía una correlación entre la disminución de los anticuerpos y la de la proteinuria al completar el tratamiento con ACTH (R2 = 0,29, P = 0,04) que mejoraba al año (R2 = 0,67, P < 0,001).
¿ CONCLUSIONES DE LOS AUTORES
Este estudio piloto sugiere que el tratamiento con ACTH en la forma de H.P. Acthar® Gel es un tratamiento potencial de la GNMI que precisa un estudio controlado aleatorizado a mayor escala. Parece que es necesaria una dosis acumulada de al menos 80 IU dos veces a la semana de 3 a 6 meses para obtener una RC. La dosis óptima está por determinar.
La seguridad a corto plazo parece buena, aunque falta por estudiar los efectos a largo plazo.
El alto coste de la terapia puede ser una limitación a su uso.
¿ COMENTARIOS DE LOS REVISORES
El H.P. Acthar Gel® (ACTH) se obtiene de procesar glándula pituitaria de cerdo. Sus componentes son péptidos melanocortínicos que incluyen ACTH y hormona estimulante de melanocitos α, β y γ, capaces de unirse a los receptores celulares melanocortínicos (MCR). Se conocen cinco tipos de MCR y la ACTH es activa en los cinco1.
La ACTH puede modificar el curso de las nefropatías proteinúricas como la GNMI. Sus potenciales mecanismos de acción son complejos. Los efectos renoprotectores incluyen inmunosupresión y antiinflamación mediada por esteroidogénesis, inmunomodulación mediada por MCR con efecto antiinflamatorio (MCR 1, 3, 5) y corrección de la dislipemia (mediado MCR 1, 5 en célula hepática). Es destacable el efecto protector sobre el podocito, ya que a través de la modulación de las apolipoproteínas parece capaz de restaurar la expresión glomerular de clusterina que protege del complejo de ataque C5b-9. Estudios experimentales (nefritis pasiva de Heyman en ratas) han identificado receptores MCR 1 en los podocitos y demostrado que el uso de agonistas como la ACTH mejoran la proteinuria y normalizan los podocitos de la membrana basal1,2.
El estudio piloto de la ACTH como Acthar® Gel apoya su posible papel del tratamiento en la GNMI con pocos efectos secundarios. Hay que subrayar que el grupo de pacientes estaba muy seleccionado, sin ningún diabético y con TA muy bien controlada que se mantiene a lo largo del estudio. El efecto secundario de aumento de peso (menor o igual a 7 kg en 5 pacientes) y la aparición de edema transitorio en relación con la medicación obliga a una supervisión cuidadosa de los pacientes.
Es destacable que en Europa tenemos una formulación distinta de ACTH, Synacthen® (tetracosáctido, análogo sintético de ACTH), que en una serie de casos con 10 GNMI obtuvo remisión total o parcial en todos con la dosis de 25 μg/kg/semana durante 6 meses3 y en un pequeño estudio aleatorizado las remisiones (14/16) fueron similares a las de los tratados con citotóxico + metilprednisolona (15/16)4.
¿ CONCLUSIONES DE LOS REVISORES
Coincidentes con las de los autores.
¿ CLASIFICACIÓN
Tema: Nefrología clínica
Subtema: Glomerulonefritis membranosa idiopática
Tipo de artículo: Tratamiento
Palabras clave: Glomerulonefritis membranosa idiopática. ACTH. Síndrome nefrótico
NIVEL DE EVIDENCIA: Moderado
GRADO DE RECOMENDACIÓN: Fuerte
(GRADE [www.gradeworkinggroup.org] divide la calidad de la evidencia en cuatro grupos: alta, moderada, baja y muy baja; y divide el grado de recomendación en dos grupos: fuerte y débil).