Oudemans-van Straaten HM, Bosman RJ, Koopmans M, et al. Citrate anticoagulation for continuous venovenous hemofiltration. Crit Care Med 2009;37:545-52.
Tipo de diseño y seguimiento
Ensayo controlado y aleatorizado, unicéntrico, con seguimiento a 3 meses.
Ética y resgistro
Aprobado por el Comité de Ética del hospital de acuerdo a la legislación holandesa y europea.
Asignación
Asignación aleatoria mediante un programa informático que asigna de forma automática al paciente una vez comprobados los criterios de inclusión y exclusión.
Enmascaramiento
No enmascarado.
Ámbito
Unidad de Cuidados Intensivos (UCI) del Hospital Universitario Onze Lieve Vrowe Gasthuis, Ámsterdam, Holanda.
Pacientes
Pacientes adultos (>18 años) ingresados en UCI con fracaso renal agudo (FRA) que requieren terapia de reemplazo renal. Se excluyen del estudio pacientes con cirrosis hepática (Child Pugh C), probabilidad elevada de sangrado (necesidad de transfusión o caída de la cifra de hemoglobina >0,5 mmol/l en las primeras 24 h), cirugía en las 24 horas previas, necesidad de anticoagulación terapéutica, sospecha de trombopenia inducida por heparina, diálisis crónica y pacientes no tributarios de técnicas de resucitación por limitación del esfuerzo terapéutico. No se excluyó a los pacientes con hepatitis isquémica o que recibiesen heparina en dosis profiláctica.
Intervenciones
Todos los pacientes recibieron hemofiltración venovenosa continua (HFVVC) posdilución con los siguientes parámetros: flujo de sangre (Qb) 220 ml/min, flujo de líquido de reposición de 4.000 ml/h y fracción de filtración por debajo del 32%. Tras 24 horas de inicio de HFVVC, si mejoraba el estado hemodinámico del paciente, el flujo del líquido de reposición disminuía hasta 2.000 ml/h.
En el grupo que recibía anticoagulación sistémica con nadroparina se procedía al cebado del circuito con 2.850 UI de nadroparina en 1 l de líquido de cebado. Asimismo, se administraba al paciente un bolo inicial de 2.850 UI endovenoso o 3.800 UI de nadroparina si el peso era superior a 100 kg, seguido de infusión continua en el circuito extracorpóreo de 380-456 UI/h, respectivamente. La anticoagulación en el grupo citrato consistía en la infusión de citrato en dosis de 3 mmol por cada litro de flujo sanguíneo, junto a profilaxis simultánea de trombosis con 1.000 UI/día de heparina no fraccionada o nadroparina 3.800 UI/día. Ante la aparición de efectos adversos que motivasen la discontinuación de la anticoagulación asignada, se realizaría el cambio a citrato, nadroparina o su suspensión según criterio clínico.
Variables de resultado
Principales: seguridad (ausencia de efectos adversos que supongan la necesidad de interrupción del tipo de anticoagulación asignado) y eficacia (supervivencia del circuito).
Secundarias: mortalidad durante la estancia hospitalaria y a los 3 meses.
Tamaño muestral
Estimado en 200 pacientes para obtener una potencia estadística del 80% con un error de tipo I del 0,05, con el supuesto de una pérdida de seguimiento del 12,5% en el grupo nadroparina y del 2% en el grupo de citrato.
Estadística
Análisis comparativo de las variables mediante t de Student, ji al cuadrado o U de Mann-Whitney. La supervivencia del circuito y la mortalidad a los 3 meses fueron analizadas mediante curvas de Kaplan-Meier y prueba de log-rank. Se realizó, además, un análisis por intención de tratar de la mortalidad hospitalaria y a los 3 meses.
Promoción y conflicto de intereses
No se menciona financiación. Los autores declaran ausencia de conflicto de intereses.
RESULTADOS PRINCIPALES
ANÁLISIS BASAL DE LOS GRUPOS
Del total de 5.712 pacientes admitidos en la UCI entre marzo del 2003 y noviembre del 2006, 365 (6,7%) tenían indicación de HFVVC. Se excluyeron 170 pacientes y 215 fueron distribuidos aleatoriamente en dos grupos: 107 al grupo citrato y 108 al grupo nadroparina. Las pérdidas durante el seguimiento fueron de 10 en el grupo citrato (4 no HFVVC; 1 fallo hepático; 1 segunda admisión en UCI; 3 no tributarios de técnicas resucitación; 1 recibía anticoagulación sistémica) y 5 en nadroparina (2 no HFVVC; 1 fallo hepático; 1 segunda admisión en UCI; 1 diálisis crónica). De este modo, finalizan el estudio 97 pacientes en el grupo citrato y 103 pacientes en el grupo heparina. Se valoraron en ambos grupos las siguientes características: edad, creatinina sérica al ingreso en UCI y al inicio de la HFVVC, APACHE, SAPS, RIFLE, SOFA, hemoglobina, número de plaquetas, tiempo de protrombina, etiología de IRA, demora en el inicio del tratamiento y duración de la HFVVC, sin encontrar diferencias estadísticamente significativas.
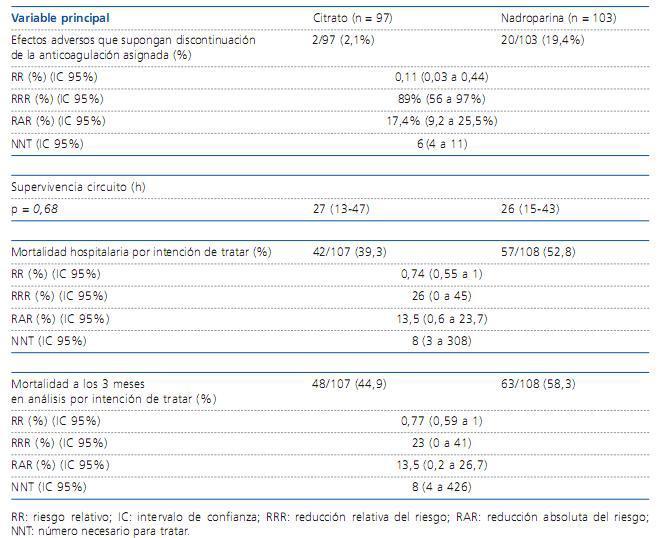
Variable principal(ver tabla 1)
Efectos adversos
En dos casos del grupo de citrato se produjeron efectos adversos que supusieron la suspensión de la anticoagulación del estudio (uno por acumulación de citrato y otro por coagulación precoz en relación con una violación del protocolo); igualmente, 20 casos del grupo de nadroparina suspendieron la anticoagulación, 16 por sangrado y 6 por trombopenia o por ambos.
CONCLUSIONES DE LOS AUTORES
La anticoagulación regional con citrato en HFVVC es igual de eficaz que la anticoagulación sistémica con nadroparina, pero ofrece un mayor perfil de seguridad. La anticoagulación con citrato reduce la mortalidad hospitalaria y a los 3 meses debido, sólo en parte, a un menor riesgo de sangrado.
COMENTARIOS DE LOS REVISORES
Ensayo clínico, controlado y aleatorizado, unicéntrico, con un diseño apropiado, que no muestra diferencias en cuanto a eficacia entre el uso de nadroparina y citrato como anticoagulación del circuito en técnicas continuas de reemplazo renal. Sin embargo, los autores afirman que existe cierta superioridad del citrato frente a la heparina de bajo peso molecular si evaluamos su seguridad. En este punto existen problemas en el desarrollo del estudio que cuestionan esta afirmación. Las heparinas de bajo peso molecular, aunque son una de las opciones para la anticoagulación de los circuitos, no son el método de referencia, ya que su dosificación en la insuficiencia renal requiere la monitorización de los niveles de anti-Xa. Pero esta dosificación no se llevó a cabo en el estudio, ya que sólo se ajustó la dosis en función del peso del paciente. Se induce de este modo una diferencia en la incidencia de sangrado debido a una monitorización más estrecha en los pacientes del grupo citrato en relación al grupo heparina mediante la determinación de los niveles de calcio a la salida del filtro. Además, existen seis pacientes en el grupo citrato que presentan sangrado y que no se han incluido en el análisis posterior de la variable seguridad, sobrestimando así la seguridad de este grupo frente al grupo heparina. Otra de las afirmaciones que se deriva del estudio es la menor mortalidad en el grupo citrato. Los autores atribuyen este hallazgo al menor riesgo de sangrado; sin embargo, en el análisis de los datos no existen diferencias significativas en la incidencia de sangrado ni en la necesidad de transfusión en los dos grupos. Además, ésta es una variable secundaria, el tamaño muestral no estaba calculado para mostrar diferencias en la mortalidad y si se realiza el análisis por intención de tratar, que incluye a todos los pacientes aleatorizados, también aquellos a los que no se realiza la técnica de HFVVC por varios motivos, no se puede descartar un beneficio marginal, pues el límite inferior del IC 95% es próximo a la ausencia de diferencia.
La terapias continuas de reemplazo renal son técnicas comúnmente utilizadas en los pacientes críticos. El éxito de estas técnicas depende de un protocolo de anticoagulación eficiente para mantener la permeabilidad del circuito de diálisis, minimizando sus complicaciones, como el sangrado derivado de una excesiva anticoagulación. La heparina no fraccionada es el anticoagulante más utilizado para las distintas técnicas de diálisis. Recientemente las heparinas de bajo peso molecular también han demostrado ser eficaces y seguras. En los pacientes críticos en los cuales la anticoagulación sistémica está frecuentemente contraindicada, la anticoagulación regional con citrato ha demostrado ser una alternativa eficaz y segura si se aplica un control metabólico estricto. Los estudios publicados al respecto no ofrecen un sólido grado de recomendación. Se propone, ante un bajo riesgo de sangrado, la utilización de heparina de bajo peso molecular y heparina no fraccionada. Si el riesgo de sangrado está aumentado, la anticoagulación con citratro debería ser de primera elección. En el caso de que existiese coagulopatía de base, debería considerarse la no anticoagulación del circuito. Es necesaria la realización de un mayor número de ensayos controlados y aleatorizados para poder establecer mayores grados de recomendación y para confirmar la disminución de la mortalidad en los pacientes tratados con citrato en lugar de con heparina.
CONCLUSIONES DE LOS REVISORES
Aunque se trata de un estudio con un tamaño muestral superior a los anteriormente publicados, sus resultados no permiten afirmar con seguridad la superioridad del citrato frente a otras técnicas de anticoagulación.
Tabla 1. Variable principal