El embolismo por cristales de colesterol es una entidad clínica causada por la embolización de microcristales de colesterol procedentes de placas ateroescleróticas que producen la oclusión de arterias de pequeño calibre. Puede producirse por iatrogenia a partir de la manipulación angioinvasiva (cirugía vascular, angiografía), por fármacos anticoagulantes o fibrinolíticos y de forma espontánea. Las manifestaciones clínicas son heterogéneas, predominando la afectación cutánea y el fallo renal. El fracaso renal clínicamente puede ser agudo, subagudo o crónico, siendo lo más frecuente el deterioro progresivo durante varias semanas. Algunos pacientes pueden precisar de diálisis, con recuperación variable de la función renal. El diagnóstico presuntivo se considera en pacientes de > 60 años con factores de riesgo cardiovascular que han estado expuestos a los conocidos factores desencadenantes y que presentan lesiones cutáneas violáceas o livedo reticularis asociado a deterioro de la función renal. No obstante, el diagnóstico definitivo es por biopsia del órgano diana, siendo la biopsia cutánea la más accesible. El tratamiento es controvertido y hasta la fecha no existe un consenso de las medidas terapéuticas que se han de utilizar. Se recomienda el control de los factores de riesgo cardiovascular, el manejo de la isquemia y la inflamación con los corticoides y los análogos de las prostaglandinas e incluso la endarterectomía. Debe evitarse la realización de procedimientos endovasculares y además suspender todo tipo de fármacos anticoagulantes. A continuación, se presenta el caso de una ateroembolia por cristales de colesterol secundaria a la administración de acenocumarol.
CASO CLÍNICO
Se trata de un varón de 71 años derivado al servicio de nefrología desde atención primaria por insuficiencia renal aguda con creatinina sérica 4,06 mg/dl. Cinco meses antes tenía una creatinina de 1,5 mg/dl. Entre sus antecedentes personales destaca hipertensión arterial en tratamiento con telmisartán/HCTZ 40/12,5 mg, glucemia alterada en ayunas, hábito tabáquico de unos 20 cigarrillos al día desde la juventud y dislipemia en tratamiento con simvastatina 20 mg. Había presentado una fibrilación auricular de comienzo indeterminado y un episodio de accidente cerebrovascular transitorio de probable etiología cardioembólica, por lo que se inició tratamiento anticoagulante con acenocumarol cuatro meses atrás, con posterior cardioversión eléctrica a ritmo sinusal. En un estudio completo por síncope cuatro meses antes, destaca el resultado de una tomografía axial computarizada torácica por describirse una marcada ateromatosis de la aorta torácica.
Clínicamente, el paciente presentaba anorexia y alteración de la sensibilidad gustativa, pérdida de peso de unos 10 kg y debilidad en las extremidades inferiores de unos tres meses de evolución.
Exploración física
El paciente está consciente, orientado, presenta buen estado general y se muestra colaborador.
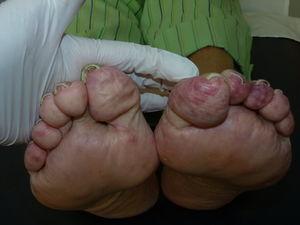
Tensión arterial: 145/70 mmHg, frecuencia cardíaca: 80 lpm. Afebril. Exploración cardiopulmonar: tonos cardíacos rítmicos sin soplos. Murmullo vesicular disminuido con estertores roncus y sibilantes dispersos en ambos campos pulmonares. El abdomen era blando, no doloroso a la palpación, ruidos hidroáereos de características normales, no soplos abdominales ni femorales. No se palpaban masas ni visceromegalia. En las extremidades inferiores destacaban lesiones eritemato-violáceas en el área pretibial bilateral asociadas a livedo reticularis, que se extendía hacia la planta de los pies y los dedos, principalmente en el tercer dedo del pie izquierdo (figura 1).
Analítica de laboratorio: destaca en el hemograma la presencia de eosinofilia (11,7 %) y, en la bioquímica, urea 104 mg/dl con creatinina 4,48 mg/dl, sistemático y sedimento de orina normal, leve disminución del complemento C3: 71,4 mg/dl (83-175), ANCAS negativo, criocrito 2 %.
Evolución
Durante la hospitalización mantiene buen estado general, niveles tensionales dentro de los parámetros normales con medicación hipotensora y diuresis conservada (1500-2000 ml/día). Ante la sospecha de enfermedad sistémica ateroembólica por colesterol, se inició desde el primer día tratamiento con metilprednisolona (0,3 mg/kg/día vía oral) y atorvastatina 80 mg, con suspensión del acenocumarol. Se interconsultó con oftalmología para la exploración del fondo de ojo en busca de las placas de Hollenhorst, siendo este normal. El índice tobillo-brazo también resultó normal. El ecocardiograma no mostró masas intracardíacas ni otros datos de interés, aunque durante su realización se observaron rachas de fibrilación auricular autolimitadas. Se llevó a cabo una biopsia cutánea que fue compatible y concluyente para el diagnóstico de ateroembolia por cristales de colesterol (figura 2). La función renal se mantuvo estable respecto a los valores previos al menos durante 7-10 días, con progresivo descenso posterior, siendo la creatinina al alta de 3,3 mg/dl. Tras el inicio del tratamiento con esteroides, las lesiones violáceas en ambas piernas fueron desapareciendo. Al alta se mantuvo el tratamiento con esteroides en igual dosis para iniciar pauta de descenso al mes, coincidiendo con la revisión en la consulta de nefrología. Se solicitó valoración por cardiología y, por tratarse de un paciente con un riesgo cardioembólico elevado con una puntuación en la escala de riesgo CHADS2 de 4, se indicó tratamiento anticoagulante con heparina de bajo peso molecular (HBPM). En la revisión ya no presentaba lesiones cutáneas, la creatinina sérica era de 2,8 mg/dl y aún mantiene tratamiento con HBPM. En la figura 3 se puede ver la evolución de la creatinina sérica desde la introducción del acenocumarol y la mejoría posterior tras el inicio del tratamiento con corticoides.
DISCUSIÓN
La ateroembolia por cristales de colesterol es una enfermedad sistémica causada por la oclusión de arterias de pequeño calibre por material ateromatoso de placas ateroescleróticas procedente frecuentemente de la arteria aorta abdominal1. La embolización puede afectar a cualquier órgano, siendo más susceptibles los riñones, la piel de las extremidades inferiores y el sistema gastrointestinal2,3.
Era una entidad poco común hasta hace unas décadas, aunque actualmente se está diagnosticando con mucha mayor frecuencia debido a la realización de procedimientos diagnósticos angiográficos, al mayor uso de tratamiento anticoagulante y al progresivo envejecimiento de la población tratada, con la consiguiente mayor prevalencia de factores de riesgo cardiovascular. Suele afectar a varones mayores de 60 años, de raza blanca, con antecedentes de enfermedad ateromatosa vascular. Se asocia a procedimientos vasculares invasivos, cirugía vascular, terapia trombolítica, y tratamiento con antagonistas de la vitamina K, aunque en ocasiones no se encuentra ningún factor desencadenante4.
En nuestro caso clínico la sospecha diagnóstica surge por la combinación de lesiones cutáneas en los miembros inferiores y fracaso renal progresivo con eosinofilia, tras inicio del acenocumarol en un paciente con factores de riesgo cardiovascular e importante ateromatosis aórtica.
Las manifestaciones clínicas de esta enfermedad son variadas e inespecíficas y dependen de la localización anatómica de las placas de ateroma, siendo más frecuente la afectación de los órganos de la mitad inferior del cuerpo, dado que es más prevalente la ateromatosis abdominal5. La combinación clínica más característica es la presencia de dolor en el área gemelar junto con livedo reticularis, pulsos periféricos conservados, eosinofilia y fallo renal5. Las manifestaciones cutáneas son las más frecuentes (57 %) y el riñón es el órgano mayormente afectado, seguido del bazo, el páncreas, el intestino, las glándulas adrenales y el hígado3.
Desde el punto de vista clínico, el fallo renal puede ser agudo, subagudo o crónico. En un 50 % de los pacientes se observa afectación renal en forma de insuficiencia renal aguda no oligúrica. En el momento del diagnóstico el 25 % tiene creatinina sérica mayor de 5 mg/dl, precisando diálisis casi el 40 % de ellos4. También puede asociarse a severa e incontrolada hipertensión arterial, siendo el infarto renal raro2.
El resultado final de la afectación renal por ateroembolia es variable: algunos pacientes desarrollan insuficiencia renal crónica y en algunos casos precisan de terapia renal sustitutiva (diálisis). Las experiencias más recientes sugieren la posibilidad de la recuperación espontánea hasta en un tercio de los casos, incluso después de necesitar durante un tiempo hemodiálisis. Esta recuperación se debe probablemente a la acción de varios factores, como son el control de la inflamación, la resolución de la necrosis tubular aguda en áreas de isquemia y la hipertrofia de las nefronas supervivientes6. En nuestro caso el paciente presentó insuficiencia renal subaguda no oligúrica, que no precisó de tratamiento renal sustitutivo con diálisis.
Por otro lado, el sistemático de orina no suele ser diagnóstico, aunque se puede observar proteinuria discreta y un sedimento con hematuria, leucocituria y cilindros gránulo-hialinos. En la analítica de sangre se suele presentar leucocitosis con eosinofilia y anemia con aumento de la velocidad de sedimentación y disminución transitoria del complemento4. En la analítica de nuestro paciente el sistemático de orina fue normal y la eosinofilia fue transitoria acompañada de leve disminución del complemento C3.
El diagnóstico diferencial se debe realizar con la nefropatía por contrastes yodados, fracaso renal agudo prerrenal y/o necrosis tubular aguda, vasculitis sistémica o renal, endocarditis infecciosa, trombosis de arteria renal y nefritis intersticial inmunoalérgica (NIIA)4. En nuestro paciente se descartó con la anamnesis la presencia de situaciones que produjeran fracaso renal agudo prerrenal y utilización de contrastes yodados. Por otra parte, el estudio inmunológico fue negativo y no existía información clínica, analítica o ecocardiográfica sugerente de proceso infeccioso para pensar en endocarditis. Además, mediante ecografía con Eco-doppler renal se descartaba la presencia de trombos renales. La posibilidad de una NIIA se descartó, a pesar de la similitud que ambas comparten con las lesiones cutáneas, eosinofilia y fallo renal, debido al tiempo transcurrido hasta la aparición de la expresión clínica, los antecedentes personales y la ausencia de infección reciente, y la introducción de acenocumarol en los meses previos, ya que se había descrito la probable relación de causalidad con la aparición de ateroembolia por colesterol.
La biopsia del órgano afectado confirma el diagnóstico de la enfermedad. El patrón de oro es la piel, cuya importancia radica en la accesibilidad, fácil realización y baja mortalidad, además del alto rendimiento de hasta un 92 %5. En la histopatología es patognomónica la visualización dentro de los vasos de la unión dermohipodérmica de hendiduras alargadas biconvexas en forma de agujas5. En nuestro caso clínico el antecedente farmacológico y las manifestaciones clínicas eran muy sugestivos de la ateroembolia por colesterol, pero la biopsia cutánea fue determinante para el diagnóstico final.
La asociación de esta enfermedad con el uso de trombolíticos y antagonistas de la vitamina K no está claramente establecida. La primera publicación que hacía referencia a esta relación causa-efecto data del año 1961, descrita por Feder y Auerbach7. Se ha sugerido que los dicumarínicos producen desestabilización de la superficie de la placa de ateroma, con pérdida gradual de fibrina que finalmente produce liberación de colesterol a la circulacion8. En la misma línea existen publicaciones que relacionan las heparinas sódica y de bajo peso molecular con la aparición de ateroembolia. Recientemente, se ha publicado un artículo de la revista Wisconsin Medical Society donde se sugiere una probable relación causal entre dabigatran y el desarrollo ateroembolia por cristales de colesterol9..
Una vez diagnosticada la ateroembolia por colesterol, se recomienda la suspensión de todos los anticoagulantes10,11. Sin embargo, es imprescindible individualizar cada caso. Debido al riesgo embolígeno de la fibrilación auricular con un episodio previo de ictus de probable origen cardioembólico, se decidió mantener el tratamiento anticoagulante con HBPM. En cuanto al tratamiento anticoagulante, en estos casos no hay una indicación establecida. Deben tratar de evitarse una vez instaurada la patología6. Sin embargo, en varios trabajos publicados la terapia anticoagulante se mantuvo por el alto riesgo que implica retirarla debido a la enfermedad de base (embolismo pulmonar, ictus isquémico cardioembólico)10,11. No hay una recomendación sobre qué anticoagulante emplear en estas situaciones. Decidimos empíricamente sustituir sintrom por HBPM, por la importante variabilidad de la anticoagulación que presentan los pacientes con sintrom, lo que podía ser un factor precipitante en placas inestables. Al alta se mantuvo con HBPM hasta la revisión en consultas, decidiendo mantenerla de manera indefinida. En este sentido, los nuevos anticoagulantes orales podrían jugar un papel primordial en la anticoagulación de estos pacientes, pues su concentración y poder anticoagulante es mucho más predecible que en el caso del sintrom. Se necesitan más datos al respecto. Existe mayor acuerdo acerca del empleo de esteroides, prostanoides y estatinas. Se recomienda el uso de esteroides en dosis que pueden oscilar entre 0,3-1 mg/kg/día oral según diversos autores3,12, pero pocos estudios han demostrado claramente que dosis bajas de corticoides (0,3 mg/kg) tengan efectos beneficiosos13. Takahashi et al.14 demostraron que dosis bajas de corticoides no fueron suficientes para mejorar y/o recuperar la normalidad de la función renal. Sin embargo, la terapia con bolus de corticoides mostró atenuación del deterioro renal13. Las dosis altas de esteroides son útiles en la enfermedad ateroembólica con fallo renal que no mejora espontáneamente13. Las estatinas se utilizan por su papel en la estabilización de la placa de ateroma y en la mejoría de la función renal6 y en algunas ocasiones se pueden emplear análogos de prostaglandinas como el iloprost en dosis de 2 ng/kg/min en perfusión intravenosa durante 12 horas/día por 14 días junto con esteroides12.
La prevención es muy importante y se hace con el control estricto de los factores de riesgo cardiovascular, evitando los estudios angiográficos invasivos y en algunas ocasiones la cirugía de endarterectomía.
El pronóstico es sombrío. Se acompaña de una alta tasa de morbimortalidad, debido en parte a una escasa respuesta al tratamiento. Nuestro paciente actualmente se encuentra con mejoría de la función renal sin lesiones cutáneas y sin otras manifestaciones sistémicas de la ateroembolia. La causa de mortalidad más frecuente es el fallo cardíaco (36 %) y el fracaso multiorgánico (17 %). El fracaso renal tan solo es responsable del 2,4 % de los fallecimientos15.
CONCLUSIÓN
La ateroembolia por cristales de colesterol es una entidad cada vez más habitual que se acompaña de una elevada morbimortalidad. Es primordial realizar un diagnóstico precoz para instaurar el tratamiento de manera temprana y evitar así la progresión del cuadro clínico y la necesidad de hemodiálisis. La relación causa-efecto entre la ateroembolia y el acenocumarol, como con otros anticoagulantes, no está establecida, por lo que se necesitan más estudios que la aclaren. El mantenimiento de este fármaco predispone a nuevos episodios de embolismo por colesterol. En los casos de alto riesgo embólico en los que se decida mantener la anticoagulación, creemos que sustituir el sintrom por otro anticoagulante más predecible tiene sustento fisiopatológico, siendo precisos estudios que aclaren este punto.
Conflictos de interés
Los autores declaran que no tienen conflictos de interés potenciales relacionados con los contenidos de este artículo.
Figura 1. Livedo reticularis bilateral en las plantas y los dedos de los pies.
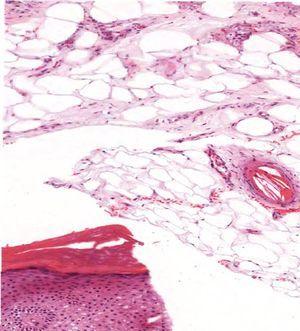
Figura 2. A nivel de panículo adiposo se evidencian vasos ocluidos por material fibrinoso con espacios claros de ángulos sugestivos de cristales de colesterol.
12450_19115_57941_es_12450_figura3.ppt
Figura 3. Evolución de la creatinina sérica.